血清降鈣素原水平對慢性阻塞性肺疾病急性加重期患者疾病嚴重程度的預測價值
毛宇光,楊永密,邱小松
(1. 江蘇省徐州民政醫院 內科重癥監護室,江蘇 徐州,221000;2. 徐州醫科大學附屬醫院 急診ICU,江蘇 徐州,221000)
?
血清降鈣素原水平對慢性阻塞性肺疾病急性加重期患者疾病嚴重程度的預測價值
毛宇光1,楊永密1,邱小松2
(1. 江蘇省徐州民政醫院 內科重癥監護室,江蘇 徐州,221000;2. 徐州醫科大學附屬醫院 急診ICU,江蘇 徐州,221000)
慢性阻塞性肺疾病; 降鈣素原; 疾病嚴重程度; 預后
慢性阻塞性肺疾病(COPD)是一種以氣流受限為特征的慢性氣道炎癥性疾病,患者在COPD發展過程中,反復發生急性加重可導致肺功能迅速惡化,嚴重影響患者的生活質量。慢性阻塞性肺疾病急性加重期(AECOPD)可由多種因素所致,最常見的原因是感染。研究[1]證明COPD是一種系統性炎癥性疾病,在COPD患者中多種炎性因子都呈現高表達。降鈣素原(PCT)是甲狀腺C細胞分泌的糖蛋白,其合成與分泌和炎癥密切相關,是全身性炎癥反應的高靈敏度標志物。作者采集檢測了94例COPD患者急性加重期的血清PCT水平,探討PCT水平對慢性阻塞性肺疾病急性加重期患者疾病嚴重程度及28 d病死率的預測價值,報告如下。
1 資料與方法
1.1 一般資料
采用回顧性病例對照研究方法,收集并分析2012年6月—2016年6月本院內科重癥監護室收治的慢性阻塞性肺疾病急性加重期患者的臨床資料,監護室住院時間>3 d。臨床診斷均符合中華醫學會呼吸病學分會制定的《慢性阻塞性肺疾病診治指南》診斷標準[2]。所有AECOPD患者測PCT水平,并記錄相關合并癥(高血壓病、冠心病、糖尿病及慢性心功能衰竭),并按照COPD指南行痰培養及藥敏實驗,給予敏感抗生素治療,應用激素、支氣管擴張劑,藥物化痰等常規藥物治療,無創機械通氣,有創機械通氣治療。
1.2 方法
血清PCT測定:采靜脈血5 mL,標本委托南京金域醫學檢驗所采用德國羅氏E601全自動免疫分析儀進行電化學發光法測定。
1.3 分組
根據血清PCT水平,將患者分為正常組(PCT<0.5 μg/L)、低水平組(0.5 μg/L≤PCT<2 μg/L)、中等水平組(2 μg/L≤PCT<5 μg/L)、高水平組(PCT≥5 μg/L)。
1.4 數據收集及評估方法
記錄患者的性別、年齡、血細胞計數、肝腎功能、凝血功能、動脈血氣分析、格拉斯哥昏迷評分(GCS)、機械通氣指標、血管活性藥物劑量、28 d病死率。根據患者入住監護室24 h內臨床指標最差值和實驗室指標計算APACHEⅡ評分及序貫器官衰竭評分(SOFA)。比較不同PCT水平患者的預后,評估PCT對非膿毒癥重癥患者28 d預后的預測價值。
1.5 統計學方法
采用SPSS19.0軟件分析數據。計量資料呈正態分布以均數±標準差表示,獨立樣本兩組間比較采用t檢驗,多組間比較采用單因素方差分析;計量資料呈非正態分布以中位數(四分位數)[M(QL,QU)]表示,兩組間比較采用非參數秩和檢驗(Kruskal-WallisU檢驗),多組間比較采用非參數多組秩和檢驗(Kruskal-WallisH檢驗)。變量間的相關性采用Pearson或Spearman相關分析。
2 結 果
共納入94例AECOPD患者,其中男54例,女40例,年齡52~76歲,平均(61.6±8.2)歲;血清PCT為4.60(1.30,9.20)μg/L,APACHEⅡ評分為(12.2±7.0)分,SOFA評分為5.0(3.0,8.0)分,28 d存活78例,死亡16例。患者血清PCT水平與APACHEⅡ、SOFA評分均呈顯著正相關(r1=0.688、r2=0.771,P=0.000)。
死亡組與存活組患者年齡比較差異無統計學意義(P>0.05),但死亡組血清PCT水平及APACHEⅡ、SOFA評分均較存活組顯著升高(P<0.01)。見表1。不同PCT水平組間年齡比較差異無統計學意義(P>0.05)。隨PCT水平升高,APACHEⅡ評分、SOFA評分、28 d病死率也顯著升高(P<0.01)。PCT中等水平組APACHEⅡ評分、SOFA評分顯著高于正常組和低水平組,高水平組各指標均顯著高于其他3組(P<0.01)。PCT中等水平組患者28 d病死率較正常組顯著增高,高水平組較正常組和低水平組顯著升高(P<0.05)。見表2。

表1 存活組和死亡組患者PCT和疾病嚴重程度比較
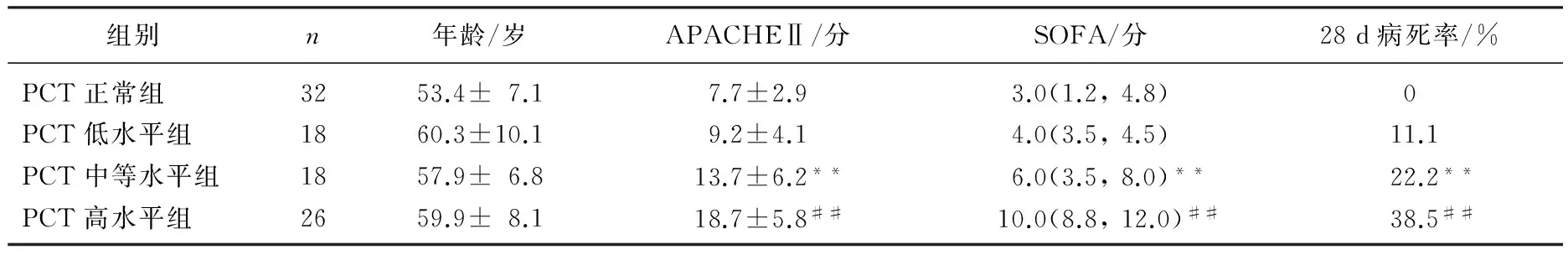
表2 不同PCT水平患者疾病嚴重程度和28 d病死率比較
3 討 論
COPD是一種包括氣道、肺實質及肺血管等組織的慢性炎癥,中性粒細胞、肺泡巨噬細胞、T淋巴細胞等炎癥細胞及肺泡上皮細胞、肺血管內皮細胞不僅參與了氣道炎癥反應,而且影響著肺內蛋白酶/抗蛋白酶系統和氧化/抗氧化系統的平衡,它們互相作用、共同調節 COPD 的發生和發展[3]。COPD主要特征為氣流受限,且氣流受限不完全可逆呈進行性發展[4]。COPD發病機制與炎癥細胞激活、浸潤并釋放炎癥因子有關,各種炎癥細胞、細胞因子及黏附因子參與其發生、發展及轉歸,相關的炎癥因子包括TNF-α和白介素等。AECOPD是指在COPD發展過程中出現的急性事件,其中以細菌感染為主,但仍有1/3的AECOPD患者急性加重的因素尚不明確,所以并不是所有的AECOPD患者需要進行抗菌治療[5]。龍仕居等[6]分析COPD患者急性加重期與緩解期痰液及血清IL-6、IL-8、TNF-α表達水平的差異,急性加重期組和緩解期組誘導痰及血清IL-6、IL-8和TNF-α明顯高于對照組,并且還會隨著患者病情的惡化而逐漸升高。AECOPD可由下呼吸道細菌感染引起,也可由病毒等非典型病原體感染和非感染因素引起。當COPD患者處于全身性炎癥反應狀態,炎癥因子水平顯著高于正常人,且與病情嚴重程度明顯相關。
PCT是降鈣素前肽蛋白,在急性炎癥反應時炎性介質及細菌毒素可刺激其分泌增加[7]。在人體正常的生理狀態下,PCT含量極少,其值<0.01 ng/mL,然而在受到細菌毒素及炎性細胞因子的刺激時,PCT的含量隨之增加,在全身炎癥反應的前2~3 h即可以升高[8]。PCT升高主要與內毒素誘導有關,血清PCT不僅可早期鑒別細菌和非細菌感染,且與細菌感染的程度相關,可作為重癥細菌感染疾病進展的標志物,而其他的感染標志物多缺乏這一特征[9]。PCT與炎癥反應嚴重程度密切相關,是炎癥反應診斷、鑒別診斷及病情和預后評估的血清標志物,TNF-α、IL-1B、IL-6和IL-8可促進其水平增加[10-12]。
APACHE II評分是評價疾病嚴重程度的評分系統,適用于ICU危重癥成人患者[13],同時也是預測ICU患者病死率的有效指標[14]。SOFA評分對于危重患者的器官功能、該病的發生及嚴重程度具有評估能力[15]。SOFA評分是1994年歐洲重癥監護醫學協會(ESICM)感染相關問題工作組制定的感染相關器官衰竭估計評分,因為這一評分的應用不僅局限于感染,以后又叫序貫器官衰竭估計評分[16]。Antonelli等[17]在臨床研究中肯定了SOFA評分對于危重病患者的病情及預后有良好的評估能力。Lilian等[18]研究表明,SOFA評分在病死率的預測上與急性生理和慢性健康狀況評分Ⅱ/Ⅲ(APACHE Ⅱ/Ⅲ)相差不多,與急性生理功能評分系統(SAPSⅡ)基本一致。近年來前瞻性、大樣本、多中心研究[19]證明,SOFA評分與預后有良好的相關性。
近年來的研究[20]提出COPD不能僅僅理解為一種肺部的慢性疾病,而應理解為以呼吸系統病變為主并伴有全身多個系統累及的慢性病變,它可能是一種慢性全身性炎癥綜合征。在 COPD 急性加重期,隨著氣道炎癥反應的發展,全身炎癥反應加重;嚴重的氣道和肺實質的感染,甚至導致系統性炎癥反應綜合征及感染中毒癥。通過全身循環中若干炎性標志物增加而反映全身炎癥是 COPD 的關鍵特征[21]。本文探討了AECOPD重癥患者PCT水平與APACHE Ⅱ、SOFA 評分的關系,結果顯示,AECOPD重癥患者血清PCT水平與APACHE Ⅱ、SOFA評分均呈正相關,PCT水平越高,APACHE Ⅱ、SOFA評分越高。因APACHE Ⅱ、SOFA 評分可以預測重癥患者的疾病嚴重程度、反映患者的預后,所以對于AECOPD重癥患者,血清PCT水平可間接提示疾病的嚴重程度。本研究發現在AECOPD重癥患者中,PCT高水平組較其他PCT水平組28 d病死率顯著升高,當PCT>4.2 μg/L時,預測28 d病死率的敏感度較高。因此,PCT 水平很可能是AECOPD重癥患者死亡風險的獨立預測因素。本研究結果顯示:不同預后患者性別和年齡比較差異無統計學意義,說明患者PCT 在不同情況下發生的變化與性別和年齡無關。
[1] 黃偉平,江穩強,胡北,等. 降鈣素原對全身炎癥反應綜合征患者病情預后的判斷價值[J]. 中國危重病急救醫學,2012,24(5): 294-297.
[2] 中華醫學會呼吸病學分會慢性阻塞性肺疾病學組. 慢性阻塞性肺疾病診治指南(2007修訂版)[J]. 中華結核和呼吸雜志,2007,30(1): 8-17.
[3] 姚婉貞,孫德俊. 慢性阻塞性肺疾病熱點問題[M]. 北京,人民衛生出版社,2009: l67- l78.
[4] Vestbo J,Hurd S S,Agusti A G,et al. Global strategy for the diagnosis,management and prevention of chronic obstructive pulmonary disease: GOLD executive summary[J]. Am J Respir Crit Care Med,2013,187(4): 347-65.
[5] Butorac-Petanjek B,Parnham M J,Popovic-Grle S. Antibiotic therapy for exacerbations of chronic obstructive pulmonary disease(COPD)[J]. J Chemother,2010,22(5): 291-7.
[6] 龍仕居,陳忠仁. 慢性阻塞性肺疾病患者急性加重期與緩解期痰液及血清IL-6、IL-8、TNF-α表達水平的差異及其臨床意義[J]. 重慶醫學,2012,41(19): 1970-1972.
[7] Simon L,Gauvin F,Amre DK,et al. Serum and procalcitonin C-reactive protein levels as markers of bacterial infection: a systematic review and meta-analysis[J]. Clin Infect Dis,2004,39(2): 206-217.
[8] Saigo M,Waters DD,Abe S,et al. Soluble fibrin,Creactive protein fibrinogen,factor ⅴⅡ,antithrombin,proteins C and S,tissue factor,D-dimer,and prothrombin,fragment 1+2 in men with acute myocardial infarction ≤45 years of age[J]. Am J Cardiol,2004,94(11): 1410-1413.
[9] 葉楓,鐘南山. 降鈣素原: 指導重癥細菌感染診療的可靠指標[J]. 中華結核和呼吸雜志,2012,35(11): 873-876.
[10] 張杰,馬晉,張穎. 等. 老年慢性阻塞性肺疾病急性加重期診斷與病情評估中血管內皮因子的應用價值[J]. 中國全科醫學,2013,16(34): 3317-3320.
[11] 柴燕玲,董昭興,鐘紅,等. 血清降鈣素原水平在慢性阻塞性肺疾病急性加重期優化抗菌治療中的臨床意義[J]. 昆明醫學院學報,2011,32(1): 63-66.
[12] 杜翠霞. 血清降鈣素原和C反應蛋白水平在感染性疾病中的診斷價值[J]. 實用心腦肺血管病雜志,2012,20(8): 1366.
[13] Knaus W A,Draper E A,Wagner D P,et al. APACHEⅡ: a severity of disease classification system[J]. Crit Care Med,1985,13(10): 818-829.
[14] Rocker G,Cook D,Sjokvist P,et al. Clinician predictions of intensive care mortality unit mortality[J]. Crit Care Med,2004,32 (5): 1149-1154. DOI: 10. 1097/01. CCM. 0000126402. 51524. 52.
[15] 曾理,胡祖鵬. SOFA評分的臨床意義及其在臨床研究中的應用[J]. 中國臨床醫學,2001,8(1): 84-85.
[16] 劉德紅,楊光田,李樹生,等. 危重病患者外周血單個核細胞核因子-KB的活性與SOFA評分的關系[J]. 中國急救醫學,2004,24(2): 119-120.
[17] Antonelli M,Moreno R,Vincent J L,et al. Application of SOFA score to trauma patients. Sequential Organ Failure Assessment[J]. Intensive Care Med,1999,25(4): 389-394.
[18] Lilian Minne,Ameen Abu-Hanna,Evert de Jonge. Evaluation of SOFA-based models for predicting mortality in the ICU: A systematic review[J]. Crit Care,2008,12(6): R161-167.
[19] Fereira F L,Bota DP,Bross A,et a1. Serial evaluation of the SOFA scOre to predict outcome in critically ill patients[J]. JAMA,200l,286(14): 1754-1758.
[20] Fabbri L M,Rabe K F. From COPD to chronic systemic inflammatory syndrome[J]. Lancet,2007,370(9589): 797-799.
[21] Pinto-Plata V M,Mullerova H,Toso JF,et al. C-reative protein in patients With COPD,control Smokers and non-smokers[J]. Thorax,2006,61(1): 23-28.
2016-07-14
楊永密,E-mail: myg966@163.com
R 441.8
A
1672-2353(2016)21-192-03
10.7619/jcmp.201621077

