HPLC-DAD法同時測定糖痹康中6種主要活性成分
魏 穎,王東超,高佳琪,秦靈靈,孫 文,張 巖,石浩霞,蘭 衛,徐暾海*,劉銅華
(1.北京中醫藥大學中藥學院,北京 100029;2.北京中醫藥大學中醫養生學北京市重點實驗室,北京 100029;3.北京中醫藥大學中醫養生學教育部重點實驗室,北京 100029;4.新疆醫科大學中醫學院,烏魯木齊 830011)
?
HPLC-DAD法同時測定糖痹康中6種主要活性成分
魏 穎1,2,3,王東超1,2,3,高佳琪1,2,3,秦靈靈2,3,孫 文2,3,張 巖2,3,石浩霞1,2,3,蘭 衛4,徐暾海1,2,3*,劉銅華2,3
(1.北京中醫藥大學中藥學院,北京 100029;2.北京中醫藥大學中醫養生學北京市重點實驗室,北京 100029;3.北京中醫藥大學中醫養生學教育部重點實驗室,北京 100029;4.新疆醫科大學中醫學院,烏魯木齊 830011)
目的 研究糖痹康顆粒6種活性成分的含量同時測定的方法。方法 采用HPLC-DAD法測定糖痹康顆粒中6種活性成分的含量,C18色譜柱(150 mm,4.6 mm,5 μm),0.1%甲酸與水-0.1%甲酸與乙腈(18%~60%)梯度洗脫;檢測λ為多波長檢測分別是:196、201、202、204、276、228 nm;用標準曲線法測定。結果 6種活性成分在5 ~ 600 μg/mL范圍內線性關系良好,回歸方程分別為:芍藥苷:Y=227 988X+182,R2=0.999 1;毛蕊異黃酮葡萄糖苷:Y=417 929X-213,R2=0.999 7;特女貞苷:Y=199 569X-312,R2=0.998 3;迷迭香酸:Y=364 936X+152,R2=0.998 1;黃芩苷:Y=64 131X+362,R2=0.999 4;小檗堿:Y=87 882X+111,R2=0.999 5。6種活性成分的加樣回收率分別為:芍藥苷:101.44%(RSD=0.48%);毛蕊異黃酮葡萄糖苷:99.99%(RSD=0.43%);特女貞苷102.07%(RSD=0.57%);迷迭香酸:98.38%(RSD=0.46%);黃芩苷:102.71%(RSD=0.485%);小檗堿:99.54%(RSD=0.77%)。結論 所建立含量測定方法簡便、快捷、可靠,可用于糖痹康顆粒的質量控制。
糖痹康顆粒;活性成分;HPLC-DAD;含量測定
糖尿病(DM)是世界上發病率最高的疾病之一,以持續高血糖為基本生化特征的一種綜合性疾病,嚴重威脅人類生命[1-5]。糖尿病周圍神經病變(DPN)是糖尿病常見并發癥之一,其發病機制十分復雜,并非單一因素所致。本課題組通過大量的前期研究[6-15]表明:糖痹康顆粒用于治療糖尿病周圍神經病變具有很好的療效。課題組組長劉銅華教授經過多年的臨床研究,認為本病主要病機為“氣陰不足,毒瘀神絡”,并在國內外首次提出“益氣養陰、解毒化瘀通絡”的新治療原則。中藥復方糖痹康是在這一治則指導下,在傳統經方黃芪桂枝五物湯基礎上,結合現代研究成果和臨床經驗創制的,先后經多年臨床驗證,不斷優化處方,其組方及制備工藝已成功申報發明專利(專利申請號:200810167551.1)。本實驗通過對糖痹康中前期研究鎖定的6種主要活性成分的含量測定方法進行研究,旨在有效的對復方中藥糖痹康顆粒進行質量評價,實驗結果表明,該方法可有效的控制糖痹康顆粒的質量。
1 儀器與試藥
儀器:島津LC-15C高效液相色譜儀(四元泵,恒溫柱箱,DAD檢測器,LC solution工作站,島津公司,日本);FY130型中藥粉碎機(天津市親斯特儀器有限公司);Millipore-Q超純水制備儀(法國密理博公司);KQ-250B型高功率超聲波清洗器(昆山市超聲儀器有限公司);DF-101S集熱恒溫加熱磁力攪拌器(鄭州長城科工貿有限公司);德國賽多利斯電子分析天平(R200D分析天平)。
材料與試劑:芍藥苷(LOT:B21148,購自上海源葉生物科技有限公司)、毛蕊異黃酮葡萄糖苷(LOT:PM0515SA13,購自上海源葉生物科技有限公司)、特女貞苷(LOT:Z21S3B1,購自上海源葉生物科技有限公司)、迷迭香酸(由中國藥品生物制品檢定所提供,批號為111871-201203)、黃芩苷(LOT:RM0523FA14,購自上海源葉生物科技有限公司)、小檗堿(LOT:Y11A6W1,購自上海源葉生物科技有限公司),6種標準品含量均≥98%,符合含量測定要求;乙腈(色譜純)為美國Fisher Scientific公司產品;甲酸(色譜純)為美國Fisher公司產品;糖痹康顆粒北京中醫藥大學藥廠制備(由黃芪、女貞子、桂枝、赤芍、黃芩、黃連、水蛭等組成,每克顆粒劑相當于3.61 g生藥)。
2 方法與結果
2.1 色譜條件 Thermo Syncronis C18色譜柱(150 mm×4.6 mm,5 μm);流動相:0.1% 甲酸與水-0.1%甲酸與乙腈(18%~60%)30 min;柱溫38 ℃,流速1.0 mL/min,進樣量20 μL,檢測λ為多波長檢測分別是:196、201、202、204、276、228 nm。
2.2 溶液的制備
2.2.1 對照品儲備液制備 分別精密稱取標準品芍藥苷、毛蕊異黃酮葡萄糖苷、特女貞苷、迷迭香酸、黃芩苷、小檗堿,1.023、1.521、1.302、1.125、1.146、1.002 mg,加甲醇配制成1 mg/mL標準品儲備液。冷藏,避光備用。
2.2.2 供試品溶液制備 精密稱取3.00 g糖痹康顆粒,置于具塞錐形瓶中,精密加入90%甲醇100 mL(超聲處理功率90 W,頻率59 Hz,30 min),過濾,旋干,再加入20%甲醇100 mL(超聲處理功率90 W,頻率59 Hz,30 min),加入至上述旋瓶中旋干,50%甲醇定容至15 mL,過濾,取續濾液。
2.3 系統適用性考察 分別吸取對照品溶液、供試品溶液、空白對照溶液各10 μL,注入液相色譜儀,在“2.1.1”條件下測定。芍藥苷:理論踏板數,分離度;毛蕊異黃酮葡萄糖苷理論踏板數,分離度;特女貞苷:理論踏板數,分離度;迷迭香酸:理論踏板數,分離度;黃芩苷:理論踏板數,分離度;小檗堿:理論踏板數,分離度均符合含量測定要求。
2.4 線性關系考察 將“2.1.2”項下對照品儲備液用20%甲醇逐級稀釋成不同濃度的對照品溶液,濃度依次為10、25、50、100、250、500 μg/mL,精密吸取對照品溶液各20 μL,在“2.1.1”項色譜條件下進樣測定,記錄峰面積,以對照品濃度(X)為橫坐標,以峰面積(Y)為縱坐標,繪制標準曲線,得到回歸方程分別為芍藥苷:Y=227 988X+182,R2=0.999 1;毛蕊異黃酮葡萄糖苷:Y= 417 929X-213,R2=0.999 7;特女貞苷:Y=199 569X-312,R2=0.998 3;迷迭香酸:Y=364 936X+152,R2=0.998 1;黃芩苷:Y=64 131X+362,R2=0.999 4;小檗堿:Y=87 882X+111,R2=0.999 5,線性范圍均為5~600 μ/mL。
2.5 精密度試驗 精密吸取一定濃度混和對照品溶液,連續進樣6次,RSD分別為,芍藥苷:0.91%;毛蕊異黃酮葡萄糖苷:1.86%;特女貞苷0.40%,迷迭香酸:1.53%;黃芩苷:1.24%;小檗堿:0.19%,均<2.0%,表明儀器精密度良好。
2.6 穩定性試驗 按“2.1.3”項操作制備供試品溶液,常溫放置,在“2.1.1”項色譜條件下測定,分別于0、2、4、12、24 h進樣,每次20 μL,記錄峰面積,樣品中各成分不同時間測定的峰面積RSD分別為,芍藥苷:1.10%;毛蕊異黃酮葡萄糖苷:1.45%;特女貞苷:0.76%;迷迭香酸:1.83%;黃芩苷:1.44%;小檗堿:0.63%,均<2.0%,表明供試品溶液在24 h內穩定。
2.7 重現性試驗 精密稱取糖痹康顆粒6份,分別按照“2.1.3”項操作制備供試品溶液,按“2.1.1”項色譜條件分別測定。計算樣品中待測成分的含量,結果 RSD分別為,芍藥苷:1.86 %;毛蕊異黃酮葡萄糖苷:2.08%;特女貞苷:1.94%,迷迭香酸:1.67 %;黃芩苷:1.58%;小檗堿:1.79%,證明重復性良好。
2.8 回收率試驗 精密稱取已知含量同一批次供試品6份,每份取樣量為供試品取樣量的50%,約1.50 g。以當前取樣含量的1∶1,分別精密加入芍藥苷、毛蕊異黃酮葡萄糖苷、特女貞苷、迷迭香酸、黃芩苷、小檗堿,按“2.1.3”項操作制備,按“2.1”項色譜條件測定。計算得平均回收率及RSD。見表1。
2.9 樣品含量測定 取樣品3批,按“2.2.2”和“2.2.3”項下的方法制成對照品溶液與供試品溶液,按“2.2.1”方法測定6種主要活性成分。結果表明,糖痹康顆粒中6種活性成分的平均含量:芍藥苷9 360.68 μg/g;毛蕊異黃酮葡萄糖苷3 070.71 μg/g;特女貞苷2 208.47 μg/g;迷迭香酸1 598.81 μg/g;黃芩苷27 267.82 μg/g;小檗堿量443.87 μg/g。
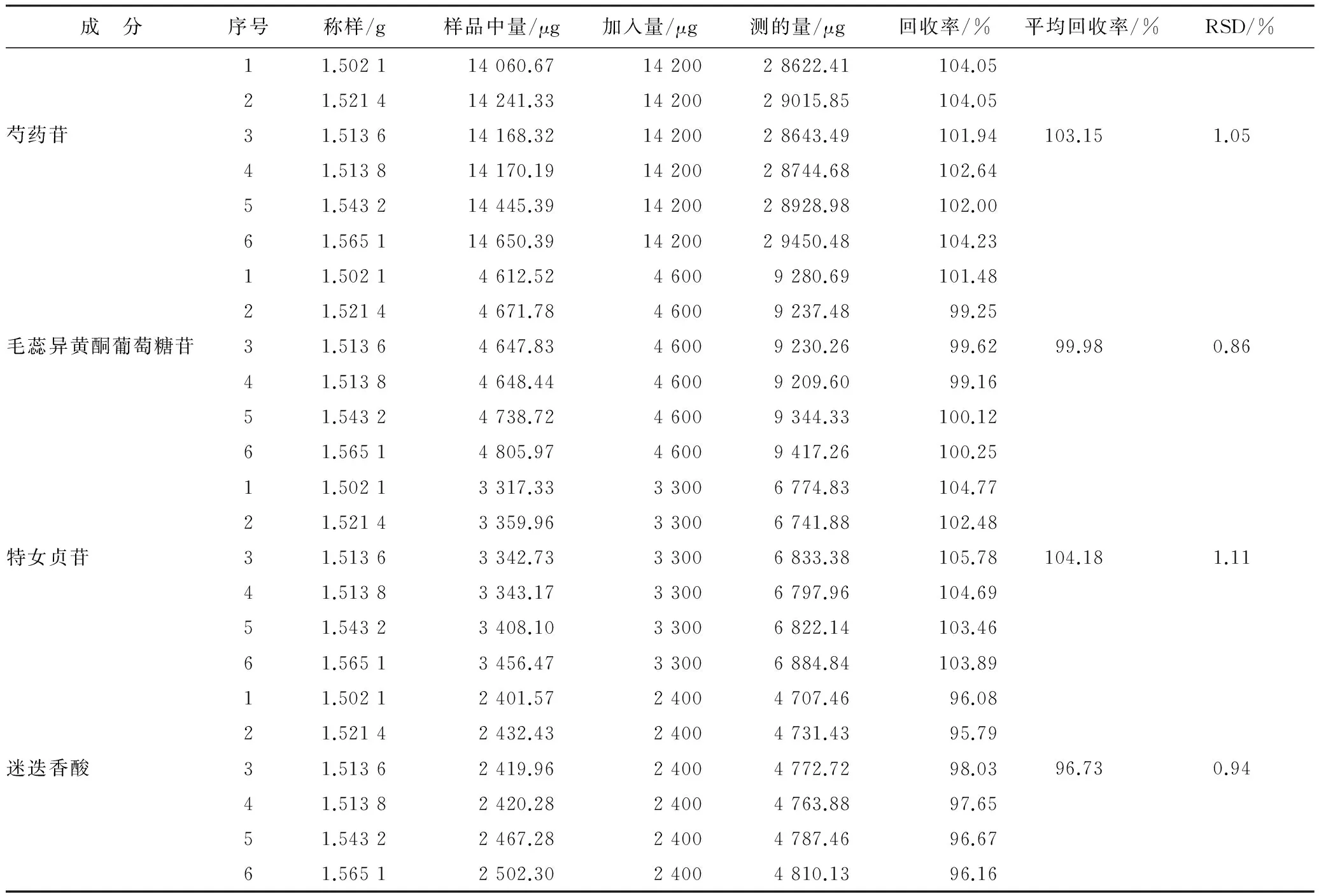
表1 6種活性成分加樣回收率實驗(n=6)
續表1

成 分序號稱樣/g樣品中量/μg加入量/μg測的量/μg回收率/%平均回收率/%RSD/%黃芩苷11.502140958.984100083917.80104.78105.460.9321.521441485.254100084918.57105.9331.513641272.564100084740.74106.0241.513841278.024100085083.70106.8451.543242079.694100084774.52104.1361.565142676.864100085752.04105.06小檗堿11.5021666.746601319.0498.8399.071.5621.5214675.306601330.5099.2731.5136671.846601319.7298.1641.5138671.936601310.3596.7351.5432684.986601347.67100.4161.5651694.706601361.48101.03
3 小結
中藥復方糖痹康經多年臨床證實對DPN具有良好療效,總有效率可達93.39%。HPLC中藥制劑分析法是質量分析中最常用的方法[16]。中藥復方糖痹康顆粒為中醫理論指導下的治療胰島素抵抗的臨床經驗方,由黃芪、女貞子、桂枝、赤芍、黃芩、黃連、水蛭、雞血藤、延胡索(醋制)等中藥提取物組成。對于糖尿病周圍神經病變有很好的療效,本課題組采用HPLC-DAD法對其6種主要活性成分芍藥苷、毛蕊異黃酮葡萄糖苷、特女貞苷、迷迭香酸、黃芩苷、小檗堿同時測定的含量測定方法進行研究。該方法樣品處理簡單、可控。色譜條件簡單,在樣品得到較好分離的基礎上,盡量減少了分析所用的時間,有很好的實用性。該方法準確可靠,可用于本品的內在質量控制。本實驗建立了同時測定糖痹康顆粒中6種主要活性成分的HPLC-DAD的含量測定方法,可以快速、有效的對糖痹康顆粒進行質量控制。
[1]ARONSON D.Hyperglycemia and the pathobiology of diabetic complications[J].Advances in Cardiology,2008(45):1-16.
[2]楊金奎.糖尿病并發癥發病機制新認識——2007年第43屆歐洲糖尿病學會年會專題報告解讀[J].國際內分泌代謝雜志,2008,28(1):18-21.
[3]鄭玲,劉秋爽,金晶,等.糖尿病并發癥治療靶點的研究進展[J].海峽藥學,2014,26(1):13-17.
[4]何永靜.老年糖尿病并發癥的臨床分析[J].當代醫學,2012,18(31):53-54.
[5]王月娟.2型糖尿病患者患病情況及慢性并發癥的相關因素分析[D].長春:吉林大學,2015.
[6]穆曉紅,劉銅華,秦靈靈,等.從血液流變學和坐骨神經傳導速度評價中藥糖痹康對大鼠糖尿病周圍神經病變的影響[J].中華中醫藥雜志,2012,27(2):378-381.
[7]張宏,劉銅華.糖痹康對高糖損傷人臍靜脈內皮細胞的保護作用[J].中華中醫藥學刊,2012,30(6):1248-1251.
[8]王佳,劉銅華.糖痹康對糖尿病周圍神經病變大鼠坐骨神經傳導速度的影響[J].中國中醫基礎醫學雜志,2010,16(3):209-211.
[9]呂翠巖,張勝容,趙文景,等.中藥復方糖痹康對糖尿病大鼠神經保護機制的研究[J].中華中醫藥學刊,2015,33(1):28-30.
[10]呂翠巖,張勝容,蔡朕,等.中藥復方糖痹康對糖尿病大鼠坐骨神經NGF,BDNF及NT-3蛋白表達的影響[J].中華中醫藥雜志,2014,29(12):3946-3949.
[11]呂翠巖,張勝容,趙文景,等.中藥復方糖痹康對糖尿病大鼠坐骨神經BDNF蛋白及BDNFmRNA表達的影響[J].中國中醫基礎醫學雜志,2015,21(2):168-171.
[12]呂翠巖,李秋明,毛穎秋,等.糖痹康對糖尿病大鼠坐骨神經NGF蛋白及NGF mRNA表達的影響[J].中國實驗方劑學雜志,2014,20(5):157-161.
[13]呂翠巖,李秋明,毛穎秋,等.糖痹康對糖尿病周圍神經病變大鼠血漿β-內啡肽的影響[J].中國中醫藥信息雜志,2014,21(4):49-51,52.
[14]呂翠巖,張勝容,趙文景,等.糖痹康對糖尿病周圍神經病變大鼠VEGF表達的影響[J].中華中醫藥雜志,2016,33(1):219-221.
[15]呂翠巖.糖痹康干預糖尿病周圍神經病變臨床及作用機制研究[D].北京:北京中醫藥大學,2014.
[16]魏穎,時曉娟,王東超,等.糖耐康顆粒含量測定方法研究[J].世界科學技術-中醫藥現代化,2015,17(6):1169-1175.
Simultaneous determination of 6 main active components in Tang-Bikang by HPLC-DAD
WEI Ying1,2,3,WANG Dongchao1,2,3,GAO Jiaqi1,2,3,QIN Lingling2,3,SUN Wen2,3,ZHANG Yan2,3,SHI Haoxia1,2,3,LAN Wei4,XU Tunhai1,2,3*,LIU Tonghua2,3
(1.College of Pharmacy Beijing University of Chinese Medicine,Beijing 100029,China;2.Health Cultivation Laboratory of the Ministry of Education,Beijing 100029,China;3.Health Cultivation Laboratory of Beijing,Beijing 100029,China;4.Traditional Chinese Medicine College of Xinjiang Medical University,Urumqi 830011,China)
Objective To study a method for simultaneous determination of 6 active components in Tang-Bikang granules.Methods Determination of 6 active ingredients of Tang-Bikang granules by HPLC-DAD method,C18column (150 mm,4.6 mm,5 m),0.1% formic acid and water-0.1% formic acid and acetonitrile (18%-60%) gradient elution;The detection wavelength is multi wavelength detection,they are:196,201,202,204,276,228 nm;Standard curve method was used.Results The 6 active ingredients in 5 μg·mL-600μg·mL shows a good linearity,and the regression equations respectively are:Peoniflorin:Y=227 988X+182,R2=0.999 1;Campanulin:Y=417 929X-213,R2=0.999 7;Specnuezhenide:Y=199 569X-312,R2=0.998 3;Rosmarinci acid:Y=364 936X+152,R2=0.998 1;Baicalin:Y=64 131X+362,R2=0.999 4;Berberine:Y=87 882X+111,R2=0.999 5.The recoveries of the 6 active components are:Peoniflorin:101.44%(RSD 0.48%);Campanulin:99.99%(RSD 0.43%);Specnuezhenide:102.07%(RSD 0.57%);Rosmarinci acid:98.38% (RSD 0.46%);Baicalin:102.71% (RSD 0.485);Berberine:99.54% (RSD 0.77%).Conclusion The establishment of the content determination method is simple,fast and reliable,and it can be used to control the quality of Tang-Bikang particles.
Tang-Bikang;ingredients;HPLC-DAD;content determination
10.13463/j.cnki.cczyy.2016.06.012
國家重大新藥創制 “治療糖尿病周圍神經病變候選藥物糖痹康臨床前研究”(1000071320025);2014年北京市教委共建成果轉化與產業項目“糖調節受損中藥保健食品產業化與社區干預療效安全性評價研究”。
魏 穎(1991-),女,博士研究生,主要從事中藥降糖活性物質基礎研究。
R284.2
A
2095-6258(2016)06-1135-04
2016-04-12)
*通信作者:徐暾海,男,博士,教授,博士研究生導師,電話-15300175337,電子信箱-Thxu@163.com

