柱前衍生超高效液相色譜法分析太子參多糖中單糖的組成
郭守斌
(江蘇省連云港市第一人民醫院藥學部,江蘇 連云港 222000)
論著
柱前衍生超高效液相色譜法分析太子參多糖中單糖的組成
郭守斌
(江蘇省連云港市第一人民醫院藥學部,江蘇 連云港 222000)
目的建立柱前衍生超高效液相色譜(UPLC)法,測定太子參多糖中單糖的組成。方法采用水提醇沉法提取太子參多糖,2 mol/L硫酸水解后加入1-苯基-3-甲基-5-吡唑啉酮進行衍生化,采用UPLC法測定太子參多糖中單糖的衍生物。采用沃特世C18超高效液相色譜柱(100.0 mm×2.1 mm,1.7μm)色譜柱,以乙腈為流動相A,0.1 mol/L磷酸鹽(pH 6.8)緩沖液為流動相B,梯度洗脫,檢測波長250 nm。通過聚類分析和主成分分析,對不同產地太子參單糖進行質量評價。結果太子參多糖由半乳糖、D-甘露糖、鼠李糖、阿拉伯糖、D-無水葡萄糖、D-葡萄糖醛酸、D-半乳糖醛酸7種單糖組成,不同產地太子參多糖中單糖組成稍有差別,通過主成分分析和聚類分析評價,10個不同產地太子參單糖聚成3類,并按照單糖含量對各產地進行排名。結論柱前衍生UPLC法表明,太子參多糖主要由半乳糖醛酸、半乳糖和阿拉伯糖構成,并且貴州施秉縣地區產太子參單糖含量較高。
太子參多糖;柱前衍生化;超高效液相色譜;聚類分析;主成分分析;單糖
Keywords:P.heterophylla polysaccharide;pre-column derivation;ultra performance liquid chromatography;cluster analysis;principal component analysis;monosaccharide
太子參為石竹科植物孩兒參的干燥塊根。性味甘、微苦,平,歸脾、肺經。臨床主要用于益氣健脾、生津潤肺,用于脾虛體倦、食欲不振、病后虛弱、氣陰不足、自汗口渴、肺燥干咳等癥候[1]。藥理學研究表明,太子參多糖具有增強機體免疫功能、降糖降脂及保護肝臟等作用,是太子參的主要有效成分之一[2-3]。太子參多糖為中性葡聚糖,有關太子參多糖含量測定的研究很多,主要采用體積排阻高效液相色譜法[4]、高效液相色譜-蒸發光散射法[5]及硫酸-苯酚比色法[6-7],其單糖組成迄今未見報道,而多糖的單糖組成分析是進行多糖質量控制和獲取多糖基本信息的重要環節。因此,本實驗以1-苯基-3-甲基-5-吡唑啉酮(3-Methyl-1-phenyl-2-pyrazolin-5-one,PMP)為衍生物,在堿性條件下與單糖縮合生成單糖-PMP衍生物,應用超高效液相色譜(ultra performance liquid chromatography,UPLC)法,對太子參多糖進行單糖組成方面的研究,并利用主成分分析和聚類分析對單糖進行評價,為太子參開發利用和質量控制提供可靠依據。
1 資料與方法
1.1 儀器與試藥
Waters ACQUITY UPLC H-CLASS超高效液相色譜儀、Empower色譜工作站購自美國沃特世公司,DFY-300型搖擺式高速萬能粉碎機(江蘇省江陰市康和藥化機械制造有限公司),TG16-WS離心機(湖南湘儀實驗室儀器開發有限公司),ABS-135S電子天平(上海梅特勒-托利多儀器有限公司),KB-500 DB超聲波清洗器(浙江省昆山市超聲儀器有限公司),LGJ-10冷凍干燥機(北京市松源華興生物技術有限公司)。
經作者鑒定為石竹科植物孩兒參的干燥塊根。D-無水葡萄糖(D-glucose anhydrous,Glu)(中國藥品生物制品檢定所,110833-201205,含量為99.5%),D-甘露糖(D-mannose,Man)(中國藥品生物制品檢定所,140651-201403,含量為99.6%),D-葡萄糖醛酸(D-glucuronic acid,GluUA)(中國藥品生物制品檢定所,140648-200602),半乳糖(Galactose,Gal)(中國藥品生物制品檢定所,100226-201105,含量為99.9%),L-阿拉伯糖(L-Arabinose,Arab)(中國藥品生物制品檢定所,1506-200001),D-半乳糖醛酸(α-D-galacturonic acid monohydrate,GalUA)(中國藥品生物制品檢定所,111646-200301),鼠李糖(L-rhamnose monohydrate,Rha)(中國藥品生物制品檢定所,111683-201502)。乙腈為色譜純,PMP為分析純,水為實驗室自制去離子水,其他試劑均為分析純。見表1。
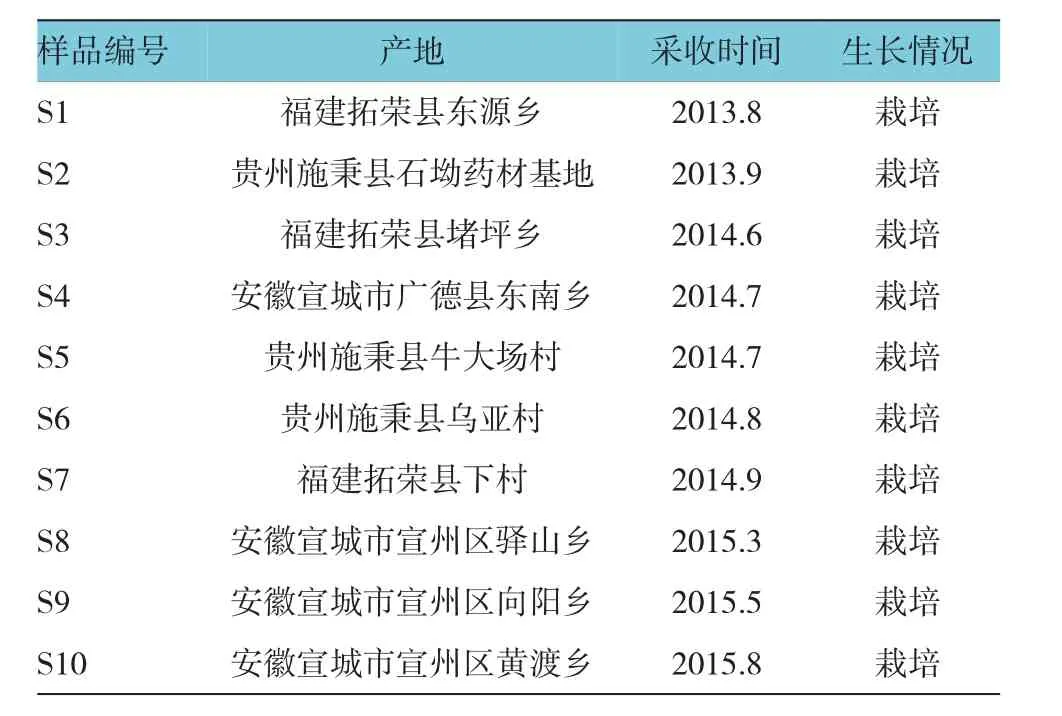
表1 太子參樣品來源
1.2 實驗方法
1.2.1 色譜條件沃特世C18超高效液相色譜柱(100.0mm×2.1mm,1.7μm);流動相:乙腈-0.05mol/L磷酸鹽緩沖液(pH 6.8),梯度洗脫(0~5 min,10%A;5~15 min,10%~15%A;15~25 min,15%~20%A);檢測波長250 nm;柱溫30℃;流速0.25 ml/min;進樣量2μl。
1.2.2 太子參多糖的提取取太子參(S1-S10)干燥粉末(過四號篩)各約6 g,精密稱定,加85%乙醇60 ml回流提取3次,3 h/次,提取液棄去,太子參藥渣加50 ml水,水浴回流提取3次,3 h/次,收集提取液,減壓濃縮至約25 ml,用Sevage法除去太子參多糖提取液中蛋白成分后,加乙醇80 ml,靜置過夜,取提取液3 000 r/min離心10 min,棄上清液,反復離心至上清液無色,沉淀物依次加無水乙醇-乙醚-丙酮洗滌3次,冷凍干燥,得太子參多糖。
1.2.3 溶液的制備①供試品溶液。精密稱取太子參多糖約20mg置安瓿中,加2mol/L硫酸溶液2.0ml,用氮氣排走空氣,封口,置水域中水解8 h,冷卻至室溫,用4 mol/L NaOH溶液調節pH至7.0,用0.45μm微孔濾膜濾過,備用。②混合對照品溶液。分別取Glu、Man、GluUA、Gal、Arab、GalUA、Rha對照品各適量,精密稱定,置10 ml量瓶中,加水溶解并稀釋至刻度,搖勻,配制成每1 ml分別含Glu1 642μmol/L、Man 1023μmol/L、GluUA682μmol/L、GalUA1568μmol/L、半乳糖1 260μmol/L、Arab 1 888μmol/L、Rha 985 μmol/L的混合對照品溶液,備用。
1.2.4 衍生化產物的制備精密量取混合對照品溶液和太子參多糖水解液各200μl置10 ml離心管中,分別依次加入200μl PMP甲醇溶液和0.3 mol/L NaOH溶液,混合均勻,置70℃水域中反應30 min,冷卻至室溫,分別加入200μl 0.3 mol/L鹽酸溶液中和,充分混勻,加入1 ml氯仿進行萃取,充分震蕩混勻,4 000 r/min離心10 min,棄去下層有機相,重復萃取3次,合并上層水相,0.45μm微孔濾膜濾過,備用[8]。
1.2.5 方法學考察①線性關系和最小檢測限。分別精密吸取混合對照品溶液0.2、0.5、1.0、2.0、4.0和10.0 ml,置10 ml容量瓶中,加水稀釋至刻度,充分搖勻,按1.2.4方法衍生化制備,配制系列濃度對照品混合溶液。按1.2.1色譜條件試驗,記錄色譜圖,以對照品摩爾濃度(X)為橫坐標,以色譜峰峰面積(Y)為縱坐標繪制標準曲線。再將最低濃度混合對照溶液稀釋至信噪比為3時所對應溶液的摩爾濃度以確定為最低檢測限(見表2)。②精密度試驗。取混合對照品溶液,按1.2.4方法進行衍生,依照1.2.1色譜條件,連續進樣6次,記錄色譜圖。結果Glu、Man、Glu UA、Gal、Arab、GalUA、Rha峰面積的相對標準偏差(relative standard deviation,RSD)分別為0.6%、0.4%、0.8%、0.7%、0.6%、0.4%和0.9%,表明儀器精密度良好。③重復性試驗。取太子參(S1)多糖6份,按1.2.3方法制備樣品溶液,再按1.2.4方法進行衍生化處理,依照1.2.1色譜條件,依次測定,記錄峰面積。結果Glu、Man、GluUA、Gal、Arab、GalUA、Rha峰面積的RSD分別為0.5%、0.7%、0.3%、0.3%、0.2%、0.7%和0.6%,表明方法重復性良好。④穩定性試驗。取太子參(S1)多糖,按1.2.3方法水解成單糖,再按1.2.4方法進行衍生化處理,分別于0、2、4、6、8和12 h測定,記錄峰面積。結果Glu、Man、GluUA、Gal、Arab、Gal UA、Rha峰面積的RSD分別為1.2%、1.3%、1.3%、1.6%、0.8%、1.1%和1.6%,表明太子參中單糖衍生物在12 h內穩定。⑤加樣回收率試驗。取已知含量太子參(S1)多糖(約10 mg)6份,精密稱定,置具塞試管中,分別精密加入相當樣品含有量的Glu、Man、GluUA、Gal、Arab、GalUA、Rha對照品,按1.2.3方法水解成單糖,再按1.2.4方法進行衍生化處理,依1.2.1色譜條件測定,記錄色譜圖。結果Glu、Man、GluUA、Gal、Arab、GalUA、Rha平均回收率分別為98.6%(RSD 1.0%)、98.9%(RSD 0.9%)、98.8%(RSD 1.2%)、99.1%(RSD 1.2%)、98.4%(RSD 1.0%)、97.8%(RSD 0.9%)和98.8%(RSD 0.6%)。
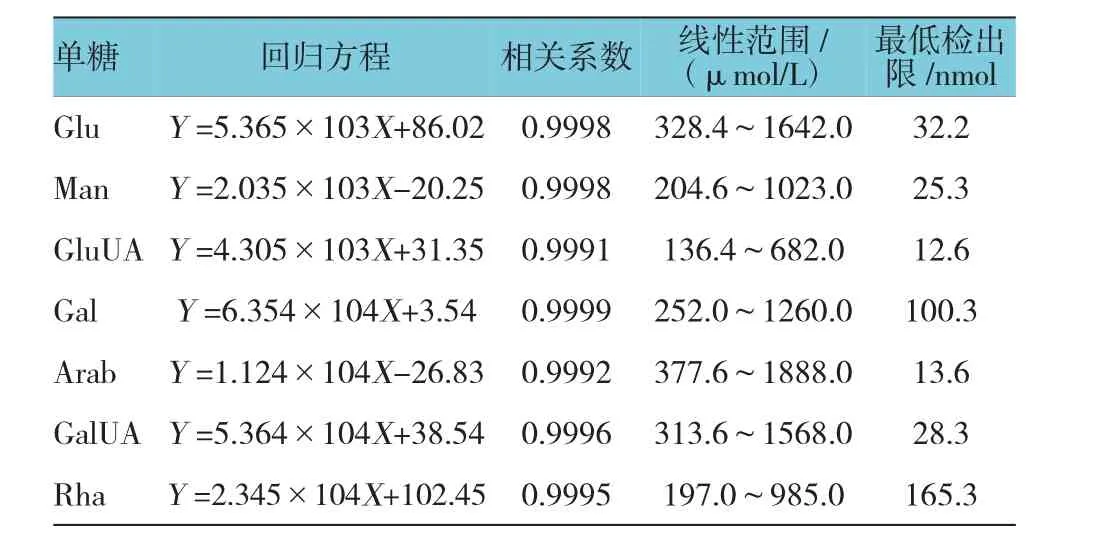
表27 種單糖衍生物的線性關系
1.2.6 樣品測定取不同產地太子參(S1-S10)多糖,按1.2.3方法水解成單糖,再按1.2.4方法進行衍生化處理,依1.2.1色譜條件測定,記錄色譜圖。采用外表一點法求得各單糖含量,并計算太子參多糖中Glu、Man、GluUA、Gal、Arab、GalUA、Rha的摩爾比。見圖1和表3。
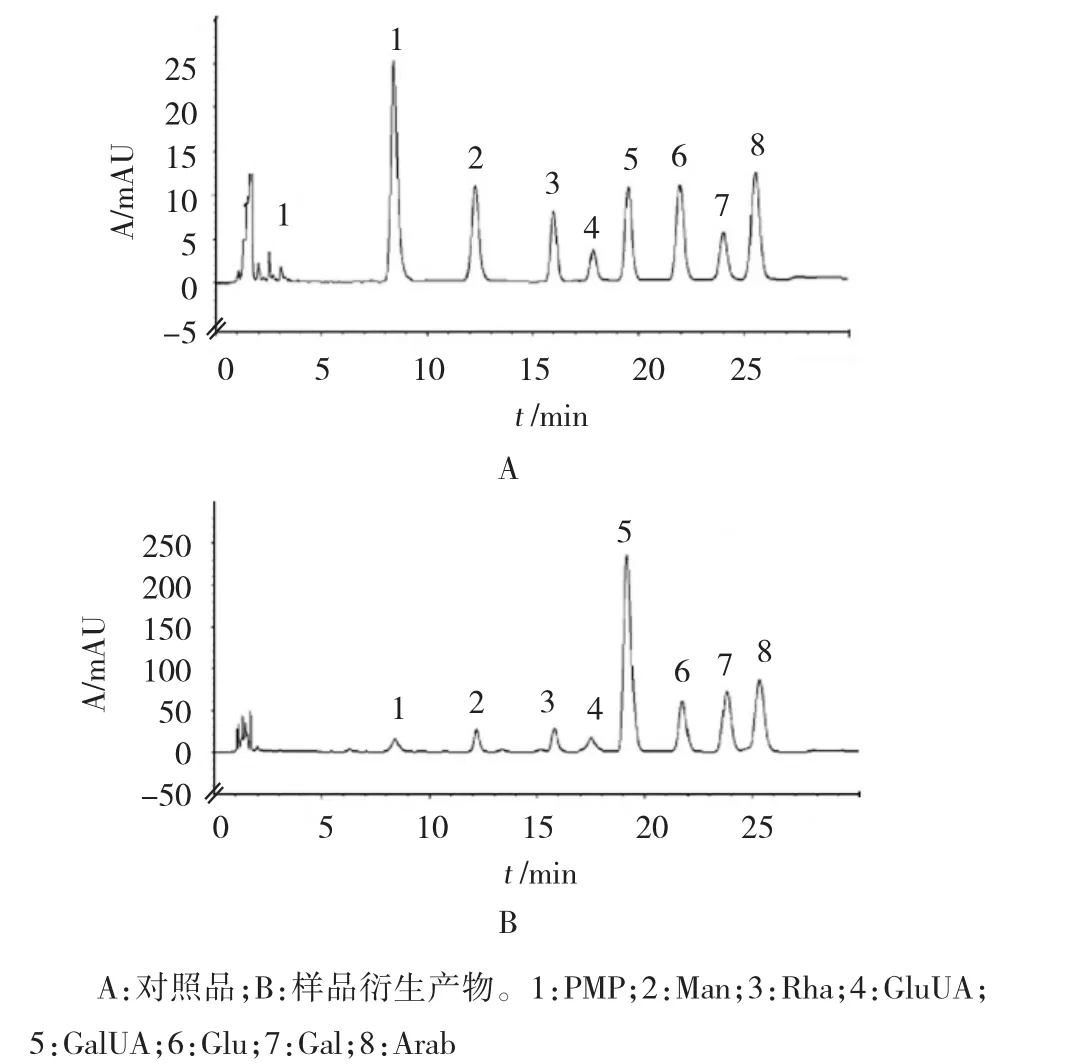
圖1 對照品與樣品衍生產物色譜圖
1.3統計學方法
采用SPSS 22.0統計軟件進行數據分析,通過聚類分析和主成分分析對10個產地太子參多糖中單糖進行評價,P<0.05為差異有統計學意義。
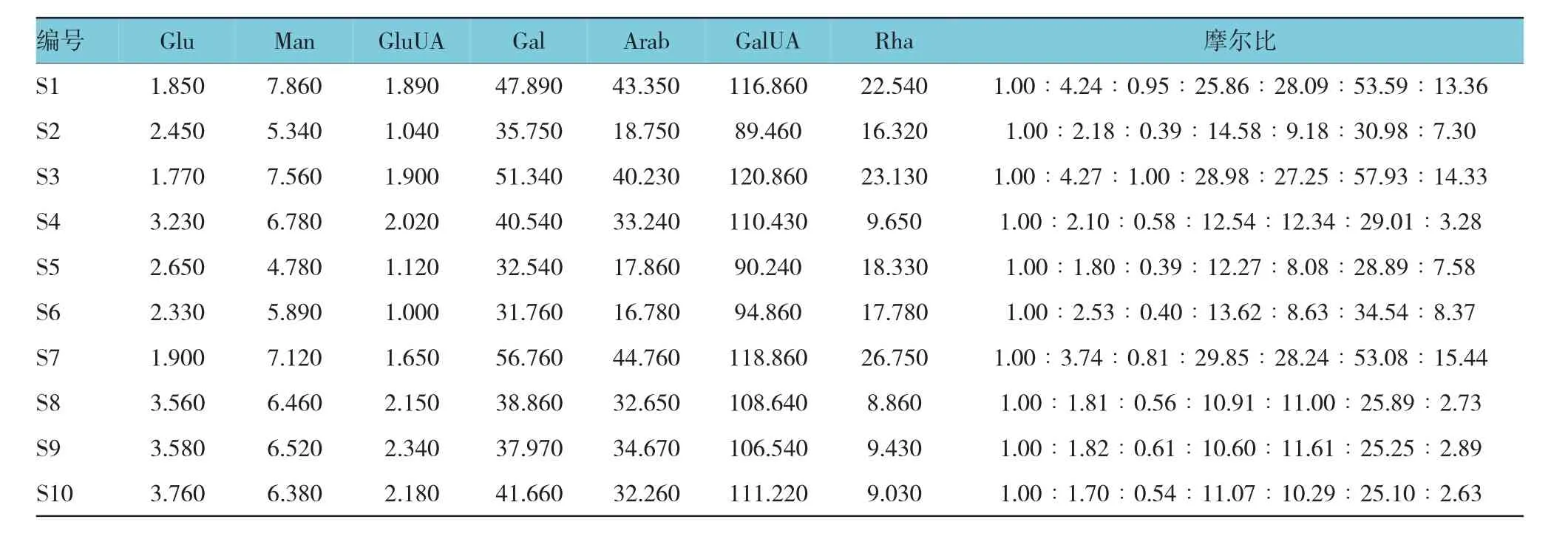
表3 太子參樣品單糖組成及含量
2 結果
2.1 主成分分析
將表2數據導入SPSS 22.0統計軟件,以各產地單糖作為變量,利用主成分分析,將7個單糖進行降維,提取出2個主成分,分析個主成分主要貢獻單糖種類,并依據主成分得分對各產地太子進行排名。分析得出的主成分特征值與貢獻率。見圖2和表4。
特征值在某種程度上可以被看成是表示主成分影響力度大小的指標,通過表3(方差分解主成分提取分析)和圖2可以看出,主成分3之前連線較為陡峭,即前3個主成分對解釋變量的貢獻最大,又有前2個成分累計貢獻值達95.906%,所以提取2個主成分。從表4可知Man、Gal、Arab、GalUA在第一主成分上有較高載荷(相關系數>0.9),說明第一主成分基本反映這些指標的信息;而Glu在第二主成分上有較高載荷。提取2個主成分基本囊括7個單糖成分,基本能反映全部指標的信息,所以決定用2個新變量來代替原來的7個變量開展評價。
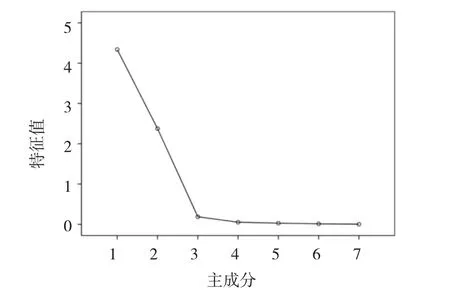
圖2 主成分分析碎石圖
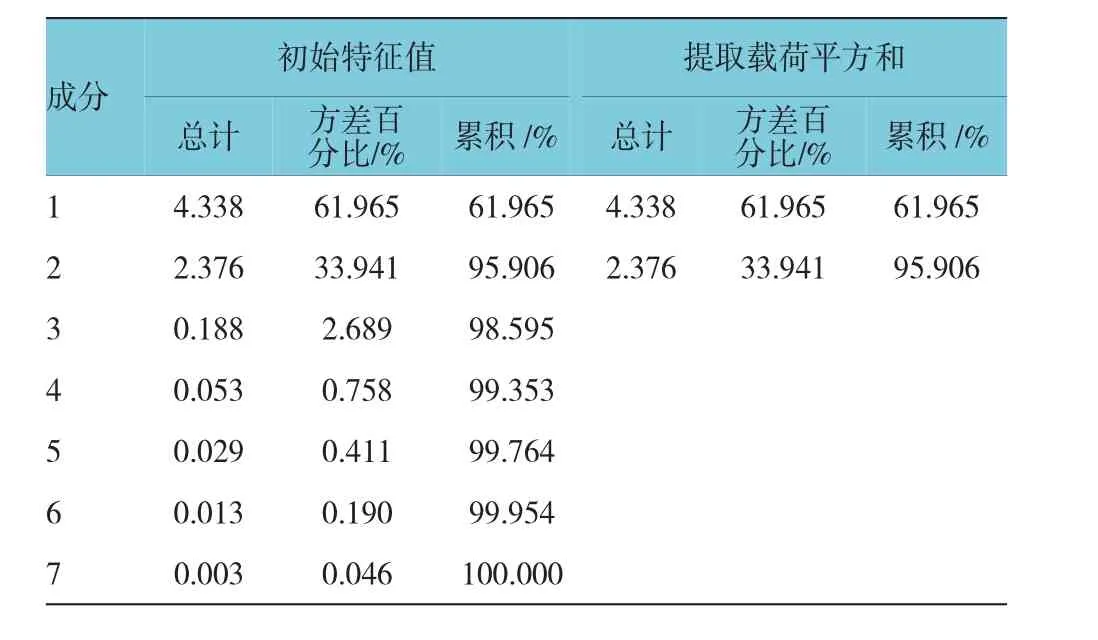
表4 主成分分析的特征值與方差貢獻率
用每個產地分別對應于2個主成分的初始因子載荷值除以主成分相對應的特征值(λ1=4.338,λ2= 2.376)開平方根即可得到每個指標分別對應的2個主成分的特征向量(特征向量代表各原指標對于主成分的重要程度),將得到的特征向量與標準化后的數據相乘,然后就可以推導出2個主成分表達式,并可算出主成分綜合模型,利用2個主成分的表達式和主成分綜合模式可計算出太子參個各產地分值,并按分值大小進行排名。見表5。
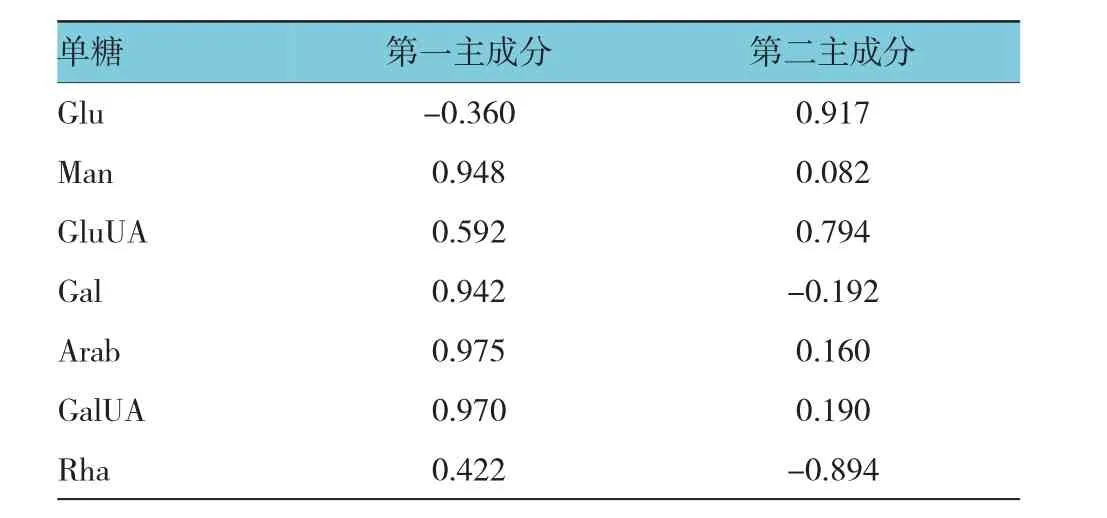
表5 初始因子載荷矩陣
第一、二主成分對7個變量的解釋有>95%的貢獻值,而Man、Gal、Arab、GalUA、Glu在第二個主成分上有較高載荷,所以用以上5個單糖指標可以對太子參多糖進行評價,可以看出以產地為福建拓榮縣的太子參較好。見表6。

表6 不同產地太子參單糖得分及排名
2.2 聚類分析
將表2數據導入SPSS 22.0統計軟件,以各產地單糖作為變量,采用組間連接法,選用歐氏距離對10個不同產地太子參單糖進行聚類分析,可看出其中來自Y福建拓榮縣太子參聚為一類,其他另外2個產地分別聚為一類,說明同一地區不同地點太子參,單糖組成及含量有著一定相似度。見圖3。
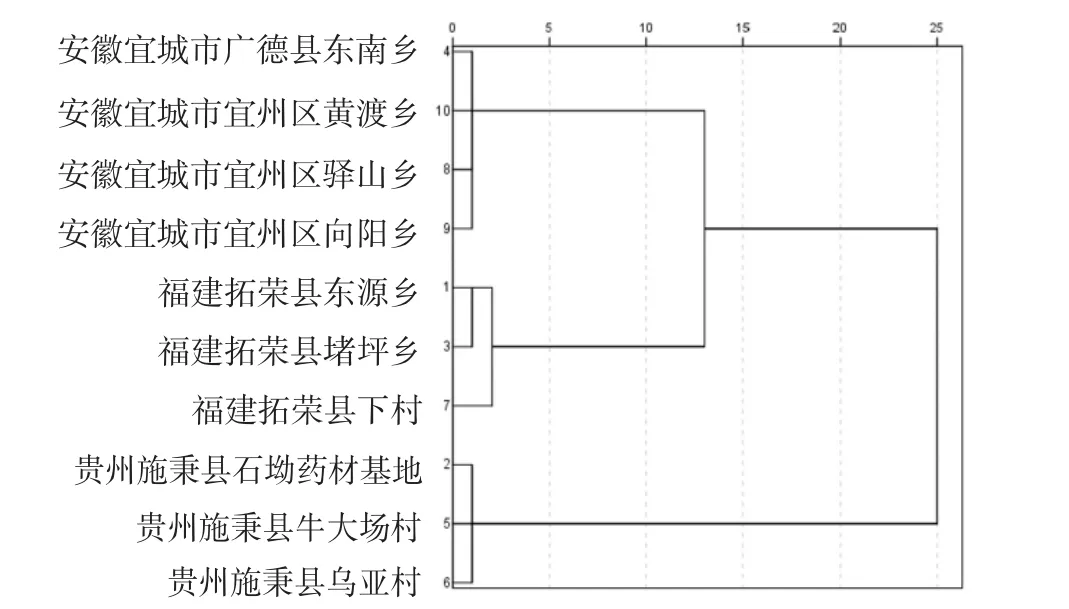
圖3 太子參單糖聚類分析圖
3 討論
太子參是一種常用又珍貴藥材,有補氣健脾、養陰益血等功效,可作為人參替代品,老少皆宜服用。多糖是其有效成分之一,有調節和促進機體免疫力等作用。而UPLC法具有分離效率高、節能、省時等優點,在中藥質量分析中運用逐漸廣泛。通常多糖水解樣品的制備過程需經過復雜干燥過程,干燥衍生化后氯仿萃取后的水層溶液,揮棄PMP殘留衍生化試劑,以達到純化單糖衍生物的目的。但在本實驗色譜條件下,PMP溶劑峰出峰時間明顯早于各單糖衍生物保留時間,所以制備過程中可以省去干燥過程,用NaOH中和水解液后,直接PMP衍生化處理,幾乎無糖損失,縮短樣品制備時間,簡化實驗操作。
本研究建立衍生化-UPLC檢測太子參多糖中單糖組成的方法,通過與標準單糖衍生物的比對,對7個色譜峰進行指認,可提供太子參多糖的單糖組成基本信息。本方法簡單靈敏,操作方便快速,為發展太子參多糖的在線定性定量UPLC檢測奠定基礎,為進一步開發利用太子參產品提供科學依據。
[1]國家藥典委員會編.中華人民共和國藥典(一部)(2015年版)[M].北京:化學工業出版社,2015:68.
[2]劉訓紅,陳彬,王玉璽.太子參多糖抗應激和免疫增強作用的實驗研究[J].江蘇中醫,2000,21(10):51-53.
[3]劉曉滿.人參多糖降糖機制的初探[D].長春:東北師范大學,2009.
[4]陳蕓蕓,王偉,丁怡,等.SE-HPLC測定太子神悅膠囊中多糖相對分子質量分布及含量[J].中國藥學雜志,2005,40(7):540-542.
[5]宋建平,曾艷萍,劉訓紅,等.HPLC-ELSD測定不同產地太子參中多糖的含量[J].上海中醫藥雜志,2008,42(10):77-79.
[6]劉訓紅,談獻和,曾艷萍,等.不同產地太子參的質量比較研究[J].現代中藥研究與實踐,2007,21(2):36-38.
[7]羅國海,盛柳青,張秋霞,等.太子參藥材主根與參尾的多糖含量比較[J].中藥研究與開發,2006,13(11):50-51.
[8]范剛,唐策,李艷,等.柱前衍生HPLC分析黃連多糖的單糖組成[J].中國實驗方劑學雜志,2014,20(11):74-78.
(童穎丹 編輯)
Analysis of monosaccharide composition ofPseudostellaria heterophyllapolysaccharides by pre-column derivatization ultra performance liquid chromatography
Shou-bin Guo
(Department of Pharmacy,the First People's Hospital of Lianyungang, Lianyungang,Jiangsu 222000,China)
Objective To establish a pre-column derivation ultra performance liquid chromatography(UPLC)for determining monosaccharide composition inPseudostellaria heterophyllapolysaccharides.Methods The polysaccharides were extracted by hot distilled water,precipitated by alcohol,and hydrolyzed with 2 mol/L sulfuric acid and derived by 1-phenyl-3-methyl-5-pyrazolone(PMP).The analysis of monosaccharide composition ofP.heterophyllapolysaccharides was carried out by reversed-phase UPLC on a Waters ACQUITY UPLC BEH HILIC C18 column(100.0 mm×2.1 mm,1.7 μm)with a mobile phase composed of 0.1 mol/L phosphate (pH 6.8)and Acetonitrile in a gradient elution manner.The detection wavelength was set at 250 nm.Cluster analysis(CA)and principal component analysis(PCA)were used to evaluateP.heterophyllamonosaccharide in different producing areas.Results TheP.heterophyllapolysaccharides were composed of galactose,D-mannose,rhamnose,arabinose,D-glucose,D-glucuronic acid and D-galacturonic acid.Totally 10 batches ofP. heterophyllapolysaccharides could be classified into three clusters,and the producing areas were sorted based on the content of monosaccharides.Conclusions The UPLC with pre-column derivation shows thatP.heterophyllapolysaccharides mainly consist of galacturonic acid,galactose and arabinose.P.heterophyllaof Shibing County has higher content of monosaccharides.
R284.1
A
10.3969/j.issn.1005-8982.2016.23.008
1005-8982(2016)23-0037-05
2016-07-14

