基于α調整的國際多中心臨床試驗目標區二分類終點有效性研究的橋接方法*
第四軍醫大學軍事預防醫學院衛生統計學教研室(710032)
虞成凱 王 陵△ 戚洋洋 李嬋娟 李 晨 蔣志偉 夏結來△
基于α調整的國際多中心臨床試驗目標區二分類終點有效性研究的橋接方法*
第四軍醫大學軍事預防醫學院衛生統計學教研室(710032)
虞成凱 王 陵△戚洋洋 李嬋娟 李 晨 蔣志偉 夏結來△
目的 探索采用合理的調整后檢驗水準α′作為國際多中心臨床試驗(MRCT)在目標區的決策依據的可行性,為MRCT在目標區通過審批提供參考。方法 利用Monte Carlo模擬構建二分類資料、優效性設計、包含目標區的MRCT數據模型,比較不同規模的MRCT在檢驗水準α=0.05水平顯示試驗組優效的前提下,目標區采用調整后檢驗水準α′作為決策依據的條件Ⅰ型錯誤率(CFPR)、條件檢驗效能(CP)隨目標區樣本量占總樣本量比例K的變化情況。結果 在不同規模的MRCT中,目標區的CFPR和CP均隨著檢驗水準α′、樣本比例K的增加而增加;當α′=0.5時,CFPR和CFPR′基本可以被控制在50%和5%左右。當樣本比例K固定時,目標區CP相對穩定,尤其當K≥30%時隨著α′的增加目標區CP幾乎不受MRCT總樣本量N的影響,且當α′不低于0.3時基本可以確保足夠的CP(≥80%)。當K≥30%且設置α′=0.5時,即使目標區試驗藥物療效略低于MRCT的療效即f≥0.8,也可以確保目標區足夠的CP和CP′(≥80%)。結論 建議MRCT在方案設計時,目標區的樣本比例不應低于30%,試驗數據在目標區的檢驗水平不能超過0.5。該標準適用于目標區試驗藥物療效略低于MRCT的療效即f≥0.8的情形,若估計目標區試驗藥物療效與MRCT的療效相當,檢驗水平可適當降低,但不建議低于0.3。
條件Ⅰ型錯誤率 條件檢驗效能 國際多中心臨床試驗 Monte Carlo模擬
當研究藥物在原地區批準上市后,申辦者可能會在一個新的地區申請注冊該藥物。然而,原地區和新地區的種族、文化和臨床實踐之間的差異及其對藥物安全性、有效性、劑量和給藥方案的影響,限制了新地區藥物監管機構接受原地區產生的臨床試驗數據的意愿。因此新地區藥物監管機構通常要求申辦者重復類似試驗,以橋接研究藥物在本地區的有效性和安全性。但是,在新地區的重復臨床評估不僅需要昂貴的研發資源而且大大延遲了新地區患者獲得新藥的時間[1]。為了解決這種困境,人用藥品注冊技術要求國際協調會(ICH)E5指南[2],即《接受國外臨床資料的種族影響因素》給出了基于橋接策略評價種族因素對研究藥物有效性和安全性影響的框架[3]。然而,大部分橋接試驗是在研究藥物經原地區批準上市后才在新地區進行,同樣存在新藥上市滯后的問題。
為了加快研究藥物在日本上市,日本厚生勞動省2007年發布的指南《全球臨床試驗的基本原則》[4]用問答的形式列出了計劃和實施國際多中心臨床試驗(multi-regional clinical trial,MRCT)的基本概念,提出在MRCT中應納入足夠多的日本病例來評價潛在的種族差異以確保新藥能夠在日本同步上市。該原則列舉了兩種估計日本地區樣本量的方法。Quan[5]等人討論了方法一,提出日本區納入的樣本量須保證本地區試驗組與對照組療效差值大于或等于整個試驗療效差值的50%的概率不低于0.8。Chen[6]等人在Quan的研究基礎上提出當MRCT在檢驗水準α=0.05的水平顯示試驗組優效于對照組時,可采用調整后檢驗水準α′作為局部地區的藥物監管部門批準研究藥物上市的決策依據。本研究將進一步研討二分類資料的MRCT采用檢驗水準α′作為目標區決策依據的可行性并探索α′的合理取值。
方法與步驟
假定一個二分類資料、優效性設計的MRCT,包括目標區和非目標區,試驗組與對照組例數比1:1,在總的檢驗水準α=0.05水平,試驗組的療效優于對照組且差別有統計學意義。
采用Monte Carlo模擬構建MRCT數據模型,比較不同規模的MRCT中目標區采用不同檢驗水準α′作為決策依據允許研究藥物上市的條件Ⅰ型錯誤率(conditional false positive rate,CFPR)和條件檢驗效能(conditional test power,CP)隨目標區樣本量占總樣本量比例的變化情況。本研究所有的數據均由模擬產生,采用SAS 9.1.3統計分析軟件編寫程序和統計分析。
1.參數設置
令MRCT的試驗組與對照組療效分別為Pt和Pr,其中目標區的試驗組與對照組療效分別為PtL和PrL,非目標區的試驗組與對照組療效分別為PtNL和PrNL,假定 Pr=PrL=PrNL,Pt=PtNL。
參考 Huang[7]等人研究的參數設置,設 Pr為0.20,為了獲得大、中、小規模的樣本量,令試驗組與對照組效應差δ分別為0.05,0.08,0.20,則對應的Pt分別為0.25,0.28,0.40,采用 PASS11.0軟件計算相應的樣本量N分別為1094,447,82。設目標區樣本量占總樣本量的比例K分別為10%,30%,50%,調整后的檢驗水準 α′分別設為0.1,0.2,…,0.9。模擬研究包括以下三個部分:①當PtL=Pr,即PtL=0.20時計算并比較目標區的CFPR;②當PtL=Pt時計算并比較目標區CP;③當PtL略低于Pt,即目標區試驗組與對照組效應差δL為 δ的f倍(即 PtL=f×δ+Pr)時計算并比較目標區 CP,其中 f設為 0.5,0.6,0.7,0.8。
2.模擬步驟
(1)根據預先設定的參數,調用SAS均勻分布隨機函數RANUNI(seed)分別生成4個包含隨機數Xi(0~1)和指示變量 Yi(0,1)的數據集(i=1,2,3,4),分別代表目標區試驗組(Y1=1|X1≤PtL,Y1=0|X1>PtL)、對照組(Y2=1|X2≤Pr,Y2=0|X2>Pr)和非目標區試驗組(Y3=1|X3≤Pt,Y3=0|X3>Pt)、對照組(Y4=1|X4≤Pr,Y4=0|X4>Pr)的臨床試驗數據。
2)將4個數據集全部合并作為MRCT的模擬數據,進行兩樣本率組間比較的卡方檢驗,P≤0.05認為有統計學差異。
3)在步驟2)的卡方檢驗顯示P≤0.05且^Pt>^Pr的前提下,將目標區試驗組與對照組數據集合并作為目標區的模擬數據,進行兩樣本率組間比較的卡方檢驗,PL≤α′認為有統計學差異。
4)重復步驟1)~3),循環10000次,計算PL≤α′且^PtL>^PrL的例數nL占P≤0.05且^Pt>^Pr的例數n的百分比。
以上四個步驟基于PtL=Pr時計算目標區CFPR,基于Pr<PtL≤Pt時計算目標區CP。
模擬結果
模擬研究①:整體來看,假定PtL=Pr時,目標區的CFPR隨著總樣本量N、目標區樣本比例K和檢驗水準α′的增加而增加(圖1),且這一變化趨勢在大樣本的MRCT中趨于穩定。當檢驗水準α′不超過0.5時基本可以控制CFPR在50%左右。
模擬研究②:當PtL=Pt時,目標區的CP隨著目標區樣本比例K和檢驗水準α′的增加而增加,當α′較大時CP的增幅逐漸平緩,且這一變化趨勢在大樣本的MRCT中趨于穩定(圖2)。值得注意的是,當K固定時,目標區的CP相對穩定,尤其當K≥30%時,隨著α′的增加目標區CP幾乎不受總樣本量N的影響,且當α′不低于0.3時基本可以確保足夠的 CP(≥80%)。
考慮到目標區與非目標區之間人種的差異,研究藥物在目標區的療效與MRCT療效并不一定相等,基于模擬研究①和②,暫定α′為0.5,進一步研究目標區試驗組療效略低于MRCT試驗組療效時目標區CP情況。
模擬研究③:當 PtL=f×δ+Pr且 α′=0.5時,目標區的CP隨著f和K的增加而增加(表1),當K固定時,CP相對穩定,幾乎不受總樣本量的影響。相對K而言,f對CP的影響并不明顯。當K=30%、f=0.8時,基本可以確保足夠的CP(≥80%)。
目標區樣本比例K的確定
考慮到本研究模擬背景是在MRCT顯示優效的前提下目標區實際無效(概率為100%)時的CFPR、以及目標區實際優效(概率為100%)時的CP,這與現實顯然是不符的。此處給一個符合常理的假定:MRCT顯示優效的研究藥物中,有90%在目標區也是優效的,10%在目標區無效。記:試驗藥物在目標區無效;:試驗藥物在目標區優效;:MRCT試驗藥物無效;:MRCT試驗藥物優效。
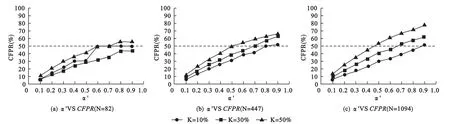
圖1 總樣本量N、目標區樣本比例K、檢驗水準α′與CFPR的變化關系
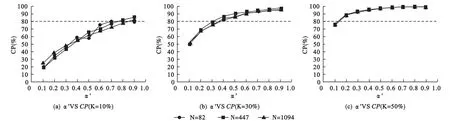
圖2 總樣本量N、目標區樣本比例K、檢驗水準α′與CP的變化關系
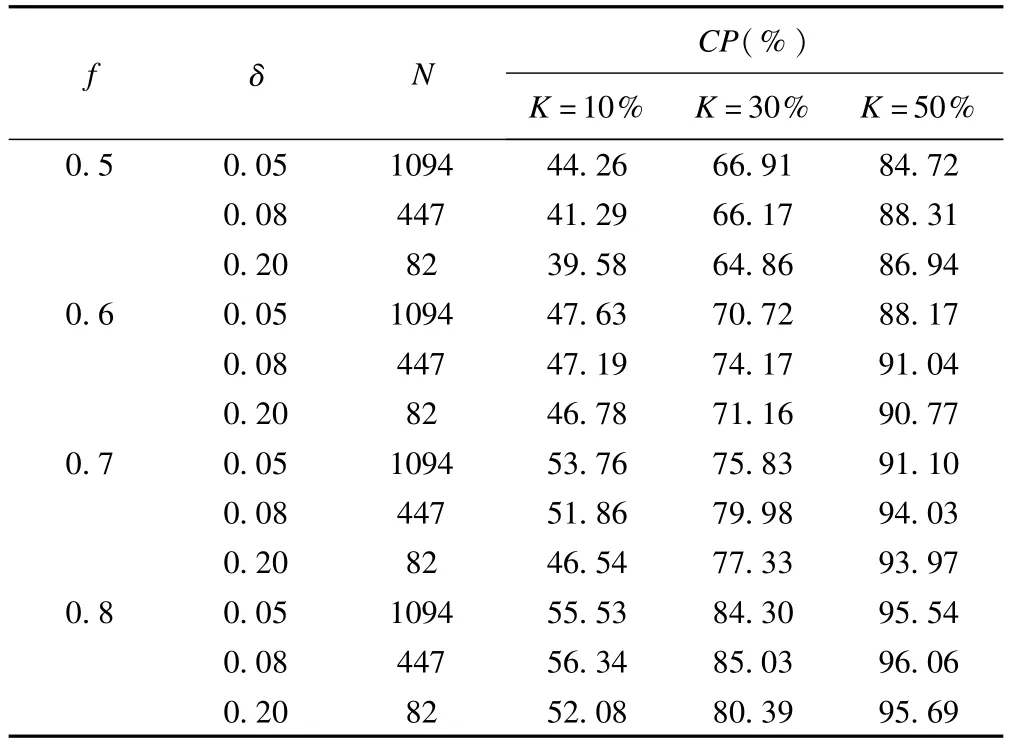
表1 目標區試驗組療效比MRCT試驗組療效略低時的CP(%)
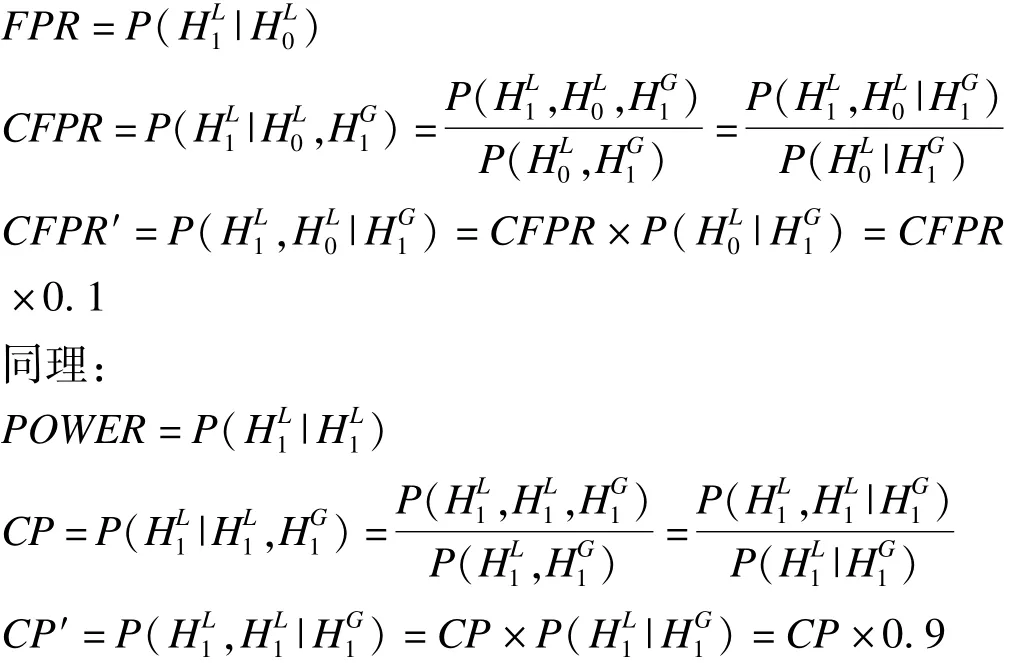
在α′=0.5的情況下,保證K在50%以內,基本可以控制 CFPR(<50%)和 CFPR′(<5%);當 K=10%時,即使 PtL=Pt,依然不能獲得預期的 CP(<70%)和CP′(<63%);當K=30%且 f≥0.8時,可以確保足夠的CP(≥80.4%)和CP′(≥72.4%);當K=30%時,不同f對應的目標區CFPR′以及CP′見表2。

表2 當K=30%時,不同f對應的目標區CFPR′以及CP′
此外,K=30%作為MRCT目標區的樣本比例,具有較好的理論解釋。根據兩樣本率組間比較卡方檢驗的樣本量計算公式[8](公式(1)),本研究 α=0.05,α′=0.5且 1-β=1-β′=0.8,分別計算樣本量后作兩者的比值(公式(2)),得到目標區樣本量占總樣本量的比例近似為30%,即目標區試驗組療效與MRCT的試驗組療效相等且K=30%時,在α′=0.5的檢驗水準下,有80%的檢驗效能能檢驗出目標區試驗組優于對照組且差別有統計學意義。
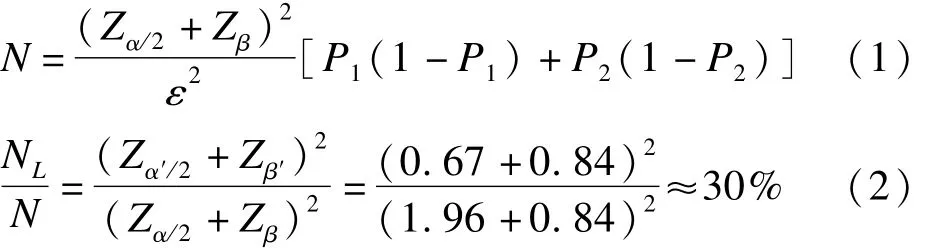
討 論
國際多中心臨床試驗為同步評價研究藥物對全球各地區患者的有效性、安全性提供了可能,然而,它也給各地區的藥物監管部門帶來了挑戰,即如何合理運用MRCT中局部區(例如目標區)的試驗數據來制定相關決策依據使得研究藥物在本地區能同步上市[9]。Chen等人同時研究了日本提出的方法一和局部區采用調整后檢驗水準α′的方法,給出了這兩種決策依據樣本量的計算以及它們之間關系[6]。然而,對于局部區的CFPR并未給出更好的控制建議和相關標準的具體意見。
本研究通過Monte Carlo模擬,在總的檢驗水準α=0.05的水平試驗組的療效優于對照組且差別有統計學意義的前提下,比較MRCT中目標區設置不同的α′對研究藥物在本地區的 CFPR、CFPR′、CP和 CP′的影響。研究發現①當α′≤0.5時能夠有效地控制CFPR′在0.05以內;②當K≥30%時,若目標區試驗藥物療效與MRCT的療效相當,設置α′≥0.3可以確保目標區足夠的CP(≥80%);③當K≥30%且設置α′=0.5時,即使目標區試驗藥物療效略低于MRCT的療效即f≥0.8,也可以確保目標區足夠的CP和CP′(≥80%)。
綜上,建議MRCT在方案設計時目標區的樣本比例不應低于30%、檢驗水平不能超過0.5。該標準適用于目標區試驗藥物療效略低于MRCT的療效即f≥0.8的情形,若估計目標區試驗藥物療效與MRCT的療效相當,檢驗水平可適當降低,但不建議低于0.3。若估計目標區試驗藥物療效遠低于MRCT的療效,例如f<0.8,應適當增大目標區的樣本比例,例如K>50%,然而一般情況下這一比例并不切實際。
[1]Liu JP,Chow SC.Bridging studies in clinical development.J Biopharm Stat,2002,12(3):359-367.
[2]International Conference on Harmonisation;guidance on ethnic factors in the acceptability of foreign clinical data;availability-FDA.Notice.Fed Regist,1998,63(111):31790-31796.
[3]Ando Y,Hamasaki T.Practical issues and lessons learned from multiregional clinical trials via case examples:a Japanese perspective.Pharm Stat,2010,9(3):190-200.
[4] Ministry Of Health LAWO and Japan,Basic Principles on Global Clinical Trials.2007.
[5]Quan H,et al.Sample size considerations for Japanese patients in a multi-regional trial based on MHLW guidance.Pharm Stat,2010,9(2):100-112.
[6]Chen X,et al.Decision rules and associated sample size planning for regional approval utilizing multiregional clinical trials.J Biopharm Stat,2012,22(5):1001-118.
[7]Huang Q,et al.Design and sample size considerations for simultaneous global drug development program.JBiopharm Stat,2012,22(5):1060-1073.
[8]Shein-Chung Chow.Sample Size Calculations in Clinical Research.Second Edition.2008,Chapman&Hall/CRC.
[9]Shih WJ.Clinical trials for drug registrations in Asian-Pacific countries:proposal for a new paradigm from a statistical perspective.Control Clin Trials,2001,22(4):357-366.
A Bridging Method Based onαAdjustment to Evaluate the Effectiveness of MRCT in Target Region for Dichotomous Endpoint
Yu Chengkai,Wang Lin,Qi Yangyang,et al
(Department of Health Statistics,Faculty of Preventive Medicine,Fourth Military Medical University(710032),Xi′an)
Objective To explore the feasibility of adopting rational adjusted significance level as the decision rule in the target region in MRCT and make reference for evaluating new drug application of MRCT in target region.Methods By Monte Carlo simulation,we studied the conditional false positive rate(CFPR)and conditional test power(CP)changing with the proportions of the sample size in target region by adopting different significance levels given that the treatment effect is shown to be significant under the significance levelα=0.05 based on overall MRCT data for dichotomous data.Results The CFPR and CP are increasing with the significance levelα′and the ratio of sample size K increasing in target region.When the significance levelα′=0.5 the CFPR and CFPR′can be controlled under the 50%and 5%in basic.When the ratio of sample size is fixed,the CP in target region is relatively stable and can′t be influenced by the sample size of local region.Especially when K≥30%,the CP in target region is almost not affected by the total sample size.Whenα′isn′t lower than 0.3,we can ensure enough CP(≥80%).Conclusion When protocol is designed,it is advisable that the ratio of sample size K shouldn′t be less than 30%.The significance levelα′in target region shouldn′t exceed 0.5.The decisional rule is suitable for the difference between the trial and the control group in target region is more than 0.8 times the difference in MRCT.If the estimated treatment effect of the drug in target region is almost like it in MRCT,the significance level can be lower,however,less than 0.3 is not recommended.
Conditional false positive rate;Conditional test power;Multi-regional clinical trial;Monte Carlo simulation
*:國家自然科學基金資助(項目編號:81273176,81302509,81473069)
△通信作者:夏結來,E-mail:jielaixia@yahoo.com;王陵,E-mail:wl.medstat@gmail.com
郭海強)

