機械張力與心律失常
顧春英 李藝
機械張力與心律失常
顧春英 李藝
心臟電活動紊亂是發生心律失常的本質原因,在諸多導致心臟電活動異常的因素中,機械張力所致的心律失常與臨床密切相關,逐漸引起越來越多的重視。經研究證實,機械電反饋異常為心律失常的重要發生機制之一。本文就機械性心律失常的細胞電生理機制與臨床進展進行闡述。
機械性心律失常;機械電反饋;張力性鉀離子通道
在競技運動場上,當運動員心前區受到撞擊時,會突然發生死亡。大家通常認為是心臟受到外傷所致,但這部分患者尸檢證實心臟完好無損。那么他們的死亡原因是什么呢?
我們先來回顧一下,早在1920年,外國學者Schott曾使用胸部錘擊成功救治一例阿斯綜合征患者[1]。直到現在,心前叩擊法在臨床上一直被沿用。臨床觀察證實,心前叩擊可以使部分快速室性心律失常恢復竇律。也就是說,外力可以使心臟電活動發生改變。
1 機械性心律失常的概念
心臟存在電活動和機械活動兩種功能。電活動在前,機械活動在后;電活動引領著機械收縮,稱為興奮-收縮偶聯,其中的機制已經被研究的比較清楚。同樣,機械收縮也將影響、調控電活動,稱為機械-電反饋。如果這個反饋作用過強,將使得心臟電活動的節律、頻率發生紊亂,稱為機械性心律失常。接下來討論機械活動如何對電活動產生影響。
首先我們來看一個實驗研究。研究對象是豬,工具為心前區撞擊的裝置,撞擊時同步記錄心電圖。研究者采用三個時間點啟動撞擊,分別為QRS波群、ST段以及T波所對應的時間點,并同步記錄心電圖。隨后研究者發現,如果在QRS波群發生時同步撞擊心前區,會引起撞擊后心搏的ST段抬高(90%)、房室阻滯(40%)、左束支阻滯(90%),見圖1、圖2。如果與ST段同步撞擊心前區,則會引起ST段抬高(80%)、左束支阻滯(40%)。而如果在T波發生時(易損期)同步撞擊,將會引起室速、室顫(90%),見圖3。

圖1 QRS波群同步撞擊所致一過性高度房室阻滯、室內阻滯以及ST-T改變
Fig.1 Transient high degree atrioventricular block,intra-ventricular block and ST-T changes resulting fromsynchronous impact by QRS complex
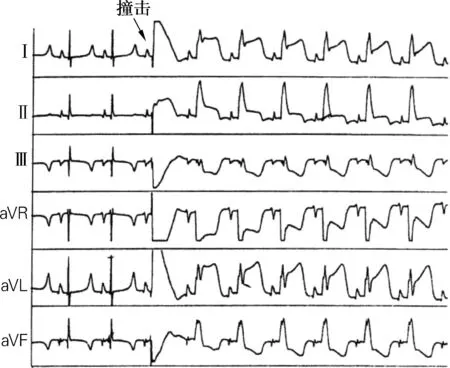
圖2 QRS波群同步撞擊所致ST段抬高
Fig.2 ST segment elevation resulting from synchronous impact by QRS complex

圖3 T波易損期同步撞擊所致室顫
2 機械性心律失常的發生機制
基礎研究證實,當心肌細胞受到張力時,出現鉀電流的增強。隨后研究者預先使用鉀通道阻滯劑阻斷鉀通道,并重復實驗,發現此時ST段未見抬高(圖4)。因此證實,心前區撞擊后ST段抬高與復極過程中鉀電流增強有關。后來進一步研究證實心肌細胞膜上存在張力敏感性鉀離子通道。該通道的特點是,受到張力時開放,使鉀離子外流增加,心肌復極時限縮短。所以心臟受到撞擊時出現鉀電流增強,復極加快。并且著力部位受到張力越大,鉀電流越強,復極越快。而同樣是遭受撞擊,心外膜心肌張力改變較內膜更為明顯,復極加快程度更大,故在二相復極期形成跨壁電位差——電流從高電位向低電位傳導,即由內膜向外膜傳導,該方向指向體表記錄電極,所以記錄到ST段的抬高(圖5)。這就是心前區撞擊后ST段抬高的發生機制。
關于QRS波群同步、ST段同步撞擊后新發傳導/束支阻滯的機制目前還不清楚。我們可以通過撞擊后QRS波明顯增寬的現象推測可能是撞擊后鈉通道出現異常,使得除極時鈉離子內流減少,引起0相除極速率及幅度減低,導致房室或室內傳導延遲,但尚無試驗依據。有待于基礎研究進一步證實(圖1、2、4)。通過這一實驗結果,推測機械外力導致患者猝死可能機制:① T波同步撞擊,即發生在易損期的撞擊,可直接誘發室速室顫;② 撞擊引起緩慢性的心律失常;③ 撞擊使得心外膜鉀電流明顯增強致二相丟失,發生二相折返,引起的RonT室早、多形性室速、室顫。我們引用一個典型案例來加深對于上述機制的理解:一名14歲小男孩踢足球時心前區被撞擊,發生猝死。所幸搶救及時,除顫3次后恢復竇律,心電圖證實ST段抬高。這個病例完全揭示全過程。

圖4 阻斷鉀通道后撞擊 ST段未見明顯抬高

圖5 心前區撞擊后ST段抬高機制
上述所闡述的內容是瞬時機械外力對心臟的影響。而臨床上,各種原因引起心肌張力升高所致的機械性心律失常并不少見。舉例說明。
首先,在一些腔內介入手術中,當具有一定張力的導管或電極接觸心室壁時,常伴有室性早搏出現;導管后撤脫離心室壁,早搏消失。這就是一個典型的機械牽張引起的心律失常。其次,二尖瓣脫垂患者,心臟收縮中晚期二尖瓣脫入左房,腱索和乳頭肌拉力達到最大,故此類患者室性早搏常發生在收縮晚期,心電圖表現為室早落在T波降支終末或緊隨T波之后。二尖瓣前葉脫垂,室早起源前乳頭肌,同理后葉脫垂室早起源后乳頭肌。從某種程度上而言,我們可以通過心電圖室早形態,大致估測脫垂瓣葉。臨床上假腱索也是一種常見的心臟解剖學異常,由于機械牽拉引發早搏。左室假腱索,其室早大多起源于左室,而右室假腱索室早則多起源于右室(圖6)。
接下來討論一下室壁瘤致心律失常機制。室壁瘤瘤體附近心肌由正常心肌、過渡帶心肌和壞死心肌組成,三者在心室收縮時所受張力不同。前文已提及,心肌張力越大,鉀電流越大,復極時間越短,即不應期越短,故在三種不同張力心肌上形成不應期的離散,易誘發心律失常。因此,引起室壁瘤死亡的惡性心律失常很大一部分與機械牽張相關。進一步引申,當心肌缺血時,心臟彩超常提示節段性室壁運動異常。心肌運動不同步,張力不均一,引起不應期離散,同樣容易誘發惡性心律失常。需引起大家重視。
我們再談談房顫。房顫發生的原因很多,其中心房壓力增高是重要因素,如二尖瓣狹窄等。臨床上減輕心房負荷治療后,部分房顫可自行轉復。有學者做了實驗研究,在房顫發作時心房壓是10 cmH2O,使用利尿劑后,隨著房壓減輕,F波的頻率變慢,房顫終止(圖7)。這提示心房顫動的發生與維持,與心房負荷密切相關。心房壓高的時候,心房肌張力升高,心肌細胞鉀電流增強,心房不應期縮短。而不應期越短,越容易誘發房顫,且越易維持房顫;當房壓下降,鉀電流減小,不應期延長,折返容易終止,故房顫可自行復律。通過房顫的發生和治療的過程,我們不難看出心房壓是房顫發生和維持的重要機制之一。
最后我們關注下慢性心衰。慢性心衰幾乎全部合并有心律失常[2]。經過幾代人努力,至今苦無良策。我們嘗試從慢性心衰發生心律失常的機制入手,結合前文提到的機械性心律失常的發生機制,或有啟發。一項基礎研究表明,心室舒張末壓(容量負荷)增加到一定程度時,將引發室性心律失常。同時,另一項試驗研究表明,在心腔內一次性注射30 mL液體,可引發一次室性早搏,該試驗說明心臟壓力在短期內迅速增加時,將引起心律失常的發生。這些心律失常的具體機制是什么?再看一個基礎研究,研究者把自律細胞分離出來作為研究對象,并給予機械牽張。發現受到機械牽張的細胞自律性增強。當心肌細胞受到持續牽張,細胞內發生鈣超載,而鈣超載可通過觸發等機制引起心律失常。同樣,折返也是心律失常的常見機制——不同張力心肌所致的不應期離散,為折返的發生創造了條件。慢性心衰時,機械牽張將通過以上機制導致心律失常,因此有學者進行如下研究:對于牽張性心律失常,給予β受體阻滯劑降低室壁張力,結果心律失常明顯減少。同時反向研究表明,給予心衰患者多巴酚丁胺,增加心肌收縮力,結果增加心律失常發生率。有關正性肌力藥物,一言概括,即心衰患者使用正性肌力藥物,目的是增加心肌收縮力,其結果卻是以誘發心律失常為代價而告終。2016年歐洲心衰指南指出:“出于安全考慮,不主張在心衰患者中使用正性肌力藥物,除非合并低血壓或灌注不足時”[3],此時挽救生命的決策優先于預后。

圖6 二尖瓣脫垂、心室假腱索合并室早起源與病變部位一致
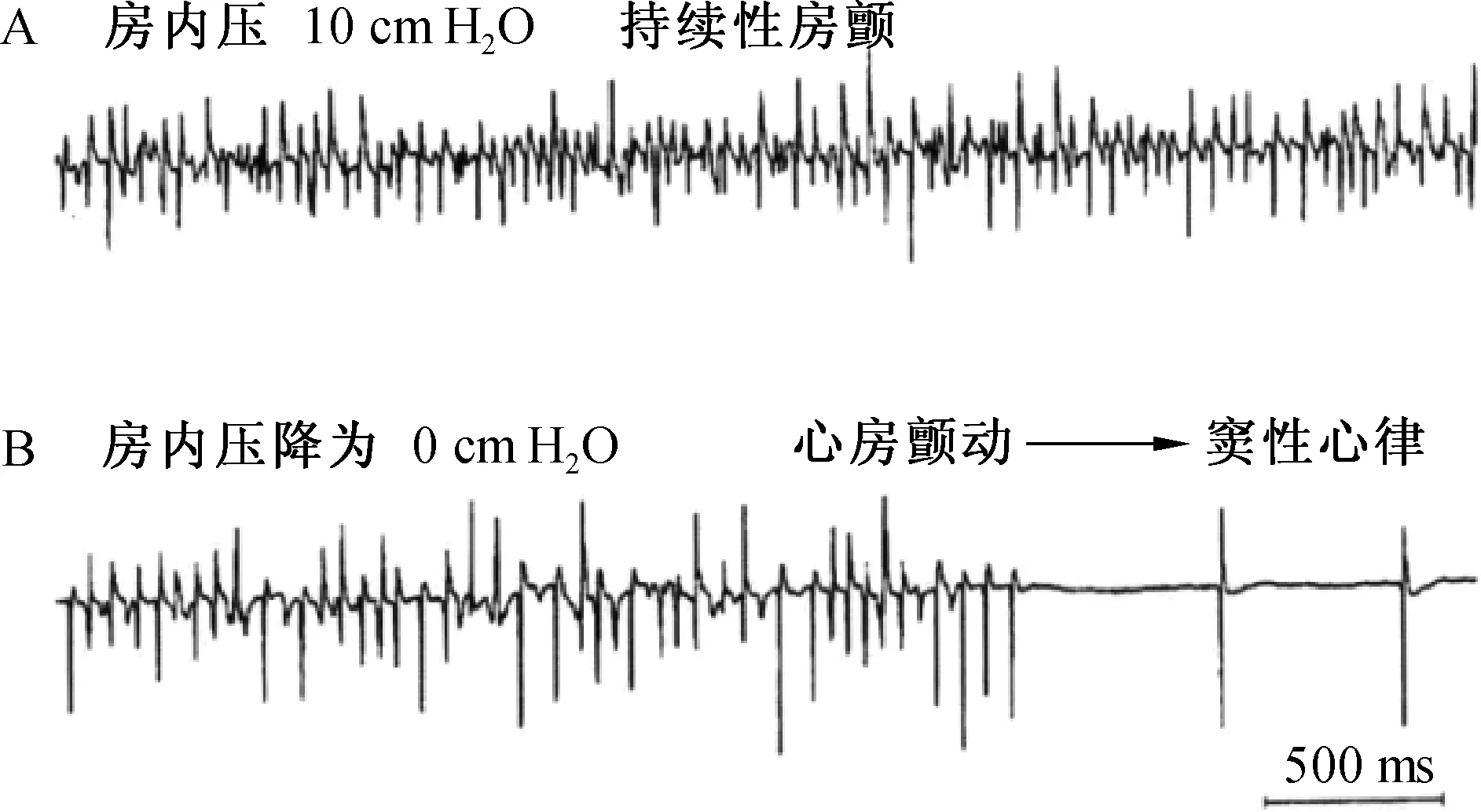
圖7 房內壓與心房顫動發作關系
3 機械性心律失常的治療
降低張力是機械性心律失常的主要治療方法,并且通過改善心肌重構,糾正收縮時的不均一性。首先,β受體阻滯劑是慢性心衰治療中的基石,在其他器質性心臟病治療方面,β受體阻滯劑也可有效降低死亡率,其中降低心肌機械張力是不可忽視的機制之一。其次是RAS系統阻滯劑,目的同樣是通過改善重構,減少心臟的機械異質性,降低張力,從根本上減少心衰患者的心律失常。
綜上所述, 機械性心律失常的發生是通過機械張力激活心肌細胞膜上的張力敏感通道, 那么針對該通道的特異性阻滯劑是抗心律失常治療上的新思路。最新研究表明,在狼蛛毒液中分離出的多肽具有選擇性抑制張力敏感通道的作用,可減少心衰房顫的發生率[4-5]。更多的張力通道阻滯劑尚在研究中。通過以上分析,我們不難得出結論:張力敏感性阻滯劑將來很可能成為新一類有效的抗心律失常藥物,特別對器質性心臟病、慢性心衰、房顫患者的治療將帶來新的希望。
[1] 郭繼鴻. 機械性心律失常[J]. 臨床心電學雜志, 2008,17(3):214-226.
[2] 蔣文平. 盡力治療心力衰竭的心律失常[J]. 中國心臟起搏與心電生理雜志,2009,23(6): 471-472.
[3] Ponikowski P,Voors AA,Anker SD,et al. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC)Developed with the special contribution of the Heart Failure Association (HFA) of the ESC[J].Eur Heart J,2016 ,37(27):2129-2200.
[4] Kohl P,Sachs F,Franz MR. Cardiac mechano-electric feedback and arrhythmias[M]. Philadephia:Elsevier Inc, 2005:4-30.
[5] Ravens U, Mechano-electric feedback and arrhythmias[J]. Prog Biophys Mol Biol,2003,82:255-266.
(本文編輯:郭欣)
Mechanical tension and arrhythmias
GuChun-ying1,LiYi2
(1. Department of Cardiac Function, Tianjin Fifth Central Hospital, Tianjin 300450;2. Department of Cardiac Function, the Central Hospital of Wuhan, Wuhan Hubei 430014, China)
The disorder of cardiac electrical activity is the essencial cause of arrhythmia. Among all the influential factors resulting in abnormalities of cardiac electrical activity, mechanical tension is an important one. Mechanical-tension-related arrhythmia is closely associated with clinical practice, and arises more and more attention gradually. It is verified by research that abnormal mechano-electrical feedback is one of the important mechanisms of arrhythmia. This paper elaborates the cellular electrophysiological mechanism of mechanical arrhythmia and research progress.[Key words] mechanical arrhythmia; mechano-electrical feedback; tension potassium ion channel
300450天津,天津市第五中心醫院心功能科(顧春英);430014 湖北 武漢,武漢市中心醫院心功能科(李藝)
顧春英,教授,主要從事復雜心律失常電生理機制的相關研究,E-mail:781269715@qq.com
R540.4
A
2095-9354(2017)01-0006-04
10.13308/j.issn.2095-9354.2017.01.002
2016-10-25)

