辣椒提取液對亞硝酸鹽清除作用的探究
丁城,劉璐,李桀驁,汪超*
(1.湖北工業大學 生物工程與食品學院,武漢 430000;2.工業發酵湖北省協同創新中心,武漢 430068;3.湖北省食品發酵工程技術研究中心,武漢 430068)
辣椒提取液對亞硝酸鹽清除作用的探究
丁城1,2,3,劉璐1,2,3,李桀驁1,2,3,汪超1,2,3*
(1.湖北工業大學 生物工程與食品學院,武漢 430000;2.工業發酵湖北省協同創新中心,武漢 430068;3.湖北省食品發酵工程技術研究中心,武漢 430068)
實驗目的是探究辣椒提取液對亞硝酸鹽的清除作用,試驗中探究了有機酸種類、有機酸添加量、水浴時間、有機酸濃度和提取溫度對亞硝酸鹽的清除作用。通過正交實驗得到最佳提取條件,結果為草酸2%,水浴時間30 min,提取溫度60 ℃和草酸添加量50 mL。在上述實驗條件下,得到辣椒提取液對亞硝酸鹽清除率達到98.6%。
辣椒;亞硝酸鹽;有機酸;清除率
在我國辣椒被廣泛種植,特別是在四川、湖南和湖北等地[1]。辣椒含有大量的辣椒堿、辣椒紅素、胡蘿卜素,以及維生素C等活性成分[2]。同時,辣椒具有許多生理活性,例如:減肥[3]、抗氧化、抑菌消炎[4]、預防胃潰瘍[5]等活性功能。因此,辣椒不僅是重要的調味品,而且在其他領域有著重要的研究。
亞硝酸鹽不僅存在于許多食品中,而且被作為食品添加劑廣泛使用[6],但是亞硝酸鹽存在嚴重的食品安全隱患。亞硝酸鹽進入人體,在一定條件下會與胺類物質結合,生成亞硝胺。研究表明:亞硝胺是一種強致癌物質。同時,短時間大量食用含有亞硝酸鹽的食品,會導致血紅細胞失去攜氧的功能,最終會導致人體缺氧[7]。
目前,對亞硝酸鹽的清除已有大量的研究,但是辣椒對亞硝酸鹽清除效果的研究尚未見報道。本文以辣椒為研究對象,用不同有機酸作為提取劑,探索最佳提取條件,為食品安全進一步提供相關理論依據。
1 實驗方法
1.1 材料
1.1.1 實驗材料
干紅辣椒:采購于武漢市武昌區某集貿市場。
1.1.2 實驗試劑
草酸、檸檬酸、乳酸、酒石酸、乙酸、對氨基苯磺酸、鹽酸萘乙二胺、亞硝酸鈉等試劑,均為分析純。
1.1.3 實驗儀器
UV-1800紫外可見分光光度計 日本島津有限公司;HK-10B粉碎機 廣東旭朗機械有限公司;HH-6型數顯恒溫水浴鍋 國華電器有限公司;KQ-500DV超聲清洗儀 昆山市超聲儀器有限公司。
1.2 辣椒提取液的制備
將干紅辣椒用粉碎機粉碎,用有機酸作為提取劑,置于50 ℃恒溫水浴30 min,然后置于超聲儀10 min,過濾,收集濾液備用。
1.3 辣椒提取液對亞硝酸鹽清除的測定
準確吸取2 mL亞硝酸鹽溶液(6 μg/mL),置于50 mL容量瓶中,然后加入10 mL辣椒提取液,搖勻,放置30 min,加入2 mL對氨基苯磺酸,搖勻,避光反應3 min,再加入1 mL鹽酸萘乙二胺,搖勻,避光反應15 min。然后定容至刻度線,在538 nm處測定吸光值,同時做空白對照。亞硝酸鹽清除率計算公式:
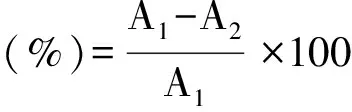
式中:A1為未加入辣椒提取液測定的吸光值;A2為加入辣椒提取液測定的吸光值。
1.4 最佳有機酸的確定
按照1.2的提取方法,準確稱取5份干紅辣椒粉(5 g),分別用100 mL檸檬酸、草酸、乙酸、酒石酸和乳酸混勻,置于50 ℃恒溫水浴30 min,然后置于超聲儀10 min,得到的辣椒提取液再與2 mL亞硝酸鹽溶液(6 μg/mL)反應,分別測定不同有機酸的亞硝酸鹽清除率。
1.5 有機酸的濃度對亞硝酸鹽清除率的影響
按照1.2的提取方法,分別用濃度為1%,2%,3%,4%,5%,6%,7%的 有機酸(1.4確定的最佳有機酸)作為提取劑,50 ℃恒溫水浴30 min,然后置于超聲儀10 min,再與2 mL亞硝酸鹽溶液(6 μg/mL)反應,分別測定不同濃度有機酸對亞硝酸鹽的清除率。
1.6 水浴時間對亞硝酸鹽清除率的影響
按照1.2的提取方法,用1.4確定的最佳有機酸作為提取劑,50 ℃恒溫水浴,水浴時間分別為10,20,30,40,50,60,70 min,然后置于超聲儀10 min,再與2 mL亞硝酸鹽溶液(6 μg/mL)反應,分別測定不同水浴時間對亞硝酸鹽的清除率。
1.7 提取溫度對亞硝酸鹽清除率的影響
按照1.2的提取方法,用1.4確定的最佳有機酸作為提取劑,稱取7份干紅辣椒粉(5 g),然后用100 mL酸混勻,再分別用20,30,40,50,60,70 ℃恒溫水浴,水浴時間為30 min,然后置于超聲儀10 min,再與2 mL亞硝酸鹽溶液(6 μg/mL)反應,分別測定不同提取溫度對亞硝酸鹽的清除率。
1.8 有機酸添加量對亞硝酸鹽清除率的影響
按照1.2的提取方法,用1.4確定的最佳有機酸作為提取劑,稱取5份干紅辣椒粉(5 g)分別為100,200,300,400,500 mL酸混勻,50 ℃恒溫水浴,水浴時間為30 min,然后置于超聲儀10 min,再與2 mL亞硝酸鹽溶液(6 μg/mL)反應,分別測定不同有機酸添加量對亞硝酸鹽的清除率。
1.9 正交實驗
通過單因素實驗分析,在此基礎上進行正交實驗,確定最佳提取條件。
2 結果與分析
2.1 有機酸的確定
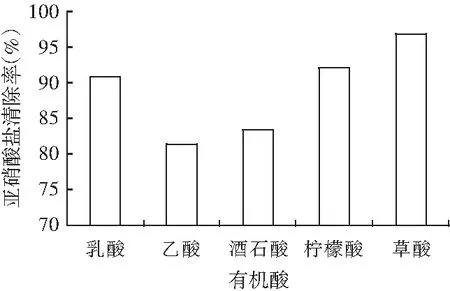
圖1 有機酸對亞硝酸鹽清除率的影響
由圖1可知,亞硝酸鹽的清除率受到有機酸種類的影響。乳酸、乙酸、酒石酸、檸檬酸和草酸對亞硝酸鹽的清除率分別為90.7%,81.4%,83.3%,91.8%,96.7%。5種酸相比較,草酸提取得到的辣椒提取液對亞硝酸鹽的清除率最高。因此,在5種有機酸中,用草酸作為提取劑,效果最佳。
2.2 有機酸的濃度對亞硝酸鹽清除率的影響
用草酸作為提取劑,探討濃度為1%,2%,3%,4%,5%,6%,7%的草酸提取得到辣椒提取液對亞硝酸鹽清除率的影響。
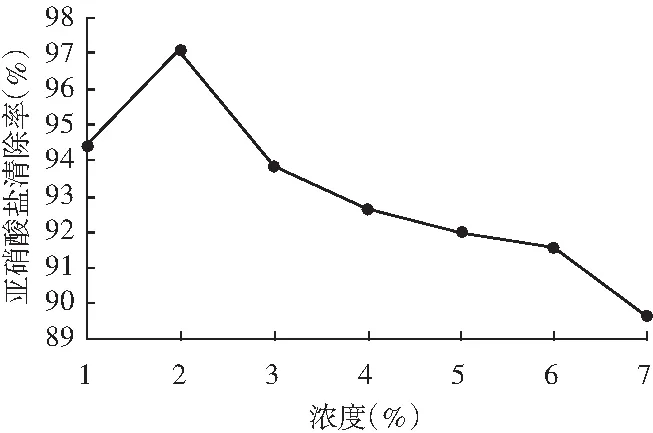
圖2 草酸濃度對亞硝酸鹽清除率的影響
由圖2可知,隨著草酸濃度的增加,辣椒提取液對亞硝酸鹽的清除率降低。用2%的草酸提取時,得到的清除率最高,為97.1%。在草酸濃度為3%時,辣椒提取液對亞硝酸鹽清除率下降的原因可能是草酸濃度的升高,導致辣椒的一些活性物質失去活性。
2.3 水浴時間對亞硝酸鹽清除率的影響
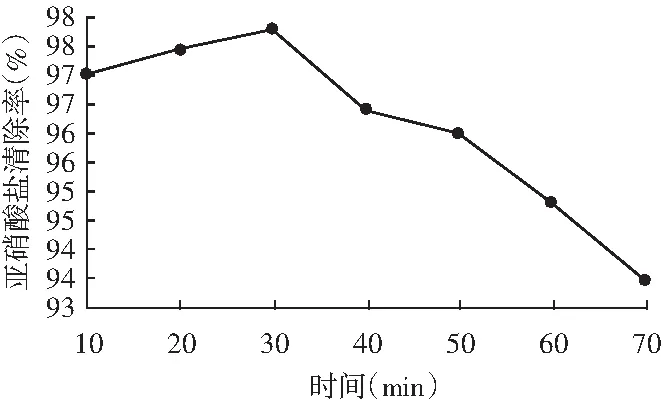
圖3 水浴時間對亞硝酸鹽清除率的影響
由圖3可知,在30 min前,隨著時間的增加,辣椒提取液對亞硝酸鹽的清除率平穩升高。但是在30 min以后,隨著水浴時間增加,清除率快速下降。30 min時,辣椒提取液對亞硝酸鹽清除率達到最大,為97.8%。因此,最佳水浴時間為30 min。
2.4 提取溫度對亞硝酸鹽清除率的影響
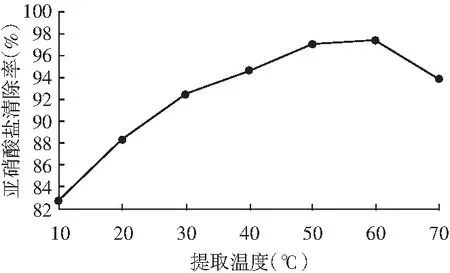
圖4 提取溫度對亞硝酸鹽清除率的影響
由圖4可知,隨著溫度升高,辣椒提取液對亞硝酸鹽清除率先升高再下降。50~60 ℃時,提取溫度對亞硝酸鹽清除率影響很小。因此,提取溫度在這個范圍內,亞硝酸鹽清除率最佳。但是溫度過高,清除率反而下降,產生這種現象的原因可能是一些抗氧化特性的物質與清除亞硝酸鹽有著密切聯系[8],溫度過高導致辣椒提取液中一些具有抗氧化性的物質遭到破壞,例如:辣椒紅素、維生素C、生物堿和多酚等物質,從而導致清除率下降。
2.5 有機酸添加量對亞硝酸鹽清除率的影響
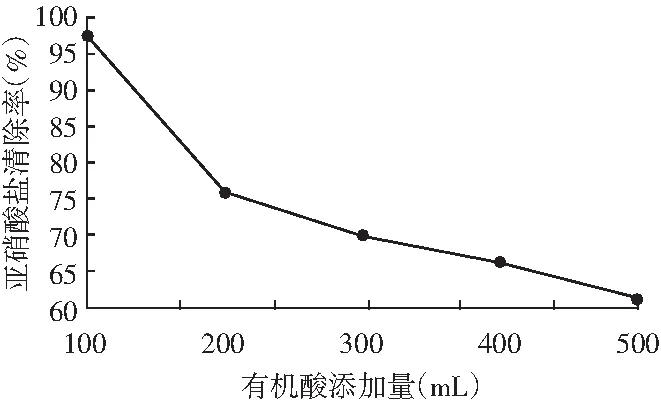
圖5 有機酸添加量對亞硝酸鹽清除率的影響
由圖5可知,隨著提取劑的添加量增大,辣椒提取液對亞硝酸鹽的清除率下降較快。在有機酸添加量為100 mL時,亞硝酸鹽清除率達到最大,為97.5%。導致這一現象的原因可能是提取時添加量過大導致具有清除亞硝酸鹽的物質濃度下降,因此,亞硝酸鹽清除率降低。所以在辣椒提取液提取時,有機酸最佳用量為100 mL。
2.6 正交實驗
在單因素實驗基礎上,設計有機酸濃度、水浴時間、提取溫度和有機酸添加量四因素三水平L9(34)的正交實驗,各個單因素水平見表1,正交實驗結果見表2。

表1 正交實驗因素水平
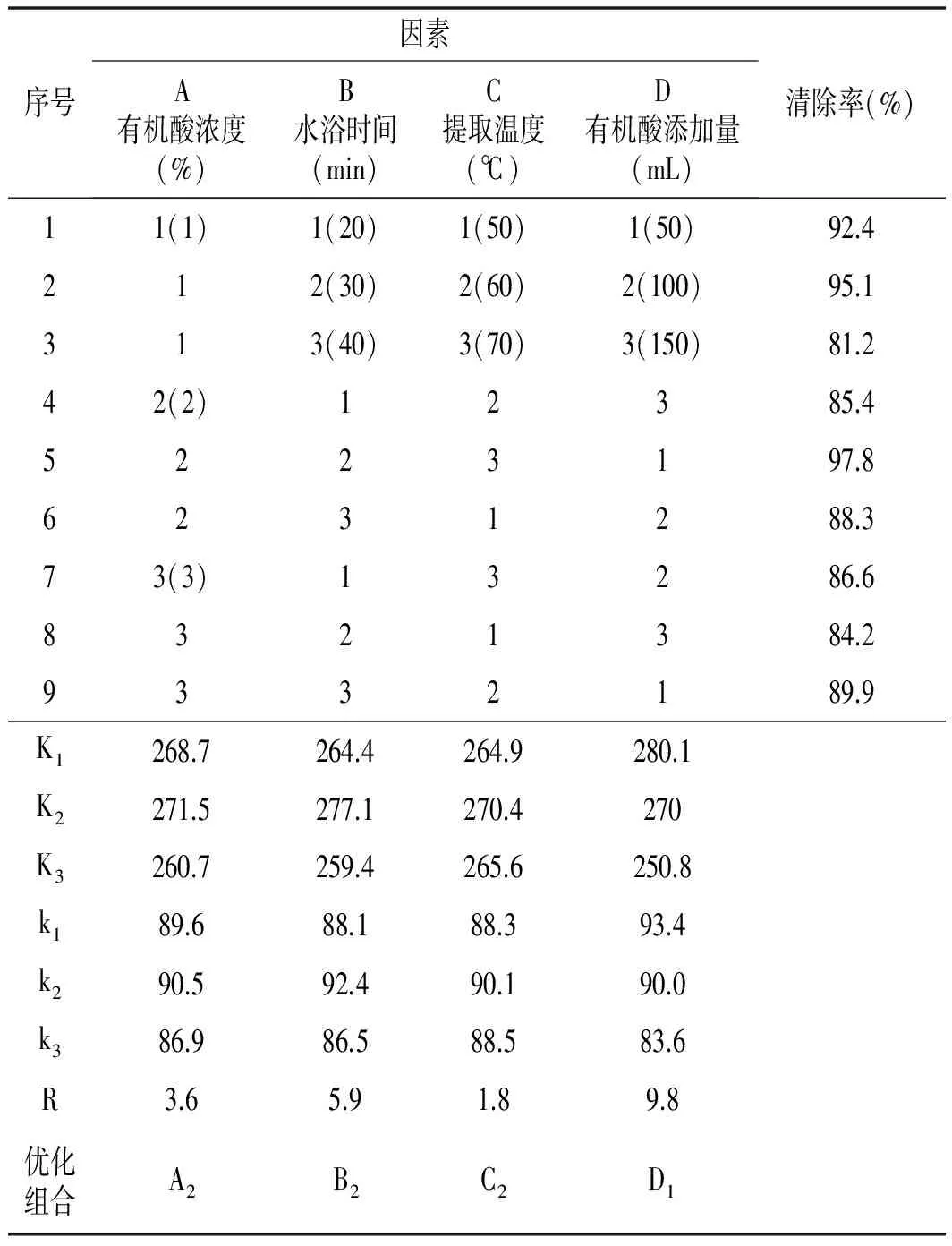
表2 正交實驗結果
由表2可知,影響辣椒提取液對亞硝酸鹽清除率的因素大小為有機酸添加量>水浴時間>有機酸濃度>提取溫度。同時由正交實驗結果可知,辣椒提取液對亞硝酸鹽清除率的最佳提取條件為A2B2C2D1,即草酸濃度為2%,水浴時間為30 min,提取溫度為60 ℃和草酸添加量為50 mL。在上述實驗條件下,進一步實驗得到辣椒提取液對亞硝酸鹽清除率達到98.6%。
3 結論
實驗結果表明辣椒提取液對清除亞硝酸鹽有明顯的效果。亞硝酸鹽是前體致癌物,在人體中能形成強致癌物質——亞硝胺[9]。因此,在食品中添加辣椒提取液,可以減少亞硝酸鹽,從而減少亞硝胺的形成。
本實驗中,探討了有機酸的種類、有機酸添加量、水浴時間、有機酸濃度和提取溫度對亞硝酸鹽清除率的影響。在此基礎上進行了正交實驗,實驗表明:辣椒提取液對亞硝酸鹽清除率的最佳提取條件為草酸濃度2%,水浴時間30 min,提取溫度60 ℃和草酸添加量50 mL,在此條件下,得到辣椒提取液對亞硝酸鹽清除率達到98.6%。
亞硝酸鹽利用范圍廣泛,特別是在腌制食品中,但是其危害不容忽視。本實驗為更深入利用辣椒,減少食品中的亞硝酸鹽,提高食品安全提供了新依據。
[1]丁青艾,伍后勝.養生保健大辭典[M].北京:科學技術文獻出版社,1997:702.
[2]李軍明.辣椒的營養保健價值[J].中國食物與營養,2010(2):68-71.
[3]Yoshioka M,Imanaga M,Ueyama H,et al.Maximum tolerable dose of red pepper decreases fat intake independently of spicy sensation in the mouth[J].The British Journal of Nutrition,2004,91(6):991-995.
[4]Materska M,Perucka I.Antioxidant activity of the main phenolic compounds isolated from hot pepper fruit (CapsicumannuumL.)[J].Journal of Agricultural and Food Chemistry,2005,53(5):1750-1756.
[5]Limlomwongse L,Chaitauchawong C,Tongyai S.Effect of capsaicin on gastric acid secretion and mucosal blood flow in the rat[J]. J. Nutr.,1979,109:773-777.
[6]徐專紅.食物中的硝酸鹽和亞硝酸鹽與人體健康[J].食品科技,1999(4):53-55.
[7]黃建蓉,王志江,徐金瑞,等.香辛料對亞硝酸鈉的清除作用[J].食品科技,2012(9):274-276.
[8]Van Acker S A.Structural aspects of antioxidant activity of flavonoids[J].Free Radical Biology and Medicine,1996,20(3):331-342.
[9]張平,葉文慧,石志華.姜汁對亞硝酸鹽清除作用的研究[J].黑龍江八一農墾大學學報,2005,17(4):73-75.
Study on the Nitrite Scavenging Activity of Pepper Extract
DING Cheng1,2,3, LIU Lu1,2,3, LI Jie-ao1,2,3, WANG Chao1,2,3*
(1.Bioengineering and Food College, Hubei University of Technology, Wuhan 430000, China;2.Research Center of Food Fermentation Engineering and Technology of Hubei,Wuhan 430068,China;3.Hubei University of Technology,Wuhan 430068,China)
Investigate the effect of pepper extract on nitrite scavenging activity, the effect of kinds of organic acids, additive amount of organic acids, water bath time, content of organic acids, and extraction temperature on nitrite scavenging activity. The optimal extraction conditions are obtained through the orthogonal experiments; the results are oxalic acid of 2%, water bath time of 30 min, extraction temperature of 60 ℃ and oxalic acid additive amount of 50 mL. Under the optimal conditions, the nitrite scavenging rate of pepper extract reaches 98.6%.
pepper;nitrite;organic acid;scavenging rate
2016-07-12 *通訊作者
丁城(1991-),男,湖北武漢人,碩士,研究方向:食品發酵與分子生物學; 劉璐(1992-),女,湖北宜昌人,碩士,研究方向:食品發酵; 李桀驁(1991-),男,湖北荊州人,碩士,研究方向:食品發酵; 汪超(1978-),男,湖北武漢人,教授,博士,研究方向:食品發酵技術、食品加工工藝和天然產物分離與構效。
TS202.3
A
10.3969/j.issn.1000-9973.2017.01.001
1000-9973(2017)01-0001-04

