超聲造影在肝癌介入干預(yù)效果評(píng)價(jià)中的應(yīng)用價(jià)值研究
雒大健,張志勇,楊 桃,李 歐,韓 越
(1.巴中市中心醫(yī)院 超聲科,四川 巴中636000;2.巴中市中心醫(yī)院 肝膽外科,四川 巴中636000;3.柳州市工人醫(yī)院,廣西 柳州545005)
超聲造影在肝癌介入干預(yù)效果評(píng)價(jià)中的應(yīng)用價(jià)值研究
雒大健1,張志勇2,楊 桃1,李 歐2,韓 越3
(1.巴中市中心醫(yī)院 超聲科,四川 巴中636000;2.巴中市中心醫(yī)院 肝膽外科,四川 巴中636000;3.柳州市工人醫(yī)院,廣西 柳州545005)
目的 探討超聲造影在肝癌介入治療療效評(píng)價(jià)中的應(yīng)用價(jià)值。方法 選取接受介入治療的肝癌患者50例(67個(gè)病灶),于治療前、治療1個(gè)月后行超聲造影檢查,并對(duì)檢查結(jié)果進(jìn)行分析。結(jié)果 67個(gè)病灶介入治療1個(gè)月后,超聲造影下顯示27個(gè)病灶內(nèi)部無(wú)增強(qiáng),徹底治療率為40.30%,直徑<3 cm病灶、≥3 cm病灶介入治療徹底率分別為83.33%、24.49%;40個(gè)病灶有增強(qiáng),直徑<3 cm病灶殘留病灶超聲造影下以周邊小團(tuán)狀高增強(qiáng)包塊為主,直徑≥3 cm病灶殘留病灶超聲造影下以周邊不規(guī)則細(xì)節(jié)狀高增強(qiáng)包塊為主;殘留病灶治療后增強(qiáng)時(shí)間較治療前延長(zhǎng),增強(qiáng)強(qiáng)度與曲線下面積治療后較治療前下降。以超聲造影為“金標(biāo)準(zhǔn)”,常規(guī)超聲評(píng)價(jià)肝癌介入治療療效的靈敏度、特異度分別為74.07%(20/27)、47.50%(19/40)。結(jié)論 超聲造影可顯示肝癌介入治療后殘留病灶的位置、形態(tài)、范圍等特點(diǎn),是肝癌介入治療后療效評(píng)價(jià)的可靠方法。
超聲造影;肝癌;介入治療;療效評(píng)價(jià)
(ChinJLabDiagn,2017,21:0054)
肝癌(hepatocellular carcinoma,HCC)是我國(guó)最常見(jiàn)的惡性腫瘤之一,以原發(fā)性肝癌多見(jiàn),目前對(duì)肝癌的治療主要是外科手術(shù)治療,其中介入治療作為一種微創(chuàng)的治療措施已經(jīng)成為肝癌常用的手術(shù)治療方法,包括經(jīng)皮穿刺肝癌熱凝固療法、經(jīng)動(dòng)脈化療栓塞術(shù)、無(wú)水乙醇注射和冷凍療法等[1-5]。一般患者采用介入治療后需要對(duì)療效進(jìn)行準(zhǔn)確的判定,臨床常采用彩色多普勒血流成像、增強(qiáng)核磁共振、增強(qiáng)CT等方法進(jìn)行療效評(píng)價(jià)。本研究主要探討超聲造影在肝癌介入治療療效評(píng)價(jià)中的應(yīng)用價(jià)值,現(xiàn)將結(jié)果報(bào)告如下。
1 資料與方法
1.1 一般資料
選取2014年3月-2015年10月期間在巴中市中心醫(yī)院接受介入治療的肝癌患者50例(67個(gè)病灶)為研究對(duì)象,均在前期經(jīng)穿刺等病理檢查確診,其中男36例、女14例,年齡41-69歲,平均(50.48±7.03)歲;原發(fā)性肝癌43例,轉(zhuǎn)移性肝癌7例;病灶直徑1.2-7.2 cm,(3.71±0.58)cm。≥3 cm的病灶49個(gè),<3 cm的病灶18個(gè),其中17例接受經(jīng)導(dǎo)管肝動(dòng)脈化療栓塞術(shù)治療,12例接受射頻消融治療,11例接受經(jīng)導(dǎo)管肝動(dòng)脈化療栓塞術(shù)+射頻消融治療,10例接受經(jīng)導(dǎo)管肝動(dòng)脈化療栓塞術(shù)+微波消融治療。
1.2 方法
儀器為GE LOGIQ E9超聲診斷儀,探頭頻率2-5 MHz,造影劑為意大利Bracco公司生產(chǎn)的SonoVue造影劑。使用時(shí)將造影劑用5 ml生理鹽水稀釋后抽取1.2 ml,從前臂淺靜脈注入,尾隨注入10 ml生理鹽水后觀察造影結(jié)果。在超聲造影檢查前先在二維超聲模式下對(duì)肝臟內(nèi)病灶位置、大小、數(shù)目、血流等情況進(jìn)行觀察并記錄,后切換到造影模式下進(jìn)行造影檢查,分別觀察、記錄動(dòng)脈期、門(mén)脈期和延遲期增強(qiáng)特點(diǎn)。
1.3 觀察指標(biāo)及療效判斷標(biāo)準(zhǔn)
觀察患者介入治療后1個(gè)月時(shí)的治療效果。根據(jù)信號(hào)有無(wú)增強(qiáng)將病灶分為完全滅活(無(wú)增強(qiáng)/無(wú)血流信號(hào))和未完全滅活(有增強(qiáng)/有血流信號(hào))[6]。觀察未完全滅活患者殘留病灶動(dòng)脈期增強(qiáng)方式,殘留病灶治療前后增強(qiáng)時(shí)間、增強(qiáng)強(qiáng)度,計(jì)算曲線下面積。
1.4 統(tǒng)計(jì)學(xué)方法
研究數(shù)據(jù)采用SPSS19.0統(tǒng)計(jì)學(xué)軟件進(jìn)行統(tǒng)計(jì)分析,計(jì)數(shù)資料比較采用χ2檢驗(yàn),計(jì)量資料比較采用t檢驗(yàn),P<0.05為差異有統(tǒng)計(jì)學(xué)意義。
2 結(jié)果
2.1 超聲造影判定治療效果分析
67個(gè)病灶介入治療1個(gè)月后,超聲造影下顯示27個(gè)病灶內(nèi)部無(wú)增強(qiáng),徹底治療率為40.30%,其中15個(gè)直徑<3 cm病灶,12個(gè)直徑≥3 cm病灶,不同直徑病灶介入治療徹底率分別為83.33%、24.49%,差異有統(tǒng)計(jì)學(xué)意義(P<0.05),見(jiàn)表1;40個(gè)病灶有增強(qiáng),直徑<3 cm病灶殘留病灶超聲造影下以周邊小團(tuán)狀高增強(qiáng)包塊為主,直徑≥3 cm病灶殘留病灶超聲造影下以周邊不規(guī)則細(xì)節(jié)狀高增強(qiáng)包塊為主,不同直徑病灶殘留病灶超聲造影動(dòng)脈期增強(qiáng)方式比較差異有統(tǒng)計(jì)學(xué)意義(P<0.05),見(jiàn)表2。

表1 不同直徑病灶治療徹底率比較 n(%)

表2 殘留病灶超聲造影動(dòng)脈期增強(qiáng)方式比較 n(%)
2.2 殘留病灶治療前后增強(qiáng)時(shí)間、增強(qiáng)強(qiáng)度和曲線下面積比較
介入治療后增強(qiáng)時(shí)間較治療前延長(zhǎng),增強(qiáng)強(qiáng)度與曲線下面積治療后較治療前下降,差異有統(tǒng)計(jì)學(xué)意義(P<0.05),見(jiàn)表3。
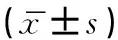
表3 殘留病灶治療前后增強(qiáng)時(shí)間、增強(qiáng)強(qiáng)度和曲線下面積比較
2.3 超聲造影與常規(guī)超聲評(píng)價(jià)肝癌介入治療療效的靈敏度、特異度比較
以超聲造影為“金標(biāo)準(zhǔn)”,常規(guī)超聲評(píng)價(jià)肝癌介入治療療效的靈敏度、特異度分別為74.07%(20/27)、47.50%(19/40),見(jiàn)表4。

表4 超聲造影與常規(guī)超聲評(píng)價(jià)肝癌介入治療療效比較 例
3 討論
肝癌在我國(guó)位居惡性腫瘤的第2位,是導(dǎo)致人口死亡的主要疾病之一,目前外科手術(shù)被認(rèn)為是治療肝癌最可靠的手段之一,但是由于在病情早期較為隱匿,臨床發(fā)現(xiàn)時(shí)已經(jīng)錯(cuò)過(guò)了最佳手術(shù)時(shí)機(jī),此時(shí)如果進(jìn)行病灶切除往往存在難度大、切除不徹底等缺點(diǎn),因此,不宜進(jìn)行病灶切除。隨著微創(chuàng)介入技術(shù)在臨床的應(yīng)用與發(fā)展,經(jīng)皮穿刺肝癌熱凝固療法、經(jīng)動(dòng)脈化療栓塞術(shù)、無(wú)水乙醇注射、冷凍療法等介入治療成為晚期肝癌的主要治療方法,其機(jī)制主要是通過(guò)阻斷腫瘤血液供應(yīng)而起到滅活腫瘤的目的,因此,準(zhǔn)確地判定腫瘤介入治療后的血液供應(yīng)、病灶大小變化等是判定肝癌介入治療是否成功的關(guān)鍵。
目前對(duì)肝癌的介入治療療效評(píng)估方法較多,如增強(qiáng)CT、核磁共振(MRI)、數(shù)字減影血管造影(DSA)等,但均有費(fèi)用昂貴、不宜短期重復(fù)操作等缺點(diǎn),因此,在臨床應(yīng)用時(shí)受到一定程度的限制。超聲檢查是一種無(wú)創(chuàng)傷性檢查方法,重復(fù)操作性好,但在肝癌的診斷和療效評(píng)價(jià)時(shí)特異性較差。超聲造影是在常規(guī)灰階超聲基礎(chǔ)上利用低聲壓和反向脈沖諧波技術(shù)抑制組織信號(hào)而特異性地接收造影劑信號(hào),可以達(dá)到診斷、評(píng)估感興趣區(qū)域病情的目的,同時(shí)造影劑無(wú)毒、安全,也可在短期內(nèi)重復(fù)應(yīng)用,因此,在臨床上已經(jīng)作為肝癌等多種疾病的診斷及治療療效評(píng)估方法應(yīng)用[7,8],有報(bào)道顯示,在顯示肝硬化背景下的肝癌時(shí)效果甚至于優(yōu)于增強(qiáng)MRI[9]。
本研究結(jié)果顯示,67個(gè)病灶介入治療1個(gè)月后超聲造影下顯示27個(gè)病灶內(nèi)部無(wú)增強(qiáng),徹底治療率為40.30%,直徑<3 cm病灶治療徹底率高于≥3 cm病灶,這可能是由于病灶較大時(shí)瘤體血液供應(yīng)的網(wǎng)絡(luò)相對(duì)較大,介入治療時(shí)無(wú)法將所有主要血液供應(yīng)血管完全堵塞,整體來(lái)說(shuō)也提示較大的肝癌病灶介入治療效果可能不及直徑<3 cm的病灶。其余40個(gè)病灶超聲造影動(dòng)脈期的聲像表現(xiàn)均明顯有增強(qiáng),門(mén)脈期、延遲期消退廓清呈等或低增強(qiáng),直徑<3 cm病灶殘留病灶超聲造影下以周邊小團(tuán)狀高增強(qiáng)包塊為主,直徑≥3 cm病灶殘留病灶超聲造影下以周邊不規(guī)則細(xì)節(jié)狀高增強(qiáng)包塊為主,小部分包塊為內(nèi)部不規(guī)則結(jié)節(jié)狀高增強(qiáng),這種強(qiáng)化方式的不同可能與腫瘤直徑、血液供應(yīng)等有關(guān)。超聲造影下的時(shí)間-強(qiáng)度分析是一種定量分析指標(biāo),可對(duì)組織灌注情況進(jìn)行對(duì)比,其中曲線下面積可預(yù)測(cè)腫瘤內(nèi)的血流量[10,11]。本研究對(duì)殘留病灶治療前后的時(shí)間-強(qiáng)度分析結(jié)果顯示,治療后增強(qiáng)時(shí)間較治療前延長(zhǎng),增強(qiáng)強(qiáng)度與曲線下面積治療后較治療前下降,說(shuō)明雖然介入術(shù)后患者病灶較治療前明顯縮小,血液供應(yīng)有所減少,但是仍然有一定的血液供應(yīng)存在,這種表現(xiàn)對(duì)于殘留病灶的判定有一定意義。以超聲造影為“金標(biāo)準(zhǔn)”,常規(guī)超聲評(píng)價(jià)肝癌介入治療療效的靈敏度、特異度分別為74.07%、47.50%,可以看出明顯低于超聲造影檢查,相對(duì)于常規(guī)超聲超聲造影檢查優(yōu)勢(shì)是極為明顯的。
綜上所述,超聲造影可以顯示肝癌介入治療后腫瘤區(qū)域灌注及荷瘤血管阻斷程度,并判斷是否有殘留以及殘留病灶的位置、形態(tài)、范圍等特點(diǎn),是肝癌介入治療后療效評(píng)價(jià)的可靠方法。
[1]European Association For The Study Of The Liver.EASL-EORTC clinical practice guidelines:management of hepatocellular carcinoma[J].Journal of Hepatology,2012,56(4):908.
[2]Bruix J,Gores G J,Mazzaferro V.Hepatocellular carcinoma:clinical frontiers and perspectives[J].Gut,2014,63(5):844.
[3]Peng ZW,Zhang YJ,Chen MS,et al.Radiofrequency ablation with or without transcatheter arterial chemoembolization in the treatment of hepatocellular carcinoma:a prospective randomized trial[J].Journal of Clinical Oncology,2013,31(4):426.
[4]Yin L,Li H,Li A J,et al.Partial hepatectomy vs.transcatheter arterial chemoembolization for resectable multiple hepatocellular carcinoma beyond Milan Criteria:a RCT[J].Journal of hepatology,2014,61(1):82.
[5]Shiina S,Tateishi R,Imamura M,et al.Percutaneous ethanol injection for hepatocellular carcinoma:20‐year outcome and prognostic factors[J].Liver International,2012,32(9):1434.
[6]袁家英,朱 紅,周智華,等.超聲造影技術(shù)應(yīng)用于肝腫瘤介入治療的臨床價(jià)值探析[J].2013,7(4):18479.
[7]夏 宇,姜玉新,戴 晴,等.肝細(xì)胞肝癌超聲造影增強(qiáng)模式對(duì)分化程度的診斷價(jià)值[J].協(xié)和醫(yī)學(xué)雜志,2014,5(1):46.
[8] 趙瑞華,譚 青,劉 磊,等.肝血管瘤超聲造影表現(xiàn)[J].中國(guó)醫(yī)藥科學(xué),2013,3(20):98.
[9] Takahashi M,Maruyama H,Shimada T,et al.Characterization of hepatic lesions(≤30 mm) with liver-specific contrast agents:a comparison between ultrasound andmagnetic resonance imaging[J].Eur J Radiol,2013,82 (1):475.
[10]Dietrich CF,Cui XW,Boozari B,et al.Contrast- enhanced ultrasound (CEUS) inthe diagnostic algorithm of hepatocellular andcholangiocellularcarcinoma,comments on theAASLD guidelines[J].Ultraschall Med,2012,7 (33):S57.
[11]Yang YL,Yang RJ,Liu X,et al.Correlations between the time-intensity parameters of contrast-enhanced ultrasound and clinical prognosis of hepatocellular carcinoma[J].Clinical imaging,2013,37(2):308.
Utilization of contrast-enhanced ultrasonography in response evaluation of hepatocellular carcinoma after interventional therapy
LUODa-jian1,ZHANGZhi-yong2,YANGTao1,etal.
(1.Departmentofultrasound,BazhongCentralHospital,Bazhong636000,China;2.Departmentofhepatobiliarysurgery,CentralHospitalofBazhong,Bazhong,Sichuan636000,China;3.Departmentofultrasound,LiuzhouWorker'sHospital,Liuzhou,Guangxi545005,China)
Objective To discuss utilization of contrast-enhanced ultrasonography in response evaluation of hepatocellular carcinoma(HCC) after interventional therapy.Methods The observation of 67 primary foci in 50 cases HCC Before and 1 month after treatment were performed by contrast-enhancedultrasound.Results After treatment,The contrast-enhanced ultrasonography examination showed that the residual and recurrent viable tumors have not identify enhancement in any of the remaining 27 lesions for the HCC patients after response evaluation,Thetreatment rate was 40.30%,diameter <3 cm and ≥3 cm lesions for thetreatment rate were 83.33% and 24.49%;After treatment,The contrast-enhanced ultrasonography examination showed that the residual and recurrent viable tumors have enhancement in any of the remaining 40 lesions for the HCC patients after response evaluation,Peripheral small cloud state High enhancement bag piece of <3 cm lesions,High enhancement surrounding small section irregular block ≥3 cm lesions;Residual lesions enhanced after treatment time is longer than before the treatment,enhance the strength and the area under the curve is lower than before treatment after treatment.The contrast-enhanced ultrasound for the “gold standard”,The sensitivity of conventional ultrasonic evaluating the effect of interventional therapy of liver cancer,specific degrees were 74.07% (20/27),47.50% (19/40).Conclusion Contrast-enhanced ultrasonography can display the position,shape and range characteristics of hepatocellular carcinoma after interventional therapy of residual lesions Position,is a reliable method of evaluating curative effect after interventional therapy of liver cancer.
Contrast-enhanced ultrasonography;Hepatocellular carcinoma;Response evaluation;Therapeutic Effective Evaluation
1007-4287(2017)01-0054-03
廣西衛(wèi)生和計(jì)劃生育委員會(huì)自籌經(jīng)費(fèi)科研課題(編號(hào):Z2015162)
R735.7
A
2016-03-26)
 中國(guó)實(shí)驗(yàn)診斷學(xué)2017年1期
中國(guó)實(shí)驗(yàn)診斷學(xué)2017年1期
- 中國(guó)實(shí)驗(yàn)診斷學(xué)的其它文章
- 骨髓增生異常綜合征克隆性7號(hào)染色體異常的發(fā)生及臨床分析
- 晚期眼MALT淋巴瘤單純放療后產(chǎn)生遠(yuǎn)位效應(yīng)1例
- pAdKDR/CD/TK雙自殺基因系統(tǒng)對(duì)肝癌細(xì)胞的殺傷作用的試驗(yàn)研究
- 頸動(dòng)脈閉塞自發(fā)再通1例
- 家庭無(wú)創(chuàng)正壓通氣對(duì)我國(guó)慢性阻塞性肺疾病穩(wěn)定期患者療效的meta分析
- 纖維蛋白膠介導(dǎo)大鼠內(nèi)皮祖細(xì)胞移植干預(yù)大鼠急性腦缺血的實(shí)驗(yàn)研究
