間質性肺炎誤診為肺癌3例并文獻復習
謝曉楓,侯英勇,宿杰阿克蘇,曽海英,黃 潔,徐一凡,張小壘
間質性肺炎誤診為肺癌3例并文獻復習
謝曉楓,侯英勇,宿杰阿克蘇,曽海英,黃 潔,徐一凡,張小壘
目的 探討間質性肺炎的臨床病理特征。方法 回顧性分析3例間質性肺炎誤診為肺癌的影像學表現和臨床病理特征,并進行隨訪和相關文獻復習。結果 男性2例,女性1例,年齡分別為51、68和59歲,其中例1有長期吸煙史,3例影像學均為典型的間質性肺炎表現,高分辨率CT示3例均為肺內散在網格狀、蜂窩狀高密度影,以下葉為主。鏡下均可見間質纖維組織增生,不同程度的炎癥細胞浸潤及肺泡上皮不典型增生。免疫表型:增生的肺泡上皮TTF-1、CK7、Napsin A均陽性,p63陰性,Ki-67增殖指數為2%~10%。3例首次病理診斷均被誤診為肺低分化腺癌,例1、3臨床分別行2次活檢,經臨床反饋或多學科協作組討論后,病理診斷均在第2次活檢后得到更正。結論 間質性肺炎伴不同程度肺泡上皮異型增生時與肺腺癌在病理學形態上可有重疊,鑒別診斷較為困難,易誤診,診斷時需密切結合其影像學表現,多學科協作討論有助于加強對該疾病的認識。
肺腫瘤;間質性肺炎;誤診;多學科協作
2002年美國胸科學會(ATS)和歐洲呼吸協會(ERS)將特發性間質性肺炎(idiopathic interstitial pneumonia, IIP)分為以下7大類:普通型間質性肺炎/特發性肺纖維化、非特異性間質性肺炎、特發性脫屑性間質性肺炎、呼吸性肺支氣管炎伴間質性肺疾病、急性間質性肺炎、特發性淋巴細胞性間質性肺炎、隱源性機化性肺炎,初步統一IIP的臨床與病理學標準[1]。IIP是由炎癥細胞浸潤和纖維組織增生構成,各亞型炎癥與纖維化所占比例不等,當伴肺泡上皮增生且出現異型時與肺癌的組織學特點相似,活檢組織鑒別診斷存在困難,臨床診斷有誤診為腺癌的可能,結合臨床和影像學資料對避免過度診斷有一定的幫助。本文現分析3例IIP誤診為肺癌的病例,以提高對該疾病的臨床病理特征的認識,避免誤診。
1 材料與方法
1.1 材料 例1,男性,51歲,吸煙史25年,1年前外院體檢發現雙肺間質性病變;6個月前我院HRCT示雙肺胸膜下網格狀高密度影,考慮雙肺間質性纖維化(圖1),PET/CT首先考慮為間質性肺炎,右肺下葉后基底段網格狀病灶中可見一大小10.7 mm×6.3 mm不規則結節影,最大SUV值為2.6,未見明確惡性病變癥象。第1次病理報告為低分化腺癌,因病理結果與臨床考慮不一致,行第2次活檢再次明確病變性質。遂復習第1次活檢病理切片及學習影像學資料,發現第1次診斷可能出現過度判斷,并將例1提交多學科協作組討論。在深入學習及與各科醫師討論后,將2次病理檢查報告均予以更正:鏡下為肺組織及支氣管壁組織,間質纖維組織增生,其間見異型細胞,呈單個、腺樣、乳頭或巢狀生長,結合影像學檢查,并經臨床病理多學科組討論,患者肺部無腫塊,僅呈肺間質纖維化影像學改變,考慮肺間質纖維化伴肺泡上皮異型增生,結合臨床處理必要時與病理科反饋及討論。例2,男性,68歲,2013年1月我院胸部CT平掃示雙肺網格狀高密度影,以右下肺為主。右下肺前基底段活檢病理報告為傾向低分化腺癌,復查影像學均考慮間質性肺炎。例3,女性,59歲,2014年4月我院CT示雙肺下葉胸膜下可見散在絮狀高密度影,并呈網格狀改變,考慮雙肺間質性炎癥,左肺小結節;2015年1月HRCT示雙肺輕度間質性炎癥。活檢病理報告為傾向腺癌可能,請密切結合臨床考慮,必要時重新活檢。入院PET/CT考慮間質性炎癥,第2次活檢病理報告為肺間質纖維組織增生,部分肺泡上皮明顯增生。
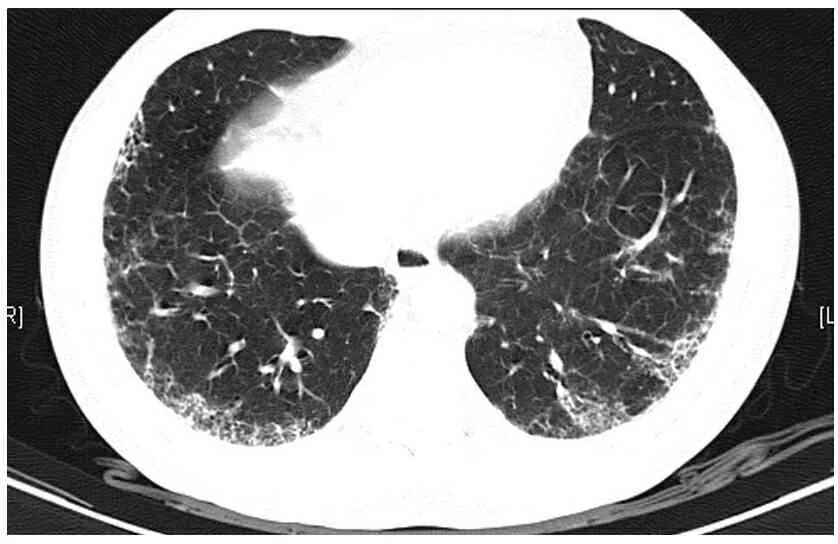
圖1 間質性肺炎改變,雙肺下葉及外周帶靠近胸膜為重
1.2 方法 活檢標本均經10%中性福爾馬林固定,常規脫水,石蠟包埋切片,制備HE切片和免疫組化染色。免疫組化采用EnVision兩步法染色,單克隆抗體Ki-67、CK7、p63購自DAKO公司,Napsin A購自Abcam公司,TTF-1購自Leica公司。
2 結果
2.1 眼觀 例1,兩次活檢均為灰白色組織5粒,直徑合計0.3 cm。例2,灰白色粟米大組織4粒。例3,兩次活檢均為灰白色組織5粒,直徑均0.2 cm。
2.2 鏡檢 腫瘤鏡下見肺組織及支氣管壁組織,3例間質均有纖維組織增生,不同程度的炎癥細胞浸潤,例1見肺泡上皮呈實性片狀排列,需與低分化癌鑒別(圖2);例2增生纖維組織及裂隙中見擠壓異型上皮細胞(圖3);例3增生纖維組織間見小片狀分布的異型上皮細胞(圖4)。

②③④圖2 肺泡上皮巢實性片狀排列,細胞有異型,需與低分化癌鑒別 圖3 增生纖維組織及裂隙中見擠壓異型上皮細胞 圖4 上皮細胞呈小片狀結構,部分散在分布,細胞有異型
2.3 免疫表型 3例增生上皮肺泡上皮源性標志物TTF-1、Napsin A、CK7均呈陽性,p63呈陰性,Ki-67增殖指數為2%~10%。2.4 隨訪 例1在獲得更正診斷后出院,口服激素治療,3個月內隨訪結果仍考慮為間質性肺炎;例2獲得低分化腺癌診斷后,未住院行進一步治療,隨訪2次CT均為間質性肺炎,最后一次隨訪HRCT示雙肺均為間質性炎癥,右肺上葉縱隔見大小20 mm×15 mm軟組織影,邊緣毛糙,見分葉及毛刺——MT待排,該例患者失訪。例3獲得更正診斷后,2次隨訪CT均考慮間質性肺炎,無不適癥狀。
3 討論
目前,IIP病因尚不明確,臨床可能出現的癥狀包括胸痛、勞動后呼吸困難及進行性呼吸困難,也可伴隨一些非特異性癥狀如乏力、發熱、杵狀指等[2]。HRCT是診斷間質性肺炎主要影像學技術[3],表現為磨玻璃、網格狀、蜂窩狀的高密度影,病變以雙肺的外周帶、胸膜下較重,自肺尖向肺底逐漸加重[4],本組病例與文獻報道一致。病理學相關機制包括炎癥性病變后肺泡上皮的損傷、修復、纖維化[5],也有相關基因以及通路方面的報道[6-7]。
許多研究均表明間質性肺炎與肺癌有相關性,臨床上表現為胸痛、呼吸困難加重或出現體重下降、咯血等。影像學顯示腫塊呈圓形或卵圓形,邊緣不規則,有分葉狀或毛刺;癌變常發生在纖維化較重的區域如肺下葉、外周帶,常見為合并鱗癌、腺癌、小細胞癌或者復合癌[8],合并癌癥的危險因素有吸煙[9]、老人、男性[10]。
鑒別間質性肺炎與肺癌的診斷非常必要,臨床工作中存在間質性肺炎與肺癌相互誤診的情況,2011年仲向東[11]報道27例肺炎型肺癌,影像學均表現為斑片狀、大片模糊陰影,臨床癥狀無特異性,其中21例被誤診為間質性肺炎、慢性阻塞性肺病或者感染性病變,誤診率高達77%;本組3例將肺泡上皮異型增生誤診為肺癌。病理醫師診斷最大的困難是不典型增生與癌變的界限。近年來臨床-影像-病理[12]多學科協作的診斷模式,有助于病理醫師對間質性肺炎的正確診斷,避免診斷過度。因此,病理醫師在診斷肺部非腫瘤性病變時,應充分了解其臨床病史及影像學資料[13],尤其對于活檢標本。疾病的發生、發展過程是動態的,而病理醫師看到的只是某一時間節點的局部病灶,在診斷時應遵守臨床-影像-病理原則,可以有效的避免因“只見樹木,不見森林”導致的誤診。
綜上所述,間質性肺炎伴肺泡上皮異型增生與肺癌組織學形態可有重疊,目前尚無肺泡上皮不典型增生與癌變界限的定義,單靠病理學形態做診斷與鑒別診斷較為困難。間質性肺炎不同區域的癌變幾率不同,故病變的不同部位形態學異質性較大,活檢組織有限,病理學結果或許未能較好的反應病變全貌,結合影像學可避免組織局限導致的誤診。部分間質性肺炎與肺癌影像學表現、病理學形態均較為相似,應與臨床-影像-病理醫師積極交流、溝通,多學科協作的模式能最大程度的資源共享,使每個患者的診療過程更加高效、精準,也給病理醫師提供良好平臺,及時的發現并解決問題,避免誤、漏診。
[1] Demedts M, Costabel U. ATS/ERS international multidisciplinary consensus classification of the idiopathic interstitial pneumonias[J]. Eur Respir J, 2002,19(5):794-796.
[2] 張蘭蘭,王 蓓. 間質性肺疾病的臨床診斷思路[J]. 臨床內科雜志, 2011,28(9):587-589.
[3] Behr J. The diagnosis and treatment of idiopathic pulmonary fibrosis[J]. Dtsch Arztebl Int, 2013,110(51-52):875-881.
[4] Khan K A, Kennedy M P, Moore E,etal. Radiological characteristics, histological features and clinical outcomes of lung cancer patients with coexistent idiopathic pulmonary fibrosis[J]. Lung, 2015,193(1):71-77.
[5] Chambers R C, Mercer P F. Mechanisms of alveolar epithelial injury, repair, and fibrosis[J]. Ann Am Thorac Soc, 2015,12(Suppl 1):S16-S20.
[6] Nathan N, Giraud V, Picard C,etal. Germline SFTPA1 mutation in familial idiopathic interstitial pneumonia and lung cancer[J]. Hum Mol Genet, 2016,25(8):1457-1467.
[7] Xie B, Zheng G, Li H,etal. Effects of the tumor suppressor PTEN on the pathogenesis of idiopathic pulmonary fibrosis in Chinese patients[J]. Mol Med Rep, 2016,13(3):2715-2723.
[8] 易祥華,羅本芳,李惠萍,等. 伴肺癌的特發性間質性肺炎七例臨床病理學分析[J]. 上海醫學, 2009,32(12):1113-1117.
[9] Song D H, Choi I H, Ha S Y,etal. Usual interstitial pneumonia with lung cancer: clinicopathological analysis of 43 cases[J]. Korean J Pathol, 2014,48(1):10-16.
[10] Lee T, Park J Y, Lee H Y,etal. Lung cancer in patients with idiopathic pulmonary fibrosis: clinical characteristics and impact on survival[J]. Respir Med, 2014,108(10):1549-1555.
[11] 仲向東. 肺炎型肺癌21例誤診分析[J]. 實用心腦肺血管病雜志, 2011,19(12):2126-2127.
[12] Raghu G, Collard H R, Egan J J,etal. An official ATS/ERS/JRS/ALAT statement: idiopathic pulmonary fibrosis: evidence-based guidelines for diagnosis and management[J]. Am J Respir Crit Care Med, 2011,183(6):788-824.
[13] 石雪迎,廖松林. 特發性肺間質纖維化的病理診斷[J]. 臨床與實驗病理學雜志, 2003,19(6):646-649.
上海市衛生和計劃生育委員會薄弱科室項目(2015ZB0201)
復旦大學附屬中山醫院病理科,上海 200032
謝曉楓,女,碩士研究生。E-mail: 18221720882@163.com 侯英勇,女,教授,博士生導師,主任醫師,通訊作者。 E-mail: houyingyong@hotmail.com
時間:2017-5-17 23:53 網絡出版地址:http://kns.cnki.net/kcms/detail/34.1073.R.20170517.2352.020.html
R 365
B
1001-7399(2017)05-0557-03
10.13315/j.cnki.cjcep.2017.05.020
接受日期: 2017-02-24

