中西醫結合治療中、重度宮腔粘連臨床觀察
劉 娜 趙 威
(河南中醫藥大學第三附屬醫院,河南 鄭州 450008)
中西醫結合治療中、重度宮腔粘連臨床觀察
劉 娜 趙 威
(河南中醫藥大學第三附屬醫院,河南 鄭州 450008)
宮腔粘連;中西醫結合;戊酸雌二醇片;黃體酮膠囊;中藥
宮腔粘連(IUA)指子宮內膜受到損傷,導致宮腔感染,進而引發組織粘連,使宮腔部分或全部閉鎖,臨床上表現為閉經或月經量過少、周期性痙攣性下腹痛、繼發不孕等[1]。近年來宮腔粘連發病率逐年遞增,宮腔鏡下宮腔粘連分解術為目前診斷和治療宮腔粘連的首選方法[2]。然而宮腔粘連經宮腔鏡分離術后再粘連的發生率為3.1%~23.5%,而中、重度宮腔粘連患者術后復發率高達48%~62.5%[3]。術后再粘連的預防至今仍是臨床治療中的難題。本研究以中西醫結合的方法治療中、重度宮腔粘連,取得良好效果,現報道如下。
一般資料
收集2014年6月—2016年1月在河南中醫藥大學第三附屬醫院住院并行宮腔鏡下宮腔粘連分解術的70例患者,采用隨機數字表法分為治療組和對照組。治療組35例,中度粘連22例,重度粘連13例。對照組35例,中度粘連23例,重度粘連12例。兩組在平均年齡、平均病程、宮腔操作次數等一般資料比較差異無統計學意義(P>0.05),具有可比性。
診斷標準:西醫診斷標準參照《婦科內鏡學》[4]《婦產科學》[5]擬定,有人工流產史、稽留流產或不全流產刮宮史、人流術后宮腔感染史;臨床表現為月經過少、繼發性閉經、繼發不孕等;彩超檢查:子宮內膜2~5 mm、內膜線不連續;宮腔鏡檢查提示宮腔粘連(中、重度)。宮腔粘連診斷標準根據歐洲婦科內鏡協會(ESGE)宮腔粘連的分類標準。
中醫辨證標準:參照《中藥新藥臨床研究指導原則(試行)》[6]《中醫婦科學》[7]擬定。腎虛血瘀證:主癥有經量明顯少于既往,經期不足2 d,或點滴即凈,色紫暗,有血塊,甚或月經停閉不行;次癥:經行小腹脹痛,腰膝酸軟,頭暈耳鳴,失眠健忘,夜尿頻多,口干不欲飲等;舌脈:舌質淡暗或淡紅,或有瘀斑、瘀點,脈弦細或沉澀。具備以上主癥及至少2項次癥,結合舌脈,即可診斷。
納入標準:符合上述診斷標準;本試驗前未進行治療,或雖經外院治療,但病情無明顯改善,已放棄原治療方案者;患者簽署知情同意書。
排除標準:合并有心腦血管、肝、腎及造血系統等嚴重疾病者;合并其他內分泌疾病,如先天性腎上腺皮質增生、分泌雄激素的腫瘤和庫欣綜合征、糖尿病、甲狀腺疾病等;生殖系統先天性缺陷和畸形者;生殖系統結核者;對研究藥物過敏者。
治療方法
對照組:宮腹腔鏡聯合經宮腔鏡下行宮腔粘連分離術后第二日開始服用戊酸雌二醇片3 mg,每日2次;第十二日起加服黃體酮膠囊0.1 g,每日2次,連服21 d停藥。術后放置宮腔氣囊,行抗感染治療,于第四日放置宮內節育器、幾丁糖。有月經者于第五日起開始一周期治療,無月經者停藥7 d后開始服下一周期治療。連續治療3個月經周期,3個月后復查宮腔鏡。
治療組:宮腔粘連分離術后第五日在對照組基礎上開始服藥。非經期藥物組成:熟地黃25 g,當歸15 g,白芍15 g,川芎10 g,菟絲子25 g,覆盆子15 g,枸杞子15 g,五味子10 g,車前子10 g,紅藤25 g,丹參20 g,甘草6 g。腎陽虛甚者加仙茅、淫羊藿各15 g;腎陰虛者加生地黃15 g,女貞子15 g;氣虛者加黃芪20 g,白術20 g;瘀熱者加蒲公英25 g,紅藤25 g。經期方劑組成:桃仁10 g,當歸15 g,川芎10 g,醋香附15 g,益母草20 g,川牛膝10 g,甘草6 g,炮姜6 g,莪術10 g,5劑。連續治療3個月經周期。
觀察指標及方法:兩組患者均于宮腔鏡檢查前1個月經周期運用陰道超聲檢測黃體期(月經第二十一至二十八日)子宮內膜情況,并于月經干凈后第三至七日行宮腔鏡檢查。服藥第三個周期月經干凈后再次進行宮腔鏡檢查。用藥前1個周期和用藥第三個周期黃體期陰道超聲檢測子宮內膜厚度,取矢狀斷面距宮底下2 cm處測量子宮前、后肌層與內膜交界面距離。
治療結果
1.療效判定標準:①月經恢復療效判定標準[6]。經量同既往為治愈;經量≥1/2既往月經量為顯效;經量≥1/3既往經量且<1/2既往經量為有效;經量無改變或<1/3既往經量為無效。②宮腔粘連療效判定標準[8]。治愈:宮腔鏡下宮腔形態正常,見雙側輸卵管開口;有效:宮腔鏡下見宮腔形態基本正常,較分離前明顯增大,見一側或雙側輸卵管開口,有局部粘連;無效:宮腔鏡下宮腔與分離前無變化。
2.結果
(1)月經恢復療效比較。見表1。

表1 治療組與對照組患者月經恢復療效比較[例(%)]
注:與對照組比較,△P<0.05
(2)宮腔粘連療效比較。見表2。

表2 治療組與對照組患者宮腔粘連術后療效比較[例(%)]
注:與對照組比較,△P<0.05
(3)治療前后子宮內膜厚度比較:治療組治療后子宮內膜厚度與治療前比較,差異有統計學意義(P<0.05),對照組治療后子宮內膜厚度與治療前比較,差異無統計學意義(P>0.05)。治療后治療組子宮內膜厚度明顯大于對照組,差異有統計學意義(P<0.05)。
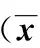
表3 治療組與對照組患者治療前后子宮內膜厚度比較±s)
注:與同組治療前比較,*P<0.05;與對照組治療后比較,△P<0.05
討論
中醫古籍中無宮腔粘連的記載,可歸屬于“月經過少”“閉經”“不孕”等范疇。中醫認為該病由于宮腔操作使胞宮、胞脈受損,致腎中精氣損傷,沖任氣血不足,精血俱損,血海空虛;或邪氣入侵與血搏結,瘀血內阻胞宮,氣血運行不暢,胞脈閉塞。腎虛、氣血沖任失調為本病的根本,血瘀為標。女子以腎為根,以血為本,治療當以補腎活血為根本原則,故選用四物湯和五子衍宗丸為基礎方,辨證加減治療。方中菟絲子、熟地黃、枸杞子補腎益精填髓,覆盆子、五味子固腎澀精,車前子活血補腎,當歸、白芍、川芎補血活血,紅藤、丹參活血散瘀止痛。本方補中有通,腎氣充,腎精足,經水有源,精血充足,則月經自復。經期用桃仁、當歸、川芎、益母草、川牛膝、炮姜、醋香附、莪術活血化瘀通經,促使子宮內膜完全剝脫,祛瘀生新。現代藥理研究表明,補腎中藥具有類雌激素樣作用,能調整“腎-天癸-沖任-胞宮軸”,改善盆腔內環境,促進子宮內膜腺體和間質的增殖與修復,活血化瘀藥物可改善宮腔內組織缺血狀態,促進吞噬細胞的吞噬功能,從而促進局部瘀血的吸收[9],達到生理性恢復粘連的目的。
宮腔粘連多繼發于宮腔創傷性手術操作和術后宮腔感染,宮腔鏡手術對于中、重度宮腔粘連的治療是最有效的,宮腔鏡術后宮腔內注入幾丁糖、雌孕激素周期治療及放置宮內節育器(IUD),均有利于預防術后宮腔再粘連[10]。本觀察結果顯示,在粘連分解術加置IUD、幾丁糖、激素替代治療基礎上,使用補腎活血中藥能提高臨床療效,中西醫結合治療能改善宮腔粘連術后患者子宮內膜厚度,有利于月經恢復,預防宮腔再次粘連,值得臨床推廣。
[1]曹澤毅.中華婦產科學[M].北京:人民衛生出版社,2005:1201.
[2]Deans R,Abbott J.Review of intrauterine adhesions[J].Minim Invasive Gynecol,2010,17(5):555-569.
[3]Zikopoulos K A,kolibianakis E M,Platteau P,et al.Livedelivery rates in subfertile women with Asherman’s syndrome after hysteroscopic adhesiolysis using the resectoscope or the versapoint system[J].Reprod Biomed On-line,2004,8(6):720-725.
[4]夏恩蘭.婦科內鏡學[M].北京:人民衛生出版社,2001:246.
[5]樂杰.婦產科學[M].7版.北京:人民衛生出版社,2008:587.
[6]鄭筱萸.中藥新藥臨床研究指導原則(試行)[M].北京:中國醫藥科技出版社,2002:168-170.
[7]馬寶璋.中醫婦科學[M].6版.上海:上海科學技術出版社,1998:189.
[8]Dawood A,AI-Talib A,Tulandi T.Predisposing factors and treatment outcome of different stages of intrauterine adhesions[J].J Obstet Gynaecol Can,2010,32(8):767-770.
[9]侯家玉,方泰惠.中藥藥理學[M].2版.北京:中國中醫藥出版社,2008.
[10]劉紅.宮腔鏡為主的綜合治療在中、重度宮腔粘連中的應用[J].中國性醫學,2012,21(4):7-10.
2016-07-15)

