正戊醛合成工藝研究
常 慧 葉軍明 孫 駿 瞿衛國 方 玲 陸 鑫
(中國石化上海石油化工股份有限公司精細化工部,上海200540)
技術進步
正戊醛合成工藝研究
常 慧 葉軍明 孫 駿 瞿衛國 方 玲 陸 鑫
(中國石化上海石油化工股份有限公司精細化工部,上海200540)
以1-丁烯和合成氣為原料,對氫甲酰化制備戊醛的工藝進行了研究。在熱力學計算的基礎上,主要考察了均相催化體系下膦/銠物質的量比、催化劑質量濃度、丁烯用量、反應溫度、時間、壓力、攪拌速度等條件對1-丁烯氫甲酰化反應的影響。在保持1-丁烯較高轉化率和戊醛較高選擇性的條件下,給出了適宜的工藝條件:反應溫度為100 ℃左右,反應壓力2.2 MPa,攪拌速率250 r/min,反應時間30 min,催化劑質量濃度300~350 mg/L,膦/銠物質的量比為400~500。
1-丁烯 均相催化 正戊醛 氫甲酰化
正戊醛是一種典型的精細化工中間體,主要用作茉莉類合成香料中產量最大的二氫茉莉酮酸甲酯(MDJ)生產的起始原料。MDJ天然存在于大花茉莉精油中,已被廣泛應用于各種香型的香水、日用洗滌用品等花香型香精的調配中,也是一些著名香水的主體香原料,且其使用范圍與比例還在不斷增加[1-2]。
烯烴氫甲酰化反應制備醛和增塑劑醇,多年來一直是均相催化領域的研究重點[3-4]。目前烯烴氫甲酰化主要有BASF、Exxon、Shell、UCC、RCH/RP工藝等[5-6],其中BASF、Exxon和Shell工藝采用鈷催化體系,UCC和RCH/RP工藝采用銠膦催化體系。雖然我國丁烯資源豐富,但化工利用率極低,因此研究1-丁烯與合成氣氫甲酰化反應生成戊醛的工藝是有效利用丁烯的途徑之一。
1 實驗部分
1.1 原料與試劑
1-丁烯,質量分數≥99.5%,大連光明特種氣體有限公司;合成氣,CO∶H2=1∶1(體積比),上海海洲特種氣體有限公司;三苯基膦乙酰丙酮羰基銠(Rh(CO)(acac)(pph3)),分析純(AR),成都格雷西亞化學技術有限公司;三苯基膦(TPP),AR,成都格雷西亞化學技術有限公司;正戊醛,AR;2-甲基丁醛,AR;正戊醛、2-甲基丁醛作為溶劑。
1.2 實驗過程
稱取一定量的正戊醛、2-甲基丁醛、TPP以及Rh(CO)(acac)(pph3),加入250 mL高壓反應釜,用合成氣置換3次,充入一定量的1-丁烯,再充入一定壓力的合成氣,攪拌、升溫,當溫度升到設定溫度后充入合成氣到所需壓力,反應進行一定時間,停止反應,降溫取樣。
1.3 樣品分析
產品采用安捷倫4890氣象色譜儀進行分析。分析條件如下:色譜柱,DM-FFAP;柱子規格,30 m×0.32 mm×0.25 μm;柱溫,初始30 ℃,升溫至200 ℃;進樣器溫度,200 ℃;檢測器溫度,220 ℃;載氣,氮氣;檢測器,FID檢測器。
2 結果與討論
2.1 熱力學計算
通過查閱基礎物性數據手冊以及運用Aspen Plus模擬軟件對1-丁烯氫甲酰化反應的反應焓(△H)、反應吉布斯自由能(△G)、反應平衡常數(K)、熵變(△S)以及1-丁烯、正戊醛、異戊醛不同溫度下的飽和蒸汽壓進行了計算(見表1),將這些數據應用于實驗中來確定反應的可行性以及反應時物料的形態。

表1 熱力學數據的計算
由于1-丁烯氫甲酰化反應在間歇攪拌釜式反應器中進行,隨著壓力和溫度的波動,反應釜中各個物質的形態會發生變化。由于1-丁烯的飽和蒸汽壓比較低(標準狀況下為0.3 MPa),在探索壓力條件實驗時,為了保證1-丁烯為液態參與反應,首先通過Aspen plus計算出1-丁烯的飽和蒸汽壓隨溫度的變化規律,如圖1所示。
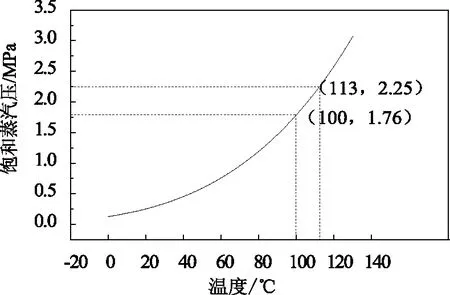
圖1 1-丁烯的飽和蒸汽壓隨溫度變化的曲線
從Aspen plus計算所得到的曲線來看:在反應溫度為100 ℃時,1-丁烯的飽和蒸汽壓為1.76 MPa。因此,為了保證1-丁烯在反應時為液態,反應選取壓力的最低值為1.8 MPa,略高于100 ℃時丁烯的飽和蒸汽壓1.76 MPa。
2.2 膦/銠物質的量比對反應的影響
在反應液中膦/銠物質的量比對1-丁烯的氫甲酰化影響極大。為此在反應溫度為100 ℃,反應時間為1 h,攪拌速度為200 r/min,催化劑質量濃度為200 mg/L,反應壓力為2.2 MPa和合成氣中H2與CO體積比為1∶1時,就膦/銠物質的量比對反應的影響進行了評價,結果見圖2。
由圖2可以看出:1-丁烯的轉化率隨著膦/銠物質的量比增加而逐漸降低,產物中戊醛的正異比則呈現相反的趨勢,逐漸緩慢升高,當膦/銠物質的量比升至500附近時,此時生成正戊醛比例達到較高值,相應的戊醛正異比為最高。繼續提高膦/銠物質的量比,反應速率有一定程度下降。為保持1-丁烯較高的轉化率和戊醛較高的正異比,合適的膦/銠物質的量比為400~500。從氫甲酰化反應機理可知,催化劑活性絡合物B和C質量濃度與TPP在反應液中的質量濃度有關,當TPP質量濃度增大時有利于活性絡合物B和C的生成,從而提高反應速率;當TPP質量濃度達到某一合理的區域時,可以催化1-丁烯轉化為正戊醛的活性絡合物B質量濃度相對較高,氫甲酰化反應速率也較快;但當反應體系中TPP過量時,由于反應液中絡合物以非活性物種三苯基膦羰基銠為主,使得反應轉化率明顯降低。
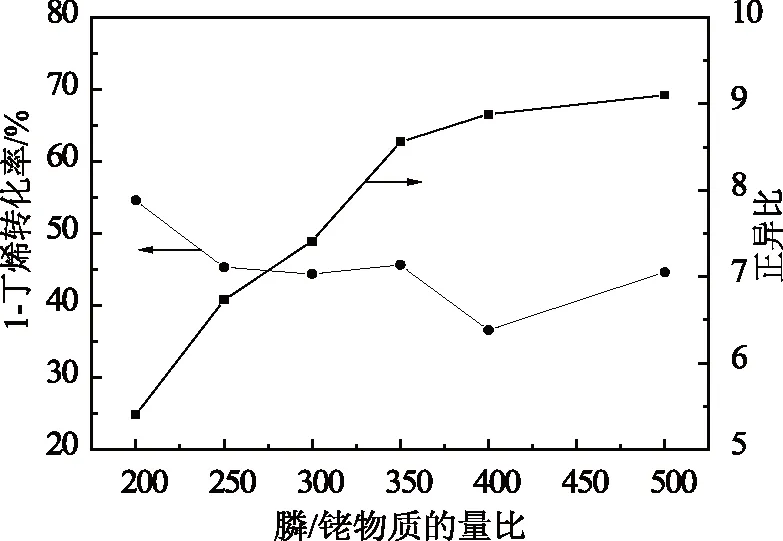
圖2 膦/銠物質的量比對氫甲酰化反應的影響
2.3 催化劑質量濃度對反應的影響
對均相催化反應而言,催化劑質量濃度的提高會相應地增加反應的速率,縮短反應時間,但由于銠為貴金屬,價格極其昂貴,故催化劑的質量濃度應處于可以確保反應效果較為理想而又盡可能減少損耗的水平。為此在溫度為100 ℃,時間為1 h,攪拌速度為200 r/min,膦/銠物質的量比為200,反應壓力為2.2 MPa和合成氣中H2與CO體積比為1∶1時,考察了催化劑質量濃度對反應的影響,結果如圖3所示。
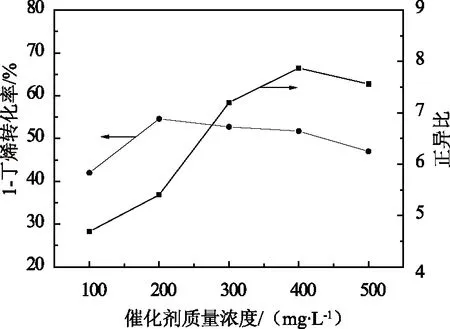
圖3 催化劑質量濃度對氫甲酰化反應的影響
從圖3中可以看出:隨著催化劑質量濃度的增加,1-丁烯的轉化率和產品中正異比均相應升高。轉化率在催化劑質量濃度為200 mg/L時達到最高值后,開始隨著催化劑質量濃度的增大而減少,這是由于隨著催化劑質量濃度的增大,催化活性物種數量也隨之增多,反應速率加快,在相同時間內,1-丁烯的轉化率增加,但是由于活性物種的形成除了與TPP質量濃度有關外,還與反應體系中CO和H2質量濃度有關,由于在提高催化劑質量濃度時反應體系中CO和H2質量濃度沒有相應增高,故只有與CO和H2質量濃度相匹配的部分催化劑量才真正具有催化活性,而其他催化劑不具有催化能力。當這些不具有催化活性的催化劑量的繼續增加,反應體系中TPP的質量濃度也同比例升高,此時對具有催化活性的絡合物質量濃度的影響相當于TPP質量濃度提高的效果,使催化劑絡合物平衡向生成絡合物A方向移動,降低了1-丁烯的轉化率。參照實驗數據,選擇催化劑質量濃度為300~350 mg/L。
2.4 1-丁烯用量對反應的影響
對作為原料1-丁烯用量的考察,實際是評價催化劑的反應速率以及反應體系中催化劑、原料、CO和H2相互之間的比例合適與否,為此在溫度為100 ℃,時間為1 h,攪拌速度為200 r/min,催化劑質量濃度為200 mg/L,膦/銠物質的量比為200,反應壓力為2.2 MPa和合成氣中H2與CO體積比為1∶1的條件下,對一定量催化劑與1-丁烯用量之間的關系進行研究,結果如圖4所示。

圖4 1-丁烯用量對氫甲酰化反應的影響
從圖4中可以看到:隨著1-丁烯用量增加,1-丁烯的轉化率出現下降而產物的正異比卻呈上升的趨勢,而且上升的趨勢比較明顯。在1-丁烯用量增大時,催化劑用量并沒有隨之增多,因此催化劑質量濃度也表現為逐漸降低,從動力學反應速率角度可以很好地解釋反應轉化率降低的原因所在。正異比升高與1-丁烯的轉化率有關,在1-丁烯轉化率較低時,正異比都較高,而在轉化率較高時,正異比則較低。發生這種現象的原因可能是生成正戊醛和異戊醛濃度對反應的熱力學平衡影響以及因為生成正戊醛的活化能低于異戊醛活化能,使得生成正戊醛速率更快。
2.5 反應時間對反應的影響
反應時間是催化劑反應速率的表征。它對反應的轉化率、正異比有著非常重要的影響。在1-丁烯氫甲酰化反應中主反應為生成正戊醛和異戊醛兩個平行反應,生成正戊醛所需的活化能要低于生成異戊醛所需的活化能。因此在1-丁烯氫甲酰化反應時,在生成正戊醛的同時,不可避免會生成一部分異戊醛,而且隨著時間的延長,正戊醛和異戊醛之比也會逐漸降低,為此在溫度為100 ℃,攪拌速度為200 r/min,催化劑質量濃度為200 mg/L,膦/銠物質的量比為200,反應壓力為2.2 MPa和合成氣中H2與CO體積比為1∶1的條件下,考察了不同時間下的反應結果(見圖5)。

圖5 反應時間對氫甲酰化反應的影響
從圖5中可以看出:隨著反應時間的延長,1-丁烯的轉化率不斷提高,反應產物的正異比卻顯著下降,因此反應時間不宜過長,控制在30 min以內為好。
2.6 反應壓力對反應的影響
反應壓力決定反應體系中CO和H2的質量濃度,而CO質量濃度可顯著影響催化劑平衡中各絡合物的濃度。當CO質量濃度較高時,有利于氫甲酰化催化活性更高的絡合物C和D生成,可提高1-丁烯的轉化率,而對目標產物正戊醛的生成只有負面效應。為了考察壓力對氫甲酰化反應的影響,在溫度為100 ℃,反應時間1 h,攪拌速度為200 r/min,催化劑質量濃度為200 mg/L,膦/銠物質的量比為200,合成氣中H2與CO體積比為1∶1的條件下,考察不同壓力下的氫甲酰化反應(見圖6)。
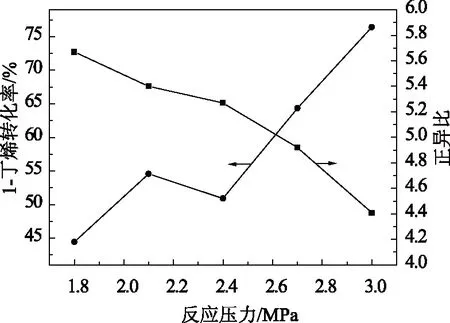
圖6 反應壓力對氫甲酰化反應的影響
從圖6可以看出:1-丁烯的轉化率隨著壓力的升高而逐漸提高,但正異比卻表現出明顯的下降趨勢。綜合考慮1-丁烯的飽和蒸汽壓、反應的轉化率以及正異比,反應壓力為1.8~2.0 MPa是比較適宜的。
2.7 反應溫度對反應的影響
對于一個反應而言,反應溫度是一個重要的考察因素。催化劑能否達到最佳催化活性,反應能否達到最佳的效果,主要依賴于反應溫度。反應溫度過低,催化劑未達到最佳的催化活性,致使反應速率降低,反應效果不好;反應溫度過高,一方面可能會導致反應會向副反應的方向發展,造成選擇性降低,另一方面溫度也會影響催化劑的壽命,溫度過高可能會縮短催化劑的使用時間,甚至會造成催化劑的失活。因此,在反應時間為1 h,攪拌速度為200 r/min,催化劑質量濃度為200 mg/L,膦/銠物質的量比為200,反應壓力為2.2 MPa和合成氣中H2與CO體積比為1∶1的條件下,就溫度與氫甲酰化反應之間的關系進行了考察(見圖7)。
從圖7中可以看出:在低溫區1-丁烯的轉化率和產物正異比均隨著溫度的升高而增大并達到峰值,之后,當溫度繼續升高,卻趨于下降。反應存在較為合適的溫度區間為100~105 ℃。這一現象可以由動力學中溫度對反應活化能、反應速率的影響和在溫度升高時,為了保持反應起始壓力的恒定,只能通過少加入合成氣來實現,而由此會降低反應液中CO濃度并降低反應速率。

圖7 反應溫度對氫甲酰化反應的影響
2.8 轉速對反應的影響
1-丁烯的氫甲酰化反應為氣-液兩相反應,反應速率除了與催化活性中心的性能有關外,還要考慮兩相間的傳質,而攪拌速率主要解決傳質對反應的影響,為此在溫度為100 ℃,時間為1 h,催化劑質量濃度為200 mg/L,膦/銠物質的量比為200,反應壓力為2.2 MPa,合成氣中H2與CO體積比為1∶1時,考察攪拌速率對于氫甲酰化反應的影響(見圖8)。

圖8 攪拌速率對氫甲酰化反應的影響
從圖8中可以看出:隨著轉速的提高,1-丁烯的轉化率逐漸增加,當轉速超過200 r/min后,繼續提高攪拌速率對1-丁烯的轉化率影響不大。
3 結論
(1)從工業角度考慮,采用產物正戊醛、異戊醛作為反應溶劑,可以降低后續分離的復雜性,選用較高的催化劑質量濃度以及較高的膦/銠物質的量比,既保證反應速率,又能得到較高的正異構比,實驗結果顯示,醛的正異構比可達到8~10。
(2)以三苯基膦乙酰丙酮羰基銠為催化劑,TPP為配體,采用均相催化體系考察1-丁烯的氫甲酰化反應效果。實驗結果表明適宜的工藝條件為:反應溫度102 ℃,反應壓力2.2 MPa,攪拌速率250 r/min,反應時間30 min,催化劑質量濃度300~350 mg/L,膦/銠物質的量比400~500。
[1] 歐文華,鄭佩莉,黃超,等.二氫茉莉酮酸甲酯的合成進展[J].香料香精化妝品,2007(3):24-32.
[2] 陳兆剛,張強華,林祥.二氫茉莉酮酸甲酯的合成研究[J].香料香精化妝品,2010(1):6-8.
[3] 肖艷,左杰,田紹友,等.混合丁烯羰基合成戊醛[J].石油化工,2015,44(8):912-918.
[4] 陳華,黎耀忠,程溥明,等.水溶性麟配體的合成方法[J],分子催化,1999,13(2):151-58.
[5] 王勝國,房德仁,李海洋,等.烯烴氫甲酰化反應的催化技術進展[J].化工時刊,2000(3):6-11.
[6] 王金梅,陳革新,趙培慶,等.丁烯氫甲酰化制戊醛分離工藝的模擬與優化[J].現代化工,2010,30(增刊1):11-14.
Study on the Synthesis of n-Pentanal
Chang Hui,Ye Junming,Sun Jun,Qu Weiguo,Fang Ling,Lu Xin
(FineChemicalDivision,SINOPECShanghaiPetrochemicalCo.,Ltd.,Shanghai200540)
The hydroformylation process for preparation of pentanal with 1-butene and synthesis gas as raw material was studied.Based on the thermodynamic calculation,the effects of Phosphine Rhodium ratio(molar ratio),catalyst concentration,butene dosage,reaction temperature,time,pressure,and stirring speed on 1-butene hydroformylation in the homogeneous catalytic system were studied.In the conditions of keeping high 1-butene conversion rate and high pentanal selectivity,the appropriate process conditions are:reaction temperature 100 ℃,reaction pressure 2.2 MPa,the stirring rate 250 r/min,the reaction time 30 min,the mass concentration of catalyst 300~350 mg/L,Phosphine Rhodium ratio 400~500.
1-butene,homogeneous catalysis,n-pentanal,hydroformylation
2017-05-02。
常慧,女,1976年出生,2003年畢業于中科院山西煤炭化學研究所,高級工程師,現從事精細化工研究工作。
1674-1099 (2017)03-0017-05
TQ224.12
A

