前列腺癌根治性外放療后患者生化復(fù)發(fā)的相關(guān)因素分析
萬福慶,劉秉乾,武玉東
(1.周口市中心醫(yī)院泌尿外科,河南 周口 466000;2.鄭州大學(xué)第一附屬醫(yī)院泌尿外科,河南 鄭州 450052)
前列腺癌根治性外放療后患者生化復(fù)發(fā)的相關(guān)因素分析
萬福慶1,劉秉乾2,武玉東2
(1.周口市中心醫(yī)院泌尿外科,河南 周口 466000;2.鄭州大學(xué)第一附屬醫(yī)院泌尿外科,河南 鄭州 450052)
目的 探討前列腺癌根治性外放療(EBRT)后患者生化復(fù)發(fā)(BCR)的相關(guān)危險(xiǎn)因素。方法 對接受EBRT的243例局限性前列腺癌患者的臨床病理資料進(jìn)行回顧性分析。記錄患者年齡、體質(zhì)量指數(shù)(BMI)、Gleason評分、臨床分期、前列腺體積、腫瘤體積、初始前列腺特異抗原(PSA)及PSA最低值、照射劑量、糖尿病、冠心病等參數(shù)以及BCR情況。根據(jù)是否出現(xiàn)BCR將患者分為復(fù)發(fā)組和非復(fù)發(fā)組。分別采用單因素分析和COX回歸模型進(jìn)行統(tǒng)計(jì)分析。結(jié)果 復(fù)發(fā)組患者術(shù)前PSA值、PSA最低值、Gleason評分、腫瘤體積、照射劑量[(38.8±70.1)ng·mL-1、(5.1±2.1)ng·mL-1、(7.6±2.1)分、(2.0±0.5)mL、(65.3±5.6)Gy]均高于非復(fù)發(fā)組[(32.2±58.5)ng·mL-1、(3.1±1.2)ng·mL-1、(5.9±1.7)分、(2.4±0.9)mL、(62.8±7.8)Gy],差異均有統(tǒng)計(jì)學(xué)意義(P均<0.05)。COX回歸分析顯示術(shù)前PSA值、Gleason評分及PSA最低值是根治性EBRT術(shù)后發(fā)生BCR的危險(xiǎn)因素(P<0.05)。結(jié)論 術(shù)前PSA值、Gleason評分及PSA最低值是局限性前列腺癌患者接受根治性EBRT術(shù)后發(fā)生BCR的主要危險(xiǎn)因素。
前列腺癌;根治性外放療;生化復(fù)發(fā)
前列腺癌根治性外放療(external beam radiotherapy,EBRT)因療效好、并發(fā)癥少等優(yōu)點(diǎn)得到了廣泛應(yīng)用[1]。EBRT后仍有患者出現(xiàn)生化復(fù)發(fā)(bichemical recurrence,BCR),BCR后臨床復(fù)發(fā)不可避免,為提高EBRT的療效,延長無BCR生存率,EBRT后影響B(tài)CR的相關(guān)因素是目前前列腺癌治療研究的熱點(diǎn)之一。雖然已有文獻(xiàn)對EBRT后影響B(tài)CR的因素進(jìn)行了報(bào)道,但是相關(guān)研究的樣本均較小,且隨訪時(shí)間較短,不同作者的研究結(jié)果并不一致。本研究對243例接受EBRT治療的局限性前列腺癌患者的臨床資料進(jìn)行了分析,旨在探討影響EBRT后BCR的相關(guān)因素,為臨床診治提供參考依據(jù)。
1 資料與方法
1.1 臨床資料 收集2008年1月至2014年5月在周口市中心醫(yī)院和鄭州大學(xué)第一附屬醫(yī)院泌尿外科及放療科接受EBRT的243例局限性前列腺癌患者,年齡51~75(66.1±7.5)歲;體質(zhì)量指數(shù)(body mass index ,BMI)為15.9~35.6(24.1±3.9)kg·m-2;術(shù)前前列腺特異抗原(prostate specific antigen,PSA)為5.8~568.9 ng·mL-1。所有患者均經(jīng)前列腺穿刺活檢病理證實(shí),經(jīng)骨掃描、盆腔MRI及胸片等影像學(xué)檢查選取臨床分期為T1~2N0M0的患者,所有患者EBRT治療前、治療中及隨訪過程中均未接受其他針對前列腺的治療。
1.2 方法
1.2.1 EBRT方案 所有患者均接收常規(guī)放療。應(yīng)用薄層螺旋CT掃描,繪制放療靶區(qū)同時(shí)建立數(shù)字重建3D模型,放療醫(yī)生根據(jù)3D模型設(shè)計(jì)放射劑量分布方案。每日照射劑量1.6~2.0Gy,每周5次,總劑量根據(jù)腫瘤體積決定,一般60~70 Gy。
1.2.2 隨訪 EBRT結(jié)束后3個(gè)月內(nèi)每月復(fù)查、3個(gè)月之后每3個(gè)月復(fù)查1次PSA。若PSA出現(xiàn)3次連續(xù)升高則進(jìn)行骨掃描、盆腔MRI、胸片等影像學(xué)檢查。以BCR作為隨訪終點(diǎn)。BCR的定義:EBRT后PSA值高于最低點(diǎn)2 ng·mL-1。
1.3 觀察指標(biāo) 記錄患者年齡、BMI、Gleason評分、臨床分期、前列腺體積、腫瘤體積、初始PSA及PSA最低值、照射劑量、糖尿病、冠心病等參數(shù)以及BCR情況。根據(jù)是否出現(xiàn)BCR將患者分為復(fù)發(fā)組和非復(fù)發(fā)組。
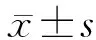
2 結(jié)果
2.1 2組患者之間相關(guān)病理參數(shù)的比較 所有患者隨訪15~72(21.9±10.5)個(gè)月。全組出現(xiàn)BCR患者93例,其中術(shù)后1 a出現(xiàn)BCR患者18例(7.4%),術(shù)后2 a出現(xiàn)BCR患者48例(19.8%),術(shù)后3 a出現(xiàn)BCR患者74例(30.5%),其3 a無BCR生存率為69.5%。
復(fù)發(fā)組患者術(shù)前PSA值、Gleason評分、腫瘤體積、照射劑量及PSA最低值高于非復(fù)發(fā)組,差異均有統(tǒng)計(jì)學(xué)意義(P均<0.05)。見表1。
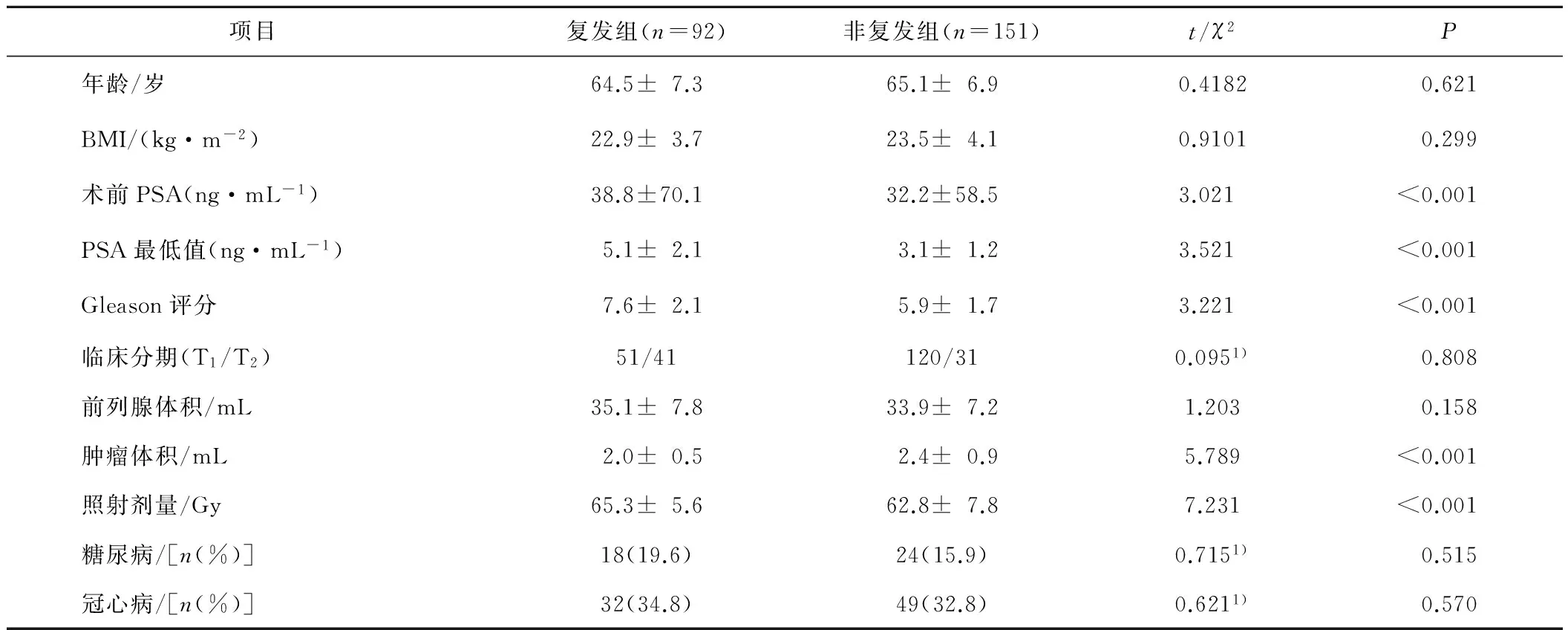
表1 2組前列腺癌患者臨床病理參數(shù)比較
注:1)為χ2
2.2 影響EBRT患者預(yù)后因素的多因素分析 COX回歸分析結(jié)果表明術(shù)前PSA值、Gleason評分及PSA最低值是根治性EBRT術(shù)后發(fā)生BCR的危險(xiǎn)因素(P<0.05)。見表2。
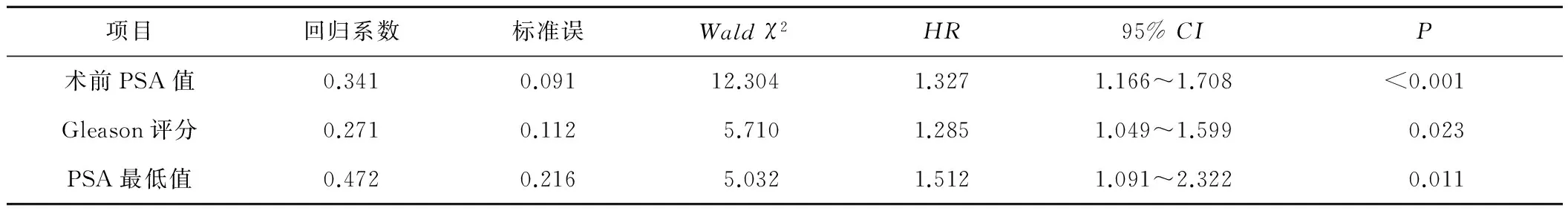
表2 COX回歸多因素分析結(jié)果
3 討論
由于新型藥物的應(yīng)用、醫(yī)療器械的更新以及手術(shù)技術(shù)的進(jìn)步,局限性前列腺癌的治療方式較多,各種方式互有優(yōu)劣。內(nèi)分泌治療并發(fā)癥少,但是不能根治前列腺癌,最終不可避免發(fā)展到激素抵抗階段;根治性手術(shù)雖可徹底治療,但是手術(shù)創(chuàng)傷重、學(xué)習(xí)曲線長,不易基層廣泛開展;EBRT適應(yīng)證廣、并發(fā)癥少,目前已廣泛應(yīng)用于臨床[2-4]。BCR對預(yù)測前列腺癌患者的生存時(shí)間具有重要意義,國外已有較多文獻(xiàn)對EBRT術(shù)后BCR的相關(guān)因素進(jìn)行報(bào)道,但是國內(nèi)相關(guān)研究較少。
對EBRT術(shù)后前列腺癌患者發(fā)生BCR的狀況目前尚未達(dá)成一致。目前已有報(bào)道稱EBRT術(shù)后3 a無BCR率為72%~90%[5],本研究對243例局限性前列腺癌患者進(jìn)行了15~72個(gè)月的隨訪,發(fā)現(xiàn)3 a無BCR生存率為69.5%。本研究的無BCR生存率低于文獻(xiàn)報(bào)道的數(shù)據(jù),可能原因是我國前列腺癌的EBRT起步較晚,經(jīng)驗(yàn)有待積累,早期患者腫瘤的臨床分期偏高、或由于不同種族的前列腺癌細(xì)胞對放射線的敏感性不同所致。
已有相關(guān)報(bào)道指出術(shù)前PSA值、Gleason評分、臨床分期及PSA最低值是EBRT術(shù)后發(fā)生BCR的危險(xiǎn)因素,EBRT術(shù)后BCR發(fā)生率與年齡、BMI、前列腺體積、腫瘤體積、照射劑量、糖尿病及冠心病等因素?zé)o關(guān)。國內(nèi)有研究對BCR的相關(guān)因素進(jìn)行單因素分析后發(fā)現(xiàn),術(shù)前PSA值、Gleason評分、照射劑量、腫瘤體積、臨床分期及PSA最低值與前列腺癌患者EBRT術(shù)后BCR密切相關(guān)[6]。我們通過分析本組患者數(shù)據(jù)發(fā)現(xiàn),復(fù)發(fā)組患者術(shù)前PSA值、Gleason評分、腫瘤體積、照射劑量及PSA最低值高于非復(fù)發(fā)組,但2組患者年齡、BMI、臨床分期、前列腺體積、腫瘤體積、照射劑量、糖尿病及冠心病發(fā)病率相近。為排除單因素分析時(shí)各參數(shù)之間相互影響,我們進(jìn)一步采用COX多因素回歸分析評估上述危險(xiǎn)因素,結(jié)果顯示,術(shù)前PSA值、Gleason評分、臨床分期及PSA最低值等因素是前列腺癌患者接受EBRT后發(fā)生BCR的獨(dú)立危險(xiǎn)因素。
需要指出的是前列腺癌患者出現(xiàn)BCR并不表示此后一定出現(xiàn)臨床復(fù)發(fā)或腫瘤特異性死亡,若患者僅出現(xiàn)BCR而無原位腫瘤增大或轉(zhuǎn)移,僅能代表殘留的前列腺細(xì)胞有活性。為明確前列腺癌患者的預(yù)后決定因素,我們需要更長時(shí)間的隨訪以及更大樣本的研究。
[1] 駱華春,程惠華,傅志超,等.小靶區(qū)調(diào)強(qiáng)放療治療前列腺癌的臨床療效觀察[J].臨床腫瘤學(xué)雜志,2016,21(11):1019-1023.
[2] Ceder JA.Targeting the mechanisms of progression in castration-resistant prostate cancer[J].Eur Urol,2015,67(3):480-481.
[3] Cooperberg MR.Progress in management of low-risk prostate cancer: how registries may change the world[J].Eur Urol,2015,67(1):51-52.
[4] Sridhar SS,Freedland SJ,Gleave ME,et al.Castration-resistant prostate cancer: from new pathophysiology to new treatment[J].Eur Urol,2014,65(2):289-299.
[5] Nepple KG,Stephenson AJ,Kallogjeri D,et al.Mortality after prostate cancer treatment with radical prostatectomy,external-beam radiation therapy,or brachytherapy in men without comorbidity[J].Eur Urol,2013,64(3):372-378.
[6] 嚴(yán)維剛,陳健,周毅,等.前列腺癌近距離照射治療后生化復(fù)發(fā)的危險(xiǎn)因素分析[J].中華泌尿外科雜志,2014,35(10):762-766.
河南省醫(yī)學(xué)科技攻關(guān)項(xiàng)目(編號:201602014)
萬福慶(1983-),男,碩士,主治醫(yī)師,主要從事前列腺癌的臨床研究。E-mail:yszhou9510@163.com
劉秉乾(1976 -),男,博士,主任醫(yī)師,主要從事前列腺癌發(fā)病機(jī)制的研究。E-mail:yszhou9510@163.com
10.3969/j.issn.1673-5412.2017.03.019
R737.25;R730.55
B
1673-5412(2017)03-0237-03
2017-01-12)

