α-硫辛酸對(duì)帕金森病大鼠腦內(nèi)黑質(zhì)多巴胺能神經(jīng)元保護(hù)機(jī)制研究
吳艷芬 陳文 王鳴飛 王偉
·論著·
α-硫辛酸對(duì)帕金森病大鼠腦內(nèi)黑質(zhì)多巴胺能神經(jīng)元保護(hù)機(jī)制研究
吳艷芬 陳文 王鳴飛 王偉
目的 探討α-硫辛酸(LA)對(duì)帕金森病(PD)大鼠模型腦內(nèi)黑質(zhì)多巴胺能神經(jīng)元的保護(hù)機(jī)制。方法 60只3月齡雄性Wistar大鼠隨機(jī)分為對(duì)照組、實(shí)驗(yàn)組和藥物干預(yù)組,每組20只。對(duì)照組大鼠給予背部皮下注射葵花油,實(shí)驗(yàn)組和藥物干預(yù)組背部皮下注射魚藤酮制備PD模型,藥物干預(yù)組大鼠同時(shí)給予LA腹腔注射;采用Western blot檢測(cè)大鼠中腦多巴胺能神經(jīng)元中酪氨酸羥化酶(TH)、轉(zhuǎn)錄因子NF-E2相關(guān)因子-抗氧化反應(yīng)元件(Nrf2-ARE)和血紅素氧合酶1(HO-1)的表達(dá)變化;采用分光光度法檢測(cè)大鼠腦內(nèi)紋狀體中丙二醛(MDA)和還原型谷胱甘肽(GSH)含量變化。結(jié)果 實(shí)驗(yàn)組大鼠中腦TH蛋白表達(dá)比對(duì)照組明顯降低(P<0.05);藥物干預(yù)組中腦TH蛋白在黑質(zhì)比魚藤酮組明顯增高(P<0.05),但是較對(duì)照組仍有明顯減少(P<0.05)。實(shí)驗(yàn)組大鼠Nrf2和HO-1蛋白表達(dá)比對(duì)照組明顯降低(P<0.05);藥物干預(yù)組Nrf2和HO-1蛋白表達(dá)比實(shí)驗(yàn)組明顯增高(P<0.05),但是較對(duì)照組仍有明顯降低(P<0.05)。與對(duì)照組相比,實(shí)驗(yàn)組大鼠紋狀體組織中脂質(zhì)代謝產(chǎn)物MDA含量明顯增加(P<0.01),藥物干預(yù)后紋狀體中MDA含量明顯減少(P<0.05),但較對(duì)照組仍明顯增高(P<0.05)。與對(duì)照組相比,實(shí)驗(yàn)組大鼠GSH的含量明顯減少(P<0.01),藥物干預(yù)后GSH明顯增加(P<0.05),但較對(duì)照組仍顯著降低(P<0.05)。結(jié)論 LA能激活Nrf2-ARE信號(hào)通路對(duì)PD大鼠模型中腦多巴胺能神經(jīng)元起到有效的神經(jīng)保護(hù)作用,改善PD樣癥狀。
帕金森病;α-硫辛酸;氧化應(yīng)激;轉(zhuǎn)錄因子NF-E2相關(guān)因子-抗氧化反應(yīng)元件;血紅素氧合酶1
帕金森病(parkinson’s disease,PD)是一種中老年人常見的神經(jīng)退行性疾病,其主要病理改變?yōu)橹心X黑質(zhì)多巴胺能神經(jīng)元的胞體內(nèi)嗜酸性包涵體形成及其變性壞死,從而導(dǎo)致腦內(nèi)多巴胺能神經(jīng)遞質(zhì)含量減少,臨床表現(xiàn)為靜止性震顫、運(yùn)動(dòng)遲緩和肌張力增高等癥狀[1]。目前PD確切的病因和發(fā)病機(jī)制尚不明確,遺傳因素、環(huán)境因素、年齡老化、氧化應(yīng)激等均可能參與PD患者腦內(nèi)多巴胺能神經(jīng)元的變性死亡過(guò)程。PD在臨床的治療中還沒(méi)有特效藥物,多為外源性補(bǔ)充多巴胺能藥物延緩病情惡化,但由于長(zhǎng)期用藥導(dǎo)致自身對(duì)多巴胺制劑敏感性降低、毒副作用不能耐受等原因,使患者不得不減少藥物服用劑量或終止治療[2-4]。因此,尋找能夠有效保護(hù)PD患者腦內(nèi)多巴胺能神經(jīng)元的藥物,提高藥物治療的安全性是當(dāng)前亟待解決的科學(xué)難題。氧化應(yīng)激是指體內(nèi)的抗氧化能力減弱,導(dǎo)致體內(nèi)的自由基過(guò)度蓄積,從而對(duì)機(jī)體產(chǎn)生一系列的負(fù)面作用,被認(rèn)為是導(dǎo)致衰老和疾病的一個(gè)重要因素。氧化應(yīng)激可在多個(gè)環(huán)節(jié)參與腦內(nèi)黑質(zhì)多巴胺能神經(jīng)元的損傷。因此,阻止氧化損傷及其誘導(dǎo)的一系列級(jí)聯(lián)反應(yīng)很可能成為治療PD極具前景的有效方法[5]。轉(zhuǎn)錄因子NF-E2相關(guān)因子(transcription factor NF-E2-related factor,Nrf2)通過(guò)與抗氧化反應(yīng)元件(antioxident response element,ARE)結(jié)合誘導(dǎo)多種內(nèi)源性多種抗氧化酶、Ⅱ相解毒酶表達(dá)上調(diào),是細(xì)胞氧化應(yīng)激反應(yīng)中的關(guān)鍵因子,具有提高機(jī)體的抗氧化和解毒能力。其中,Nrf2-ARE 信號(hào)通路誘導(dǎo)的內(nèi)源性保護(hù)基因血紅素氧合酶1(heme oxygenase-1,HO-1)在抗氧化損傷方面起著重要作用[6,7]。Nrf2-ARE信號(hào)通路是機(jī)體內(nèi)最為重要的內(nèi)源性抗氧化損傷通路之一。α-硫辛酸(LA)又名1,2-二硫戊環(huán)-3-戊酸,是1937年在馬鈴薯中發(fā)現(xiàn)的一種B 族維生素,由于其具有強(qiáng)大的抗氧化能力,被譽(yù)為“萬(wàn)能抗氧劑”[8]。本研究探討LA對(duì)PD大鼠模型腦內(nèi)多巴胺能神經(jīng)元保護(hù)作用及其機(jī)制,為帕金森病的治療提供新的思路。
1 材料與方法
1.1 實(shí)驗(yàn)動(dòng)物及分組 12周齡雄性Witstar 大鼠60只,體重(300±20)g,由河北醫(yī)科大學(xué)實(shí)驗(yàn)動(dòng)物中心提供(合格證號(hào):SCXK冀2008-1-003)。將實(shí)驗(yàn)大鼠隨機(jī)分為對(duì)照組、實(shí)驗(yàn)組和藥物干預(yù)組,每組20只。所有大鼠在同一實(shí)驗(yàn)室按照清潔級(jí)標(biāo)準(zhǔn)飼養(yǎng),期間所有大鼠自由進(jìn)食進(jìn)水,房間保持穩(wěn)定的溫度(24℃)和濕度(40%)。
1.2 動(dòng)物模型的制備及藥物干預(yù) 對(duì)照組大鼠給予背部皮下注射葵花油1 ml·kg-1·d-1,實(shí)驗(yàn)組和藥物干預(yù)組大鼠按照2.0 mg·kg-1·d-1背部皮下注射魚藤酮(魚藤酮溶解在葵花籽油中充分震蕩混勻),藥物干預(yù)組大鼠在魚藤酮注射前半小時(shí)給予LA 20 mg·kg-1·d-1腹腔注射,共30 d。
1.3 實(shí)驗(yàn)動(dòng)物的取材及組織勻漿制備 每組各取8只大鼠斷頭處死,在冰板上分離中腦和紋狀體液氮速凍后,-80℃保存?zhèn)溆谩驖{制備時(shí),取紋狀體和中腦稱重,放入勻漿器,按1∶9(組織重量與裂解液體積比)比例加入RIPA裂解液,勻漿器放在冰浴中,超聲勻漿器以2 000 r/min勻漿20次,然后吸至1 ml離心管中。4℃放置30 min。低溫離心10 000 g,30 min。小心吸出上清分裝,-80℃儲(chǔ)存?zhèn)溆谩?/p>
1.4 蛋白濃度的測(cè)定(BCA 法) 蛋白濃度的測(cè)定按照BCA蛋白測(cè)定試劑盒說(shuō)明書上的步驟,取一酶標(biāo)板,各孔加入 200 μl BCA 工作液,取稀釋樣品 10 μl加入各孔中,在振蕩器上將各酶版孔中的液體混勻,將酶標(biāo)儀開機(jī)問(wèn)題調(diào)至37℃,將酶標(biāo)版放入30 min,然后562 nm下比色測(cè)定。并根據(jù)所測(cè)樣品的吸光值,在標(biāo)準(zhǔn)曲線上即可查到相應(yīng)蛋白含量(μg)/樣品稀釋液總體積(10 μl)×樣品稀釋倍數(shù)即為樣品實(shí)際濃度(μg/μl)。
1.5 Western blot 取各組實(shí)驗(yàn)大鼠腦組織勻漿樣品50 μg總蛋白常規(guī)變性后自然冷卻,經(jīng)10% SDS-PAGE凝膠電泳分離,電泳轉(zhuǎn)移至NC膜上,用5%脫脂奶粉室溫封閉2 h后,加入抗體稀釋液稀釋的兔TH單克隆抗體(1∶5 000,Sigma)、兔Nrf2和HO-1單克隆抗體(1∶1 000,Abcom),4℃過(guò)夜。NC膜以TTBS洗3次。羊抗兔IgG 熒光抗體(1∶2 000,Rocland 公司)室溫避光1 h,TTBS漂洗5 次,遠(yuǎn)紅外熒光掃描成像系統(tǒng)掃描并測(cè)定目標(biāo)蛋白光密度值,所得值與Actin (1∶5 000,Santa Cruz)蛋白的光密度值比值后,做統(tǒng)計(jì)學(xué)分析。
1.6 分光光度法檢測(cè)腦組織丙二醛(MDA)和谷胱甘肽(GSH)的含量測(cè)定 取大鼠紋狀體腦組織,在4℃RIPA裂解液勻漿, 低溫離心10 000 g 30 min,取上清,BCA法測(cè)定蛋白濃度。具體檢測(cè)MDA和GSH的實(shí)驗(yàn)方法按所購(gòu)試劑盒說(shuō)明書進(jìn)行。
2 結(jié)果
2.1 一般狀況 與對(duì)照組相比,實(shí)驗(yàn)組大鼠毛色變黃變臟,體態(tài)呈弓背屈曲狀、主動(dòng)活動(dòng)減少、動(dòng)作遲緩、行走時(shí)多向一側(cè)旋轉(zhuǎn)。實(shí)驗(yàn)組大鼠在第10、13、15、19天時(shí)各死亡1只,藥物干預(yù)組大鼠腹腔注射LA后上述癥狀有明顯改善,在另第13、14天時(shí)各死亡1只。
2.2 Western blot實(shí)驗(yàn)結(jié)果
2.2.1 TH在大鼠中腦黑質(zhì)多巴胺能神經(jīng)元中的表達(dá)改變:實(shí)驗(yàn)組大鼠中腦TH蛋白表達(dá)比對(duì)照組明顯降低(P<0.05);藥物干預(yù)組中腦TH蛋白在黑質(zhì)比魚藤酮組明顯增高(P<0.05),但是較對(duì)照組仍有明顯減少(P<0.05)。見圖1,表1。
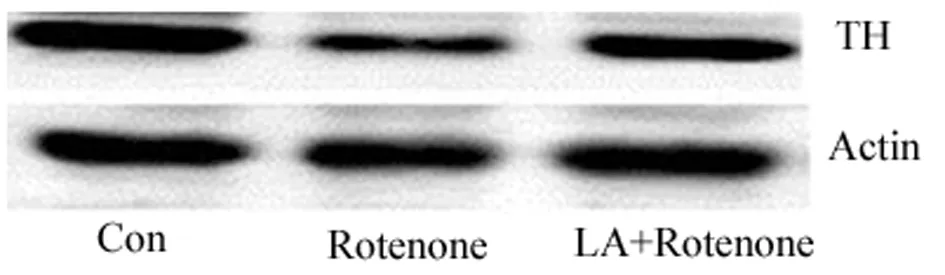
圖1 TH蛋白在各組大鼠中腦黑質(zhì)中的表達(dá)
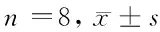
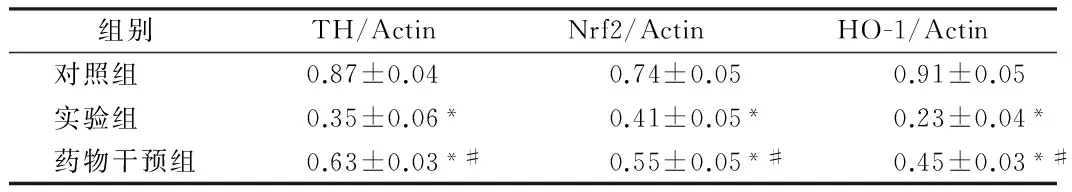
組別TH/ActinNrf2/ActinHO-1/Actin對(duì)照組 0.87±0.040.74±0.050.91±0.05實(shí)驗(yàn)組 0.35±0.06*0.41±0.05*0.23±0.04*藥物干預(yù)組0.63±0.03*#0.55±0.05*#0.45±0.03*#
注:與對(duì)照組比較,*P<0.05;與實(shí)驗(yàn)組比較,#P<0.05
2.2.2 Nrf2和HO-1在大鼠中腦黑質(zhì)多巴胺能神經(jīng)元中的表達(dá)改變:實(shí)驗(yàn)組大鼠Nrf2和HO-1蛋白表達(dá)比對(duì)照組明顯降低(P<0.05);藥物干預(yù)組Nrf2和HO-1蛋白表達(dá)比實(shí)驗(yàn)組明顯增高(P<0.05),但是較對(duì)照組仍有明顯降低(P<0.05)。見圖2,表1。

圖2 Nrf2和HO-1蛋白在3組大鼠中腦黑質(zhì)中的表達(dá)
2.3 大鼠紋狀體中氧化應(yīng)激參數(shù)的改變 與對(duì)照組相比,實(shí)驗(yàn)組大鼠紋狀體組織中脂質(zhì)代謝產(chǎn)物MDA含量明顯增加(P<0.01),藥物干預(yù)后紋狀體中MDA含量明顯減少(P<0.05),但較對(duì)照組仍明顯增高(P<0.05)。與對(duì)照組相比,實(shí)驗(yàn)組大鼠GSH的含量明顯減少(P<0.01),藥物干預(yù)后GSH明顯增加(P<0.05),但較對(duì)照組仍顯著降低(P<0.05)。見表2。
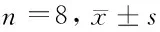

組別MDA(nmol/mgprot)GSH(mg/gprot)對(duì)照組 6.21±1.5558.73±4.58實(shí)驗(yàn)組 22.13±2.04*31.40±2.61*藥物干預(yù)組13.25±2.21*#42.46±2.11*#
注:與對(duì)照組比較,*P<0.05;與實(shí)驗(yàn)組比較,#P<0.05
3 討論
PD的特征性病理改變是黑質(zhì)內(nèi)多巴胺能神經(jīng)元受損,導(dǎo)致腦內(nèi)多巴胺能神經(jīng)遞質(zhì)含量減少,從而臨床表現(xiàn)為運(yùn)動(dòng)障礙為主的臨床綜合征。PD發(fā)病后病情進(jìn)展迅速,到疾病晚期患者的生活不能自理,完全需要家人護(hù)理和照顧,給家庭和社會(huì)帶來(lái)了沉重的經(jīng)濟(jì)負(fù)擔(dān)。隨著中國(guó)人口老齡化的到來(lái),PD的發(fā)病率也逐年增加,目前還沒(méi)有特效藥物能治療該病,臨床上的藥物多為暫時(shí)緩解患者的癥狀,但是不能有效逆轉(zhuǎn)中腦黑質(zhì)多巴胺能神經(jīng)元的損傷,隨著患者病情加重,藥物還會(huì)引起患者出現(xiàn)異動(dòng)癥和癥狀波動(dòng)等不良反應(yīng),隨著治療時(shí)間的延長(zhǎng),患者對(duì)藥物的療效會(huì)越來(lái)越差[10]。所以,尋找PD的病因和治療藥物是擺在廣大科研工作者面前的重大難題。
關(guān)于PD的病因和發(fā)病機(jī)制在神經(jīng)科學(xué)界近年開展了大量的科學(xué)研究。研究發(fā)現(xiàn),PD的主要病因?yàn)榧易暹z傳因素和外界環(huán)境毒素的接觸,其中環(huán)境因素在PD發(fā)病過(guò)程中的作用越來(lái)越受到醫(yī)學(xué)科研工作者的重視[11]。魚藤酮為脂溶性,可透過(guò)血腦屏障進(jìn)入中樞神經(jīng)系統(tǒng),其進(jìn)入神經(jīng)系統(tǒng)后可以神經(jīng)元內(nèi)的線粒體電子傳遞脫氫酶結(jié)合并使其失去活性,導(dǎo)致神經(jīng)元對(duì)氧的利用障礙和能量產(chǎn)生不足,最終導(dǎo)致神經(jīng)元的凋亡和壞死。近年研究發(fā)現(xiàn),中腦黑質(zhì)多巴胺能神經(jīng)元對(duì)魚藤酮的毒性較敏感,魚藤酮進(jìn)入中樞神經(jīng)系統(tǒng)后可以特異性的對(duì)多巴胺能神經(jīng)元產(chǎn)生神經(jīng)毒性[12]。實(shí)驗(yàn)大鼠長(zhǎng)期慢性接觸魚藤酮后可以出現(xiàn)類PD樣癥狀,表現(xiàn)為活動(dòng)減少、行走時(shí)向一側(cè)旋轉(zhuǎn)等癥狀,病理研究后發(fā)現(xiàn)大鼠腦內(nèi)出現(xiàn)多巴胺能神經(jīng)元減少,同時(shí)在神經(jīng)元出現(xiàn)了PD特征性病理變化嗜酸性包涵小體以及腦內(nèi)紋狀體酪氨酸羥化酶(tyrosine hydroxylase,TH)的表達(dá)顯著降低。我們通過(guò)給予大鼠背部皮下注射魚藤酮后發(fā)現(xiàn),該藥物可以導(dǎo)致大鼠出現(xiàn)運(yùn)動(dòng)減少和行走時(shí)向一側(cè)旋轉(zhuǎn)等類帕金森樣癥狀,表明魚藤酮是制備PD動(dòng)物模型有效藥物,這與以往的研究結(jié)果一致。目前用于制備PD動(dòng)物模型的兩種毒性物質(zhì)六羥多巴(6-OHDA)和MPTP 均需多巴胺轉(zhuǎn)運(yùn)體將其攝取,選擇性地?fù)p傷腦內(nèi)的多巴胺能神經(jīng)元,從而導(dǎo)致實(shí)驗(yàn)動(dòng)物出現(xiàn)類PD樣癥狀。但實(shí)驗(yàn)動(dòng)物多巴胺能神經(jīng)元內(nèi)始終沒(méi)有嗜酸性包涵體的出現(xiàn)。然而,長(zhǎng)期慢性給予實(shí)驗(yàn)動(dòng)物魚藤酮可以損傷其腦內(nèi)的黑質(zhì)多巴胺能神經(jīng)元,同時(shí)在神經(jīng)元內(nèi)可有嗜酸性包涵小體形成,該動(dòng)物模型對(duì)左旋多巴藥物治療較為敏感[13]。以上的實(shí)驗(yàn)證據(jù)表明,魚藤酮所致的PD模型更接近自然發(fā)生的疾病狀態(tài);為PD的發(fā)病機(jī)制和治療藥物的篩選提供了較為適宜的動(dòng)物模型。
氧化應(yīng)激是指機(jī)體抗氧化能力減弱,產(chǎn)生大量氧自由基和氮自由基,過(guò)量的自由基可以對(duì)DNA和脂質(zhì)等產(chǎn)生不可逆性損傷,從而導(dǎo)致機(jī)體疾病發(fā)生。科學(xué)研究發(fā)現(xiàn),氧化應(yīng)激被認(rèn)為是導(dǎo)致衰老和疾病的一個(gè)重要因素。因此抗氧化損傷,減少腦內(nèi)氧自由基的蓄積應(yīng)是延緩疾病進(jìn)展的一條重要途徑[14]。
谷胱甘肽(GSH)是一種肽類化合物,由谷氨酸、半胱氨酸和甘氨酸三種氨基酸共價(jià)鍵結(jié)合而成,它是對(duì)機(jī)體保護(hù)的主要肽類物質(zhì)之一,能有效地和體內(nèi)的過(guò)氧化物及某些重金屬離子結(jié)合而降低其毒性,經(jīng)過(guò)機(jī)體的代謝將其排出體外,維持體內(nèi)的還原狀態(tài),是體內(nèi)重要的抗氧化劑和自由基清除劑[15]。因此機(jī)體內(nèi)GSH含量是衡量抗氧化能力的重要指標(biāo)。本實(shí)驗(yàn)中,魚藤酮背部皮下注射的大鼠腦內(nèi)紋狀體中GSH 含量顯著低于對(duì)照組,我們的結(jié)果表明,PD大鼠腦內(nèi)出現(xiàn)了氧化應(yīng)激狀態(tài),產(chǎn)生了大量的氧自由基,而自身的抗氧化能力下降,導(dǎo)致氧自由基堆積,造成神經(jīng)元的損傷。MDA 是機(jī)體內(nèi)脂質(zhì)發(fā)生過(guò)氧化反應(yīng)的終產(chǎn)物,具有較強(qiáng)的細(xì)胞毒性,能引起機(jī)體蛋白質(zhì)、DNA等交聯(lián)聚合,對(duì)機(jī)體產(chǎn)生不可逆性損傷。由于MDA 為氧化代謝產(chǎn)物,其再體內(nèi)的含量可以直接反映體內(nèi)脂質(zhì)過(guò)氧化程度和引起脂質(zhì)過(guò)氧化的自由基的水平[16]。本實(shí)驗(yàn)中,魚藤酮背部皮下注射的實(shí)驗(yàn)組大鼠腦內(nèi)MDA 含量明顯升高,提示在PD大鼠腦內(nèi)發(fā)生了氧化應(yīng)激反應(yīng),使脂質(zhì)過(guò)氧化過(guò)程增強(qiáng)。既往也有研究報(bào)道,PD患者腦內(nèi)發(fā)生了氧化應(yīng)激反應(yīng),可以損傷腦內(nèi)的多巴胺能神經(jīng)元[17],這與我們的研究結(jié)果一致。
LA是一種硫醇類化合物,眾多研究結(jié)果提示,LA具有強(qiáng)大的親電性和較強(qiáng)的清除活性氧的能力,抑制其對(duì)脂質(zhì)、蛋白質(zhì)和DNA 等生物大分子的損傷,抑制細(xì)胞氧化應(yīng)激,是機(jī)體理想的抗氧化劑。同時(shí),LA可保護(hù)機(jī)體免受各種有害因素的侵襲,包括解毒、抗炎及清除過(guò)量重金屬離子等。基于以上生物學(xué)特性,LA已廣泛應(yīng)用與臨床疾病的輔助治療,包括心血管疾病、認(rèn)知障礙性疾病、糖尿病等與氧化應(yīng)激和炎癥相關(guān)性疾病[18]。
Nrf2 是機(jī)體內(nèi)的一種重要的核轉(zhuǎn)錄因子,其本身的結(jié)構(gòu)為亮氨酸拉鏈,機(jī)體的正常情況下,Nrf2 的氨基端和Keap1 蛋白特異地結(jié)合,使Nrf2 的活性受到抑制,從而穩(wěn)定地存在細(xì)胞的胞漿內(nèi)。當(dāng)機(jī)體發(fā)生氧化應(yīng)激反應(yīng),產(chǎn)生過(guò)度的氧自由基可以作為誘導(dǎo)劑有效的導(dǎo)致Nrf2 磷酸化后與Keap1解離,解離后的Nrf2能夠進(jìn)入細(xì)胞核與抗氧化反應(yīng)元件(ARE)結(jié)合,從而誘導(dǎo)機(jī)體內(nèi)源性抗氧化酶、Ⅱ相解毒酶表達(dá)上調(diào),提高細(xì)胞的抗氧化和解毒能力,具有顯著細(xì)胞保護(hù)作用[19]。HO-1和NQO1為Nrf2-ARE結(jié)合后誘導(dǎo)產(chǎn)生的重要的抗氧化酶。研究證實(shí),在腦血管病、癲癇、癡呆和糖尿病周圍神經(jīng)病變等神經(jīng)系統(tǒng)疾病中上調(diào)Nrf2、HO-1或者NQO1的表達(dá)能起到神經(jīng)保護(hù)作用[20]。我們的前期研究發(fā)現(xiàn),PD大鼠模型腦組織中Nrf2、HO-1和NQO1的表達(dá)明顯降低[21],其受損程度和黑質(zhì)多巴胺能神經(jīng)元的表達(dá)呈正相關(guān)。本實(shí)驗(yàn)研究發(fā)現(xiàn),給予PD大鼠模型腹腔注射LA后能激活Nrf2-ARE通路,誘導(dǎo)其下游產(chǎn)物表達(dá)增強(qiáng),改善腦內(nèi)的氧化應(yīng)激狀態(tài),從而對(duì)黑質(zhì)多巴胺能神經(jīng)元起到保護(hù)作用。
本研究發(fā)現(xiàn),給予PD大鼠模型LA腹腔注射能有效激活Nrf2-ARE通路,使Nrf2進(jìn)入細(xì)胞核誘導(dǎo)其下游產(chǎn)物HO-1和NQO1表達(dá)增強(qiáng),改善腦內(nèi)的氧化應(yīng)激狀態(tài),可以對(duì)黑質(zhì)多巴胺能神經(jīng)元起到保護(hù)作用,從而改善PD大鼠模型的運(yùn)動(dòng)障礙癥狀。我們的研究證實(shí)氧化應(yīng)激損傷在PD患者的發(fā)病過(guò)程中指著重要的病理作用,抗氧化劑LA能有效地保護(hù)帕金森模型腦內(nèi)的多巴胺能神經(jīng)元,為PD的臨床治療提供了新的靶點(diǎn),同時(shí)為臨床藥物的選擇提供了新的思路。
1 Sveinbjornsdottir S.The clinical symptoms of Parkinson’s disease.J Neurochem,2016,139:318.
2 George S,Brundin P.Immunotherapy in Parkinson’s Disease:Micromanaging Alpha-Synuclein Aggregation.J Parkinsons Dis,2015,5:413-424.
3 Phillipson OT.Management of the aging risk factor for Parkinson’s disease.Neurobiol Aging,2014,35:847-857.
4 Hirsch EC.Future drug targets for Parkinson’s disease.Bull Acad Natl Med,2012,196:1369-1377.
5 Taylor JM,Main BS,Crack PJ.Neuroinflammation and oxidative stress:co-conspirators in the pathology of Parkinson’s disease.Neurochem Int,2013,62:803-819.
6 Satoh T,McKercher SR,Lipton SA.Nrf2/ARE-mediated antioxidant actions of pro-electrophilic drugs.Free Radic Biol Med,2013,65:645-657.
7 Zhang DD.Mechanistic studies of the Nrf2-Keap1 signaling pathway.Drug Metab Rev,2006,38:769-789.
8 Rochette L,Ghibu S,Richard C,et al.Direct and indirect antioxidant properties of α-lipoic acid and therapeutic potential.Mol Nutr Food Res,2013,57:114-125.
9 Surmeier DJ,Sulzer D.The pathology roadmap in Parkinson disease.Prion,2013,7:85-91.
10 Tatar A,Korkmaz M,Yayla M,et al.Anti-inflammatory and anti-oxidativeeffects of alpha-lipoic acid in experimentally induced acute otitis media.J Laryngol Otol,2016,130:616-623.
11 Nandipati S,Litvan I.Environmental Exposures and Parkinson’s Disease.Int J Environ Res Public Health,2016,13Pii:E881.
12 Johnson ME,Bobrovskaya L.An update on the rotenone models of Parkinson’s disease:their ability to reproduce the features of clinical disease and model gene-environment interactions.Neurotoxicology,2015,46:101-116.
13 Xiong N,Long X,Xiong J,et al.Mitochondrial complex I inhibitor rotenone-induced toxicity and its potential mechanisms in Parkinson’s disease models.Crit Rev Toxicol,2012,42:613-632.
14 Sita G,Hrelia P,Tarozzi A,et al.Isothiocyanates Are Promising Compounds against Oxidative Stress,Neuroinflammation and Cell Death that May Benefit Neurodegeneration in Parkinson’s Disease.Int J Mol Sci,2016,17pii:E1454.
15 Segura-Aguilar J,Paris I,Mu?oz P,et al.Protective and toxic roles of dopamine in Parkinson's disease.J Neurochem,2014,129:898-915.
16 Rekaik H,Blaudin de Thé FX,Prochiantz A,et al.Dissecting the role of Engrailed in adult dopaminergic neurons--Insights into Parkinson disease pathogenesis.FEBS Lett,2015,21:3786-3794.
17 Hall J,Prabhakar S,Balaj L,et al.Delivery of Therapeutic Proteins via Extracellular Vesicles:Review and Potential Treatments for Parkinson’s Disease,Glioma,and Schwannoma.Cell Mol Neurobiol,2016,36:417-427.
18 Papanas N,Ziegler D.Efficacy of α-lipoic acid in diabetic neuropathy.Expert Opin Pharmacother,2014,15:2721-2731.
19 Joshi G,Johnson JA.The Nrf2-ARE pathway:a valuable therapeutic target for the treatment of neurodegenerative diseases.Recent Pat CNS Drug Discov,2012,7:218-229.
20 Wang W,Wu Y,Zhang G,et al.,Activation of Nrf2-ARE signal pathway protects the brain from damage induced by epileptic seizure.Brain Res,2014,1544:54-61.
21 蘇軍紅 祁秀峰 申向輝,等.Nrf2-ARE通路在PD大鼠黑質(zhì)中的表達(dá)改變.中國(guó)醫(yī)藥導(dǎo)報(bào),2014,35:8-11.
Protecive effects of alpha-lipoic acid on brain substantia nigra dopaminergic neurons in rats with Parkinson’s disease and its action mechanism
WUYanfen*,CHENWen*,WANGMingfei,etal.
*DepartmentofEndocrinology,TheFirstHospitalofHandanCity,Hebei,Handan056001,China
Objective To investigate the protecive effects of alpha-lipoic acid (LA) on brain substantia nigra dopaminergic neurons in rats with Parkinson's disease (PD) induced by rotenone, and to explore its action mechanism.Methods Sixty healthy male Wistar rats (3-month age) were randomly divided into three groups:control group, experimental group and drug intervention group,with 20 rats in each group. The rats in control group were given sunflower oil by subcutaneous injection, however,the rats in experimental group and drug intervention group were given rotenone by subcutaneous injection to establish PD models,moreover,the rats in drug intervention group were given LA simultaneously by peritoneal injection.The expression levels of tyrosine hydroxylase (TH), transcription factor NF-E2 related factors, anti-oxidant response elements (Nrf2-ARE) and heme oxygenase 1 (HO-1) in brain substantia nigra of rats were detected by Western Blot,moreover, the levels of malondialdehyde (MDA) and reduced glutathione (GSH) in brain striatum of rats were detected by spectrophotometric method.Results The expression levels of TH protein in mesencephalon of rats in experimental group were significantly lower than those in control group (P<0.05),however, the expression levels of TH protein in brain substantia nigra of rats in drug intervention group were significantly higher than those in experimental group (P<0.05), but which in drug intervention group were significantly lower than those in control group (P<0.05). The expression levels of Nrf2 and HO-1 protein in experimental group were significantly lower than those in control group (P<0.05),however, which in drug intervention group were significantly higher than those in experimental group (P<0.05),moreover,which in drug intervention group were significantly lower than those in control group (P<0.05). As compared with those in control group, the levels of MDA in striatum tissues of rats in experimental group were significantly increased (P<0.05),however, after drug intervention,the levels of MDA were significantly decreased (P<0.05),but which were still significantly higher than those in control group (P<0.05). As compared with those in control group, the levels of GSH in experimental group were significantly decreased (P<0.01), however, after drug intervention,the levels of GSH were significantly increased (P<0.05), but which were still significantly lower than those in control group (P<0.05).Conclusion LA can effectively activate the Nrf2-ARE signal pathway to relieve the injury of dopaminergic neurons in brain of rats,moreover,which can improve the symptoms of PD.
Parkinson’s disease; α-lipoic acid; oxidative stress; transcription factor NF-E2-related factor /antioxident response element; heme oxygenase-1
10.3969/j.issn.1002-7386.2017.14.006
項(xiàng)目來(lái)源:河北省邯鄲市科學(xué)技術(shù)研究與發(fā)展計(jì)劃項(xiàng)目(編號(hào):1423108128)
056001 河北省邯鄲市第一醫(yī)院內(nèi)分泌科(吳艷芬、陳文),神經(jīng)內(nèi)科(王偉);河北省邯鄲市婦幼保健院(王鳴飛)
王偉,056001 河北省邯鄲市第一醫(yī)院神經(jīng)內(nèi)科;
E-mail:sunnywangwei@163.com
R 742.502
A
1002-7386(2017)14-2105-05
2017-01-26)
- 河北醫(yī)藥的其它文章
- 四種腫瘤標(biāo)志物聯(lián)合檢測(cè)對(duì)膽管癌診斷價(jià)值
- 酮咯酸氨丁三醇用于肛瘺術(shù)后鎮(zhèn)痛對(duì)患者不同狀態(tài)疼痛評(píng)分、PCA按壓次數(shù)和BCS評(píng)分的影響
- 纖維強(qiáng)化樹脂與常規(guī)義齒修復(fù)牙周炎伴牙列缺損的效果比較
- 通心絡(luò)、氨氯地平和阿托伐他汀鈣聯(lián)合治療高血壓合并冠心病的療效觀察
- 慢性心力衰竭患者血清同型半胱氨酸、尿酸和血脂水平的變化及意義
- 個(gè)性化延續(xù)性護(hù)理干預(yù)在精神分裂癥患者康復(fù)中的應(yīng)用

