銅綠假單胞菌脂多糖對白色念珠菌生物膜的影響
鄧 娟 孫 偉 馬立艷 蘇建榮
(首都醫(yī)科大學(xué)附屬北京友誼醫(yī)院臨床檢驗中心,北京 100050)
?
銅綠假單胞菌脂多糖對白色念珠菌生物膜的影響
鄧 娟 孫 偉 馬立艷 蘇建榮*
(首都醫(yī)科大學(xué)附屬北京友誼醫(yī)院臨床檢驗中心,北京 100050)
目的 研究銅綠假單胞菌脂多糖(lipopolysaccharide,LPS)對白色念珠菌生物膜形成的抑制作用。 方法 甲基四氮鹽[(2,3-bis-(2-methoxy-4-nitro-5-sulphophenyl)-2H-tetrazolium-5-carboxanilide,XTT]減低法用于檢測銅綠假單胞菌LPS對白色念珠菌生物膜形成不同階段生成量的影響,同時,利用倒置顯微鏡觀察生物膜形態(tài)學(xué)改變;實時定量聚合酶鏈?zhǔn)椒磻?yīng)(quantitative real time polymerase chain reaction,qRT-PCR)法檢測銅綠假單胞菌LPS對白色念珠菌生物膜菌絲特異基因(hypha specific genes,HSGs)表達(dá)的影響。結(jié)果 銅綠假單胞菌LPS可以抑制白色念珠菌生物膜的形成,以及使菌絲特異基因HWP1、ALS1、ALS3、ECE1和SAP4的表達(dá)分別下調(diào)8.3~12.8、1.1~3.0、2.0~4.6、1.3~3.8和6.2~7.6倍。結(jié)論 銅綠假單胞菌LPS可以通過抑制白色念珠菌菌絲的形成從而抑制其生物膜的形成。
銅綠假單胞菌;脂多糖;白色念珠菌;生物膜;基因
白色念珠菌能夠黏附在導(dǎo)尿管、心臟支架、靜脈插管、人工關(guān)節(jié)等人體植入物上形成生物膜,從而對機體造成損害及對抗真菌藥物產(chǎn)生明顯耐藥性[1]。因此,減少或阻斷生物膜的形成可以有效提高抗真菌治療效果,提高病人生存率。
銅綠假單胞菌是人體常見的機會致病菌,也是醫(yī)院獲得性血流感染的常見致病菌,而脂多糖是銅綠假單胞菌的主要致病成分之一。脂多糖(lipopolysaccharide,LPS)是革蘭陰性桿菌細(xì)胞壁的特有結(jié)構(gòu),又名內(nèi)毒素,其可通過促炎反應(yīng)和免疫調(diào)節(jié)機制引起發(fā)熱、糖代謝紊亂、內(nèi)毒素休克等[2]。
本研究通過構(gòu)建體外白色念珠菌生物膜模型,采用甲基四氮鹽[(2,3-bis-(2-methoxy-4-nitro-5-sulphophenyl)-2H-tetrazolium-5-carboxanilide,XTT]法檢測不同濃度銅綠假單胞菌脂多糖對白色念珠菌生物膜形成的影響,期望能為臨床治療革蘭陰性菌和白色念珠菌混合感染提供一定幫助,也期望能為研發(fā)新型抗真菌藥物提供一定的實驗室依據(jù)。
1 材料與方法
1.1 材料
1)菌株:白色念珠菌標(biāo)準(zhǔn)菌株SC 5314 1株,白色念珠菌 ATCC 90028 1株,臨床血培養(yǎng)陽性標(biāo)本分離的白色念珠菌37株,均來自首都醫(yī)科大學(xué)附屬北京友誼醫(yī)院臨床檢驗中心細(xì)菌室,使用前脫脂牛奶-70 ℃保存。
2)培養(yǎng)基:沙保弱(Sabouraud’s Dextrose Agar, SDA)培養(yǎng)基購自英國Oxiod公司;RPMI-1640培養(yǎng)液購自美國Gibco公司;酵母氮源培養(yǎng)基(Yeast Nitrogen Medium,YNB)購自美國Difco公司,稱取YNB 3.35 g、葡萄糖10 g,加蒸餾水定容至500 mL,0.45 μm微孔濾器過濾除菌,4 ℃保存。
3)主要試劑:銅綠假單胞菌LPS、XTT、甲萘醌均購自美國Sigma公司:LPS用RPMI-1640溶液調(diào)整成100 μg/mL~1 ng/mL濃度;XTT用無菌PBS緩沖液(Solarbio公司,中國)稀釋配成0.5 mg/mL飽和溶液,0.22 μm微孔濾器過濾除菌,分裝后-20 ℃冰箱凍存;甲萘醌用丙酮(北京化學(xué)試劑廠,分析純)新鮮配制成濃度為10 mmol/L溶液。qRT-PCR試劑購自日本Takara公司。
4)儀器:恒溫?fù)u床(中國杭州奧盛科技有限公司),酶標(biāo)儀(伯樂生命科技公司,美國),細(xì)胞計數(shù)板(NanoEnTek公司,韓國),倒置顯微鏡(Olympus公司,日本),ABI 7500型熒光定量PCR儀(ABI公司,美國)。
1.2 方法
1)念珠菌生物膜的制備:將從-70 ℃冰箱保存的待測菌株接種于SDA培養(yǎng)基上,37 ℃、5%(體積分?jǐn)?shù))CO2培養(yǎng)18 h。取一接種環(huán)菌量至YNB培養(yǎng)液中,37 ℃搖床(75 r/min)培養(yǎng)過夜,離心,棄上清,PBS液離心洗滌2次(4 000 r/min,5 min)。用含或不含有不同濃度LPS(100 μg/mL~1 ng/mL)RPMI-1640液體培養(yǎng)基稀釋菌液,顯微鏡下用細(xì)胞計數(shù)板將菌液濃度調(diào)整至5×106細(xì)胞/mL。取100 μL上述菌液接種至無菌96孔板中,37 ℃搖床(75 r/min)培養(yǎng)90 min,然后用PBS輕輕洗滌2次,以洗掉未黏附的念珠菌細(xì)胞,再加入含或不含不同濃度LPS(100 μg/mL~1 ng/mL)RPMI-1640液體培養(yǎng)基200 μL,繼續(xù)培養(yǎng)24 h和48 h,每隔24 h換液1次。陰性對照孔為不含LPS的RPMI-1640培養(yǎng)基。實驗在不同時間重復(fù)3遍。
2)XTT減低法進行生物膜定量分析:在24、48 h時刻點,棄去96孔板中培養(yǎng)液,每孔用200 μL PBS緩沖液洗2遍,然后每孔加入40 μL XTT、2 μL甲萘醌、158 μL PBS緩沖液,37 ℃避光孵育3 h后,用酶標(biāo)儀測定念珠菌生物膜在490 nm處的吸光度值(A值)。
3)倒置相差顯微鏡觀察生物膜形態(tài):按1.2中1)的步驟進行念珠菌SC 5314生物被膜的制備,24 h和48 h時刻點在倒置顯微鏡下觀察念珠菌生物膜形態(tài)并拍攝照片。
4)實時熒光定量PCR :①提取總RNA及cDNA反轉(zhuǎn)錄:選取白色念珠菌SC 5314和隨機抽取的2株臨床菌株,用含100 μg/mL銅綠假單胞菌脂多糖的RPMI-1640液調(diào)整菌液濃度為5×106個細(xì)胞/mL,實驗對照組為不含銅綠假單胞菌脂多糖的菌液,同時設(shè)置空白對照組。取3 mL上述菌液加入到6孔無菌孔板中,37 ℃進行生物膜培養(yǎng)24 h,收集生物膜細(xì)胞后進行總RNA提取。反轉(zhuǎn)錄反應(yīng)條件:5×gDNA Eraser Buffer 2 μL+gDNA Eraser 1 μL+總RNA 3 μL+PrimeScript RT Enzyme MixⅠ1 μL+RT Primer Mix 1 μL+5×PrimeScript Buffer 24 μL+RNase-free H2O 8 μL,混勻后按37 ℃ 15 min,85 ℃ 5 s,4 ℃ 2 min進行反轉(zhuǎn)錄。②引物設(shè)計與合成:根據(jù)相關(guān)文獻選定白色念珠菌菌絲特異基因包括:HWP1、ALS1、ALS3、ECE1、SAP4,內(nèi)參基因為ACT1,委托北京天一輝遠(yuǎn)公司合成引物,各引物序列詳見表1。③qRT-PCR反應(yīng)體系如下:2×SYBR Mixture 10 μL+上、下游引物各0.8 μL+Rox reference DyeⅡ 0.4 μL+cDNA模板 2 μL+ddH2O水6 μL,總體系為20 μL,95 ℃ 30 s預(yù)變性后,反應(yīng)條件為:95 ℃ 5 s→60 ℃ 30 s,共40循環(huán)。每個樣本重復(fù)3次,每次檢測均3個試驗管,3個內(nèi)參管,最終檢測結(jié)果取平均值,采用2-△△Ct法進行數(shù)據(jù)的相對定量分析。

表1 RT-PCR 實驗所用的引物及其序列
PR-PCR:real time polymerase chain reaction.
1.3 統(tǒng)計學(xué)方法

2 結(jié)果
2.1 不同濃度銅綠假單胞菌LPS對念珠菌生物膜形成的影響
與對照組相比,在生物膜形成階段(24 h)和生物膜成熟階段(48 h),銅綠假單胞菌脂多糖100 μg/mL濃度對白色念珠菌生物膜形成抑制率最高,分別為82.05%(32/39)和71.79%(28/39)(表2)。不同濃度銅綠假單胞菌LPS對白色念珠菌生物膜的影響可從XTT結(jié)果分析中得出,每株白色念珠菌的XTT值均有所差異,本實驗中列出白色念珠菌標(biāo)準(zhǔn)菌株 SC 5314菌株的XTT結(jié)果(表3)。
2.2 銅綠假單胞菌脂多糖對白色念珠菌生物膜形態(tài)的影響
白色念珠菌在含100 μg/mL濃度銅綠假單胞菌脂多糖的RPMI-1640液體培養(yǎng)基中培養(yǎng)24 h和48 h,通過倒置顯微鏡觀察發(fā)現(xiàn),白色念珠菌對照組形成的生物膜中含有大量呈交織狀態(tài)的菌絲,而實驗抑制組生物膜多數(shù)為酵母相,偶見少量菌絲形成(圖1)。

表2 不同濃度銅綠假單胞菌LPS抑制白色念珠菌生物膜形成的菌株數(shù)

表3 不同濃度的銅綠假單胞菌LPS對白色念珠菌生物膜影響的XTT結(jié)果分析
2.3 銅綠假單胞菌脂多糖對白色念珠菌菌絲特異基因表達(dá)量的影響
為了探究銅綠假單胞菌脂多糖抑制白色念珠菌菌絲形成進而影響生物膜形成的分子機制,選取了以往文獻[3]中證實與白色念珠菌菌絲形成密切相關(guān)的基因(HWP1、ALS1、ALS3、ECE1、SAP4)進行檢測。結(jié)果顯示,在100 μg/mL銅綠假單胞菌脂多糖作用下,通過相對基因表達(dá)量的比較,可見3株受試菌株的菌絲特異基因在24 h時刻點均受到不同程度的影響,且其變化總趨勢具有一致性(表4)。菌絲特異基因HWP1、ALS1、ALS3、ECE1和SAP4分別下調(diào)8.3~12.8、1.1~3.0、2.0~4.6、1.31~3.8和6.2~7.6倍,以HWP1和SAP4下調(diào)最明顯(圖2)。
3 討論

圖1 100 μg/mL銅綠假單胞菌脂多糖對白色念珠菌SC 5314菌株生物膜形成的影響
C.albicanscells were grown in RPMI-1640 medium at the 100 μg/mL concentration ofPseudomonasaeruginosaLPS at 37 ℃ for 24 h and 48 h.At the end of incubation an aliquot was withdrawn from each sample and photographed at 40×magnification.LPS:lipopolysaccharide.
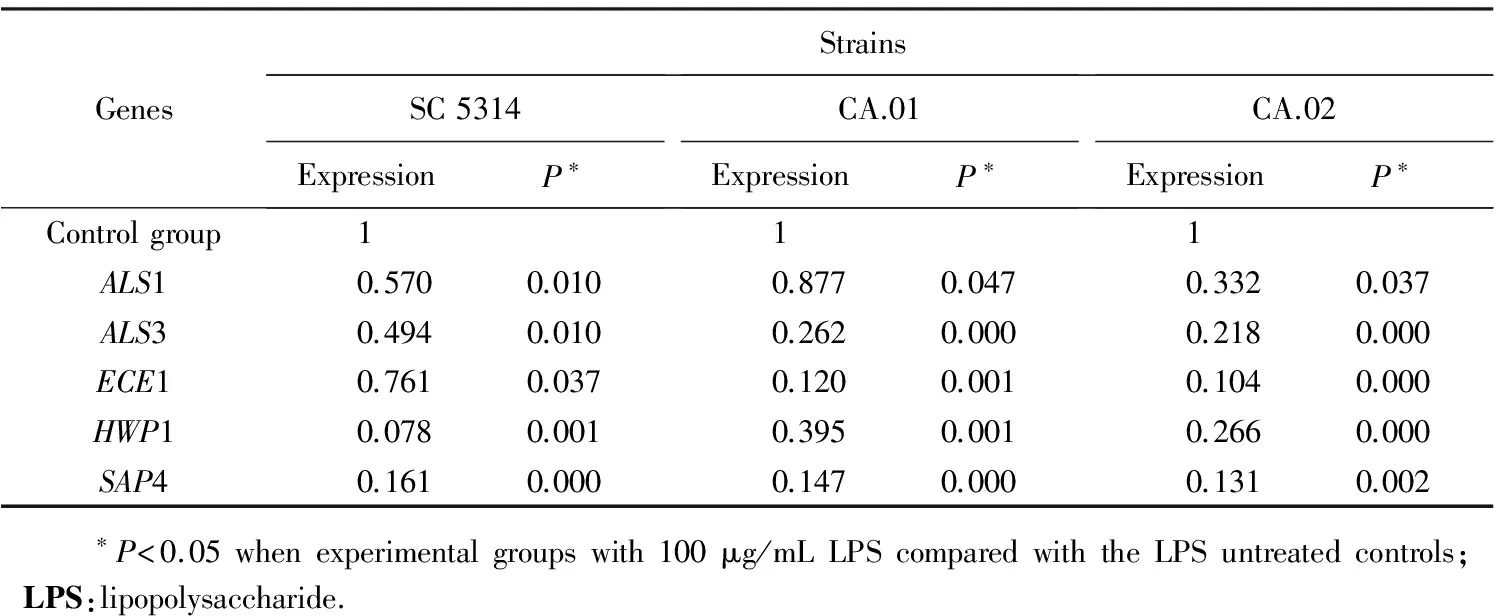
表4 100 μg/mL銅綠假單胞菌LPS對白色念珠菌菌絲特異基因相對表達(dá)量

圖2 銅綠假單胞菌脂多糖對白色念珠菌菌絲特異基因的表達(dá)
*P<0.05vscontrols; LPS:lipopolysaccharide.
白色念珠菌是一種二相型真菌,可在孢子相和菌絲相間進行形態(tài)學(xué)轉(zhuǎn)換。臨床上,大部分白色念珠菌感染以生物膜形態(tài)發(fā)生,成熟的白色念珠菌生物膜是一個由孢子、假菌絲及菌絲形成的致密網(wǎng)狀結(jié)構(gòu),可使得白色念珠菌致病性增強[1],導(dǎo)致生物膜狀態(tài)白色念珠菌血癥成為臨床治療的難點。Perumal等[4]研究發(fā)現(xiàn)白色念珠菌的藥物易感性與菌體密度存在著顯著關(guān)系,當(dāng)菌體密度越大時,其藥物易感性越低。
Fourie等[5]揭示了銅綠假單胞菌和白色念珠菌生物膜產(chǎn)生不同花生四烯酸類物質(zhì)及其對彼此代謝活性的影響。秦金喜等[6]通過交叉條帶法測定銅綠假單胞菌對念珠菌的抑制活性,結(jié)果證明銅綠假單胞菌可產(chǎn)生抗念珠菌活性的抗菌物質(zhì)。 Ke?eli ?zcan 等[7]發(fā)現(xiàn)銅綠假單胞菌通過分泌綠膿素抑制發(fā)揮抗白色念珠菌活性。Bandara等[8]報告了通過共聚焦熒光顯微鏡和掃描電鏡觀察到銅綠假單胞菌脂多糖抑制白色念珠菌菌絲的形成從而影響白色念珠菌生物膜的形成。Burd等[9]在小鼠體內(nèi)注射白色念珠菌和大腸桿菌脂多糖,發(fā)現(xiàn)大腸桿菌脂多糖可增加白色念珠菌的毒力。Akagawa等[10]發(fā)現(xiàn),當(dāng)給感染白色念珠菌的小鼠注射脂多糖后,其腎臟的菌落數(shù)明顯高于對照組。Sabra等[11]闡述了2種不同化學(xué)類型的銅綠假單胞菌脂多糖在一定生存條件下,脂多糖表型的改變可能在細(xì)菌黏附和存活過程中起著重要作用。
念珠菌生物膜的形成,可人為地劃分為3個階段:黏附階段(1~2 h)、生物膜形成階段(12~24 h)和生物膜成熟階段(30~72 h)[12]。本實驗用XTT減低法驗證了白色念珠菌脂多糖對白色念珠菌生物膜的代謝活性,結(jié)果顯示銅綠假單胞菌脂多糖對白色念珠菌生物膜的形成具有抑制作用。倒置顯微鏡下觀察其形態(tài)學(xué)改變發(fā)現(xiàn)銅綠假單胞菌脂多糖抑制白色念珠菌菌絲形成,且發(fā)現(xiàn)脂多糖抑制組在48 h白色念珠菌生物膜菌絲量多于24 h,可能與脂多糖藥物半衰期有關(guān),隨著藥物作用時間的延長,藥物對菌絲的抑制作用有所下降。
白色念珠菌菌絲的形成是其主要致病特點,HWP1、ALS1和ALS3具有編碼白色念珠菌細(xì)胞壁糖蛋白成分,促進菌絲形成的作用[13-15];ECE1是菌絲誘導(dǎo)基因,可刺激菌絲的形成和延長[16];SAP4可編碼分泌型天冬氨酸蛋白酶4,調(diào)節(jié)白色念珠菌從酵母相轉(zhuǎn)換成菌絲相的過程[17]。本實驗用qRT-PCR方法檢測了銅綠假單胞菌脂多糖對上述基因的轉(zhuǎn)錄水平,結(jié)果表明,銅綠假單胞菌脂多糖能顯著下調(diào)上述菌絲特異基因的表達(dá),從而影響相應(yīng)蛋白的表達(dá)。
綜上所述,銅綠假單胞菌脂多糖具有一定的抗真菌效果,銅綠假單胞菌脂多糖可通過下調(diào)白色念珠菌菌絲特異基因的轉(zhuǎn)錄水平,抑制白色念珠菌菌絲的形成,從而減弱白色念珠菌的致病性,發(fā)揮抗白色念珠菌生物膜形成的作用。
[1] Cuéllar-Cruz M, Vega-González A, Mendoza-Novelo B,et al.The effect of biomaterials andantifungals onbiofilm formation by candida species:a review.[J].Eur J Clin Microbiol Infect Dis,2012,31(10):2513-2527.
[2] Michalek S M,Moore R N,McGhee J R,et al. The primary role of lymphoreticular cells in the mediation of host responses to bacterial endotoxim. [J].J Infect Dis,1980,141(1):55-63.
[3] Haque F, Alfatah M, Ganesan K, et al. Inhibitory effect of sophorolipid on candida albicans biofilm formation and hyphal growth[J]. Sci Rep,2016, 6:23575.
[4] Perumal P,Mekala S,Chaffin W L. Role for cell density in antifungal drug resistance in candida albicans biofilms. [J].Antimicrob Agents Chemother,2007,51(7):2454-2463.
[5] Fourie R, Ells R, Kemp G, et al.Pseudomonasaeruginosaproduces aspirin insensitive eicosanoids and contributes to the eicosanoid profile of polymicrobial biofilms with Candida albicans.[J]Prostaglandins Leukot Essent Fatty Acids,2017, 117:36-46.
[6] 秦金喜,李仲興,楊永昌,等.銅綠假單胞菌代謝產(chǎn)物體外對白假絲酵母菌等的抑菌活性研究[J].中國感染控制雜志,2012,11(4):257-260,256.
[7] Ke?eli ?zcan S, Dündar D, S?nmez Tamer G. Anti-candidal activity of clinicalpseudomonasaeruginosastrains and in vitro inhibition of Candida biofilm formation[J]. Mikrobiyol Bul,2012, 46(1):39-46.
[8] Bandara H M, K Cheung B P,Watt R M,et al.Pseudomonasaeruginosalipopolysaccharide inhibits Candida albicans hyphae formation andalters gene expression during biofilm development[J].Mol Oral Microbiol,2013,28(1):54-69.
[9] Burd R S,Raymond C S,Dunn D L. Endotoxin promotes synergistic lethality during concurrent escherichia coli and Candida albicans infection[J].J Surg Res,1992,52(6):537-542.
[10] Akagawa G,Abe S,Yamaguchi H. Mortality of Candida albicans-infected mice is facilitated by superinfection of Escherichia coli or administration of its lipopolysaccharide[J]. J Infect Dis,1995,171(6):1539-1544.
[11] Sabra W,Lünsdorf H,Zeng A P. Alterations in the formation oflipopolysaccharide and membrane vesicles on the surface ofPseudomonasaeruginosaPAO1 under oxygen stressconditions. [J].Microbiology,2003,149(Pt 10):2789-2795.
[12] Xia J, Qian F, Xu W, et al. In vitro inhibitory effects of farnesol and interactions between farnesol and antifungals against biofilms of Candida albicans resistant strains[J].Biofouling, 2017, 33(4):283-293.
[13] Desai J V,Mitchell A P. Candida albicans biofilm development and its genetic control[J].Microbiol Spectr,2015, 3(3).doi:10.1128/microbiolspec.MB-0005-2014.
[14]馬賢德, 張威,關(guān)洪全.白色念珠菌感染對脾虛模型小鼠T細(xì)胞亞群的影響[J].中國醫(yī)科大學(xué)學(xué)報,2015,44(12):1070-1074.
[15]賀政新,侯天文,李瑋,等.白念珠菌烯醇化酶1的原核表達(dá)及多克隆抗體制備[J].解放軍醫(yī)藥雜志,2016,28(1):35-39.
[16] Sudbery P E. Growth of candida albicans hyphae[J].Nat Rev Microbiol,2011, 9(10):737-748.
[17] Nas T,Kalkanci A,F(xiàn)idan I,et al. Expression of ALS1, HWP1 and SAP4 genes in Candida albicans strains isolated from women with vaginitis[J].Folia Microbiol (Praha),2008,53(2):179-183.
編輯 陳瑞芳
Effects ofPseudomonasaeruginosalipopolysaccharide on biofilm ofCandidaalbicans
Deng Juan,Sun Wei, Ma Liyan, Su Jianrong*
(ClinicalLaboratoryCenter,BeijingFriendshipHospital,CapitalMedicalUniversity,Beijing100050,China)
Objective To explore the inhibitory effects ofPseudomonasaeruginosalipopolysaccharide onCandidasalbicansbiofilms. Methods [(2,3-bis-(2-methoxy-4-nitro-5-sulphophenyl)-2H-tetrazolium-5-carboxanilide,XTT] reduction assay was used to elucidate the effect ofPseudomonasaeruginosalipopolysaccharide on biofilm formation ofCandidaalbicans,and inverted microscope was used to observe the morphological changes ofCandidaalbicansbiofilms; expression analysis ofCandidaalbicanshypha specific genes was done by quantitative real time polymerase chain reaction(PCR). Results The data showed thatPseudomonasaeruginosalipopolysaccharide inhibitsCandidasbiofilm formation,and the expressions ofHWP1,ALS1,ALS3,ECE1,SAP4 were downregulated 8.3 to 12.8 times,1.1 to 3.0 times,2.0 to 4.6 times,1.3 to 3.8 times and 6.2 to 7.6 times. ConclusionPseudomonasaeruginosalipopolysaccharide modulatedCandidaalbicansbiofilm formation by inhibiting the hyphal development.
Pseudomonasaeruginosa;lipopolysaccharide;Candidasalbicans;biofilm;genes
時間:2017-07-16 17∶16 網(wǎng)絡(luò)出版地址:http://kns.cnki.net/kcms/detail/11.3662.r.20170716.1716.018.html
10.3969/j.issn.1006-7795.2017.04.019]
R379.4
2016-11-21)
*Corresponding author, E-mail:youyilab@163.com

