茚三酮顯色分光光度法測定食品中α-氨基酸含量的方法探討
丁永霞
(菏澤市疾病預防控制中心,山東菏澤 274010)
茚三酮顯色分光光度法測定食品中α-氨基酸含量的方法探討
丁永霞*
(菏澤市疾病預防控制中心,山東菏澤 274010)
1 材料與方法
1.1 儀器
UV—2550紫外可見分光光度計,日本島津公司;FA2004N電子分析天平,上海精密科學儀器公司;石英比色皿(1cm);玻璃比色皿;容量瓶;移液管;吸管;蒸餾燒瓶;加熱套;pH試紙。
1.2 試劑
鹽酸溶液,濃度6 mol/L,分析純;甘氨酸,優級純;茚三酮試劑,分析純;乙酸,分析純;乙酸鈉,分析純;NaOH溶液,濃度1 mol/L,分析純;酚酞指示劑。
乙酸-乙酸鈉緩沖溶液(pH=5.5):精確稱取50 g乙酸鈉 (CH3COONa·3H20) 于燒杯中,加入150mL蒸餾水,用移液管移取2.50mL冰醋酸,加熱溶解,冷卻后轉移到250mL容量瓶中,用餾水定容至刻度。
茚三酮乙二醇溶液(質量濃度3%):精確稱取3 g水合茚三酮,加入50mL乙二醇,低溫加熱溶解后,轉移至100mL容量瓶中,用乙二醇定容至刻度,轉移到試劑瓶后置于0℃~5℃冰箱中保存備用(臨用時配)。
甘氨酸標準儲備液:準確稱取0.1000 g甘氨酸標準品,加餾水溶解定容到100mL容量瓶中,搖勻,轉移到玻璃試劑瓶后置于0℃~5℃冰箱中備用,此溶液質量濃度為1000 μg/mL。
1.3 樣品處理與測定方法
1.3.1 樣品處理
精確稱取5 g樣品于蒸餾燒瓶中,加入30mL 6 mol/L的鹽酸溶液,在100℃的沸水浴中加熱水解10 h。冷卻后過濾,并用少量的水沖洗過濾漏斗中的殘渣,將溶液定容至100mL容量瓶中。取1.00mL樣品溶液于燒杯中,加入20mL蒸餾水、2滴酚酞試劑,用1 mol/L的NaOH溶液滴定,使其pH值在5~7之間,記錄所需NaOH溶液的體積。取出1.00mL樣品溶液于50mL容量瓶中,加入所需體積的NaOH溶液,配置pH值在5~7之間的樣品稀釋溶液,備測。
1.3.2 測定方法
分別吸取樣品稀釋液 2.00mL和0.0 μg/mL、10.0 μg/mL、25.0 μg/mL、50.0 μg/mL、75.0 μg/mL 的甘氨酸系列標準溶液2.0mL置于20mL比色管中,加入乙酸-乙酸鈉緩沖溶液(pH=5.5) 5.0mL,充分搖勻后,加2.0mL質量濃度3%的茚三酮乙二醇溶液,搖勻,于沸水浴中加熱,顏色變化后計時20min,計時結束后取出試管,冷卻至室溫,倒入比色皿中,以0.0 μg/mL的甘氨酸溶液為參比,在566nm波長處測定吸光度,并繪制標準曲線,計算出樣品含量,同時做試劑空白。樣品及標準溶液的吸光度值見表1。
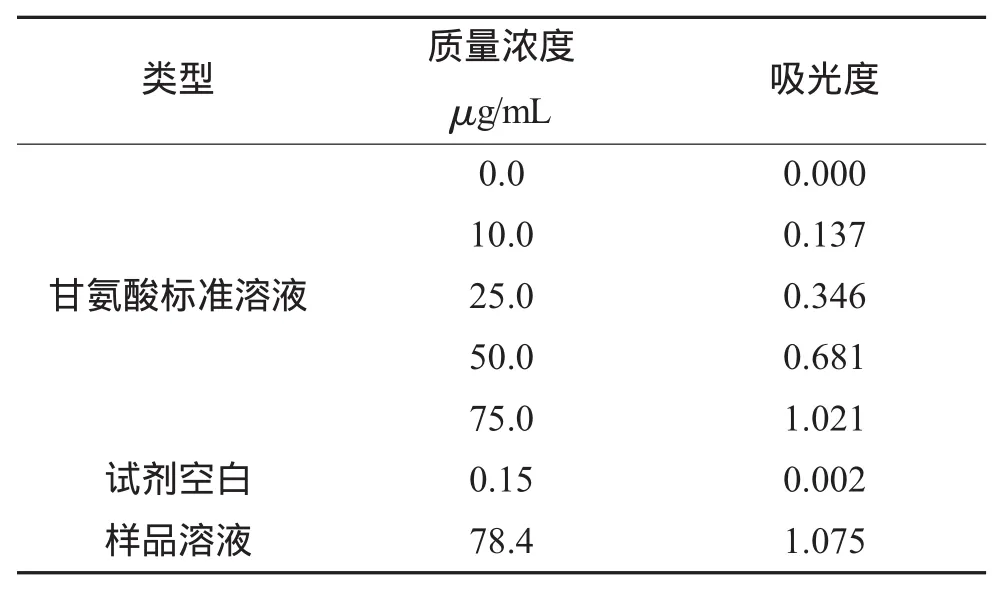
表1 樣品及標準溶液的吸光度
根據測定結果求得其回歸方程為y=0.0137x+0.0035,相關系數R2=0.9996。結果表明,標準溶液的濃度在 0 μg/mL~100 μg/mL 范圍內有良好的線性關系。
2 結果與討論
2.1 最大吸收波長的選擇
用紫外分光光度計(1cm石英比色皿)對樣品顯色溶液進行比色(范圍190nm~700nm),發現最高峰值在可見區566nm處,換玻璃比色皿對溶液進行驗證(范圍400nm~700nm),最高峰值仍在566nm處,故選取566nm為最大吸收波長。吸收光譜見圖1和圖2。
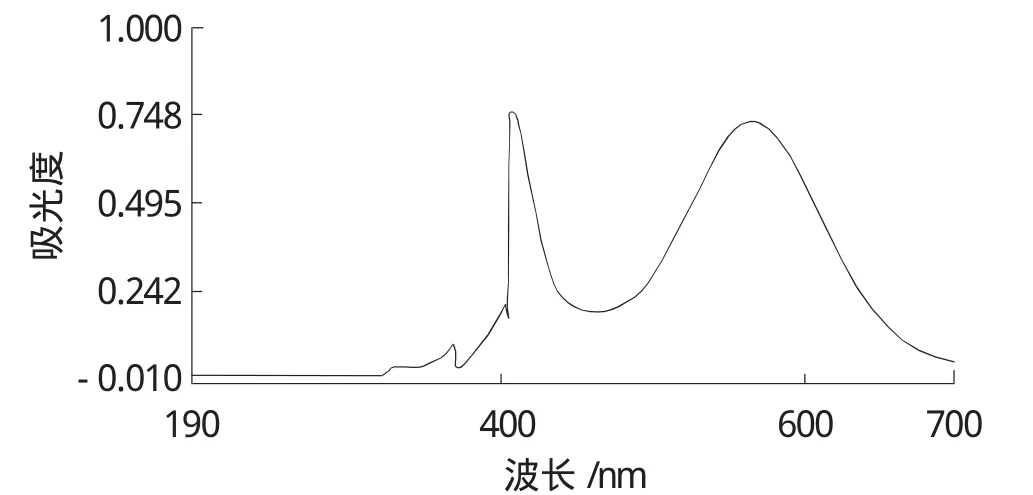
圖1 樣品顯色液紫外可見區光譜圖
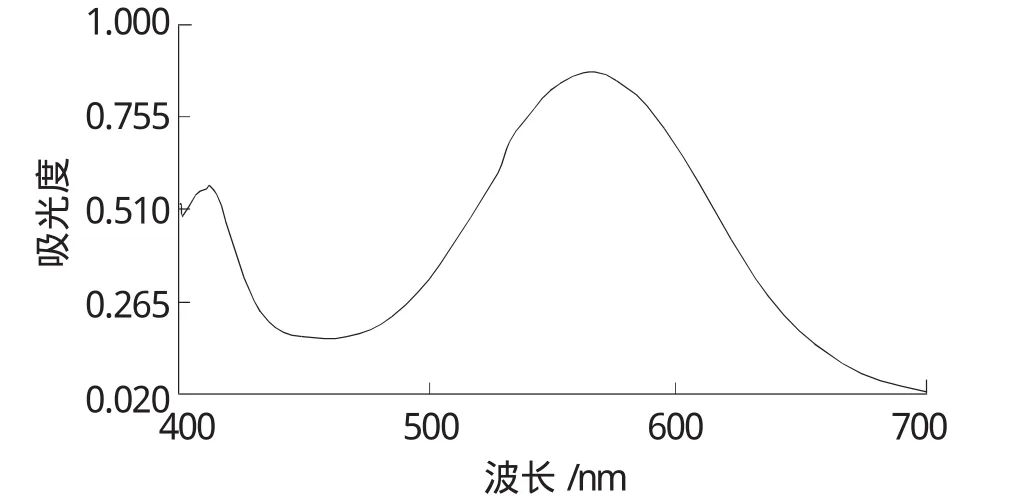
圖2 樣品顯色液可見區光譜圖
2.2 加熱時間的影響
取6.0mL質量濃度為100 μg/mL的甘氨酸標準工作液于50mL比色管中,加入15.0mL乙酸-乙酸鈉緩沖液(pH=5.5) 和6.0mL質量濃度3%的茚三酮乙二醇溶液,搖勻,于沸水浴中加熱,當溶液有顏色變化時開始計時,每過5min取出約5mL溶液,冷卻,測定其吸光度,結果見表2、圖3。由圖3可知,加熱20min時吸光度數值基本穩定,因此選擇20min時為最佳加熱時間。
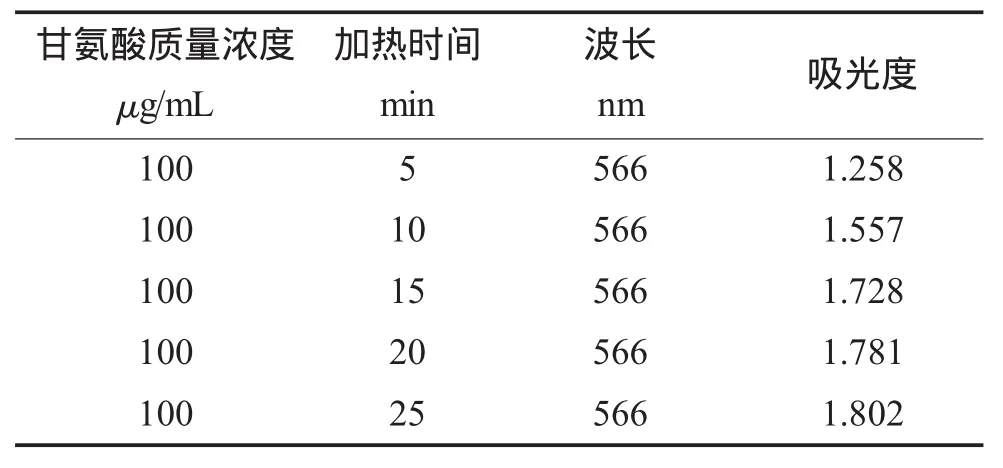
表2 不同反應時間測得吸光度
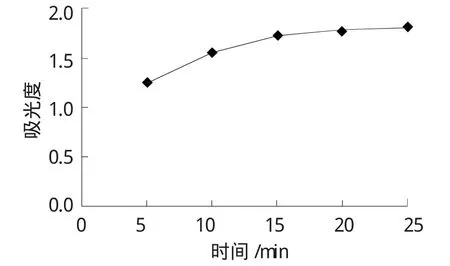
圖3 不同顯色時間對吸光度的影響
2.3 顯色劑用量的影響
取2.0mL質量濃度為100 μg/mL的甘氨酸標準工作液于試管中,各加入5.0mL乙酸-乙酸鈉緩沖液 (pH=5.5),分別加入 1.0mL、2.0mL、3.0mL、4.0mL質量濃度3%茚三酮乙二醇溶液,在沸水中水浴加熱,待顯色20min時取出測吸光度。測定的各顯色體系的吸光度見表3、圖4。
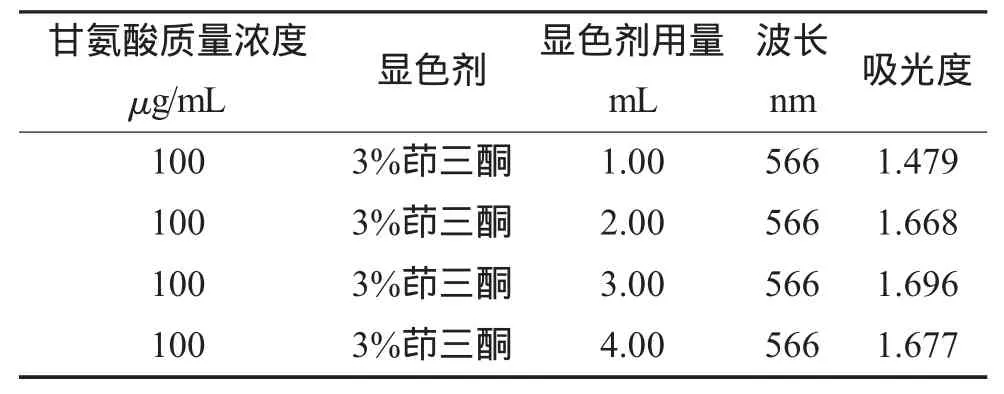
表3 不同顯色劑用量測得吸光度
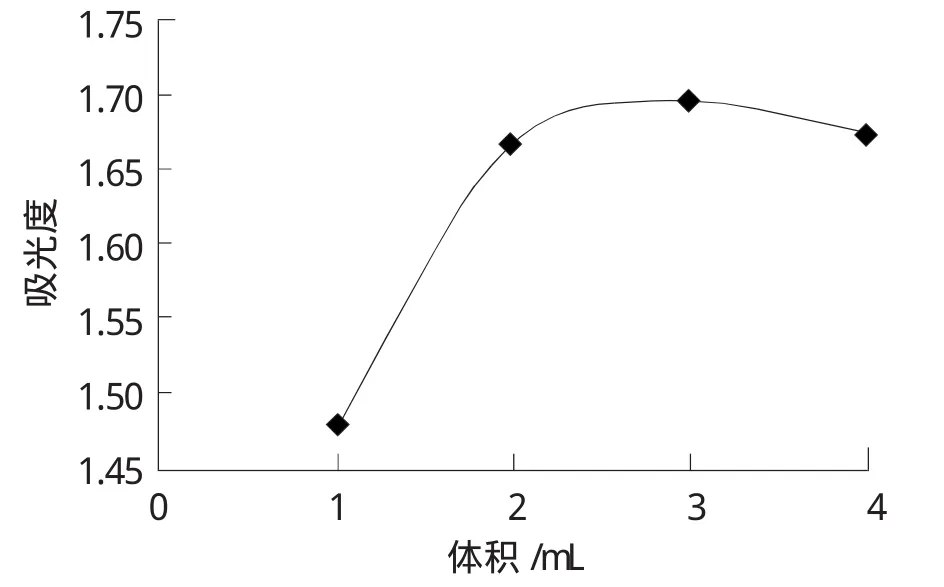
圖4 不同顯色劑用量對吸光度的影響
由圖4可知,隨著顯色劑用量的增加,吸光度不斷增大,當顯色劑用量超過3.0mL時吸光度開始下降,顯色劑用量為2.0mL時的顯色穩定度好、顯色速度較快,因此選擇顯色劑用量為2.0mL。
2.4 精密度測定
取2.00mL樣品稀釋液進行多次測定(n=5),計算其α-氨基酸總含量,結果見表4。
由表4可以看出,樣品稀釋液的α-氨基酸含量為78.53 μg/mL,標準偏差為0.33,相對標準偏差為0.42%。
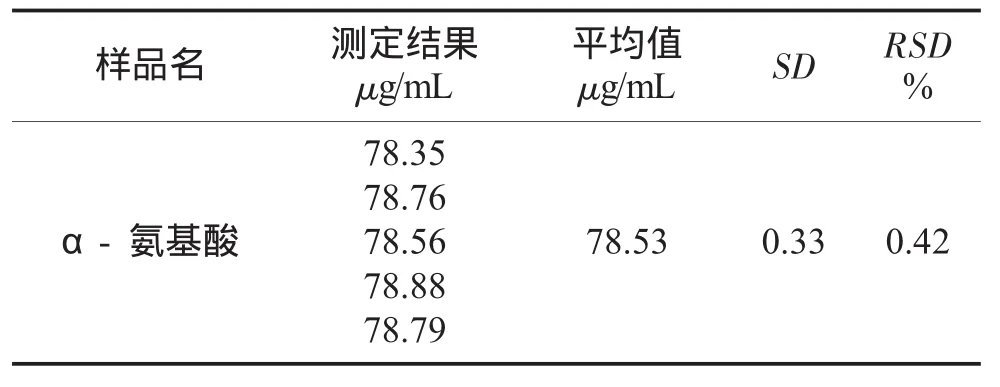
表4 樣品液中α-氨基酸含量測定的重復性
2.5 回收率測定
為了確定測量的準確度,取一定量的樣品液,測定其α-氨基酸總量作為本底量,以5 μg/mL、10 μg/mL的甘氨酸分別作為加標量,測定回收率,結果見表5。
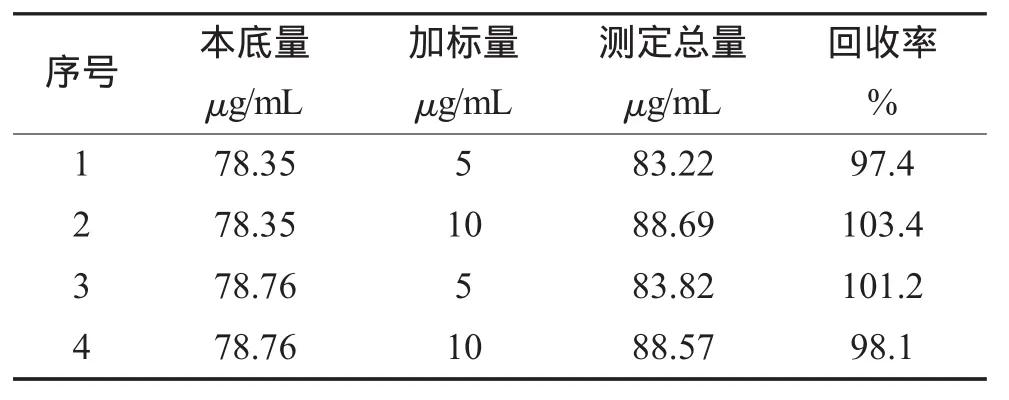
表5 回收率試驗結果
由表5數據可知,回收率在97.4%~103.4%范圍內,表明該方法測定結果準確可靠。
3 結論
本研究采用茚三酮顯色分光光度法測定食品中的α-氨基酸總含量,該方法具有操作簡單、快速和重現性較好等優點,通過試驗得出最佳試驗條件為:pH值5.5,沸水浴加熱20min,最佳吸收波長566nm。此試驗條件下,該方法的變異系數0.42%,平均加標回收率為100.02%。
[1]鐘秋珍,瑋玲,林武,等.5個楊桃品種果實氨基酸含量及組成分析[J].福建果樹,2011,5(3):5-8.
[2]史修周,陳昌生,謝潮添,等.壇紫菜氨基酸提取工藝影響條件的優化與分析[J].臺灣海峽,2011,30(1):132-138.
[3]劉慧燕,德力格爾桑,方海田.茚三酮比色法測定牛肉中游離氨基酸的試驗研究[J].加工工藝,2005,6(2):23-25.
[4]王昂,王麗麗,儀宏,等.茚三酮比色法測定谷氨酸含量的研究[J].中國調味品,2005,8(8):50-52.
[5]張振華.α-氨基酸與茚三酮顯色反應影響因素的探討[J].邵陽高等專科學校學報,2000,13(1):42-44.
Determination of alpha amino acid in food by ninhydrin color spectrophotometry
DING Yongxia*
(Heze citycenter for disease control and prevention,ShandongHeze 274010,China)
采用茚三酮顯色分光光度法測定食品中α-氨基酸的總含量,通過試驗摸索,確定了以甘氨酸為標準品、茚三酮為顯色劑的測定方法。試驗結果表明,該方法的最佳反應條件為:pH值5.5,在沸水浴中加熱顯色20min,常溫條件下的最大吸收波長566nm。用甘氨酸配制系列標準溶液,通過標準曲線法對待測溶液進行定量分析,其相關系數為0.9995,回收率在95.5%~104.3%范圍內,表明該方法具有操作簡便、結果準確、重現性良好的特點。
茚三酮;分光光度法;α-氨基酸;甘氨酸
The method ofdeterminate alpha aminoacid in food on the basis ofglycine,ninhydrin as chromogenic agent was established.The results show that the optimum reaction conditions were pH 5.5,in a boiling water bath heating chromogenic 20min,under the condition ofroomtemperature the maximumabsorption wavelength of566nm.Prepared with glycine series of standard solution,standard curve method for quantitative analysis of the test solution,the correlation coefficient is 0.9995,the recovery rate from 95.5%to 104.3%range.The method is with simple operation,accurate results and good reproducibility.
ninhydrin;spectrophotometry;alpha aminoacid;glycine
TS207.4
A
1673-6044(2017)01-0055-03
10.3969/j.issn.1673-6044.2017.01.016
*丁永霞,女,1963年出生,1996年畢業于曲阜師范大學化學系化學專業,副主任技師。
2016-12-10

