格列齊特在糖尿病腎病治療中帶來腎獲益的研究進展
趙 嵐,王 玲(上海交通大學醫學院附屬新華醫院藥劑科,上海200092)
格列齊特在糖尿病腎病治療中帶來腎獲益的研究進展
趙 嵐*,王 玲(上海交通大學醫學院附屬新華醫院藥劑科,上海200092)
目的:探討口服降糖藥物格列齊特在糖尿病腎病治療中帶來的腎獲益。方法:查閱近年來國內外相關文獻,就格列齊特在糖尿病腎病治療中帶來的腎獲益進行歸納和總結。結果與結論:糖尿病腎病的發生與發展和高血糖、氧化應激和內皮功能障礙等密切相關。格列齊特為傳統降糖藥物,相關循證研究顯示,該藥可為糖尿病腎病患者帶來腎獲益,原因為其具有顯著的降糖作用,以及其化學結構中獨特的氮雜環結構。其中,該氮雜環結構能夠接受活性自由基活性氧簇的電子,并發生構象變化,使自由基形成穩定結構,從而清除自由基,起到抗氧化應激、改善內皮功能的作用,是格列齊特帶來腎獲益效果的關鍵原因。同時,格列齊特能夠顯著降低糖尿病腎病患者發生微量白蛋白尿的風險,帶來腎獲益,但其具體機制還有待進一步研究驗證。
糖尿病腎病;格列齊特;高血糖;氧化應激;內皮功能障礙;氮雜環;腎獲益
糖尿病腎病是由糖尿病引起的嚴重和危害性極大的一種慢性并發癥,是糖尿病全身性微血管病變的表現之一。其臨床特征為蛋白尿、漸進性腎功能損害、高血壓和水腫等,晚期則出現嚴重腎功能衰竭。相關數據顯示,全球糖尿病患者腎病的發病率高達27.9%,我國糖尿病患者腎病的發病率為27.6%[1-2]。糖尿病腎病是終末期腎病的第二大病因,隨著糖尿病發病率的不斷升高,糖尿病腎病可能成為終末期腎病的首要病因[3-4]。降糖藥物對糖尿病患者血管類并發癥的影響一直是該領域關注的熱點。降糖藥物的大型臨床研究中,僅格列齊特、利拉魯肽和恩格列凈等少數藥物可使腎病患者獲益[5-8]。其中,格列齊特作為上市30余年的磺脲類藥物,從最初的普通劑型發展至現在的緩釋劑型,研究者們在臨床應用中積累了豐富的經驗。目前,臨床已掌握格列齊特在糖尿病腎病治療中腎獲益的證據,但探討其獲益機制的研究較為罕見。鑒于此,筆者查閱近年來國內外相關文獻,就格列齊特在糖尿病腎病治療中的腎獲益的研究進行歸納和總結,旨在探討其獲益機制。
1 糖尿病腎病發生機制
糖尿病腎病的主要病理特征是腎小球肥大、基底膜增厚以及細胞外基質(ECM)聚集,可進展至腎小球硬化和腎小管間質纖維化,臨床表現為早期微量白蛋白尿,逐步進展為大量白蛋白尿,最終導致腎功能衰竭。目前,已知糖尿病腎病的發病機制包括遺傳易感、表觀遺傳調控、氧化應激、炎癥反應、細胞因子激活和腎血流動力學改變等,其發病機制復雜,至今尚未完全闡明[9]。其中,以慢性高血糖為中心作用導致的血流動力學和代謝因素在糖尿病腎病的病理生理學中具有關鍵作用,糖尿病及其伴發的各種代謝紊亂(如高血壓、高血脂、游離脂肪酸水平的增加、胰島素抵抗和脂肪細胞因子水平的改變等)參與了糖尿病腎病的發生與發展[9-10]。持續的高血糖可引起腎小球基底膜增厚、腎血管通透性增加和血管新生等[9]。另外,胰島素抵抗、脂聯素水平降低等因素與蛋白尿、內皮細胞功能障礙均密切相關[11]。
糖尿病腎病的本質是腎纖維化,從其分子機制來看,氧化應激和內皮功能障礙在糖尿病腎病的發生與發展過程中具有核心作用。高血糖可引起活性氧簇(ROS)過度生成,使體內氧化和抗氧化系統失衡,進而引起組織細胞受損[9]。ROS可激活蛋白激酶C(PKC)通路、多元醇通路、氨基己糖通路,使糖基化終末產物(AGEs)生成增加,同時可活化下游的信號分子[如細胞外信號調節激酶(ERK)、核轉錄因子κB(NF-κB)、激活蛋白1(AP-1)等],最終啟動氧化應激[9]。腎作為氧化應激的靶器官之一,易受氧化應激損傷。氧化應激通過多種途徑引起腎小球內高壓、高灌注、高濾過,足細胞凋亡、破損,ECM代謝紊亂,無菌性炎癥反應等,加快糖尿病腎病的發生與發展[12-13]。另一方面,在高血糖狀態下,PKC通路、多元醇通路和氧化應激機制被激活且產生過量的AGEs和ROS,損傷內皮一氧化氮合酶(NOS),降低一氧化氮(NO)的生成,同時刺激腎素-血管緊張素系統(RAS)產生血管緊張素Ⅱ損傷內皮細胞。此外,腎小球足細胞與內皮細胞相互作用,進一步加重內皮細胞損傷,從而進一步損傷和破壞濾過屏障的結構和功能,導致持續性蛋白尿,使腎小球濾過率(GFR)降低、內皮分泌功能失調,促進糖尿病腎病的發生與發展[14]。可見,糖尿病腎病的治療除控制高血糖外,改善氧化應激和內皮功能障礙可能也是重要措施。
2 格列齊特在糖尿病腎病治療中帶來的腎獲益
2.1 格列齊特通過控制血糖使腎獲益
高血糖能夠引起一系列的血流動力學異常、代謝異常以及氧化應激和內皮功能障礙等,在糖尿病腎病發生與發展中具有關鍵作用。格列齊特是《中國2型糖尿病防治指南(2013年版)》推薦的臨床療效較好的口服降糖藥物,能使糖化血紅蛋白(HbA1c)降低1%~1.5%[15]。Landman GW等[16]的一項Meta分析納入19項研究的內容,旨在比較格列齊特與其他降糖藥物的療效和安全性,其中3 083例患者接受格列齊特治療,3 155例患者接受其他降糖藥物治療。結果顯示,格列齊特較其他降糖藥物的降糖療效更顯著,HbA1c的降低幅度更大,其降幅差異達0.12%。ADVANCE研究是一項全球、多中心的大型研究,共納入11 140例2型糖尿病患者,其中5 571例患者接受以格列齊特緩釋片(30~120 mg,qd)為基礎的強化治療,5 569例接受標準治療方案(根據各研究中心當地相關指南制訂降糖治療方案)[5]。該研究旨在評估以格列齊特緩釋片為基礎的強化降糖方案(降糖目標為HbA1c≤6.5%)對主要心血管終點事件的影響。結果顯示,70%的患者使用格列齊特緩釋片的劑量達120 mg/d,通過強化血糖控制使血糖水平達標率增至81%,平穩控制血糖的中位時間長達5年[17]。
于是,研究者們提出格列齊特可通過有效控制糖尿病腎病患者的血糖水平帶來腎獲益[18]。ADVANCE研究以格列齊特緩釋片進行強化血糖控制,使患者血糖長期平穩控制在較好水平(降糖目標為HbA1c≤6.5%,且長期維持平穩狀態)[5,18]。該系列研究經過5年的隨訪,結果顯示以格列齊特緩釋片為基礎的強化降糖治療方案組與標準治療組比較,與腎相關的不良事件發生率降低了21%(P=0.006),新發微量白蛋白尿風險降低了9%(P=0.012),新發大量白蛋白尿的風險降低了30%(P<0.001),發生終末期腎病(需持續透析或腎移植)的風險降低了65%(P=0.002)。ADVANCE研究的后續觀察隨訪研究ADVANCE-ON納入8 494例患者,按ADVANCE研究的分組繼續隨訪,旨在檢驗ADVANCE研究中強化血糖控制具有長期的血管獲益的假說[6]。該研究中位隨訪時間為5.4年,其結果顯示以格列齊特緩釋片為基礎的強化降糖組患者的血糖保持平穩,與標準治療組患者比較,發生終末期腎病(需持續透析或腎移植)的風險降低了46%(P=0.007)。這意味著格列齊特緩釋片在ADVANCE和ADVANCE-ON兩個共長達10年的研究中均顯示出長期的腎獲益[5-6]。
蛋白尿是腎病較為常見的病理變化產物,也是腎病發病過程中的微觀癥候。研究顯示,格列齊特在控制血糖水平的同時,還能夠有效改善微量白蛋白尿[19-21]。楊文英等[19]進行了7個中心、為期3年的隨機對照前瞻性研究,共納入285例糖尿病腎病患者,分為格列齊特和格列本脲2種治療方案組,定期監測患者空腹及餐后2 h血糖以及HbA1c水平,直至達到控制目標,并每年檢查眼底及尿中微量白蛋白的排量。治療3年后的患者數據顯示,格列齊特治療與尿微量白蛋白排量增加≥20 μg/min的狀態呈負相關(P=0.009 6)。該研究還證實了格列齊特對防止患者尿微量白蛋白輕度進展的作用優于格列本脲。Yanagawa T等[20]的研究旨在探討格列齊特和吡格列酮對糖尿病腎病患者微量白蛋白尿的影響,納入的40例患者分別接受格列齊特(21例)和吡格列酮(19例)治療12周,結果顯示兩者均能較好地改善患者的微量白蛋白尿。可見,格列齊特通過對血糖水平的嚴格控制,可有效改善患者蛋白尿,顯示出格列齊特對腎的保護作用,提示格列齊特顯著的降糖作用是其具有腎保護作用的基礎。
2.2 格列齊特的化學結構帶來腎保護作用
格列齊特的獨特化學結構是其具有腎獲益的另一關鍵因素。磺脲類藥物化學結構的共同之處在于其存在相同的磺脲基團,而在其他側鏈結構上存在差異。格列齊特、格列本脲和格列美脲3種磺脲類藥物的化學結構見圖1。與其他磺脲類藥物不同的是,格列齊特的化學結構上無苯胺酸基團,其他基團結構上則多出1個氮雜環,這一氮雜環結構能夠接受活性自由基ROS的電子,并發生構象變化,使自由基形成穩定結構,從而發揮清除自由基及抗氧化應激的作用[22-24]。在活性氧自由基和氧化應激受到改善或抑制后,誘導細胞凋亡的途徑激活也受到抑制,從而可進一步減少腎細胞凋亡、腎組織損傷和內皮功能損傷,進而延緩糖尿病腎病的發生與發展[23,25-26]。研究表明,格列齊特能夠明顯清除活性氧自由基,改善氧化應激,且改善氧化應激的能力明顯優于其他磺脲類藥物[22,27-30]。此外,格列齊特還能顯著改善2型糖尿病患者血流介導的血管舒張及循環內皮祖細胞水平,從而改善內皮功能[28]。
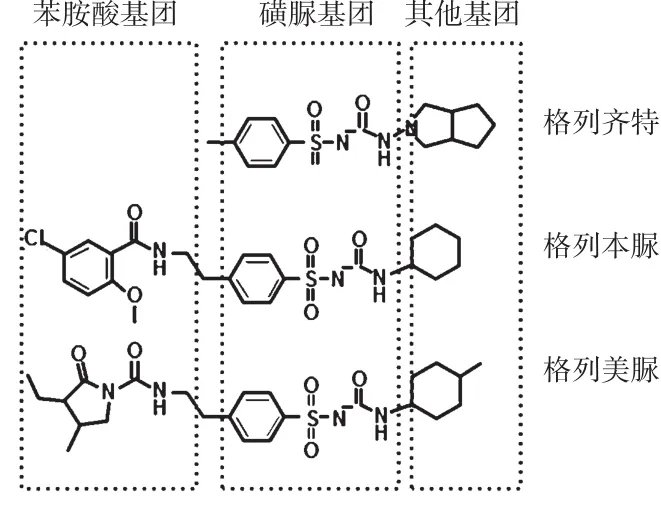
圖1 格列齊特、格列本脲和格列美脲的化學結構
因此,在與其他藥物控制血糖水平等效的情況下,格列齊特具有更好的腎保護作用。Lee YH等[31]的研究納入4 486例糖尿病腎病患者,旨在比較不同磺脲類藥物(格列齊特和格列美脲)治療糖尿病腎病患者的臨床結局。該研究的中位隨訪時間為4.8年,其亞組分析顯示,血糖控制達標(HbA1c<7%)的患者中格列齊特組患者終末期腎病(需持續透析或腎移植)的發生風險(P=0.017)和血肌酐顯著增加(持續為基線測量值的3倍)的風險(P=0.022)均明顯低于格列美脲組。該項研究中,格列齊特和格列美脲組患者整體的終末期腎病發生風險和持續血肌酐倍增風險均無明顯差異(P>0.05);而在血糖控制達標的亞組分析中,格列齊特組患者顯示出顯著的腎獲益。由此推斷,對于血糖控制良好的糖尿病腎病患者,格列齊特相比格列美脲的腎獲益可能來自于藥物本身,即格列齊特的氮雜環結構對改善氧化應激和內皮功能障礙具有一定作用。
3 結語
綜上所述,糖尿病腎病的發生與發展和高血糖、氧化應激和內皮功能障礙等密切相關。格列齊特為傳統降糖藥物,相關循證研究顯示,該藥可為糖尿病腎病患者帶來腎獲益,原因為格列齊特帶來顯著的降糖作用,以及其化學結構中獨特的氮雜環結構。其中,該氮雜環結構能夠接受活性自由基ROS的電子,并發生構象變化,使自由基形成穩定結構,從而清除自由基,起到抗氧化應激、改善內皮功能的作用,是格列齊特帶來腎獲益的關鍵原因。多項臨床研究顯示,格列齊特能夠顯著降低糖尿病腎病患者發生微量白蛋白尿的風險,帶來腎獲益,但其具體機制還有待進一步研究驗證。
[1]Litwak L,Goh SY,Hussein Z,et al.Prevalence of diabetes complications in people with type 2 diabetes mellitus and its association with baseline characteristics in the multinationalA1chieve study[J].Diabetol Metab Syndr,2013,5(1):57.
[2]Bhalla V,Zhao B,Azar KM,et al.Racial/ethnic differences in the prevalence of proteinuric and nonproteinuric diabetic kidney disease[J].Diabetes Care,2013,36(5):1215-1221.
[3]Liu ZH.Nephrology in China[J].Nat Rev Nephrol,2013,9(9):523-528.
[4]中華醫學會內分泌學分會.中國成人糖尿病腎臟病臨床診斷的專家共識[J].中華內分泌代謝雜志,2015,31(5):379-385.
[5]ADVANCE Collaborative Group,Patel A,MacMahon S,et al.Intensive blood glucose control and vascular outcomes in patients with type 2 diabetes[J].N Engl J Med,2008,358(24):2560-2572.
[6]Zoungas S,Chalmers J,Neal B,et al.Follow-up of bloodpressure lowering and glucose control in type 2 diabetes[J].N Engl J Med,2014,371(15):1392-1406.
[7]Marso SP,Daniels GH,Brown-Frandsen K,et al.Liraglutide and cardiovascular outcomes in type 2 diabetes[J].N Engl J Med,2016,375(4):311-322.
[8]Wanner C,Inzucchi SE,Lachin JM,et al.Empagliflozin and progression of kidney disease in type 2 diabetes[J].N Engl J Med,2016,375(4):323-334.
[9]曾龍驛,江瑋.重視糖尿病腎病發生機制的研究[J].中華醫學雜志,2016,96(17):1313-1314.
[10]Elmarakby AA,Abdelsayed R,Yao Liu J,et al.Inflammatory cytokines as predictive markers for early detection and progression of diabetic nephropathy[J].EPMA J,2010,1(1):117-129.
[11]Fragoso A,Mendes F,Silva AP,et al.Insulin resistance as a predictor of cardiovascular morbidity and end-stage renal disease[J].J Diabetes Complications,2015,29(8):1098-1104.
[12]Mima A.Inflammation and oxidative stress in diabetic nephropathy:new insights on its inhibition as new therapeutic targets[J].J Diabetes Res,2013,doi:10.1155/2013/248563.
[13]楊楠楠,剛曉坤,劉青,等.糖尿病腎病與氧化應激[J].中國老年學雜志,2013,33(5):1237-1239.
[14]趙鵬鳴,王儉勤,梁耀軍,等.內皮細胞損傷在糖尿病腎病發病機制中的作用[J].中國糖尿病雜志,2016,24(7):669-672.
[15]中華醫學會糖尿病學分會.中國2型糖尿病防治指南:2013年版[J].中華糖尿病雜志,2014,6(7):447-498.
[16]Landman GW,de Bock GH,van Hateren KJ,et al.Safety and efficacy of gliclazide as treatment for type 2 diabetes:a systematic review and meta-analysis of randomized trials[J].PLoS One,2014,9(2):e82880.
[17]Zoungas S,Chalmers J,Kengne AP,et al.The efficacy of lowering glycated haemoglobin with a gliclazide modified release-based intensive glucose lowering regimen in the ADVANCE trial[J].Diabetes Res Clin Pract,2010,89(2):126-133.
[18]Perkovic V,Heerspink HL,Chalmers J,et al.Intensive glucose control improves kidney outcomes in patients with type 2 diabetes[J].Kidney Int,2013,83(3):517-523.
[19]楊文英,甘佩珍,金之欣,等.格列齊特對糖尿病微血管病變的影響:多中心3年前瞻性研究[J].中華內分泌代謝雜志,2001,17(3):144-147.
[20]Yanagawa T,Araki A,Sasamoto K,et al.Effect of antidiabetic medications on microalbuminuria in patients with type 2 diabetes[J].Metabolism,2004,53(3):353-357.
[21]Erdmann E.Microalbuminuria as a marker of cardiovascular risk in patients with type 2 diabetes[J].Int J Cardiol,2006,107(2):147-153.
[22]Lau CS,Belch JJ.The in vitro free radical scavenging activity of tenidap,a new dual cyclo-oxygenase and 5-1ipoxygenase inhibitor[J].Mediators Inflamm,1992,1(2):141-143.
[23]Gribble FM,Reimann F.Sulphonylurea action revisited:the post-cloning era[J].Diabetologia,2003,46(7):875-891.
[24]Schernthaner G.Gliclazide modified release:a critical review of pharmacodynamic,metabolic,and vasoprotective effects[J].Metabolism,2003,52(8 Suppl 1):29-34.
[25]Ruiz M.Diamicron(gliclazide)MR:the secretagogue with clinical benefits beyond insulin secretion[J].Medicographia,2013,35:81-89.
[26]皇甫冰,高繼萍,楊霞,等.氧化應激與腎臟細胞凋亡[J].中國比較醫學雜志,2015,25(2):54-60.
[27]Onozato ML,Tojo A,Goto A,et al.Radical scavenging effect of gliclazide in diabetic rats fed with a high cholesterol diet[J].Kidney Int,2004,65(3):951-960.
[28]Chen LL,Yu F,Zeng TS,et al.Effects of gliclazide on endothelial function in patients with newly diagnosed type 2 diabetes[J].Eur J Pharmacol,2011,659(2/3):296-301.
[29]張慧娟,劉曉民,王月影,等.格列齊特對2型糖尿病患者氧化應激狀態的影響[J].中國糖尿病雜志,2007,15(12):748-749.
[30]O’Brien RC,Luo M,Balazs N,et al.In vitro and in vivo antioxidant properties of gliclazide[J].J Diabetes Complications,2000,14(4):201-206.
[31]Lee YH,Lee CJ,Lee HS,et al.Comparing kidney outcomes in type 2 diabetes treated with different sulphonylureas in real-life clinical practice[J].Diabetes Metab,2015,41(3):208-215.
R587.2
A
1001-0408(2017)29-4170-04
DOI10.6039/j.issn.1001-0408.2017.29.39
*主管藥師。研究方向:臨床藥學。電話:021-25077205。E-mail:zhaolanxh@aliyun.com
2016-12-17
2017-06-22)
(編輯:陶婷婷)

