螺旋CT在進展期胃癌術前分期中的應用
鄭啟元,顧祿壽,王好微
(1.甘肅省武威腫瘤醫院,甘肅 武威 733000;2.重慶云陽益康醫院,重慶 云陽 404500)
螺旋CT在進展期胃癌術前分期中的應用
鄭啟元1,顧祿壽2,王好微1
(1.甘肅省武威腫瘤醫院,甘肅 武威 733000;2.重慶云陽益康醫院,重慶 云陽 404500)
目的 通過與術后病理結果比較,評價多排螺旋CT在進展期胃癌術前TNM分期中的應用價值。方法 對28例經胃鏡證實的胃癌患者行多層螺旋CT平掃及雙期增強掃描,確定腫瘤浸潤深度(T)、淋巴結轉移(N)、遠處轉移(M),并與手術后病理結果進行對照分析。結果28例患者多層螺旋CT與手術病理檢查結果比較顯示TNM判斷準確率為18例(64.23%)。T分期判斷準確率為23例(82.14%),N分期判斷準確率為21例(75.00%),M判斷準確率為(100%)。結論 MSCT在進展期胃癌的術前分期中具有重要的參考價值。
胃癌;增強CT;TNM分期
胃癌是最常見的消化系統惡性腫瘤,胃癌根據腫瘤的浸潤深度分為早期胃癌和進展期胃癌。目前首選的治療方法是手術切除,術前準確評估腫瘤的TNM分期對于腫瘤的治療尤為重要;胃癌術前確診最簡單的方法是胃鏡檢查,然而外科醫生關注更重要的是腫瘤的浸潤深度,有無淋巴結轉移及遠處轉移。以往研究發現局部浸潤和淋巴結轉移是影響進展期胃癌患者生存率和預后的相關重要因素[1]。超聲內鏡、CT、MRI均可用于腫瘤的術前分期并各具優勢,其中螺旋CT應用普及率最高,已經成為首選的影像學檢查方法。關于胃癌的CT診斷與術前分期的應用報道很多,與術后病理對照TNM符合率各有不同。筆者根據所收集的影像病理對照資料,探討影響胃癌術前正確分期的各種因素,旨在客觀評價螺旋CT在胃癌術前分期中的優勢與不足。
1 資料與方法
1.1 臨床資料 選擇甘肅省武威腫瘤醫院2015~2016年經胃鏡確診并經手術病理證實的進展期胃癌患者28例,其中男25例,女3例,年齡44~74歲,平均年齡(58±8)歲。所有患者均在術前1周內行平掃及MSCT雙期增強檢查,所有患者均為首次發現病灶,未經抗腫瘤等治療。臨床表現主要為上腹脹痛不適,黑便。
1.2 檢查方法 采用美國GE Brightspeed16層螺旋CT機,病人空腹,于檢查前肌注鹽酸(氫溴酸)山莨菪堿20 mg,待口干后服溫開水400~1 000 mL,使胃部最大限度充盈。患者取仰臥位,掃描前進行屏氣訓練,掃描范圍膈頂至臍部。掃描參數:120 kv,Auto mA,層厚 5 mm,螺距 1.375∶1,矩陣512×512。利用高壓注射器以3~4 mL/s的速率經肘靜脈團注碘海醇80 mL,濃度300 mgI/mL,延遲25~30 s后進行動脈期掃描,65~70 s靜脈期掃描。
記錄包括胃癌位置、厚度、雙期病變強化特點,進行胃癌T分期。記錄淋巴結轉移部位、數目、大小、強化特點進行N分期,記錄肝臟等實質臟器有無異常強化、腹膜有無異常增厚及腹水進行M分期,
TNM分期結果由2名高年資放射科醫生共同閱片確定。1.3 胃癌分期診斷標準 采用UICC第5版TNM分期標準進行分期。用T表示浸潤深度:T1,腫瘤侵及黏膜和(或)黏膜肌或黏膜下層;T2,腫瘤侵及肌層或漿膜下;T3,腫瘤侵透漿膜;T4,腫瘤侵犯鄰近結構。用N表示淋巴結轉移:N0,無淋巴結轉移;N1,1~6個區域性淋巴結轉移;N2,7~15個區域性淋巴結轉移;N3,超過15個區域性淋巴結轉移。用M表示遠處轉移:M0,無遠處臟器轉移;M1,有遠處臟器轉移(包括肝、肺、腹膜、腎、腹腔淋巴結和腹水)。
2 結果
多層螺旋CT雙期增強掃描對胃癌術前TNM分期總準確率為64.23%,T分期總準確率為82.14%,其中T2準確率50%,T3準確率86.96%,T4準確率66.67%,N分期總準確率為75.00%,其中N075.00%、N166.67%、N270.59%、N380.00%。M分期準確率為100%。
2.1 胃癌的T分期 與手術病理分期對照組織病理檢查結果。見表1。
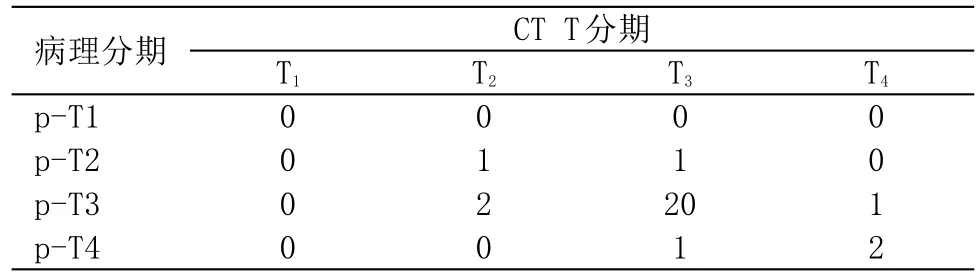
表1 手術病理與螺旋CT胃癌T分期對照(n)
2.2 胃癌N分期 與手術病理分期對照組織病理檢查結果。見表2。
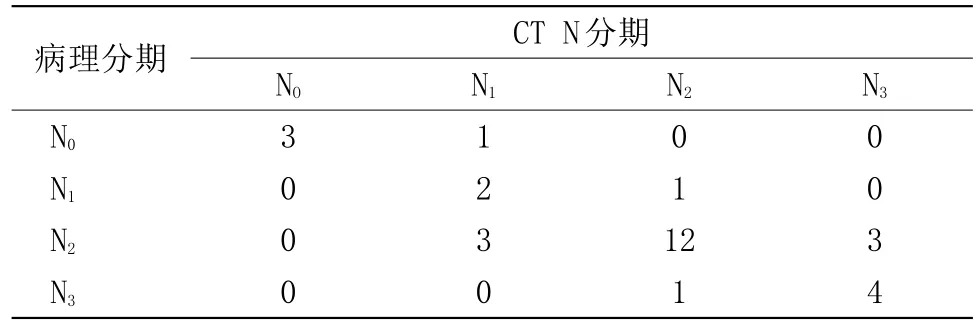
表2 手術病理與螺旋CT胃癌N分期對照(n)
2.3 胃癌患者MDCT TNM分期與手術病理分期對照對照組織病理檢查結果。見表3。
3 討論
3.1 胃癌的增強CT表現與T分期 胃癌T分期是用于判斷腫瘤原發灶對胃壁的浸潤深度,對于能否手術切除至關重要。基于多層螺旋CT快速掃描、薄層重建、高分辨率成像優勢,使胃癌術前檢測及準確分期成為可能[2]。在MSCT增強圖像上,充盈良好的胃腔胃壁厚度通常在5 mm以下,當局部胃壁增厚大于5 mm,動脈期出現黏膜下層早期強化或門靜脈期強化持續推進貫穿全層,使胃壁原有的分層結構消失作為胃癌的診斷金標準[3]。充盈良好的胃腔胃壁一般顯示為兩層或三層結構,其中兩層結構最多見,顯示率約為60%[4]。當胃壁顯示為雙層結構時,外層為肌層及漿膜層,增強后僅輕度強化。內層結構為黏膜層及黏膜下層,呈明顯線樣強化。少數情況下胃壁可以顯示為三層結構,外層結構代表肌層與漿膜層,增強后呈輕中度強化。中層結構代表黏膜下層,其相對于粘膜層顯示為低密度;內層結構為黏膜層,增強后呈明顯線樣強化;單層型早期胃癌表現為胃壁正常或略顯增厚,有或無異常強化;多層型胃壁異常增厚強化區可見中外層結構清晰顯示;進展期胃癌在動脈早期可見黏膜下層早期強化,門靜脈期時病灶強化區持續推進擴大,貫穿整個病灶。在門靜脈期觀察胃壁有無全層強化,漿膜面及周圍脂肪間隙是否毛糙以及與鄰近結構脂肪間隙消失與否,是區分T2,T3及T4期病灶的關鍵。本研究全部為進展期胃癌患者,T分期總準確率達82.14%,由于胃癌周圍脂肪間隙內存在微浸潤和炎癥反應,MSCT對于T2、T3的區分存在過度和不足,其中T2期誤判為T3期1例,T3期誤判為T2期2例,因此,當胃癌的漿膜輪廓征象不規則或有索條凸出時,應結合其他征象來作出正確的分期。Chen CY等人報道,軸位結合MPR可以將胃癌T分期的準確率由73%提高到89%[5]。胃癌的能譜曲線不僅可以反應腫瘤的浸潤深度,利用單能量模式重建增強影像進行物質分離定量分析有助于癌腫胃周脂肪浸潤的判定[6],所以利用MPR重建及能譜曲線變化規律進行綜合分析,有助于提高T分期的準確率。
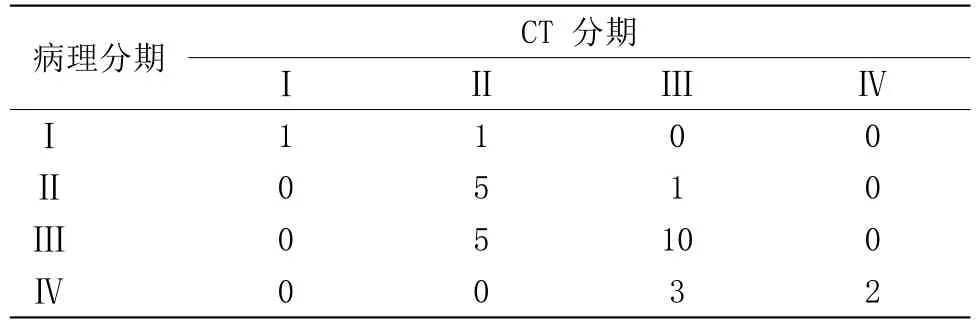
表3 手術病理與螺旋CT胃癌TNM分期對照(n)
3.2 胃癌的淋巴結轉移與分期 淋巴結轉移是胃癌轉移的重要途徑之一,進展期胃癌患者若出現胃周淋巴結轉移其術后五年生存率明顯減低,術前評估淋巴結轉移情況對于胃癌預后及臨床治療決策具有重要的意義,可以幫助選擇合理的淋巴結切除范圍,提高患者生存率。目前胃癌術前分期中最有爭議的是轉移淋巴結的判定,雖然淋巴結大小與轉移率呈顯著正相關,但有部分淋巴結存在假陽性與假陰性,喬英等[7]發現,蠶噬狀、囊狀、周邊高密度中心低密度相對高密度及花斑者,呈串珠狀排列并融合,對血管產生壓迫和腫塊狀增大的淋巴結,增強并有強化首先考慮轉移。唐磊提出了測量淋巴結均徑及徑線和的方法,通過CT檢出淋巴結的數目聯合徑線和對于術前N分期具有積極意義[8]。在一項Meta分析中[9],影像學N分期準確率在50%~70%不等。本研究中N分期整體準確率為75.00%,其判斷標準及準確性與喬英、Meta分析數據基本一致。本研究顯示絕大部分轉移淋巴結無論大小,首先從鄰近腫瘤部位發生第一站轉移,然后隨支配血管繼續向下一站轉移,在上述引流區域發現異常腫大淋巴結,對判斷淋巴結轉移有一定幫助。MDCT對于胃小彎、賁門、腹主動脈旁、腹腔干周圍轉移淋巴結敏感性較高,胃竇部、脾動脈旁淋巴結敏感性較差。
胃癌遠處轉移主要轉移部位包括肝臟、肺及腹膜腔,其中肝臟轉移最常見[10]。本研究中所有患者以肝臟轉移瘤和腹水作為遠處轉移征象,術中均未發現肝臟典型轉移瘤及可疑癌性腹水,故M0期的準確率為100%。
綜上所述,MDCT對胃癌浸潤深度的評價一致性高,可以作為評價胃癌T分期的可靠方法,對胃癌淋巴結轉移的評價一致率不夠理想,對遠處轉移評價較為準確,對肝轉移、腹膜后淋巴結轉移評價較為準確,但對無腹水的腹腔種植轉移小結節或網膜種植轉移小結節敏感性不高,容易漏診。
[1] Pye JK,Crumplin ME,Biffin A,et al.One—year survey of carcinoma of the oesophagus and stomach in Wales[J].Br J Surg,2001,88:278-285.
[2] 楊旋彪,許茂杰.多層螺旋CT對胃癌的診斷價值[J].當代醫學,2012,18(7):5-6.
[3] 曾凡勇,金彪,張海兵.64排螺旋CT多期增強掃描對進展期胃癌術前評估的價值[J].中國腫瘤臨床與康復,2013,20(11):1221-1223.
[4] Zhang H,Pan Z,Du L,et al.Advanced gastric cancer and perfusion imaging using a multidetector row computed tomography:correlation with prognostic determinants[J].Korean Journal of Radiology,2008,9(2):119-127.
[5] Chen CY,Hsu JS,Wu DC,et al.Gastric cancer:preoperative local staging with 3D multi-detector row CT-correlationwithsurgicalandhistopathologic results[J].Radiology,2007,242(2):472-482.
[6] Bolus DN.Dual-energy computed tomographic canners:principles,comparisons,and contrasts[J].J Comput Assist Tomogr,2013,37:944-947.
[7] Qiao Ying,Li Jianding,Zhang Ruiping,et al.Diagnostic vaIue of tri-phasic enhanced spiral CT in the diagnosis of lymph node metastasis of gastric carcinoma[J].Radiol Practice,2006,21(5):507-510.
[8] Tang Lei,Zhang Xiaopeng,Sun Yingshi,et al.Comparison study of CT indicators and pathological N staging in lymph node metastasis of gastric cancer[J].Chin J GastroIntestinal Surg,2008,11(6):529-532.
[9] Seevaratnam R,Cardoso R,McGregor C,et al.How useful is preoperative imaging for tumor,node,metastasis(TNM)staging of gastric cancer?A meta-analysis[J].Gastric Cancer,2012,15(Suppl 1):S3-S18.
[10]徐月陽,牛建華,袁明,等.64排螺旋CT與組織病理對胃癌患者TNM分期的對照研究[J].中華實用診斷與治療雜志,2013,27(9):875-877.
10.3969/j.issn.1009-4393.2017.30.036

