煙草磷酸酶基因NtPP2C16的克隆、表達載體構建及表達分析
張雪薇,劉 侖,魯黎明,李立芹
(四川農業大學 農學院,四川 成都 611130)
煙草磷酸酶基因NtPP2C16的克隆、表達載體構建及表達分析
張雪薇,劉 侖,魯黎明,李立芹
(四川農業大學 農學院,四川 成都 611130)
2C型絲氨酸/蘇氨酸蛋白磷酸酶(PP2C-type protein phosphatases,PP2C)是ABA信號轉導途徑中的關鍵組分,在植物生長發育、細胞周期調節及應對逆境脅迫的過程中發揮重要的作用。為探究PP2C基因在煙草適應非生物脅迫中的功能,從煙草栽培品種K326中克隆到了一個PP2C同源基因,該基因開放閱讀框為1 617 bp,編碼538個氨基酸殘基。同源性分析結果顯示,該基因所編碼的蛋白與絨毛狀煙草PP2C16的親緣關系最近,故命名為NtPP2C16。生物信息學分析表明,NtPP2C16催化區域上具有PP2C家族進化中相對保守的11個結構亞區。qRT-PCR研究分析結果表明:該基因的表達顯著受ABA和H2O22種信號分子誘導,并且響應干旱、高鹽、低溫和低鉀脅迫。成功構建NtPP2C16-pBI121過表達載體,為解析NtPP2C16參與煙草非生物逆境脅迫響應提供一定的理論依據。
煙草;NtPP2C16;克隆;序列分析;表達
蛋白磷酸酶和蛋白激酶參與催化的蛋白質可逆磷酸化反應不僅是存在于生物體內的一種最為普遍的調節方式,也是植物細胞信號轉導過程中的重要機制之一[1]。蛋白磷酸酶根據底物分子去磷酸化氨基酸殘基的不同,主要可分為三大類:Ser/Thr型蛋白磷酸酶(Protein serine/threonine phosphatases,PSPs)、Tyr型蛋白磷酸酶(Protein tyrosine phosphatases,PTPs)和雙重底物特異性蛋白磷酸酶(Dual specific protein phosphatase,DSPs ),近年研究還發現His型蛋白磷酸酶,能催化His殘基的去磷酸化,PP2C蛋白是一類依賴Mg2+或Mn2+的單體Ser/Thr蛋白磷酸酶[2-3]。PP2Cs是一類多基因家族,廣泛的參與逆境信號的傳遞過程,目前已經從模式植物擬南芥和水稻中分別鑒定到80,78個PP2C家族成員[4]。
研究發現,擬南芥中PP2C類蛋白磷酸酶參與脫落酸(Abscisic acid,ABA)、茉莉酸(Jasmonic acid,JA)、水楊酸(Salicylic acid,SA)等多種信號轉導途徑[5-7]。擬南芥PP2C類蛋白A亞族成員ABI1、ABI2、HAB1、HAB2、AHG1、PP2CA等,能與一種正調控因子SnRK2(SNF1-related protein kinase)蛋白激酶互作,在ABA信號通路參與的植物對逆境脅迫的適應性反應過程中起負調控作用[8-10]。擬南芥中G類PP2C蛋白AtPP2CG1能夠調控擬南芥對鹽脅迫的響應,且該調控依賴于ABA,AtPP2CG1是鹽脅迫和ABA信號轉導的正調控因子[11]。擬南芥中AtPP2CA能夠與保衛細胞外向K+通道GORK相互作用,調節K+的轉運和氣孔關閉[12]。水稻中編碼一類PP2C蛋白的基因OsPP18過表達能增強水稻對滲透和氧化脅迫的耐受性,該途徑不依賴于ABA[13]。玉米ZmPP2C2基因過表達能提高轉基因植株對低溫的耐受性,通過激活抗氧化系統降低胞內H2O2的積累量[14]。擬南芥PP2C蛋白能與一種微管相關蛋白MASP1結合,在干旱脅迫中起負調控作用[15]。綜上所述,PP2C家族基因的功能與ABA信號轉導、非生物逆境脅迫以及細胞內H2O2水平密切相關。
煙草作為我國重要的經濟作物之一,保障我國煙草產區的產量和質量對于我國財政收入以及煙區農業經濟發展尤為重要。低鉀、干旱、鹽堿、冷害等非生物脅迫嚴重影響煙葉的產量及品質[16]。PP2C類蛋白磷酸酶在植物適應或抵制非生物脅迫的過程中發揮著重要作用,本研究從煙草K326中克隆到一個NtPP2C16基因,對NtPP2C16基因編碼的蛋白進行生物信息學相關分析,運用qRT-PCR分析該基因在不同組織中的表達水平以及在信號分子和非生物逆境脅迫下的表達模式,并成功構建NtPP2C16-pBI121過表達載體。對于闡明煙草響應外界非生物脅迫的分子機制和相關信號轉導途徑具有重要意義,為有效利用基因工程技術改良品種提供一定的理論基礎和科學依據。
1 材料和方法
1.1試驗材料及主要試劑
供試植物材料為煙草栽培品種K326(Nicotianatabacumcv.K326),由四川農業大學農學院保存。將煙草種子進行表面消毒,75%乙醇1 min,20%次氯酸鈉溶液20 min,無菌水反復清洗5次,隨后將種子置于MS培養基上發芽生長15 d,挑取長勢一致的煙草幼苗分別進行H2O2、ABA、干旱、高鹽、低溫及低鉀處理,每個處理設有3個重復,處理相應時間(0,3,6,12,24 h)后進行整株取樣。H2O2、ABA、干旱、高鹽處理培養基是在MS培養基中分別加入H2O2(10 mmol/L)、ABA(1 μmol/L)、PEG6000(5%)、NaCl(200 mmol/L)。低溫處理時將待處理材料放置4 ℃的光照培養箱中。低鉀處理時將待處理材料轉移至低鉀MS培養基中,低鉀MS培養基是將MS培養基中的KH2PO4替換為NH4H2PO4,并去掉KNO3。其余成分相同,經測定鉀離子濃度為10 μmol/L。
E.coli感受態DH5α購自Vazyme Biotech公司,TRIzol試劑、高保真酶Pfu、pMD19-T和pBI121載體、cDNA 合成試劑盒,SYBR Green Master Mix、限制性內切酶、DNA Ligation Kit 2.0等試劑購自TaKaRa,通用型DNA純化回收試劑盒購自TIANGEN,引物合成與測序由上海生工生物工程技術有限公司完成。
1.2試驗方法
1.2.1 目的基因克隆 運用同源克隆的方法,根據GenBank數據庫收錄的絨毛狀煙草PP2C16序列(LOC104108656),設計一對NtPP2C16引物:NtPP2C16-F:5′-TCTAGAATGGAGGAGTTGTCTCCAGC-3′,
NtPP2C16-R:5′-CCCGGGTTAACATTTGCTCTTGAATT-3′,下劃線部分分別為XbaⅠ和SmaⅠ酶切位點。以煙草葉片RNA反轉錄的cDNA第一條鏈為模板,PCR擴增NtPP2C16的ORF全長,擴增反應條件為:94 ℃ 5 min;94 ℃ 30 s,55 ℃ 30 s,72 ℃ 2 min,34 個循環;72 ℃ 10 min。目的片段經回收純化、補A、連接pMD19-T克隆載體、轉化E.coliDH5α 后,氨芐青霉素抗性篩選,菌落PCR 鑒定陽性克隆,送至上海生工生物工程技術有限公司進行測序。
1.2.2 生物信息學分析 ProtParam(http://web.expasy.org/protparam/)預測NtPP2C16蛋白的分子量、等電點等理化性質;SOPMA(https://npsa-prabi.ibcp.fr/)和SWISS-MODEL (https://swissmodel.expasy.org/)在線預測NtPP2C16蛋白的二三級結構;SMART(http://smart.embl-heidelberg.de/)分析蛋白的保守結構域;NetPhos3.1(http://www.cbs.dtu.dk/services/NetPhos/)分析蛋白磷酸化位點;PSORT(http://psort1.hgc.jp/form.html)預測NtPP2C16的亞細胞定位;Signal-P4.1(http://www.cbs.dtu.dk/services/SignalP/)預測蛋白信號肽;BlastP比對分析,MEGA5軟件以Neighbor-joining法構建系統進化樹。
1.2.3 表達分析 Primer 5.0設計NtPP2C16基因qRT-PCR引物:NtPP2C16-qF:5′-GCCTCTGAACCTATT
GCC-3′,NtPP2C16-qR:5′-TGCCACGATAAAGGACTG-3′;
煙草18 SrRNA為內參,引物序列為18S-F:5′-CCTACGCTCTGTATACATTAGC-3′;18S-R:5′-GTGTTGA
GTCAAATTAAGCCGC-3′。基因的相對表達量計算方法為2-ΔΔCt法,每組樣品設置3個重復。
1.2.4 構建過表達載體 重組克隆載體NtPP2C16-pMD19-T與表達載體pBI121用內切酶XbaI和SmaⅠ進行雙酶切,酶切體系10 μL:10×T Buffer 1 μL,BSA 1 μL,XbaⅠ 1 μL,SmaⅠ 1 μL,NtPP2C16-pMD19-T/pBI121載體4 μL,ddH2O 2 μL。目的片段回收純化、連接pBI121表達載體,轉化E.coliDH5α,卡那霉素抗性篩選,菌落PCR檢測鑒定陽性克隆,搖菌提取質粒,酶切檢測并送至上海生工生物工程技術有限公司進行測序。
2 結果與分析
2.1NtPP2C16基因克隆
以煙草幼苗葉片RNA反轉錄的cDNA第一條鏈為模板,PCR擴增,1%瓊脂糖凝膠電泳結果表明,PCR產物大小為1 500~2 000 bp(圖1),長度大小與預期目標相符。回收純化目的片段后,連接pMD19-T載體,轉化E.coliDH5α。運用菌落PCR方法鑒定陽性克隆,挑選陽性克隆送至上海生工生物工程有限公司進行測序,測序結果顯示:目的片段大小為1 617 bp。
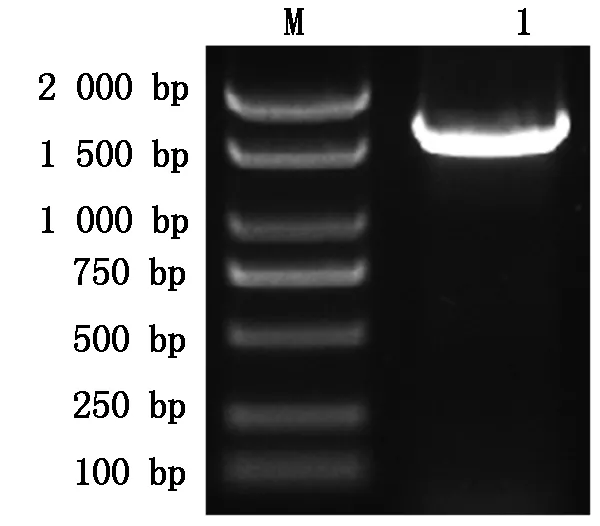
M.Marker 2000 bp;1.NtPP2C16基因。M.Marker 2000 bp;1.NtPP2C16 gene PCR product.
2.2構建NtPP2C16-pBI121過表達載體
將重組克隆載體NtPP2C16-pMD19-T與表達載體pBI121分別進行雙酶切,連接轉化E.coli感受態后,挑選單菌落進行菌落PCR,篩選構建成功的陽性克隆,搖菌提取質粒,XbaⅠ和SmaⅠ雙酶切進行檢測(圖2)。并送至上海生工生物工程有限公司進行測序,測序結果顯示:目的片段大小為1 617 bp,表明NtPP2C16-pBI121過表達載體構建成功。
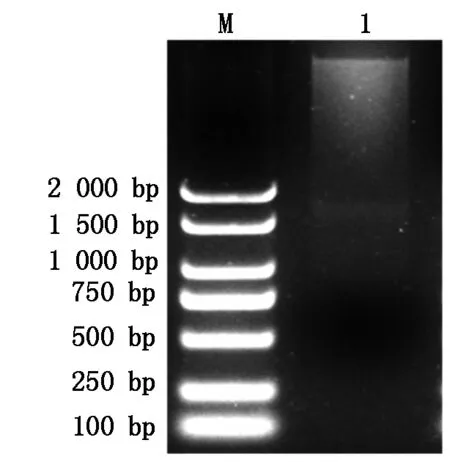
M.Marker 2000 bp;1.NtPP2C16基因酶切片段。M.Marker 2000 bp;1.NtPP2C16 gene digested fragments.
2.3NtPP2C16蛋白序列分析
2.3.1 NtPP2C16蛋白理化性質及疏水性分析 ProtParam預測NtPP2C16蛋白的理化性質分析結果表明,該蛋白編碼538個氨基酸殘基:絲氨酸Ser (55,10.2%)、纈氨酸Val(51,9.5%)、亮氨酸Leu(48,8.9%)、谷氨酸Glu(46,8.6%)、丙氨酸Ala(38,7.1%),而酪氨酸Tyr(7,1.3%)和色氨酸Trp(7,1.3%)含量較低。該蛋白預測的分子量為58.4 kDa,理論等電點pI為4.82,不穩定系數(Instability index)是43.17,該蛋白可能是一個不穩定的蛋白。該蛋白總的親水性平均指數為-0.108,DNAMAN軟件進行的疏水性分析結果顯示,預測該蛋白屬于親水性蛋白(圖3)。
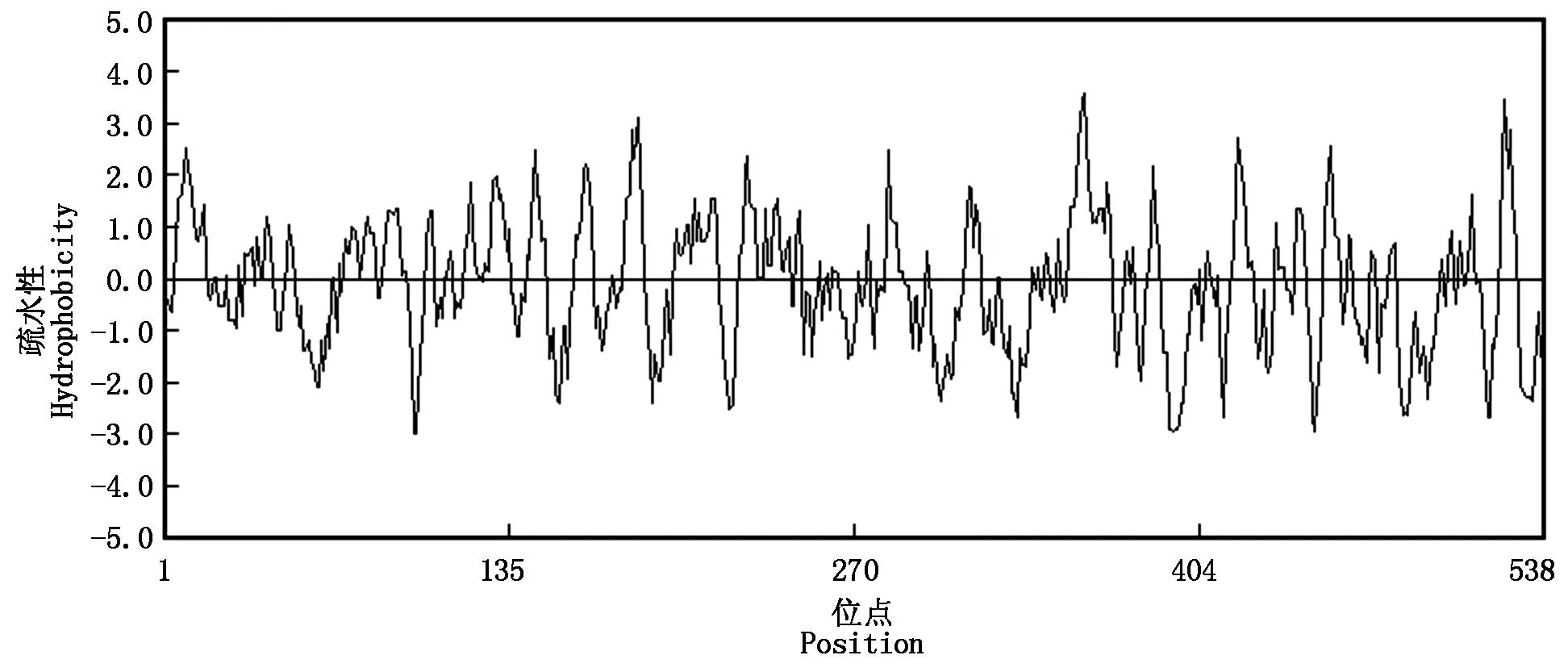
圖3 NtPP2C16疏水區預測Fig.3 Hydrophobic region prediction of NtPP2C16
2.3.2 NtPP2C16蛋白二三級結構預測 IBCP在線工具SOPMA預測NtPP2C16蛋白二級結構,結果顯示:該蛋白中36.99%的氨基酸參與無規則卷曲(Random coil),31.41%氨基酸參與α-螺旋(Alpha helix),22.49%的氨基酸參與延伸鏈(Extended strand),僅有9.11%的氨基酸參與β-轉角(Beta turn),由此可見,該蛋白二級結構的最大元件為無規則卷曲。SWISS-MODEL預測NtPP2C16蛋白三級結構,與二級結構預測進行比照,結果較為統一(圖4)。
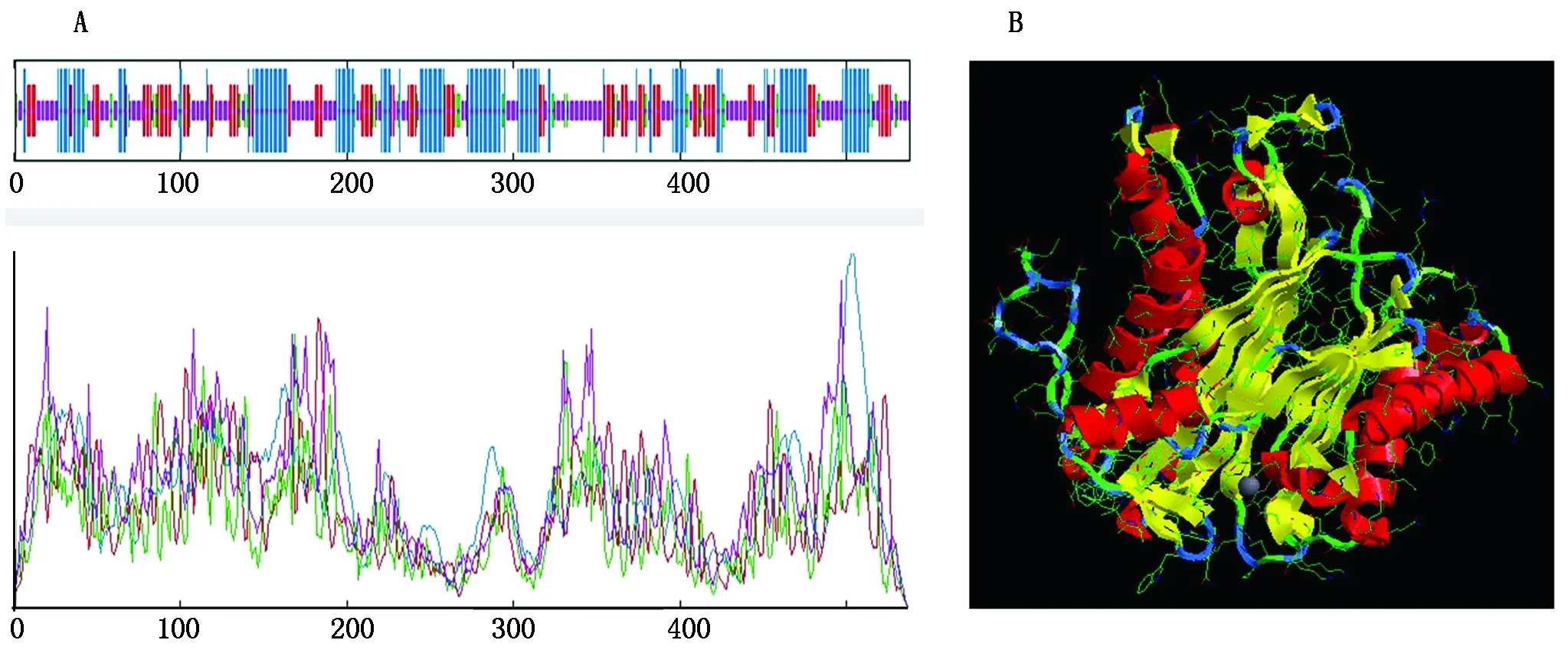
A.二級結構;B.三級結構。A.Secondary structure;B.Tertiary structure.
2.3.3 NtPP2C16蛋白磷酸化位點分析 NetPhos 3.1是利用神經網絡預測真核細胞蛋白質中絲氨酸(Serine) 、蘇氨酸(Threonine)和酪氨酸(Tyrosine)磷酸化位點工具,NetPhos中的內設閾值為0.5,高于0.5,被認為是可能的磷酸化位點。NetPhos 3.1對NtPP2C16蛋白中磷酸化位點分析結果表明(圖5),NtPP2C16中含有35個Ser激酶磷酸化位點,5個Thr激酶磷酸化位點和3個Tyr激酶磷酸化位點。說明NtPP2C16蛋白能被激酶所磷酸化,從而參與非生物逆境脅迫響應過程的調控。
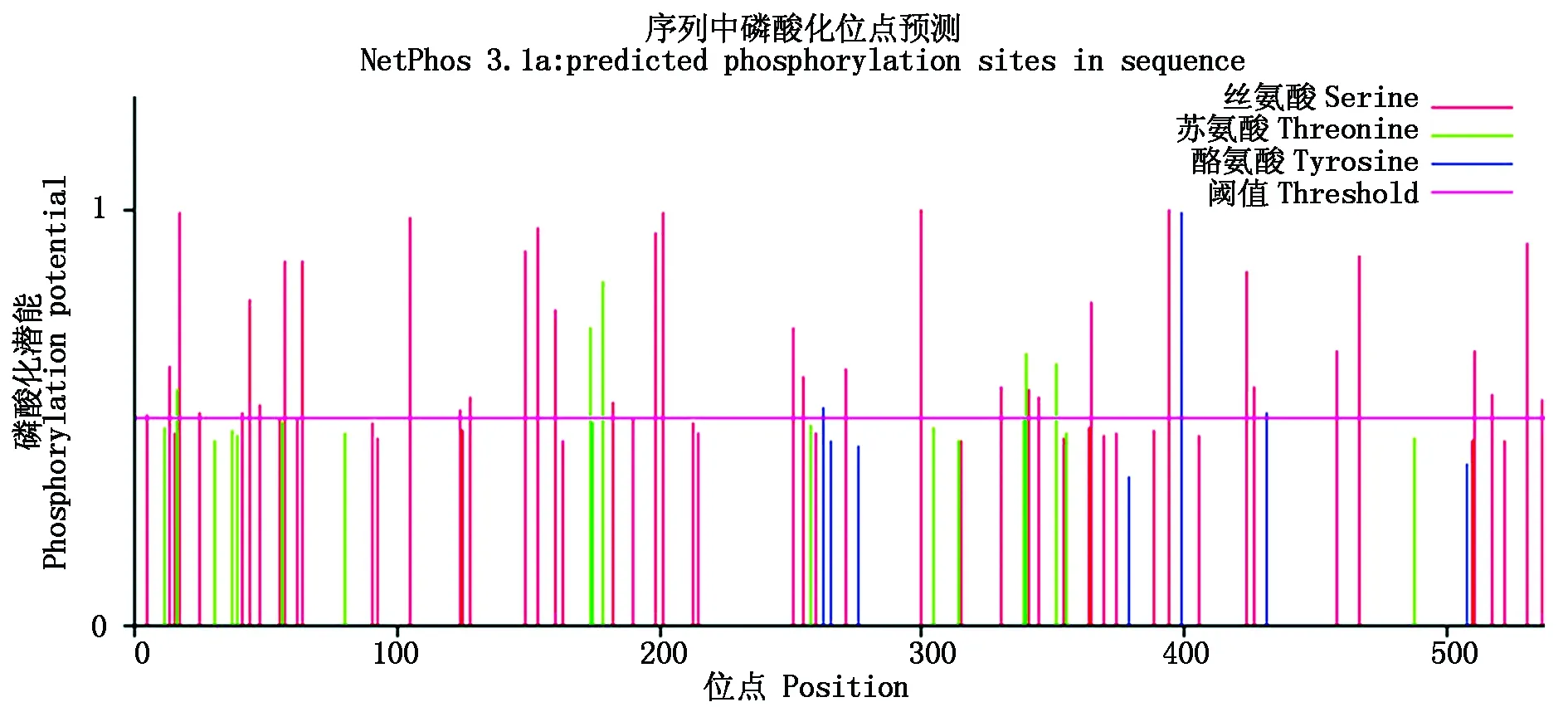
圖5 NtPP2C16的磷酸化位點預測Fig.5 Phosphorylation site prediction of NtPP2C16
2.3.4 NtPP2C16蛋白保守結構域及亞細胞定位分析 SMART軟件分析NtPP2C16蛋白保守結構域,結果表明(圖6),該蛋白含有PP2C家族典型的結構域,位于第210-528位氨基酸。對蛋白質信號肽的分析有助于蛋白質功能域的區分及蛋白質的細胞定位,利用Signal-P4.1軟件預測結果表明:該蛋白不是分泌蛋白,不存在信號肽。利用PSORT在線預測NtPP2C16的亞細胞定位,結果顯示,在質膜上占0.460,在內質網膜上占0.100,在內質網腔中占0.100,預測NtPP2C16可能定位在質膜上。
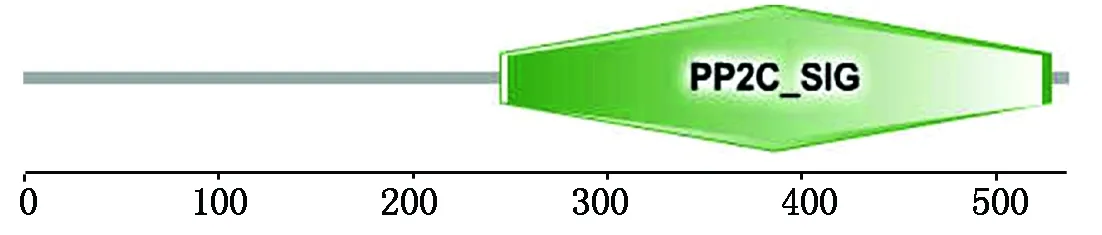
圖6 NtPP2C16的結構域分析Fig.6 Structure domain analysis of NtPP2C16
2.3.5 NtPP2C16同源性分析 通過與模式植物擬南芥中PP2C蛋白ABI1、ABI2、HAB1和HAB2進行多重序列對比,發現NtPP2C16具有PP2C家族典型的結構特征,即催化區域上含有進化中相對保守的11個結構亞區[17](圖7-A),NtPP2C16蛋白的C端比較保守,N端含有一段保守性較弱的延伸區域。將NtPP2C16氨基酸序列與其他植物同源性比較近的PP2C16序列進行聚類分析,結果表明,NtPP2C16與絨毛狀煙草PP2C16、林煙草PP2C16、漸窄葉煙草PP2C16等具有較高的氨基酸序列同源性,分別為99%,99%,97%;與中國白梨PP2C16、蘋果PP2C16的同源性最低,為61%(圖7-B)。
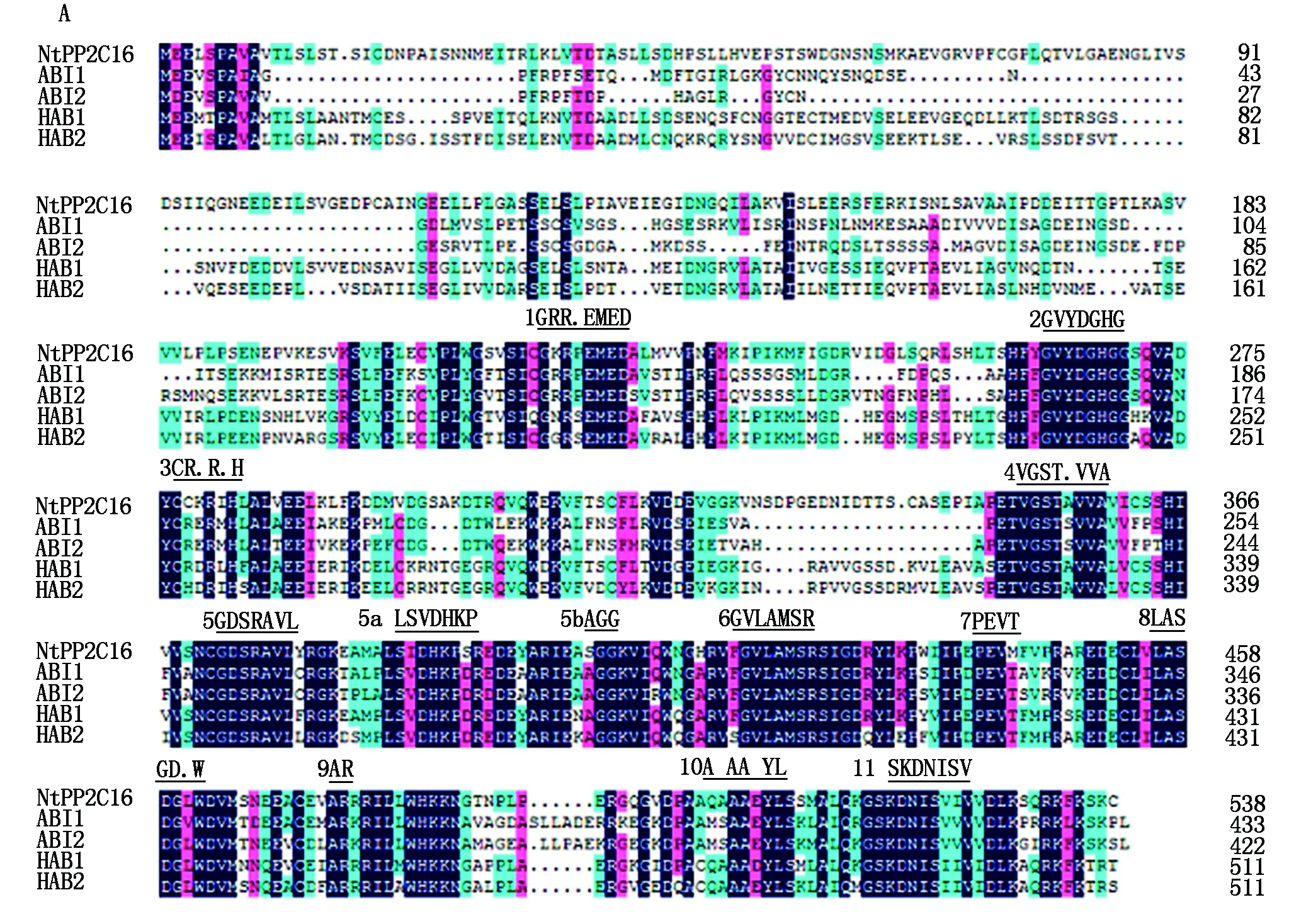
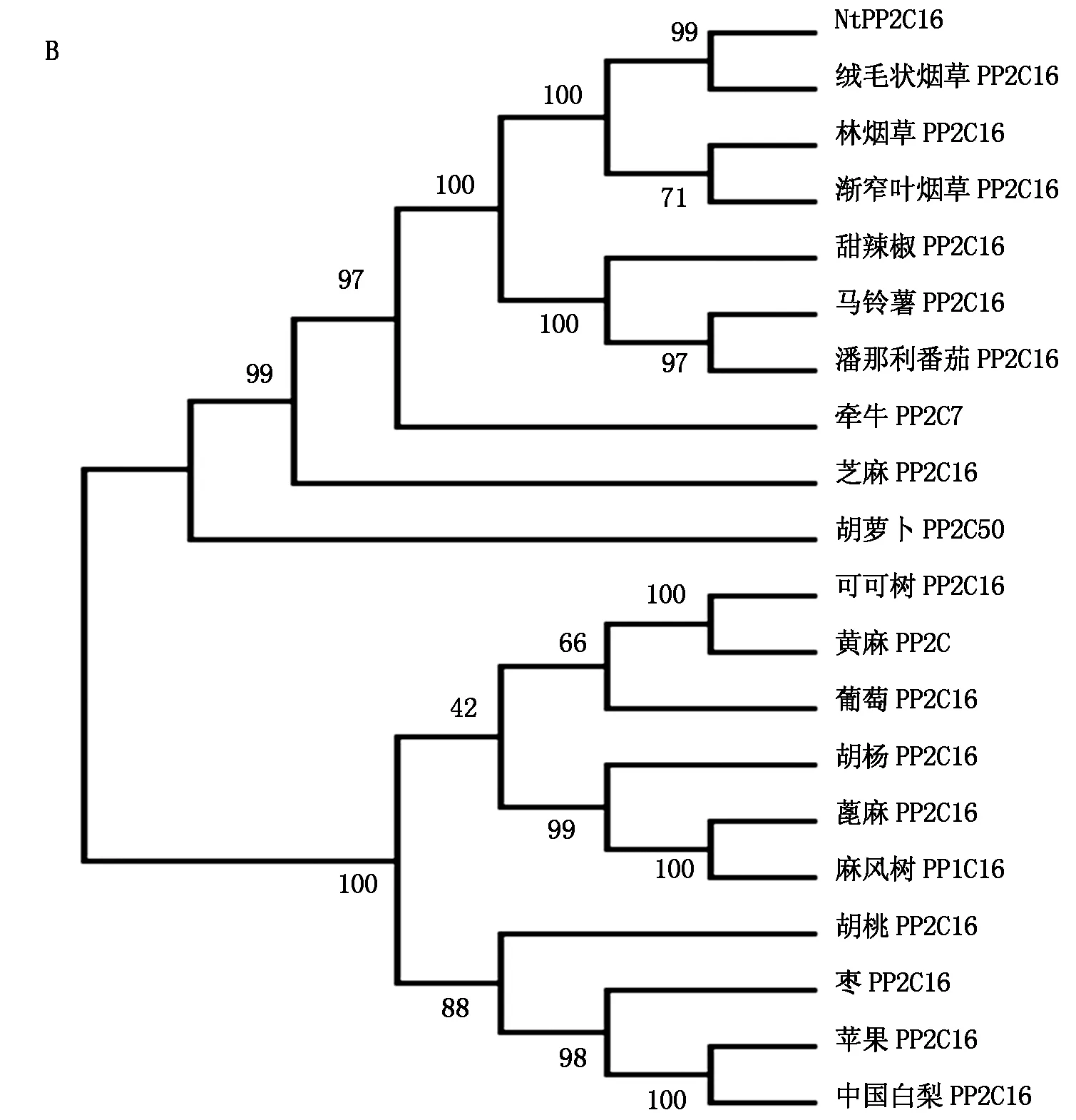
A.NtPP2C16蛋白多重序列比對;B.NtPP2C16蛋白系統進化樹。A.Multiple sequence alignment of NtPP2C16;B. Phylogenetic tree of NtPP2C16.
2.4NtPP2C16的組織表達分析
提取K326幼苗期的根、莖、葉以及成熟期的花RNA,反轉錄成cDNA為模板,進行qRT-PCR反應,分析NtPP2C16在各個組織的表達量,分析結果表明(圖8-A),NtPP2C16的表達量在葉中較高,莖中次之,根中表達量最低。說明NtPP2C16基因在煙草K326各個組織中均有表達,但主要在煙草植株的葉和莖中表達,在不同組織中的表達豐度不同表明該基因的表達存在組織特異性。
2.5NtPP2C16在信號分子處理下的表達分析
10 mmol/L H2O2及1 μmol/L ABA處理煙草K326幼苗,對NtPP2C16基因的表達進行分析。結果表明,H2O2和ABA處理的早期3 h時,NtPP2C16基因的表達量都上升到最大值,分別為對照(0 h)的3.19倍(圖8-B)和2.99倍(圖8-C)。這些結果表明,NtPP2C16能夠響應逆境脅迫相關的信號分子調控,其表達顯著受到H2O2和ABA的誘導(P<0.05)。

圖8 NtPP2C16的不同組織及信號分子處理下的表達模式Fig.8 Expression pattern of NtPP2C16 in different tissues and under signal molecular treatment
2.6NtPP2C16在非生物逆境脅迫處理下的表達分析
5%PEG6000、200 mmol/L NaCl、4 ℃及10 μmol/L K+模擬干旱、高鹽、低溫及低鉀脅迫,對NtPP2C16在逆境脅迫下的表達模式進行分析。結果表明,PEG、NaCl和低溫處理后,該基因的表達量都在6 h時達到最大值,分別為對照(0 h)的2.19倍(圖9-A)、8.60倍(圖9-B)和4.70倍(圖9-C)。低鉀處理下,NtPP2C16的表達在處理早期3 h受到顯著抑制(P<0.05),僅為對照(0 h)的0.24倍(圖9-D)。上述結果表明,NtPP2C16基因能夠參與非生物逆境脅迫,其表達響應干旱、高鹽、低溫以及低鉀處理。
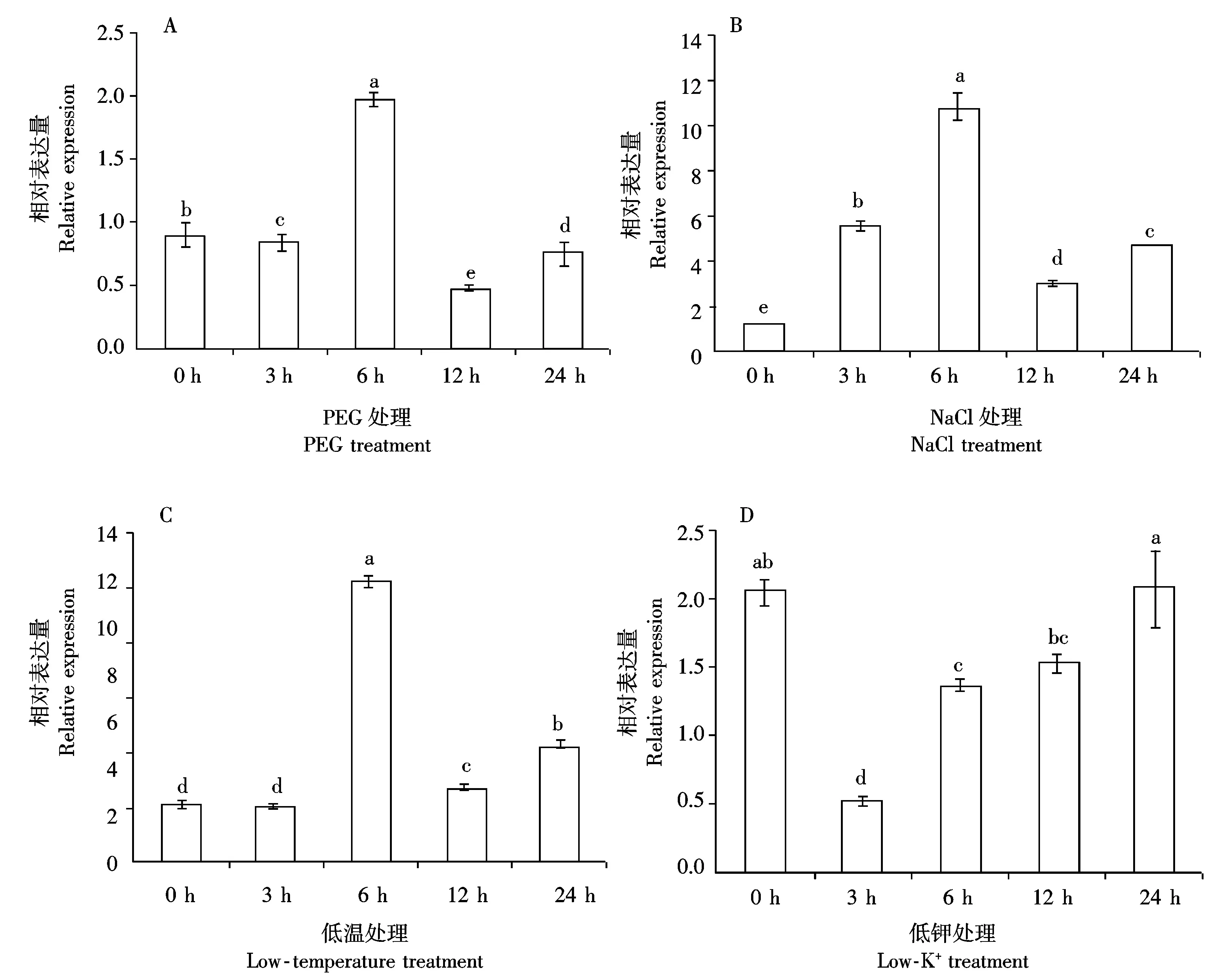
圖9 NtPP2C16在非生物逆境脅迫下的表達模式Fig. 9 Expression pattern of NtPP2C16 under abiotic stress
3 討論
本研究從普通煙草栽培品種K326中克隆到一個PP2C家族成員NtPP2C16的cDNA序列,其ORF為1 617 bp,編碼538個氨基酸。SMART分析和多重序列對比發現,該基因編碼的蛋白具有PP2C家族保守的功能結構域,包含11個蛋白激酶催化結構域,其中包括與二價金屬離子結合的MED、DGH、DG、D殘基和與磷酸鹽離子結合的R殘基。該蛋白的氨基酸同源區域主要位于C端的催化結構域,而N端的保守性相對較弱,含有一段延伸區域,此區域可能參與調控PP2C的活性或者在底物的特異性識別過程中起作用,包括一些轉錄因子特征序列和激酶互作區域等,PP2C結構的復雜性賦予它不同的功能[18]。
組織表達分析結果表明,NtPP2C16基因的表達具有組織特異性,在煙草葉和莖中的表達量較高,在根中的表達量最低,與水稻OsBIPP2C1和OsBIPP2C2的組織表達模式較為一致[19]。白菜BcABI1的表達量在花和葉片中較高,在莖中最低[20],擬南芥AtPP2C46基因的表達量在花中最高,在根中最低[21]。盡管PP2C同源基因序列較為保守,但PP2C家族中不同成員的組織表達模式存在差異,不同物種間PP2C同源基因的功能也存在差異,并發揮著特定的作用。
植物遭受外界逆境脅迫會引起體內代謝水平的變化,ABA、H2O2、乙烯等一些信號分子會顯著積累,這些信號分子通過參與多種信號轉導途徑的交互作用,形成復雜的信號網絡調控植物對逆境脅迫的應答,在植物應對生物和非生物逆境脅迫的適應性過程中發揮著至關重要的作用。qRT-PCR分析結果表明:ABA信號分子處理后,NtPP2C16的表達受到顯著誘導,與歐美楊PdPP2C在ABA處理后的表達模式類似[22],而玉米ZmPP2C在ABA處理后的表達卻受到顯著抑制[23]。H2O2信號分子處理后,NtPP2C16在誘導的早期轉錄水平就達到最大值,與二穗短柄草BdPP2C1在H2O2處理后的表達模式不同,BdPP2C1的表達受到H2O2的顯著抑制[24]。
非生物逆境脅迫下,NtPP2C16的轉錄水平均出現顯著變化,該基因的表達受干旱、高鹽和低溫脅迫誘導,這一結果與雙子葉植物擬南芥中的一些PP2C基因的表達模式相似。大多數的擬南芥A類PP2C家族基因的轉錄水平都能被滲透、高鹽、低溫等非生物脅迫和ABA誘導[25]。而與小麥、水稻、玉米等單子葉植物中的一些PP2C基因的表達模式不同,小麥TaPP2C59的表達受到低溫和高鹽脅迫抑制[26],水稻中5個A類PP2C基因能被低溫脅迫抑制[27],玉米ZmPP2C的表達受干旱抑制[23]。因此,猜測PP2C基因家族的表達模式可能在單子葉和雙子葉植物中發生了分化。NtPP2C16的表達還顯著受低鉀脅迫的抑制,擬南芥中AtPP2CA能與鉀離子通道AKT2和AKT3互作,調控鉀離子的轉運和膜極化[28-29]。因此,猜測NtPP2C16參與煙草抵御干旱、高鹽、低溫及低鉀非生物脅迫刺激的應答反應,調控著相關信號分子的轉導途徑。研究NtPP2C16將有助于理解煙草對逆境脅迫的應答機制。在隨后的研究工作中,將利用CRISPR基因編輯技術或過量表達的方法構建轉基因株系。通過分析轉基因株系應對非生物脅迫的表型,并測定相關的生理指標和檢測Marker 基因的表達,同時利用酵母雙雜交試驗驗證與鉀離子通道蛋白的互作,闡明NtPP2C16在非生物逆境脅迫中的功能及作用機制。
[1] Hunter T. Protein kinases and phosphatases:the yin and yang of protein phosphorylation and signaling[J]. Cell,1995,80(2):225-236.
[2] Cohen P. The structure and regulation of protein phosphatases[J]. Annual Review of Biochemistry,1989,58(1):453-508.
[3] Cohen P T. Novel protein serine/threonine phosphatases:variety is the spice of life[J]. Trends in Biochemical Sciences,1997,22(7):245-251.
[4] Xue T,Wang D,Zhang S,et al. Genome-wide and expression analysis of protein phosphatase 2C in rice andArabidopsis[J]. BMC Genomics,2008,9(1):550.
[5] Meyer K,Leube M P,Grill E. A protein phosphatase 2C involved in ABA signal transduction inArabidopsisthaliana[J]. Science,1994,264(5164):1452-1455.
[6] Schweighofer A,Kazanaviciute V,Scheikl E,et al. The PP2C-type phosphatase AP2C1,which negatively regulates MPK4 and MPK6,modulates innate immunity,jasmonic acid,and ethylene levels inArabidopsis[J]. The Plant Cell,2007,19(7):2213-2224.
[7] Nishimura N,Okamoto M,Narusaka M,et al. ABA hypersensitive germination2-1 causes the activation of both abscisic acid and salicylic acid responses inArabidopsis[J]. Plant & Cell Physiology,2009,50(12):2112-2122.
[8] Gosti F,Beaudoin N,Serizet C,et al. ABI1 protein phosphatase 2C is a negative regulator of abscisic acid signaling[J]. The Plant Cell,1999,11(10):1897-1910.
[9] Soon F F,Ng L M,Zhou X E,et al. Molecular mimicry regulates ABA signaling by SnRK2 kinases and PP2C phosphatases[J]. Science,2012,335(664):85-88.
[10] Komatsu K,Suzuki N,Kuwamura M,et al. Group a PP2Cs evolved in land plants as key regulators of intrinsic desiccation tolerance[J]. Nature Communications,2013,4(7):375-381.
[11] Liu X,Zhu Y,Zhai H,et al. AtPP2CG1,a protein phosphatase 2C,positively regulates salt tolerance ofArabidopsisin abscisic acid-dependent manner[J]. Biochemical and Biophysical Research Communications,2012,422(4):710-715.
[12] Lefoulon C,Boeglin M,Moreau B,et al. TheArabidopsisAtPP2CA protein phosphatase inhibits the GORK K+efflux channel and exerts a dominant suppressive effect on phosphomimetic-activating mutations[J]. The Journal of Biological Chemistry,2016,291(12):6521-6533.
[13] You J,Zong W,Hu H,et al. A stress-responsive NACl-regulated protein phosphatase gene rice protein phosphatase18 modulates drought and oxidative stress tolerance through abscisic acid-independent reactive oxygen species scavenging in rice[J]. Plant Physiology,2014,166(4):2100-2114.
[14] Hu X,Liu L,Xiao B,et al. Enhanced tolerance to low temperature in tobacco by over-expression of a new maize protein phosphatase 2C,ZmPP2C2[J]. Journal of Plant Physiology,2010,167(15):1307-1315.
[15] Bhaskara G B,Wen T N,Nguyen T T,et al. Protein phosphatase 2Cs and microtubule-associated stress protein 1 control microtubule stability,plant growth,and drought response[J]. The Plant Cell,2017,29(1):169-191.
[16] 司叢叢,劉好寶,曲平治. 煙草鉀離子通道及轉基因煙草抗逆性的研究進展[J]. 中國農學通報,2010,26(2):45-49.
[17] Bork P,Brown N P,Hegyi H,et al. The protein phosphatase 2C (PP2C) superfamily:detection of bacterial homologues[J]. Protein Science:a Publication of the Protein Society,1996,5(7):1421-1425.
[18] Shi Y. Serine/threonine phosphatases:mechanism through structure[J]. Cell,2009,139(3):468-484.
[19] 胡學博. 水稻蛋白磷酸酶2C基因OsBIPP2C1和OsBIPP2C2的克隆鑒定與功能分析[D]. 杭州:浙江大學,2004.
[20] 胡 帥. 白菜蛋白磷酸酶2C基因BcABI1的分離與表達分析[D]. 杭州:浙江大學,2012.
[21] 鄧克勤,郭新紅,汪啟明,等. 擬南芥磷酸酶基因亞細胞定位與組織表達[J]. 西北植物學報,2009,29(2):234-239.
[22] 郭 鵬,張士剛,邢 鑫,等. 歐美楊PdPP2C基因的克隆與功能分析[J]. 北京林業大學學報,2015,37(2):100-106.
[23] 徐云峰. 玉米根系蛋白磷酸酶ZmPP2C基因的克隆,表達特性及轉化的研究[D]. 泰安:山東農業大學,2005.
[24] 顏 彥,胡 偉. 二穗短柄草2C型蛋白磷酸基因BdPP2C1的克隆及表達分析[J]. 熱帶作物學報,2014,35(12):2391-2396.
[25] Chan Z. Expression profiling of ABA pathway transcripts indicates crosstalk between abiotic and biotic stress responses inArabidopsis[J]. Genomics,2012,100(2):110-115.
[26] 胡 偉,顏 彥,何艷臻. 小麥TaPP2C59基因的克隆及表達分析[J]. 麥類作物學報,2014,34(10):1334-1340.
[27] Singh A,Giri J,Kapoor S,et al. Protein phosphatase complement in rice:genome-wide identification and transcriptional analysis under abiotic stress conditions and reproductive development[J]. BMC Genomics,2010,11(1):435.
[28] Chérel I,Michard E,Platet N,et al. Physical and functional interaction of theArabidopsisK(+) Channel AKT2 and phosphatase AtPP2CA[J]. The Plant Cell,2002,14(5):1133-1146.
[29] Vranová E,T?htiharju S,Sriprang R,et al. The AKT3 potassium channel protein interacts with the AtPP2CA protein phosphatase 2C[J]. Journal of Experimental Botany,2001,52(354):181-182.
Cloning,ConstructionofExpressionVectorandExpressionAnalysisofNtPP2C16inNicotianaTabacum
ZHANG Xuewei,LIU Lun,LU Liming,LI Liqin
(College of Agronomy,Sichuan Agricultural University,Chengdu 611130,China)
2C protein phosphatase (PP2C) is a key component in the ABA signal transduction pathway and plays a pivotal role in plant growth and development,cell cycle regulation and adaptation to adversity stresses.To explore the function of thePP2Cgene in tobacco adaptation to abiotic stress,aPP2Chomologous gene was cloned from the tobacco cultivar K326,which contained a 1 617 bp ORF encoding 538 amino acid. The homology analysis showed that the gene had high homology with PP2C16 ofNicotianatomentosiformis. So it was namedNtPP2C16. Bioinformatics analysis showed that the NtPP2C16 catalytic region had 11 structural sub-regions which were relatively conservative in the PP2C family evolution. qRT-PCR analysis revealed that the expression of this gene was significantly induced by ABA and H2O2signal molecules,and responded to drought,high salt,low temperature and low potassium stresses.NtPP2C16-pBI121 overexpression vector was constructed successfully,the results provided some basis for analysis ofNtPP2C16 responsing to abiotic stresses in tobacco.
Tobacco;NtPP2C16;Cloning;Sequence analysis;Expression
2017-08-11
植物生理學與生物化學國家重點實驗室開放課題(SKLPPBKF1505;SKLPPBKF1506)
張雪薇(1993-),女,四川自貢人,在讀碩士,主要從事煙草分子生物學研究。
李立芹(1974-),女,山東東阿人,副教授,博士,碩士生導師,主要從事植物分子生物學研究。
Q78;S572.03
A
1000-7091(2017)05-0078-08
10.7668/hbnxb.2017.05.012

