胰十二指腸切除術后感染的危險因素分析與防護對策
楊菊紅
·調查研究·
胰十二指腸切除術后感染的危險因素分析與防護對策
楊菊紅
目的:探討胰十二指腸切除術(PD)后感染的危險因素和護理預防。方法:回顧性分析2012年3月~2017年7月我院肝膽外科70例行PD術患者的臨床資料,根據患者術后是否發生感染分為感染組38例和未感染組32例,觀察感染組患者感染發生部位分布及細菌培養類型,收集患者的術前、術中及術后等一般資料并進行單因素分析,并將有統計學意義單因素進行多元logistic回歸分析,探討PD術后感染發生的危險因素。結果:感染組患者感染部位主要為腹腔、呼吸道、切口、泌尿系統和深靜脈導管,引起患者感染的菌種主要為:大腸埃希菌、肺炎克雷伯菌、銅綠假單胞菌、金黃色葡萄球菌。兩組患者在術前TB、糖尿病、手術時間、術后白蛋白、術后胰瘺及術后胃排空延遲等方面比較,差異具有統計學意義(P<0.05),術前高TB、糖尿病、術后低白蛋白、術后胰瘺等為PD術后發生感染的獨立危險因素(P<0.05)。結論:術前高膽紅素血癥、術前糖尿病、術后低白蛋白、術后胰瘺等是PD術后患者發生感染的獨立危險因素,圍術期根據感染發生的危險因素制定規范護理措施。
胰十二指腸切除術;感染;危險因素;護理
10.3969/j.issn.1672-9676.2017.23.041
目前,胰十二指腸切除術(PD)已經成為胰頭及壺腹周圍惡性腫瘤、膽總管下段、十二指腸惡性腫瘤,以及某些良性病變如慢性胰腺炎、胰腺漿液性囊腺瘤等疾病首選治療方式。PD手術不僅需要切除膽囊[1]。十二指腸全部、胃竇部、膽總管等臟器和組織,而且需要對臟器和組織旁淋巴進行清除,同時在手術過程中要進行消化道吻合術,具有操作復雜、手術時間長、手術范圍廣,加之患者術前多伴有梗阻性黃疸及肝腎功能損害,導致患者PD術后并發癥和死亡的發生率較高[2]。隨著外科醫師手術技術和手術器械不斷發展,同時對圍術期患者規范化管理和綜合護理不斷加強,使得PD患者術后死亡率下降到5%以下,但患者術后并發癥發生率仍高達20%~40%,其中患者術后并發癥主要包括胰瘺、腹腔及消化道出血、膽瘺、感染、胃排空延遲等,不僅延長患者住院時間,增加醫療負擔,還給患者及家屬帶來沉重心理壓力[3-4]。研究顯示,感染作為PD術后常見并發癥之一,其發生率占據PD術后并發癥的1/3以上,特別是在術后并發胰瘺、出血等患者中發生率更高,同時由于患者本身營養不良、機體抵抗力差,術后感染可能導致全身炎癥反應綜合征,嚴重者甚至導致患者死亡[5]。而臨床關于PD術后常見并發癥如胰瘺、腹腔出血及胃排空延遲等相關危險因素的研究報道較多,而對于術后感染的相關危險因素的研究報道少見[6]。本研究通過探討PD術后感染的相關危險因素,同時指導綜合護理措施對于預防PD術后感染,旨在為臨床上預防和降低PD術后感染的發生提供理論依據,現報道如下。
1 對象與方法
1.1 研究對象 選擇2012年3月~2017年7月我院肝膽外科行胰十二指腸切除術的70例患者的臨床資料,收集患者的一般資料包括年齡、性別、既往腹部手術史、既往病史(冠心病、高血壓、糖尿病等)、有無黃疸,術中資料(包括手術時間、術中出血量)、胰腸吻合時間、術中是否輸血,術后資料包括患者術后血紅蛋白、白蛋白、病理診斷、腸內營養及術后并發癥(胰瘺、出血、胃排空延遲、感染)等。診斷標準:腹腔感染即患者術后體溫超過38 ℃,血常規檢查白細胞計數>10 000×109/L,同時伴有腹痛、腹脹和腹膜炎體征(明顯壓痛、反跳痛、肌緊張)等腹部癥狀,持續24~48 h以上或由腹腔引流管引出膿性引流液,細菌培養陽性或影像學檢查確診或經手術證實以及其他感染癥狀包括切口感染、肺部感染等。根據患者術后是否發生感染分為感染組38例和未感染組32例,兩組患者在性別、年齡、病理類型等方面比較,差異無統計學意義(P>0.05),具有可比性。
1.2 方法 術前所有患者經心電圖、心臟彩超、肝、腎功能更和血生化等相關輔助檢查明確各個重要臟器的功能情況,患者選取手術方式:54例患者選擇標準的PD術式,16例選擇保留幽門的PD術式,消化道重建采用Child重建方法,胰腸吻合方式分為常規傳統胰腺-空腸套入式吻合技術和U型交鎖縫合技術進行胰腺-空腸套入式吻合兩種,所有手術均由同一醫療團隊完成。術后患者進入重癥監護室,根據患者情況給予補液,維持術后患者水電解質及酸堿平衡,術后給予適量相關抗生素進行預防感染及應用生長抑素等抑制胰腺分泌。同時進行術后護理,患者術后常規在外科ICU監護1~2 d,監測體溫、心率、血壓、呼吸、血氧飽和度等生命體征指標,監測腹腔及胃腸引流物顏色及量,并注意保護引流管暢通,協助患者進行翻身、拍背、促進排痰及促進胃腸功能恢復等護理,并對術后出現并發癥采取對癥護理措施。
1.3 觀察指標 觀察感染組患者感染發生部位分布及細菌培養類型,收集患者的術前、術中及術后等一般資料并進行單因素分析,并將有統計學意義單因素進行多元logistic回歸分析,探討PD術后感染發生的危險因素。

2 結 果
2.1 75例患者發生感染的單因素分析結果比較 兩組患者在性別、年齡、BMI指數、病理類型、術前(ALT)、天冬氨酸酶(AST)、糖鏈抗原(CA199)、術前白蛋白、術前減黃、術中出血量、術后輸血、術后血紅蛋白及術后出血等比較,差異不具有統計學意義(P>0.05),而在術前膽紅素(TB)、糖尿病、手術時間、術后白蛋白、術后胰瘺及術后胃排空延遲等比較,差異具有統計學意義(P<0.05)。見表1。
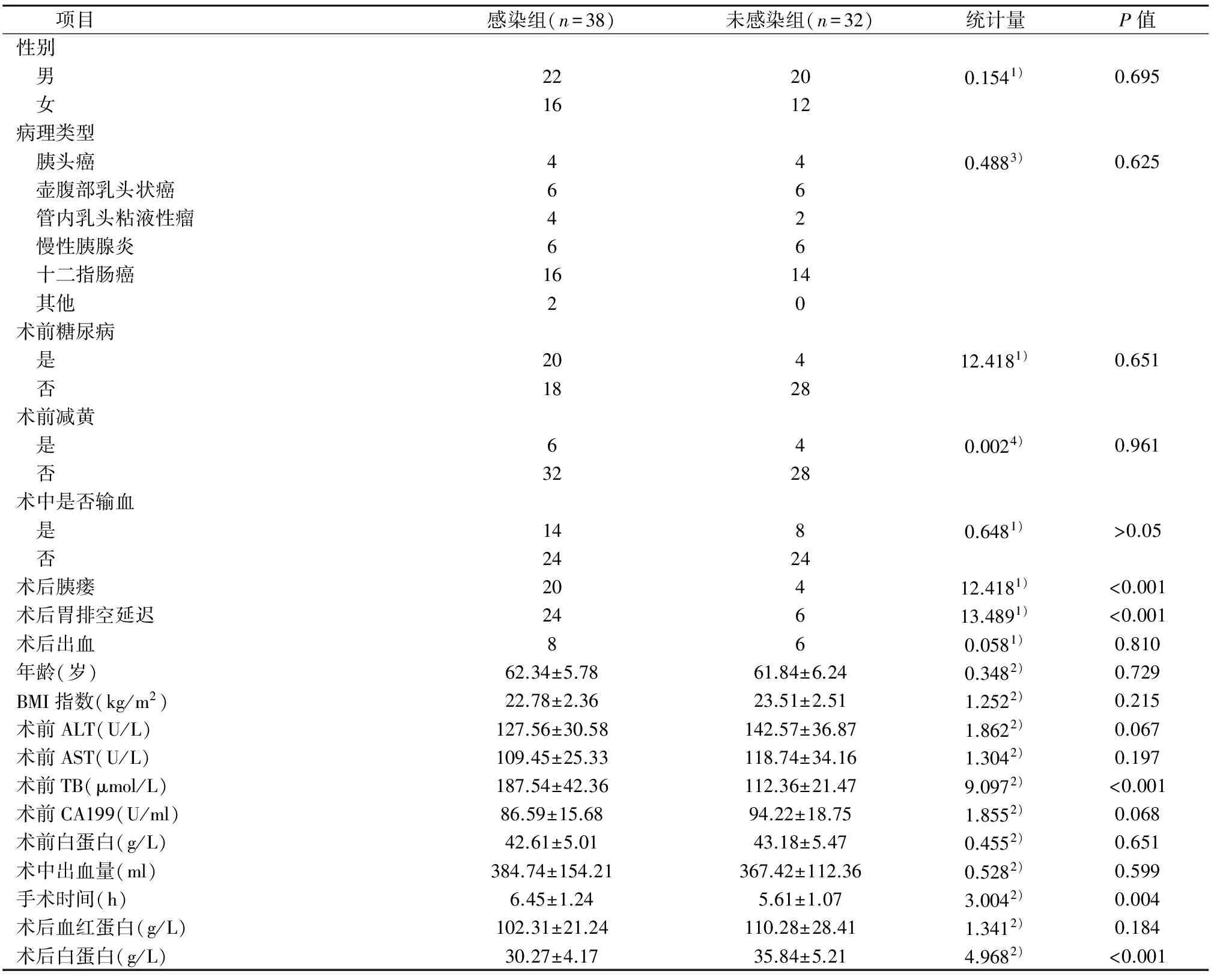
表1 75例患者術前、術中及術后發生感染的單因素結果分析比較

2.2 患者發生感染的多因素logistic回歸分析 將上述單因素分析中具有統計學差異的因素納入多因素logistic回歸分析,結果顯示,術前高BL、糖尿病、術后低白蛋白、術后胰瘺等為PD術后發生感染的獨立危險因素,其中術后發生胰瘺影響最為顯著。見表2。

表2 多因素logistic回歸分析
2.3 感染組患者感染部位及細菌培養結果 感染組患者共38例,且術后細菌培養共檢出菌種70株,其中感染部位分布為:腹腔、呼吸道、切口、泌尿系統和深靜脈導管,菌種種類分別為:大腸埃希菌、肺炎克雷伯菌、銅綠假單胞菌、金黃色葡萄球菌和其他。見表3。
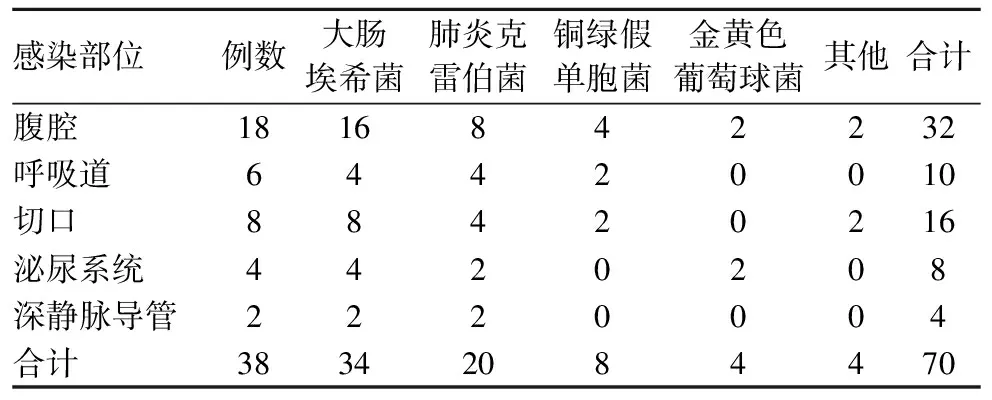
表3 感染組患者感染部位及細菌培養結果
3 討 論
近年來,隨著手術方法、圍手術期護理、腸外營養支持及影像、及麻醉技術等不斷進步和發展,使得PD術后死亡顯著降低[7]。國外學者對650例行PD術患者隨訪調查發現,患者在行PD術后死亡率僅為1.40%[8]。雖然臨床上在減少患者死亡率方面取得較大進步,但術后感染、胰瘺、出血等并發癥發生率并未得到明顯改善,這可能與PD手術操作時間長、切除范圍廣、消化道重建復雜等有關[9]。感染作為PD術后一種嚴重并發癥,同時患者術前免疫力低下合并感染時引起患者全身炎癥性反應,嚴重者會發展成感染性休克及器官衰竭而引起患者死亡[10]。國內研究報道顯示,PD術后感染發生率為30%~44%,而患者術后常合并高熱不退、食欲不振、腹部不適等癥狀,容易誘發患者全身感染或腹腔出血,加重患者病情,增加住院時間和住院費用,給患者及家屬帶來沉重心理負擔和經濟負擔[11]。因此,分析影響PD術后發生感染的相關危險性因素具有重要作用,同時在用于指導護理人員進行護理干預方面具有重要臨床意義。
本研究通過對患者的年齡、性別、BMI指數、病理類型、術前ALT,AST,TB,CA199、術前白蛋白、術前糖尿病及減黃、術中出血量、術后輸血、手術時間、術后血紅蛋白、術后白蛋白、術后胰瘺、術后胃排空延遲及術后出血等可能影響PD術后感染的因素進行研究分析,單因素分析結果顯示,感染組和非感染組患者在術前TB、糖尿病、手術時間、術后白蛋白、術后胰瘺及術后胃排空延遲差異具有統計學意義(P<0.05),同時將有差異單因素進行多元logistic回歸分析顯示,術前高TB、糖尿病、術后低白蛋白、術后胰瘺等為PD術后發生感染的獨立危險因素,其中術后發生胰瘺影響最為顯著。本研究通過結合研究結果和文獻報道,對術前高TB、糖尿病、術后白蛋白及術后胰瘺等影響PD術后感染的危險因素進行討論,同時指導醫護人員進行相應護理措施進行干預。
3.1 高膽紅素血癥與PD術后感染的關系及護理措施 研究顯示,行PD術患者術前大多數伴有長期高TB癥,這主要與患者本身胰腺受損有關,特別是對于胰頭癌患者,機體內膽總管受到壓迫,導致膽汁排泄障礙,導致膽紅素升高[12]。近年來,有學者認為對于重度梗阻性黃疸患者在圍手術期給予膽管引流,使其血清總TB含量降低,使患者對PD手術耐受能力增加,從而減少術后感染的發生[13]。但也有學者認為,術前減黃可能延長PD手術操作時間,同時術前減黃操作可能會損傷膽道,引起術中出血等并發癥,因此不建議梗阻性黃疸患者圍術期進行術前減黃操作[14]。本研究結果顯示,術前減黃不是PD術后患者感染發生的危險因素,但考慮到樣本數量較少,缺乏有力證據,因此對于術前減黃能夠降低患者術后感染率有待進一步探討研究。但本研究結果顯示,高TB是PD術后感染發生的危險因素,因此對于高TB患者而言,采取減黃和保肝為主要治療措施,在條件合適情況下給予患者膽管引流和輔助肝酶誘導劑,增加肝臟處理膽紅素能力,降低血清中TB含量,同時根據患者白蛋白及病情程度合理指導飲食,從而達到減少術后感染發生的目的。
3.2 糖尿病與PD術后感染的關系及護理措施 行PD術患者術前合并糖尿病、高血壓等慢性疾病常伴有心腦血管、肝臟、腎臟等臟器病理生理變化,患者機體免疫力低下、抗感染能力降低、手術耐受力差,術后恢復慢均會增加術后感染并發癥發生風險。其可能機制為術后手術對患者損傷較大,機體代償機制激發,合并糖尿病患者機體糖代謝受阻,引起代謝性酸中毒等水、電解質平衡紊亂;同時機體高糖狀態下,細胞免疫功能低下;高血糖還會使局部微血管發生病變,導致局部供血差,膠原纖維合成減少,組織修復細胞增殖受阻,傷口愈合延遲,容易引起局部感染[15]。端傳友等[16]對179例行PD術患者臨床資料進行分析發現,術前合并糖尿病患者在PD術后發生感染并發癥的風險顯著高于非糖尿病合并患者。本研究中結果顯示,感染組患者中合并糖尿病患者顯著高于非感染組患者(P<0.05),且根據多元logistic回歸分析顯示,術前糖尿病是PD術后感染發生的獨立危險因素,這可能與患者在長期高血糖狀態,機體免疫力低下和機體組織器官發生病理改變容易引起感染等有關[17]。因此,在術前應積極對患者經行糖尿病信息采集和病理性篩查,同時在醫囑指導下進行胰島素治療,并做好場內和腸外營養護理,圍手術期實時監測并控制好患者血糖水平。
3.3 術后低白蛋白與PD術后感染的關系及護理措施 白蛋白在維持機體正常生理功能起著重要作用,而行PD患者自身存在肝功能損害和營養不良等癥狀,同時PD手術時間長,術中出血量大,營養物質流失嚴重,當患者血液白蛋白含量較低時,會增加手術風險,術后出現大量腹水,或者行胰腸吻合術時會出現水腫等癥狀,增加PD術后感染的發生[18]。國外學者在動物實驗研究中發現,血漿中白蛋白含量過低會使胰腸吻合口的白細胞浸潤減少、血管生成能力降低,膠原纖維和成纖維細胞含量降低,不利于吻合愈合[19]。本研究結果顯示,術后低白蛋白為PD術后患者感染并發癥發生的危險因素,這與刑進等[20]研究結論相一致。因此,對于PD術患者圍手術期出現低蛋白癥的患者應該積極糾正低蛋白血癥,加強營養攝入,在禁食期間給予全胃腸道外營養治療、輸血等,用以補充熱量和蛋白質,糾正低蛋白血癥,從而降低術后感染的風險。
3.4 術后胰瘺與PD術后感染的關系及護理措施 雖然圍手術期處理得到不斷完善,以及胰腸吻合方式不斷進步,但PD術后胰瘺仍然是PD術后主要并發癥之一,目前關于影響PD術后胰瘺的因素有很多,包括年齡、術前TB水平、術中失血量、胰腸吻合方式、殘存胰腺質地、胰管直徑等均是相關因素。而胰液內含有腐蝕性消化酶類,一旦出現胰腸吻合口瘺,會導致胰液進入腹腔,引起局部彌漫性腹膜炎癥,進而發展成腹腔感染,引起敗血癥等全身感染[21]。本研究顯示,感染組患者術后胰瘺發生率顯著高于非感染組(P<0.05),且經logistic回歸分析表明,術后出現胰瘺患者感染發生率比未出現胰瘺患者感染發生率高,提示PD術后一旦出現胰瘺,很可能導致腹腔感染或出血,嚴重者甚至出現多功能器官障礙,威脅患者生命安全。因此,為減少PD術后感染的發生,應當積極預防PD術后胰瘺的發生,臨床上為減少術后胰瘺的護理措施主要包括PD術后盡早補充營養,一方面能夠提高白蛋白水平有利于胰腺創面、斷端或吻合口愈合,從而減少胰瘺發生,另一方面給予適量生長抑素抑制胰酶的分泌,減少對吻合口刺激;同時術中仔細操作,盡量縮短手術時間,減少術中出血;根據胰腺質地及胰管直徑,選擇采用胰管空腸黏膜對黏膜吻合或者端端套入式吻合方式;對于PD術后患者出現胰瘺,在確定無胰腺出血或感染時,先對患者進行保守治療,治療時應注意保持引流管通暢、控制感染、進食控制及營養支持及水、電解質平衡。
綜上所述,術前高膽紅素血癥、術前糖尿病、術后低白蛋白、術后胰瘺等是PD術后患者發生感染的獨立危險因素,護理人員應當根據患者術前、術中及術后不同情況,充分了解患者病情后針對具體患者制定個性化圍術期護理方案,最大限度降低術后感染并發癥的發生率。但考慮到本研究病例數量有限,對感染類型未進行具體分類探討,同時PD術后感染發生受多種因素影響,還有待于更深入研究。
[1] 李學璐,朱丹丹,楊春明,等.微創胰十二指腸切除術新進展[J].中國普通外科雜志,2015,24(3):402-407.
[2] 徐宜梅,李 翔.腹腔鏡輔助下胰十二指腸切除術的配合技巧[J].護理實踐與研究,2013,10(1):139-141.
[3] 陳 東,陳 偉,殷曉煜,等.胰十二指腸切除術后并發癥發生的相關因素分析[J].中華消化外科雜志,2012,11(4):331-334.
[4] 楊海軍,原曉勇.胰十二指腸切除術后早期并發癥危險因素分析[J].山東醫藥,2013,53(2):71-73.
[5] 劉 媛,譚錦風,付小艷,等.快速康復外科理念在胰十二指腸切除術圍術期護理中的應用[J].護理實踐與研究,2016,13(18):63-64.
[6] 汪明慶,熊茂明,胡孔旺,等.改良Child術式預防胰十二指腸切除術后并發癥的應用研究[J].肝膽外科雜志,2014,22(1):30-33.
[7] 俞士卉.胰十二指腸切除術后嚴重并發癥的觀察與護理對策[J].安徽醫藥,2014,18(1):193-195.
[8] Mohammed S,Evans C,Vanburen G,et al.Treatment of bacteriobilia decreases wound infection rates after pancreaticoduodenectomy[J].HPB,2013,16(6):592-598.
[9] 王妮妮,朱國玲,許文青,等.胰十二指腸切除術后出血的觀察和護理策略[J].中華全科醫學,2014,12(12):2027-2028.
[10] 朱宏達,馬塵超,白岳青,等.胰十二指腸切除術后腹腔并發癥發生及引流留置時間預測[J].肝膽胰外科雜志,2014,26(5):372-375.
[11] 李慶東,鄧和軍.胰十二指腸切除術后嚴重并發癥的臨床分析[J].檢驗醫學與臨床,2015,12(11):1604-1605.
[12] 邵 卓,楊件新,金 鋼,等.個體化快速康復措施對胰十二指腸切除術后圍手術期并發癥的影響[J].中華胰腺病雜志,2015,15(3):163-168.
[13] 袁晟光,梁科偉,劉 杰,等.術前不同引流方式減黃對梗阻性黃疸大鼠部分肝切除術后肝功能和肝再生的影響[J].山東醫藥,2012,52(48):42-45.
[14] 岳 平,張金鐸,把永江,等.膽管惡性梗阻術前減黃的現狀及進展[J].中國普外基礎與臨床雜志,2017,24(5):644-648.
[15] 鄭四鳴,陸才德,周新華,等.糖尿病對胰腺癌胰十二指腸切除術后并發癥的影響[J].中華普通外科雜志,2013,28(9):649-653.
[16] 端傳友,王新波.糖尿病對胰腺癌患者胰十二指腸切除術后早期并發癥的影響[J].中國綜合臨床,2016,32(2):160-164.
[17] 孫建軍,陳敏勝.影響胰十二指腸切除術后早期并發癥的危險因素分析[J].中國醫師進修雜志,2012,35(5):24-27.
[18] 王義濤,郭 濤,齊浩龍,等.腸內營養與腸內營養聯合腸外營養在胰十二指腸切除術后患者中的應用比較[J].臨床外科雜志,2015,23(3):192-194.
[19] 陸建文,呂 毅,殷國志,等.胰十二指腸切除術后患者早期腸內營養與腸外營養的比較[J].中華肝膽外科雜志,2015,21(10):686-690.
[20] 邢 進,尚 東.胰十二指腸切除術后感染相關危險因素分析[J].大連醫科大學學報,2015,37(2):165-168.
[21] 陳正民,黃 強,劉臣海.胰十二指腸切除術后胰瘺的危險因素分析[J].重慶醫學,2015,44(29):4156-4158.
Riskfactorsanalysisandprotectivecountermeasuresofinfectionsafterpancreatoduodenectomy
YANGJu-hong
(Zhangjiagang First People’s Hospital,Zhangjiagang 215600)
Objective: To explore the risk factors and nursing prevention of infections after pancreatoduodenectomy (PD). Methods: To make a retrospective analysis of clinical data of a total of 70 patients undergoing PD in the department of hepatobiliary surgery of our hospital from March 2012 to July 2017. The patients were divided into infected group of 38 cases and uninfected group of 32 cases in terms of postoperative infections. The distribution of infection sites and type of bacterial culture were observed and the preoperative, intraoperative and postoperative general data was collected for single factor analysis. In addition, a multivariate logistic regression analysis was made for the statistically significant single factors to explore the risk factors of infections after PD. Results: The infection sites of patients in the infected group mainly included abdominal cavity, respiratory tract, incision, urinary system and deep venous catheter. The main pathogens causing infections were Escherichia coli, Klebsiella pneumoniae, Pseudomonas aeruginosa, and Staphylococcus aureus. The preoperative TB, diabetes, operation time, postoperative albumin, postoperative pancreatic fistula and postoperative delayed gastric emptying were compared between the two groups, and the differences were statistically significant(P<0.05). The preoperative TB, diabetes, postoperative albumin and postoperative pancreatic fistula were the risk factors for infections after PD(P<0.05). Conclusion: The preoperative hyperbilirubinemia, preoperative diabetes, postoperative hypoalbuminemia and postoperative pancreatic fistula are independent risk factors for infection after PD. The standardized perioperative nursing measures should be formulated according to the risk factors for infection.
Pancreaticoduodenectomy; Infection; Risk factors; Nursing
215600 張家港市 張家港市第一人民醫院普外科
楊菊紅:女,本科,副主任護師
2017-07-28)
(本文編輯 劉學英)

