腹腔鏡Heller括約肌切開聯合Dor胃底折疊術治療賁門失弛緩癥臨床效果
紀 濤,吳繼敏,胡志偉,汪忠鎬
·手術經驗·
腹腔鏡Heller括約肌切開聯合Dor胃底折疊術治療賁門失弛緩癥臨床效果
紀 濤,吳繼敏,胡志偉,汪忠鎬
目的探討腹腔鏡Heller括約肌切開聯合Dor胃底折疊術治療賁門失弛緩癥的臨床效果及安全性。方法選取2009年1月—2015年12月我院收治的行腹腔鏡Heller括約肌切開聯合Dor胃底折疊術的賁門失弛緩癥198例,分別于術前1 d、術后1個月行吞咽困難癥狀評分、生活質量評分及體重評估,觀察食管高分辨率測壓、上消化道造影、胃鏡檢查變化,記錄手術并發癥發生情況。結果所有患者均順利完成手術,31例失訪,167例獲得隨訪,隨訪6~84(65.3±10.6)個月,術中及術后均無明顯并發癥發生。術后吞咽困難多數明顯緩解,出現反流、胃灼熱12例,吞咽慢6例,腹脹5例,緩解不明顯3例。42例術后6~9個月復查,食管高分辨率測壓均無食管下括約肌(LES)基礎壓升高,食管體部靜息壓均低于胃內壓;胃鏡檢查示LES進鏡均無阻力;上消化道造影示均無蠕動波,18例擴張程度較術前減輕。術前及術后吞咽困難評分、生活質量評分、體重比較差異均有統計學意義(P<0.05)。結論腹腔鏡Heller括約肌切開聯合Dor胃底折疊術治療賁門失弛緩癥安全性高,并發癥較少,能明顯改善患者吞咽困難,提高生活質量。
食管失弛癥;括約肌切開術,內窺鏡;胃底折疊術
賁門失弛緩癥是一種以食管蠕動功能消失和食管下括約肌(LES)松弛致功能不良所引發的以吞咽障礙為主要臨床表現的疾病,發病率較低。相關數據顯示,國外賁門失弛緩癥發病率為1/10萬~3/10萬[1]。賁門失弛緩癥主要治療方式有內鏡下肉毒素注射、內鏡下擴張、腹腔鏡Heller括約肌切開術及經口隧道下括約肌切開術(POEM),其中POEM是目前研究熱點,該術式的遠期療效及并發癥尚缺乏大型、多中心、隨機對照臨床試驗,故臨床未推廣應用[2-3]。腹腔鏡Heller括約肌切開術已有50余年的臨床應用經驗,且有大量研究證實,腹腔鏡Heller括約肌切開聯合Dor胃底折疊術治療賁門失弛緩癥技術較為成熟[4]。本研究探討腹腔鏡Heller括約肌切開聯合Dor胃底折疊術治療賁門失弛緩癥的臨床療效,現將結果報告如下。
1 資料與方法
1.1一般資料 選取2009年1月—2015年12月我院收治的賁門失弛緩癥198例,均經食管高分辨率測壓、上消化道造影及胃鏡檢查確診,其中男100例,女98例;年齡11~72(47.3±10.5)歲;病程0.75~40(13.6±4.5)年。
1.2診斷標準 ①食管高分辨率測壓:表現為食管蠕動消失,吞咽時LES不能松弛,基礎壓升高,食管體部靜息壓高于胃內壓。本組均食管蠕動消失、吞咽時LES不能松弛,其中121例LES基礎壓升高,142例食管體部靜息壓高于胃內壓。②上消化道造影:上段食管呈不同程度擴張、延長與彎曲,無蠕動波,末端變細,LES緊閉呈“鳥嘴”征。本組均無蠕動波,其中166例擴張明顯(直徑>4 cm),106例上段食管可見延長、彎曲。③胃鏡檢查:可見食管擴張、體部張力降低,LES緊縮或關閉,稍用力鏡身可通過,并排除腫瘤等偽賁門失弛緩癥。本組172例LES緊縮或關閉,稍用力鏡身可通過;181例可見食管擴張。以高分辨率測壓示食管蠕動收縮消失、吞咽時LES松弛障礙、胃鏡檢查排除腫瘤等是診賁門失弛緩癥的必要條件。
1.3臨床表現及診治過程 本組均有吞咽困難,其中189例以吞咽困難為主,6例以反流癥狀為主,3例以嘔吐癥狀為主。21例行球囊擴張治療,其中10例3個月后復發,6例癥狀緩解不明顯,5例癥狀緩解;8例行內鏡下肉毒素注射治療,3個月后癥狀復發;29例餐前予硝酸酯或鈣離子拮抗劑治療,其中12例因效果不明顯停用,8例2個月后因無效停用,3例出現藥物相關性低血壓,6例出現頭痛。患者由于吞咽困難,多數體重下降,最高達15 kg。
1.4手術治療 本組均采用氣管插管全身麻醉,取仰臥“大”字體位,頭高足低。于臍上緣行10 mm的橫行切口,置氣腹針造CO2氣腹,氣腹壓設置為14 mmHg,在腹腔鏡直視下于左、右鎖骨中線肋緣下、劍突下、左腋前線肋緣下共置入3個5 mm和1個10 mm的穿刺套管,其中劍突下穿刺套管放入巴布科克鉗抓住食管裂孔上方筋膜以托起肝臟,顯露賁門食管處。離斷肝胃韌帶,保留迷走神經肝支,剪開右膈角內側腹膜及食管前方腹膜,分離腹段食管,用超聲刀縱向切開胃食管連接處的食管前壁肌層,完全切斷食管環肌層達黏膜下層,分離1/2食管周徑。術中行胃鏡檢查以觀察食管、胃有無穿孔,若無穿孔,將胃底折疊覆蓋于切開的食管肌層和膨出的黏膜上,間斷縫合食管肌層切口邊緣和胃底壁漿肌層,并固定于右膈角上。術后保留胃管48 h,48 h后進流質飲食,1周后轉為軟食或普食。
1.5觀察指標 分別于術前1 d、術后1個月評估吞咽困難、生活質量及體重變化,記錄術中及術后并發癥發生情況,術后6~9個月復查食管高分辨率測壓、上消化道造影、胃鏡檢查以評估臨床療效。
1.5.1吞咽困難癥狀評分[4]:根據發作頻率將癥狀頻次分為6個等級,分別計0~5分;根據吞咽困難嚴重程度將癥狀程度分為6個等級,分別計0~5分。癥狀評分=癥狀程度評分+癥狀頻次評分。
1.5.2生活質量評分[5]:以賁門失弛緩癥的所有癥狀對患者生活質量的影響程度來劃分,共分為4個等級,分別計0~3分,分值越高代表對患者的生活質量影響越大。
1.5.3其他指標:均于清晨空腹安靜狀態下測量體重。
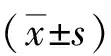
2 結果
所有患者均順利完成手術,手術時間平均(85.1±7.2)min,術中出血平均(23.2±9.1)ml,住院時間平均(6.5±1.8)d,術中未發生氣胸、食管穿孔等嚴重并發癥,無中轉開腹及死亡,術后進流質飲食均通暢,術后1周恢復正常飲食。
失訪31例,167例獲得隨訪,隨訪6~84(65.3±10.6)個月。術后吞咽困難多數明顯緩解,其中3例緩解不明顯,6例吞咽慢,5例腹脹,12例出現反流、胃灼熱。42例術后6~9個月復查,食管高分辨率測壓均無LES基礎壓升高,食管體部靜息壓均低于胃內壓;胃鏡檢查示LES處進鏡均無阻力;上消化道造影示均無蠕動波,18例擴張程度較術前減少。術前及術后吞咽困難評分、生活質量評分、體重比較差異均有統計學意義(P<0.05),見表1。對術后不同隨訪時間、評分及體重進行多因素方差分析,差異均無統計學意義(P>0.05)。
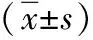
表1 腹腔鏡Heller括約肌切開聯合Dor胃底折疊術治療167例賁門失弛緩癥相關指標比較
3 討論
3.1發病機制 賁門失弛緩癥以吞咽困難為主要表現,病因及發病機制尚未完全明確,屬于神經源性疾病,多數學者傾向于感染后自身免疫功能障礙,是基因易感人群由免疫介導對病毒的反應[6],因釋放一氧化氮的抑制性神經缺失,致一氧化氮執行功能降低,LES松弛[7],但膽堿能神經較少受到損傷[8],仍能執行收縮功能,故吞咽時食物不能通過LES進入胃內。在疾病早期,食管體部可能仍存在蠕動,隨著疾病進展,蠕動逐漸消失,吞咽時不能推進食物和LES緊閉致吞咽困難。
3.2臨床特點 賁門失弛緩癥主要臨床表現為吞咽困難、食物停留在胸部,亦可表現為食物反流、不能解釋的胸痛、胃灼熱、咳嗽及反復發生的肺炎。吞咽困難主要由LES不能松弛所致,且為發作性,與食物種類無明確關系。由于進食困難,隨著病程延長,95.45%的患者體重下降。
3.3診斷及鑒別診斷 懷疑賁門失弛緩癥的患者可行上消化道造影、食管高分辨率測壓、胃鏡檢查。上消化道造影顯示上段食管呈不同程度的擴張、延長與彎曲,無蠕動波,典型癥狀為食管下段擴張,末端變細,LES緊閉呈“鳥嘴”征,具有特異性[9-10]。本組術前上消化道造影均無蠕動波,其中166例擴張明顯,106例上段食管延長、彎曲。
食管高分辨測壓診斷賁門失弛緩癥的標準如下:①食管蠕動消失;②吞咽時LES松弛;③LES基礎壓升高;④食管體部靜息壓高于胃內壓[11],其中第1、2條是必備條件。食管高分辨率測壓檢查時間短,患者無明顯不適,診斷準確性高,同時還能將賁門失弛緩癥與彌漫性食管痙攣、LES高壓、胡桃夾食管等其他食管動力病變進行鑒別診斷[12]。本組食管高分辨率測壓示198例均蠕動消失、吞咽時LES不能松弛,121例LES基礎壓升高,142例食管體部靜息壓高于胃內壓。胃鏡檢查可見食管擴張、體部張力降低,LES緊縮或關閉,但稍用力鏡身可通過。本組172例LES緊縮或關閉,稍用力鏡身可通過;181例可見食管擴張。有研究顯示,約44%的疑診賁門失弛緩癥的患者胃鏡檢查正常[13]。食管蠕動停止還可見于胃食管反流病、糖尿病、血管疾病等,且測壓結果不能區分真偽賁門失弛緩癥,故疑診患者必須行胃鏡檢查。
3.4治療方法與體會 由于賁門失弛緩癥的發病原因尚未明確,目前臨床治療以降低LES壓力,促進重力引起的食管排空,以緩解癥狀,改善生活質量,預防、減輕或改善食管擴張,減少食管癌的發生為主。治療方法主要有藥物治療、內鏡下治療和手術治療。藥物治療包括鈣離子拮抗劑(硝苯地平等)、硝酸酯類,但效果不明顯,且有頭痛、低血壓等不良反應,易耐藥[4]。本組29例曾使用硝酸酯或鈣離子拮抗劑治療,均效果不佳,且有一定的不良反應。
內鏡下治療主要為擴張、肉毒素注射和POEM。內鏡下肉毒素注射治療的機制是使肉毒素和突觸前受體結合,抑制神經末梢乙酰膽堿的釋放,從而使LES松弛,但長期療效不盡人意,66%的患者2年內復發[2]。擴張治療的機制是利用外力造成LES撕裂,進而達到LES松弛的目的。內鏡下球囊擴張已廣泛用于臨床[14]。內鏡下治療還包括內鏡下支架植入術、微波治療及支架植入聯合微波治療,其中支架植入及微波治療等研究相對較少,其療效、安全性尚待大規模的試驗觀察。POEM是經胃鏡于胃食管交界處(GEJ)上方切開黏膜層,分離黏膜下層并建立隧道至GEJ下方胃底約3 cm處,自隧道入口自上而下縱向切開環形肌,用金屬夾關閉隧道入口。有文獻報道POEM手術的成功率為90%~100%,與腹腔鏡Heller括約肌切開術的成功率相當[4,15],在手術時間、術后疼痛評分及止痛藥物的應用方面,POEM及腹腔鏡Heller括約肌切開術無明顯差異,且POEM的住院時間明顯縮短[16]。有研究發現,在初步使用POEM治療過程中,可出現較嚴重并發癥,如食管穿孔、隧道黏膜穿孔、食管狹窄等[15,17]。部分學者發現在治療過程中可無嚴重并發癥發生[18-19]。一項單中心、大型臨床試驗表明POEM嚴重并發癥發生率為3.2%[20]。不同文獻報道其并發癥發生率不一致,究其原因為術者水平參差不齊,而POEM對術者要求較高,需熟練操作內鏡,并深入了解食管的病理、生理機制,及時處理手術過程中出現的并發癥[21]。一項對500例賁門失弛緩癥進行為期3年的隨訪研究發現,POEM術后Eckardt評分及LES壓力明顯提高,未出現致死性并發癥,且嚴重并發癥發生率僅為3.2%,表明該術式具有較高的安全性及有效性[20]。盡管POEM具有較廣闊的應用前景,但缺乏足夠的臨床研究,故其尚不能作為賁門失弛緩癥的首選方法。
賁門失弛緩癥的手術治療主要是賁門肌切開術,通過切開沿食管縱軸的賁門肌并在黏膜外剝離以松弛LES,打破了LES的環形包繞,效果較好。Campos等[4]研究發現,腹腔鏡下Heller括約肌切開術以近90%的功能恢復成功率及0.1%的病死率成為賁門失弛緩癥治療的首選方法。腹腔鏡下Heller括約肌切開主要并發癥為反流,嚴重者出現食管及胃穿孔。為減少或避免術后反流,賁門肌切開后可經食管前方或后方加部分胃底折疊,且Dor方案可避免或防治術后穿孔、反流,多數醫生選擇經食管前方案。與未行部分胃底折疊的患者比較,賁門肌切開術加部分胃底折疊術后反流的發生率由31%降至9%,且無吞咽困難[4]。有學者發現,腹腔鏡Heller括約肌切開聯合Dor胃底折疊術治療賁門失弛緩癥的并發癥發生率為6%,病死率0.1%,術中食管或胃穿孔發生率為7%,穿孔多在術中修復,僅0.7%的患者出現術后穿孔,且長期緩解率明顯優于球囊擴張[4]。本組均未出現穿孔,其中6例吞咽慢,5例腹脹,12例出現反流、胃灼熱,但術后癥狀均明顯改善,生活質量顯著提高。
綜上,腹腔鏡Heller括約肌切開聯合Dor胃底折疊術治療賁門失弛緩癥可明顯緩解癥狀,改善生活質量,值得臨床推廣應用。
[1] Ruffato A, Mattioli S, Lugaresi M L,etal. Long-term results after Heller-Dor operation for oesophageal achalasia[J].Eur J Cardiothorac Surg, 2006,29(6):914-919.
[2] Inoue H, Minami H, Kobayashi Y,etal. Peroral endoscopic myotomy (POEM) for esophageal achalasia[J].Endoscopy, 2010,42(4):265-271.
[3] Minami H, Isomoto H, Yamaguchi N,etal. Peroral endoscopic myotomy for esophageal achalasia: clinical impact of 28 cases[J].Dig Endosc, 2014,26(1):43-51.
[4] Campos G M, Vittinghoff E, Rabl C,etal. Endoscopic and surgical treatments for achalasia: a systematic review and meta-analysis[J].Ann Surg, 2009,249(1):45-57.
[5] Boeckxstaens G E. Achalasia: virus-induced euthanasia of neurons[J].Am J Gastroenterol, 2008,103(7):1610-1612.
[6] Wong R K, Maydonovitch C L, Metz S J,etal. Significant DQw1 association in achalasia[J].Dig Dis Sci, 1989,34(3):349-352.
[7] Tutuian R, Castell D O. Review article: oesophageal spasm-diagnosis and management[J].Aliment Pharmacol Ther, 2006,23(10):1393-1402.
[8] Holloway R H, Dodds W J, Helm J F,etal. Integrity of cholinergic innervation to the lower esophageal sphincter in achalasia[J].Gastroenterology, 1986,90(4):924-929.
[9] Howard P J, Maher L, Pryde A,etal. Five year prospective study of the incidence, clinical features, and diagnosis of achalasia in Edinburgh[J].Gut, 1992,33(8):1011-1015.
[10] Stylopoulos N, Bunker C J, Rattner D W. Development of achalasia secondary to laparoscopic Nissen fundoplication[J].J Gastrointest Surg, 2002,6(3):368-378.
[11] Spechler S J, Castell D O. Classification of oesophageal motility abnormalities[J].Gut, 2001,49(1):145-151.
[12] DeMeester T R. Surgery for esophageal motor disorders[J].Ann Thorac Surg, 1982,34(3):225-229.
[13] Lemme E M, Domingues G R, Pereira V L,etal. Lower esophageal sphincter pressure in idiopathic achalasia and Chagas disease-related achalasia[J].Dis Esophagus, 2001,14(3-4):232-234.
[14] Gutschow C A, Holscher A H. Myotomy for esophageal achalasia-laparoscopic versus peroral endoscopic approach[J].Endoscopy, 2010,42(4):318-319.
[15] Swanstrom L L, Kurian A, Dunst C M,etal. Long-term outcomes of an endoscopic myotomy for achalasia: the POEM procedure[J].Ann Surg, 2012,256(4):659-667.
[16] Marano L, Pallabazzer G, Solito B,etal. Surgery or Peroral Esophageal Myotomy for Achalasia: A Systematic Review and Meta-Analysis[J].Medicine (Baltimore), 2016,95(10):e3001.
[17] Von Renteln D, Fuchs K H, Fockens P,etal. Peroral endoscopic myotomy for the treatment of achalasia: an international prospective multicenter study[J].Gastroenterology, 2013,145(2):309-311.
[18] Costamagna G, Marchese M, Familiari P,etal. Peroral endoscopic myotomy (POEM) for oesophageal achalasia:preliminary results in humans[J].Dig Liver Dis, 2012,44(10):827-832.
[19] Higgins J P, Green S. Cochrane Handbook for Systematic Reviews of Interventions 5.1.0. Oxford: Wiley Online Library[DB/OL].http://www.cochrane-handbook.org
[20] Inoue H, Sato H, Ikeda H,etal. Per-Oral Endoscopic Myotomy: A Series of 500 Patients[J].J Am Coll Surg, 2015,221(2):256-264.
[21] Zhou P H, Li Q L, Yao L Q,etal. Peroral endoscopic remyotomy for failed Heller myotomy: a prospective single-center study[J].Endoscopy, 2013,45(3):161-166.
ClinicalEffectoflaparoscopicHellerSphincterotomyCombinedwithDorFundoplicationinTreatmentofCardiochalasia
JI Tao, WU Ji-min, HU Zhi-wei, WANG Zhong-gao
(Department of Gastroesophageal Reflux Disease, General Hospital of PLA Rocket Force, Beijing 100088, China)
ObjectiveTo investigate clinical effect and safety of laparoscopic Heller sphincterotomy combined with Dor fundoplication in treatment of cardiochalasia.MethodsA total of 198 cardiochalasia patients undergoing laparoscopic Heller sphincterotomy combined with Dor fundoplication during January 2009 and December 2015 were recruited in this study. Dysphagia symptoms score, score of life quality and body weight were evaluated on 1 d before operation and in 1 month after operation, and changes of high-resolution pressure measurement, upper digestive tract angiography and gastroscope examination were also observed, and incidence rate of postoperative complications were recorded.ResultsThe surgeries were successful for all patients, and 31 patients were lost follow-up, and 167 patients were followed up for 6-84 (65.3±10.6) months, and there were no obvious complications during and after surgeries. After surgeries, dysphagia was obviously relieved, and there were 12 patients with reflux and heartburn, 6 patients with slowly hypopharyngeal food, 5 patients with abdominal distension and 3 patients with little relief. With postoperative 6-9 months review for 42 patients, oesophageal high-resolution pressure measurement showed no elevated lower esophageal sphincter (LES) basic pressure, and resting pressure of esophageal body was lower than that of gastric pressure; gastroscopy showed that there was no resistance when mirror was entering the LES; Upper gastroenterography showed that there was no peristaltic wave, and postoperative extension degrees in 18 patients were decreased compared with those before surgeries. There were significantly differences in dysphagia score, life quality score and body weight before and after surgeries (P<0.05).ConclusionLaparoscopic Heller sphincterotomy combined with Dor fundoplication in treatment of cardiochalasia is safe with few complications, and it can improve dysphagia symptom and improve quality of life.
Esophageal achalasia; Sphincterotomy, endoscopic; Fundoplication
首都臨床特色應用研究資助項目(Z141107002514109)
100088 北京,解放軍火箭軍總醫院胃食管反流病科
吳繼敏,E-mail:drwujimin@qq.com
R571
A
1002-3429(2017)12-0060-04
10.3969/j.issn.1002-3429.2017.12.025
2017-07-14 修回時間:2017-08-16)

