血管緊張素受體腦啡肽酶抑制劑在心力衰竭治療中的研究進展及展望
李小榮,鄭旭輝,李新立
心力衰竭指由于心臟結構和(或)功能異常,引起靜息或負荷時心輸出量減少和(或)心腔內壓力增高,從而導致的一種臨床綜合征[1,2],是各種心血管疾病的嚴重和終末階段,致殘致死性高,嚴重威脅人類的健康。心力衰竭的治療目標不僅僅是改善癥狀、提高生活質量,更重要的是拮抗腎素-血管緊張素-醛固酮系統(RAAS)和交感神經系統,防止和延緩心肌重構的發展,從而降低心力衰竭的住院率和死亡率[1]。在心力衰竭的治療中,藥物治療是基礎。過去30余年來心力衰竭的藥物治療取得了較大的進展,伊伐布雷定、左西孟旦、重組人腦利鈉肽、血管緊張素受體腦啡肽酶抑制劑(ARNI)等新型藥物相繼應用于臨床,取得了較好的療效并獲得了各國指南的認可、推薦[2-4]。本文就ARNI在治療心力衰竭中的作用機制、研究歷程及展望進行闡述。
1 血管緊張素受體腦啡肽酶抑制劑的作用機制
沙庫巴曲纈沙坦是首個ARNI類藥物,也是其代表藥物,它是血管緊張素Ⅱ受體拮抗劑(ARB)纈沙坦和腦啡肽酶抑制劑(NEPI)沙庫巴曲兩種成分以1:1摩爾比例結合而成的鹽復合物,同時具有ARB和NEPI的作用,可以通過同時抑制血管緊張素受體和腦啡肽酶,起到利鈉利尿、舒張血管以及預防和逆轉心肌重構的作用(圖1)[5]。
1.1 抑制腎素-血管緊張素-醛固酮系統
心力衰竭時心排血量降低,腎血流量隨之減低,RAAS即被激活,血管緊張素Ⅱ和醛固酮分泌增加,從而導致全身水鈉潴留,同時也啟動了心肌細胞和組織的重塑,加速了心功能的惡化。血管緊張素轉換酶抑制劑(ACEI)和ARB抑制循環RAAS可達到擴張血管,抑制交感神經興奮的作用,進而改善心力衰竭時的血流動力學、減輕淤血癥狀;而抑制心臟組織中RAAS,則可改善和延緩心室重構,延緩心力衰竭進展,降低心力衰竭遠期死亡率,改善預后[6]。
1.2 抑制腦啡肽酶
利鈉肽主要包括心房鈉尿肽(ANP)、腦啡肽酶(NEP)和C型利鈉肽(CNP)[7]。ANP主要存在于心房組織中;B型利鈉肽(BNP)主要存在于腦組織、心房心室組織中,心肌肥厚時,心房和心室中表達增加。ANP和BNP可結合并激活利鈉肽受體,使環磷酸鳥苷(cGMP)生成增多而發揮血管舒張、尿鈉排泄和利尿的生理作用,另外還可抑制腎素的分泌和醛固酮的產生,減少心肌血管重構、細胞凋亡、心室肥厚和纖維化,減少腎臟纖維化,改善腎臟血流動力學[7,8]。心房及心室擴張、心室功能障礙和心力衰竭時ANP和BNP表達顯著增加,作用于心臟、脈管系統、腦、腎臟和腎上腺等組織即可發揮相應作用[8]。重組人BNP具有擴張靜脈和動脈(包括冠狀動脈),促進鈉排泄和利尿、抑制RAAS和交感神經系統等多重作用,靜脈應用可改善血液動力學,我國指南推薦用于急性失代償性心力衰竭[4]。
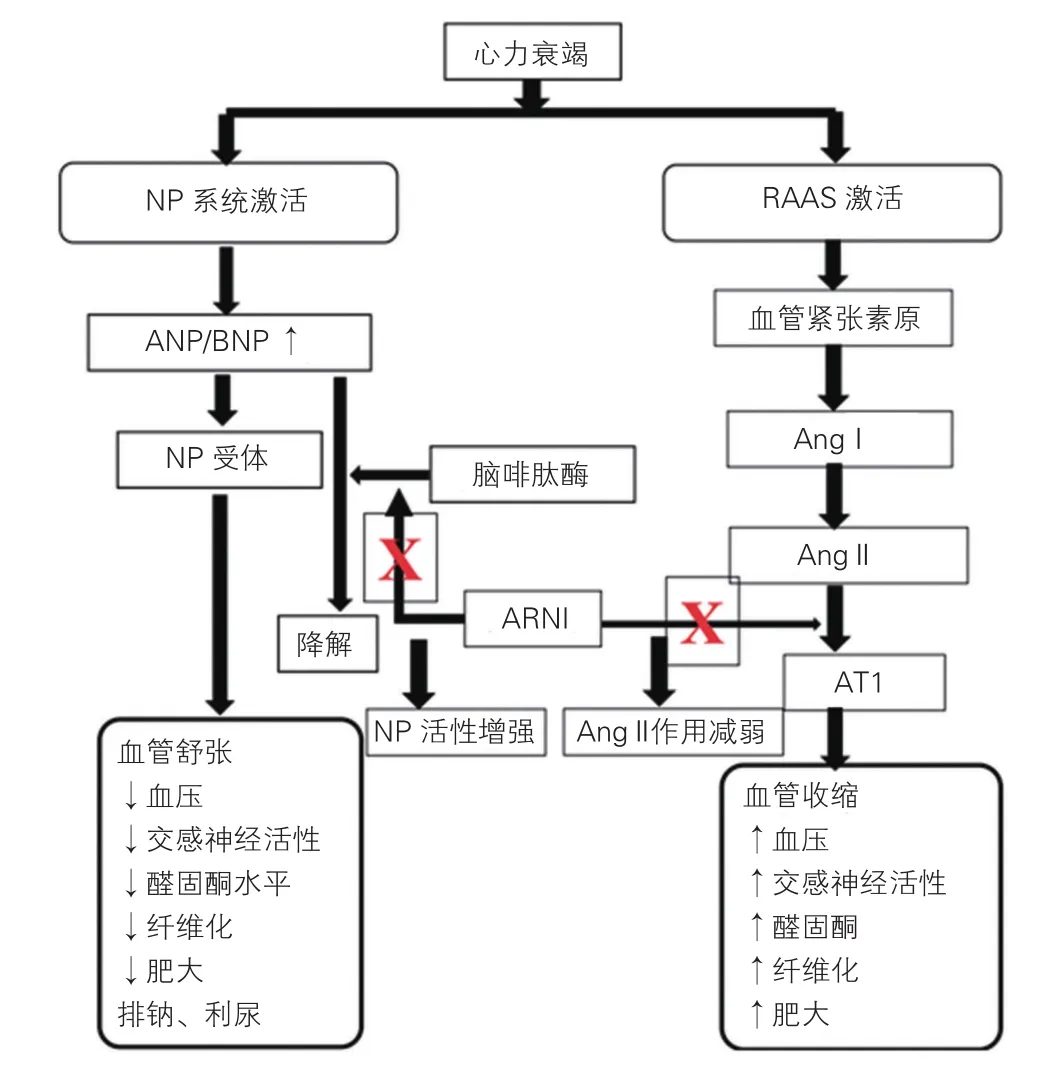
圖1 血管緊張素受體腦啡肽酶抑制劑作用機制示意圖
NEP屬于一種中性肽鏈內切酶,可降解包括ANP、BNP、CNP、緩激肽、血管緊張素Ⅰ和Ⅱ、內皮素-1在內的多種肽類[9]。阻斷NEP則可防止內源性利鈉肽的降解[10]。Sybertz等發現抑制NEP可升高ANP水平,并提高ANP促尿鈉排泄和利尿的作用[11]。動物實驗亦證明NEPI可引起利尿,并抑制醛固酮的激活[12]。NEPI可使利鈉肽降解最小化,從而使利鈉肽、緩激肽濃度升高而舒張血管,但同時也使得血管緊張素Ⅰ、Ⅱ和內皮素-1濃度升高[13],二者作用相互抵消,故單獨使用NEPI或對心力衰竭沒有太大影響[14]。ARNI有ARB和NEPI的雙重作用,可以同時抑制血管緊張素的不利作用,發揮利鈉肽的有利作用。
2 血管緊張素受體腦啡肽酶抑制劑用于心力衰竭治療的研究歷程
外源性重組人BNP用于急性失代償性心力衰竭可改善呼吸困難,降低肺動脈楔壓,但外源性重組人BNP多為靜脈制劑。為增強內源性BNP作用,人們研發出抑制利鈉肽分解的NEPI,但研究表明使用NEPI單藥治療或對心力衰竭幾乎沒有影響[14]。隨后人們將藥物研發轉向雙重抑制,即同時抑制RAAS及 NEP。
2000年,首個ACE-NEP抑制劑奧馬曲拉在慢性心力衰竭患者的初步臨床研究中顯示出療效。IMPRESS研究為前瞻性、隨機、雙盲的臨床試驗,共納入573例充血性心力衰竭患者,受試者紐約心臟協會(NYHA)心功能分級Ⅱ~Ⅳ級,左心室射血分數(LVEF)≤40%且目前接受ACEI治療;所有患者隨機接受賴諾普利(20 mg,n=284)和奧馬曲拉(40 mg,n=289)治療,隨訪24周。結果顯示,奧馬曲拉組心血管不良事件率低于賴諾普利組(7% vs 12%,P=0.04),奧馬曲拉組死亡、因心力衰竭住院,或中斷治療等終點事件明顯降低(P=0.035)[15]。
然而,2002年的OVERTURE研究顯示,ACE-NEP抑制劑也可帶來嚴重的安全性問題[16]。OVERTRUE研究是一項隨機、雙盲、安慰劑對照試驗,納入5 770例NYHA 心功能Ⅱ~Ⅳ級心力衰竭患者,分別給予奧馬曲拉40 mg(n=2 886)或依那普利10 mg bid(n=2 884)治療,平均隨訪14.5個月。研究顯示,兩組間因心力衰竭死亡或住院的時間無明顯差異(P=0.187),但奧馬曲拉組出現嚴重血管性水腫(0.8% vs 0.5%),這可能與ACENEP抑制劑同時抑制NEP和ACE導致緩激肽水平升高相關。
鑒于ACE-NEP抑制劑的不良反應,人們推測,ARB不會抑制緩激肽的降解,若以一種ARB取代奧馬曲拉中的ACEI是否可以降低血管性水腫的發生風險?2003年,諾華制藥公司申請了第一種ARNI的專利。2006年,首個ARNI類藥物沙庫巴曲纈沙坦問世。2012年公布的PARAMOUNT研究[17]及其后續分析顯示[18],沙庫巴曲纈沙坦在射血分數保留的心力衰竭(HFpEF)患者中顯示出獲益。PARAMOUNT研究是一項隨機、雙盲、多中心、平行對照的試驗,共納入149例NYHA心功能Ⅱ~Ⅲ級的心力衰竭患者,受試者LVEF≥45%,N末端B型利鈉肽原(NT-proBNP)> 400 pg/ml;所有患者隨機接受沙庫巴曲纈沙坦 200 mg bid或纈沙坦160 mg bid進行治療。隨訪36周后發現,沙庫巴曲纈沙坦治療后NT-proBNP水平、高敏肌鈣蛋白T(hs-TnT)水平均有顯著下降,而沙庫巴曲纈沙坦組嚴重不良事件發生率較纈沙坦還低(15% vs 20%)。
同時,對于射血分數降低的心力衰竭(HFrEF)患者,沙庫巴曲纈沙坦亦能使其獲益顯著。PARADIGM-HF試驗[19]是一項多中心、隨機、雙盲試驗,共納入8 442例NYHA心功能Ⅱ~Ⅳ級的BNP水平升高的HFrEF患者(LVEF≤40%),所有患者隨機接受沙庫巴曲纈沙坦200 mg bid或依那普利10 mg bid進行治療。隨訪27個月后發現,沙庫巴曲纈沙坦組心血管死亡、因心力衰竭住院、全因死亡均顯著下降,心力衰竭癥狀和體力限制得到了明顯改善。同時ARNI避免了奧馬曲拉引起的嚴重血管性水腫這一致命性不良反應,腎功能損害、高血鉀、咳嗽等不良反應發生率也較低,極大地提高了患者的耐受性。
3 血管緊張素受體腦啡肽酶抑制劑在心力衰竭中的應用
2016年歐洲心臟病學會(ESC)急慢性心力衰竭診治指南[2]和2017年美國心臟病學會(ACC)/美國心臟協會(AHA)/美國心力衰竭協會(HFSA)聯合發布的心力衰竭管理指南均對ARNI的使用作了推薦[3,20]。2016年ESC指南建議對于ACEI、β受體阻滯劑和醛固酮受體拮抗劑優化治療后仍有癥狀的HFrEF非臥床患者,推薦使用ARNI替代ACEI,以進一步降低心力衰竭住院和死亡風險(Ⅰ,B)。2017年ACC/AHA/HFSA心力衰竭管理指南推薦LVEF≤35%的HFrEF患者可以使用ARNI治療(Ⅰ,B),推薦所有NYHA心功能Ⅱ~Ⅲ級、可以耐受ACEI/ARB治療的慢性癥狀性HFrEF患者更換為ARNI(Ⅰ,A)。
結合當前各國指南和相關臨床試驗,推薦符合下列條件的患者可考慮使用 ARNI:(1)LVEF≤ 40%;(2)NYHA 心功能Ⅱ~Ⅳ級;(3)既往無因ACEI/ARB治療導致的血管性水腫或不可接受的副作用[21],推薦采用100 mg bid的起始劑量,當患者耐受,2~4周后加倍至目標維持劑量200 mg。對于部分血壓低或未使用過ACEI/ARB的患者,推薦采用50 mg bid的起始劑量;由于在估算腎小球濾過率(eGFR)<30 ml/(min·1.73 m2)的重度腎功能損害患者中用藥經驗非常有限,因此這類患者應慎用,推薦采用50 mg bid的起始劑量;中度肝功能損害(Child-Pugh B級)患者,也推薦采用50 mg bid的起始劑量。對于收縮壓在100~110 mmHg(1 mmHg=0.133 kPa)的患者,應考慮推薦采用50 mg bid的起始劑量。收縮壓<100 mmHg的患者,開始治療時需慎重,注意監測血壓變化。血鉀水平>5.4 mmol/L的患者不可啟動治療。
PARADIGM-HF研究[19]顯示沙庫巴曲纈沙坦比依那普利更容易導致癥狀性低血壓,但兩組因低血壓導致的停藥率相仿。沙庫巴曲纈沙坦組患者發生血管性水腫(無呼吸道狹窄)的數量較依那普利組有增加的趨勢,但無統計學意義(P=0.13)。在PARADIGM-HF研究雙盲階段,12%的沙庫巴曲纈沙坦治療患者和14%的依那普利治療患者報告了高鉀血癥不良事件。PARAMETER顯示,在老年高血壓高危患者中,沙庫巴曲纈沙坦比奧美沙坦降壓效果更強[22]。因此,在使用沙庫巴曲纈沙坦時,應密切監測血鉀、血壓情況,根據血壓、癥狀及檢查結果及時調整用量;此外為減少血管性水腫的發生,使用時禁止合用ACEI,也不建議在使用ACEI最后一劑36小時之內使用,因兩者皆會影響緩激肽系統,合用會明顯增加血管性水腫發生的風險。有使用ACEI/ARB導致血管性水腫病史的患者亦不可使用。
4 思考與展望
沙庫巴曲纈沙坦是近年來心力衰竭藥物治療中的一個突破性進展,并有望成為治療慢性心力衰竭的基石藥物。目前,這種藥物已在美國、歐盟通過審批[23],并獲得了歐美指南一致推薦,中國也于2017-07-26獲批上市。但需要注意的是,目前大多數沙庫巴曲纈沙坦相關研究來源于國外Ⅲ期臨床藥物試驗,國內研究對象人數較少,仍有諸多問題需要注意、思考。
第一,就ARNI對于HFpEF的作用,基于小樣本PARAMOUNT研究的陽性研究結果,目前已經啟動了PARAGON試驗(NCT01920711)。該試驗計劃入組4 300例LVEF > 45%的患者[24],沙庫巴曲纈沙坦是否可以改善HFpEF的預后,改變HFpEF目前藥物治療的困境,值得期待。
其次,發生心力衰竭時會導致腎臟功能的進行性惡化,臨床上通常會使用RAAS阻滯劑來保護腎臟,沙庫巴曲纈沙坦保護腎臟功能是否會優于RAAS阻滯劑,有待相關研究進一步證實。
第三,對于沙庫巴曲纈沙坦使用時機,目前ESC指南建議在采用“金三角”藥物治療后仍有癥狀的HFrEF患者,推薦使用ARNI替代ACEI。而ACC/AHA/HFSA心力衰竭管理指南指出對于NYHA心功能Ⅱ或Ⅲ級,能夠耐受ACEI或ARB的慢性有癥狀的HFrEF患者,推薦以ARNI替代ACEI或ARB。但是否所有慢性心力衰竭患者,只要無禁忌證,就可以使用沙庫巴曲纈沙坦取代傳統的ACEI/ARB,或直接起始就使用沙庫巴曲纈沙坦,尚待進一步研究。
最后,使用沙庫巴曲纈沙坦后,體內內源性利鈉肽升高,血清BNP水平升高,目前所用的檢測BNP的方法均會受到一定影響[25],那么在解釋BNP水平時就需要考慮到ARNI的影響。
[1] 李小榮, 李新立. 強調多學科合作以優化藥物和器械管理——2016年歐洲心臟病學會急慢性心力衰竭診斷治療指南解讀[J]. 中國循環雜志, 2016, 31 (z2): 129-133. DOI: 10. 3969/j. issn. 1000-3614. 2016. 增刊. 034.
[2] Ponikowski P, Voors AA, Anker SD, et al. 2016 ESC guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). Developed with the special contribution of the Heart Failure Association (HFA) of the ESC[J]. Eur Heart J, 2016, 37(27): 2129-2200. DOI: 10. 1093/eurheartj/ehw128.
[3] Yancy CW, Jessup M, Bozkurt B, et al. 2017 ACC/AHA/HFSA focused update of the 2013 ACCF/AHA guideline for the management of heart failure: a report of the American College of Cardiology/American Heart Association task force on clinical practice guidelines and the Heart Failure Society of America[J]. Circulation, 2017, 136(6): e137-e161.DOI: 10. 1161/CIR. 0000000000000509.
[4] 中華醫學會心血管病學分會, 中華心血管病雜志編輯委員會. 中國心力衰竭診斷和治療指南2014[J]. 中華心血管病雜志, 2014,42(2): 98-122. DOI: 10. 3760/cma. j. issn. 0253-3758. 2014. 02. 004.
[5] 邱爽, 楊波, 平海芹, 等. 血管緊張素受體腦啡肽酶抑制劑在心力衰竭中的研究進展[J]. 中國循環雜志, 2015, 30(11): 1131-1133.DOI: 10. 3969/j. issn. 1000-3614. 2015. 11. 024.
[6] Ghazi L, Drawz P. Advances in understanding the renin-angiotensinaldosterone system (RAAS) in blood pressure control and recent pivotal trials of RAAS blockade in heart failure and diabetic nephropathy[J].F1000Res. 2017, (F1000 Faculty Rev): 297. DOI: 10. 12688/f1000research. 9692. 1.
[7] Díez J. Chronic heart failure as a state of reduced effectiveness of the natriuretic peptide system: implications for therapy[J]. Eur J Heart Fail, 2017, 19(2): 167-176. DOI: 10. 1002/ejhf. 656.
[8] Rubattu S, Sciarretta S, Valenti V, et al. Natriuretic peptides: an update on bioactivity, potential therapeutic use, and implication in cardiovascular diseases[J]. Am J Hypertens, 2008, 21(7): 733-741.DOI: 10. 1038/ajh. 2008. 174.
[9] Liu Y, Studzinski C, Beckett T, et al. Circulating neprilysin clears brain amyloid[J]. Mol Cell Neurosci, 2010, 45(2): 101-107. DOI: 10.1016/j. mcn. 2010. 05. 014.
[10] Erd?s EG, Skidgel RA. Neutral endopeptidase 24. 11 (enkephalinase)and related regulators of peptide hormones[J]. FASEB J, 1989, 3(2):145-151.
[11] Sybertz EJ, Chiu PJ, Vemulapalli S, et al. SCH 39370, a neutral metalloendopeptidase inhibitor, potentiates biological responses to atrial natriuretic factor and lowers blood pressure in desoxycorticosterone acetate-sodium hypertensive rats[J]. J Pharmacol Exp Ther, 1989, 250(2): 624-631.
[12] Martin FL, Stevens TL, Cataliotti A, et al. Natriuretic and antialdosterone actions of chronic oral NEP inhibition during progressive congestive heart failure[J]. Kidney Int, 2005, 67(5): 1723-1730. DOI: 10. 1111/j. 1523-1755. 2005. 00269. x.
[13] Ferro CJ, Spratt JC, Haynes WG, et al. Inhibition of neutral endopeptidase causes vasoconstriction of human resistance vessels in vivo[J]. Circulation, 1998, 97(23): 2323-2330.
[14] Cleland JG, Swedberg K. Lack of efficacy of neutral endopeptidase inhibitor ecadotril in heart failure. The international ecadotril multicentre dose-ranging study investigators[J]. Lancet, 1998, 351(9116):1657-1658.
[15] Rouleau JL, Pfeffer MA, Stewart DJ, et al. Comparison of vasopeptidase inhibitor, omapatrilat, and lisinopril on exercise tolerance and morbidity in patients with heart failure: IMPRESS randomised trial[J].Lancet, 2000, 356 (9230): 615-620.
[16] Packer M, Califf RM, Konstam MA, et al. Comparison of omapatrilat and enalapril in patients with chronic heart failure: the Omapatrilat Versus Enalapril Randomized Trial of Utility in Reducing Events(OVERTURE) [J]. Circulation, 2002, 106 (8): 920-926.
[17] Solomon SD, Zile M, Pieske B, et al. The angiotensin receptor neprilysin inhibitor LCZ696 in heart failure with preserved ejection fraction: a phase 2 double-blind randomised controlled trial[J]. Lancet,2012, 380(9851): 1387-1395. DOI: 10. 1016/S0140-6736(12)61227-6.
[18] Jhund PS, Claggett BL, Voors AA, et al. Elevation in high-sensitivity troponin T in heart failure and preserved ejection fraction and influence of treatment with the angiotensin receptor neprilysin inhibitor LCZ696[J]. Circ Heart Fail, 2014, 7(6): 953-959. DOI: 10.1161/CIRCHEARTFAILURE. 114. 001427.
[19] McMurray JJ, Packer M, Desai AS, et al. Angiotensin-neprilysin inhibition versus enalapril in heart failure[J]. N Engl J Med, 2014, 371(11): 993-1004. DOI: 10. 1056/NEJMoa1409077.
[20] Yancy CW, Jessup M, Bozkurt B, et al. 2016 ACC/AHA/HFSA focused update on new pharmacological therapy for heart failure: an update of the 2013 ACCF/AHA guideline for the management of heart failure:a report of the American College of Cardiology/American Heart Association task force on clinical practice guidelines and the Heart Failure Society of America[J]. Circulation, 2016, 134 (13): e282-293.DOI: 10. 1161/CIR. 0000000000000435.
[21] Kang G, Banerjee D. Neprilysin inhibitors in cardiovascular disease[J].Curr Cardiol Rep, 2017, 19 (2): 16. DOI: 10. 1007/s11886-017-0827-0.
[22] Williams B, Cockcroft JR, Kario K, et al. Effects of sacubitril/valsartan versus olmesartan on central hemodynamics in the elderly with systolic hypertension: The PARAMETER Study[J]. Hypertension, 2017, 69 (3):411-420. DOI: 10. 1161/hypertensionaha. 116. 08556.
[23] Fala L. Entresto (sacubitril/valsartan): first-in-class angiotensin receptor neprilysin inhibitor FDA approved for patients with heart failure[J]. Am Health Drug Benefits, 2015, 8(6): 330-334.
[24] Braunwald E. The path to an angiotensin receptor antagonistneprilysin inhibitor in the treatment of heart failure[J]. J Am Coll Cardiol, 2015, 65(10): 1029-1041. DOI: 10. 1016/j. jacc. 2015. 01.033.
[25] Lippi G, Sanchis-Gomar F. Monitoring B-type natriuretic peptide in patients undergoing therapy with neprilysin inhibitors. An emerging challenge?[J]. Int J Cardiol, 2016, 219: 111-114. DOI: 10.1016/j.ijcard. 2016. 06. 019.

