超聲降解落葉松中阿拉伯半乳聚糖及其活性的研究
郭怡帆 ,林圣翔,劉煥燕,賀亮*
(1.浙江省蕭山中學,杭州 311201;2.CATS Academy Boston,Massachusetts 02184;3.浙江省森林資源生物與化學利用重點實驗室,浙江省林業科學研究院森林食品所,杭州 310023)
各種降解方法中,物理法降解最為簡單、綠化、無污染。超聲降解作為一種物理降解法已在環境、化工、食品等領域得到高度關注[8]。本文以落葉松林木采伐加工后的剩余木屑為原料提取出阿拉伯半乳聚糖并進行超聲降解,通過測定降解后多糖的·OH清除率變化來探究超聲功率、降解溫度、降解時間、料液比對多糖降解過程的影響,并確定最適宜降解條件,進而比較多糖降解前后體外抗氧化效果,為后續阿拉伯半乳聚糖的開發研究奠定了基礎。
1 材料與方法
1.1 材料與儀器
落葉松林木采伐加工后的剩余木屑,來自中國大興安嶺;500Da透析袋。
30%H2O2、FeSO4、水楊酸、DPPH、乙醇,購自國藥集團化學試劑有限公司,均為分析純。
旋轉蒸發器RE-52AA,上海亞榮生化儀器廠;BS224S電子天平,北京塞多利斯儀器系統有限公司;UV-9100紫外可見分光光度計,北京瑞利分析儀器公司;臺式高速冷凍離心機,美國Thermo公司;真空冷凍干燥機,美國LABCONCO公司;超聲波細胞破碎儀,昆山市超聲儀有限公司。
1.2 方法
1.2.1 阿拉伯半乳聚糖(AG)的提取
稱取20g松針木屑,以料液比1∶200、提取溫度70℃、浸提取時間1h,提2次。將粗提液抽濾,合并兩次濾液并濃縮,以1∶4(V/V)的比例加入95%的乙醇,在4℃的環境下靜置20h,離心,取出沉淀凍干,得松針粗糖。
1.2.2 阿拉伯半乳聚糖降解的單因素試驗
通過單因素試驗考察超聲功率、降解溫度、降解時間、料液比對松針多糖清除·OH能力的影響。降解反應后,離心除去沉淀,取上清液;考察其抗氧化活性,初步確定適宜多糖降解的相應水平范圍。
1.2.2.1 超聲功率對抗氧化活性的影響。稱取0.5g松針多糖,放入圓底燒瓶中,溶于100mL蒸餾水中,在溫度為60℃的條件下,分別以50W、100W、150W、200W、250W超聲降解1h。
1.2.2.2 降解溫度對抗氧化活性的影響。稱取0.5g松針多糖,放入圓底燒瓶中,溶于100mL蒸餾水中,在超聲功率為150W的條件下,分別以溫度40℃、50℃、60℃、70℃、80℃、90℃超聲降解1h。
1.2.2.3 降解時間對抗氧化活性的影響。稱取0.5g松針多糖,放入圓底燒瓶中,溶于100mL蒸餾水中,在超聲功率150W、溫度70℃的條件下,分別降解0.5h、1h、1.5h、2h、2.5h。
1.2.2.4 料液比對抗氧化活性的影響。按照料液比1∶100、1∶150、1∶200、1∶250、1∶300稱取0.5g松針多糖,放入圓底燒瓶中,在超聲功率為150W、溫度70℃的條件下降解2h。
1.2.3 阿拉伯半乳聚糖降解的正交試驗
根據單因素試驗結果,建立正交試驗L9(34)的因素水平表(表1)進行正交試驗,以降解松針多糖對自由基的清除能力為檢測指標,確定最佳降解工藝參數,計算最佳得率,其計算公式如下:

多糖得率
1.2.4 降解阿拉伯半乳聚糖對·OH清除率的測定
試劑配置:8.8mmol/L的H2O2溶液100mL ;9.0mmol/L的FeSO4溶液50mL;9.0mmol/L的水楊酸乙醇液50mL,0.5g/mL降解前后阿拉伯半乳聚糖溶液各100mL。
對于高分子溶液,在一定的超濾壓力下,隨著凝膠層厚度的增加,超濾通量會不斷減少。如圖5所示,本實驗的超濾通量-超濾時間的關系基本符合這一規律。在超濾運行的初期,因為膜表面無其他物質,阻力較小,因此超濾通量維持較穩定狀態;隨著超濾的不斷進行,在膜表面迅速吸附有機膠體等物質,超濾通量下降較快[21,22]。綜合考慮超濾通量及壓力,試驗選擇兩條曲線交點的時間,即超濾時間60 min。
試驗步驟:分別取降解前后阿拉伯半乳聚糖樣品液1mL,FeSO4溶液1.0mL,水楊酸乙醇液1.0mL,H2O2溶液1.0mL混合均勻,37℃水浴30min,510nm處測定吸光值。
·OH清除率計算公式如下:
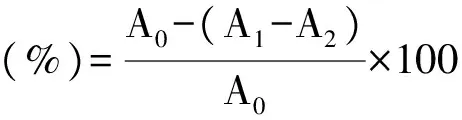
1.2.5 降解阿拉伯半乳聚糖對DPPH自由基清除率的測定
試劑配置:0.075mmol/L的DPPH乙醇液100mL,0.5g/mL的降解前后阿拉伯半乳聚糖溶液各100mL;
試驗步驟:分別取降解前后阿拉伯半乳聚糖溶液各0.5mL;添加DPPH乙醇液3mL,混 合均勻,置于黑暗處放置30min,517nm處測定吸光值。
DPPH自由基清除率計算公式如下:
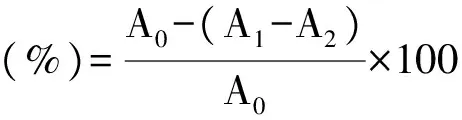
2 結果與分析
2.1 降解阿拉伯半乳聚糖工藝的優化
2.1.1 單因素試驗
2.1.1.1 降解溫度對阿拉伯半乳聚糖·OH清除率的影響。
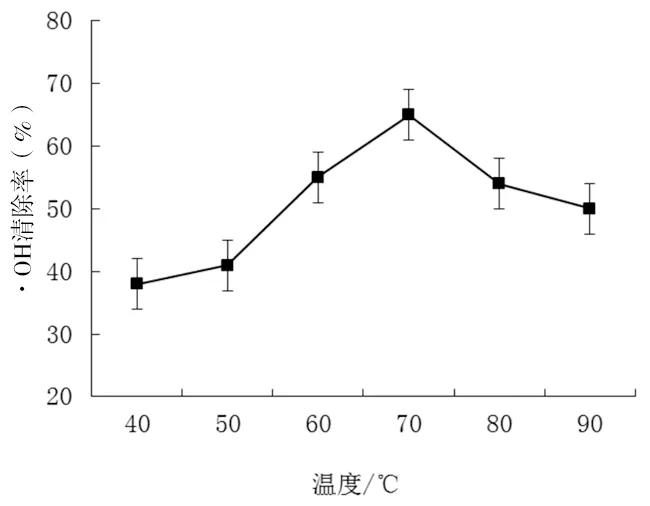
圖1 (a)不同降解溫度對阿拉伯半乳聚糖·OH清除率的影響
由圖1(a)可以看出:隨著溫度的升高,降解阿拉伯半乳聚糖對·OH清除率呈先升高后降低的趨勢。當溫度為70℃時,清除率最高為65.05%;當溫度高于70℃時,清除率開始下降。雖然溫度能提高化學反應的速度,但當降解溫度過高時,具有活性的多糖片段減少,降解效果降低,故其最適宜溫度為70℃[4]。
2.1.1.2 降解時間對阿拉伯半乳聚糖·OH清除率的影響。
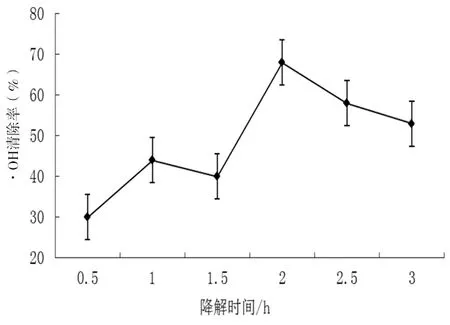
圖1 (b)不同降解時間對阿拉伯半乳聚糖·OH清除率的影響
由圖1(b)可以看出:隨著降解時間的延長,對·OH清除率呈先升高后降低的趨勢;當時間達到2h時,清除率達到最大值為62.12%,之后開始下降,為此最適宜降解時間為2h。
2.1.1.3 料液比對阿拉伯半乳聚糖·OH清除率的影響。
由圖1(c)可以看出:隨著料液比增加,對·OH清除率呈先升高后降低的趨勢;當料液比為1∶250時,清除率最高。提取液用量比較少時,由于多糖高分子之間相互作用形成膠團,影響多糖降解效果;提取液用量過多時,多糖降解程度增大,部分多糖被降解為小分子質量的多糖、寡糖等,由于透析時損失,保留下的活性多糖含量低,綜合考慮選用1∶250為最佳料液比[4]。
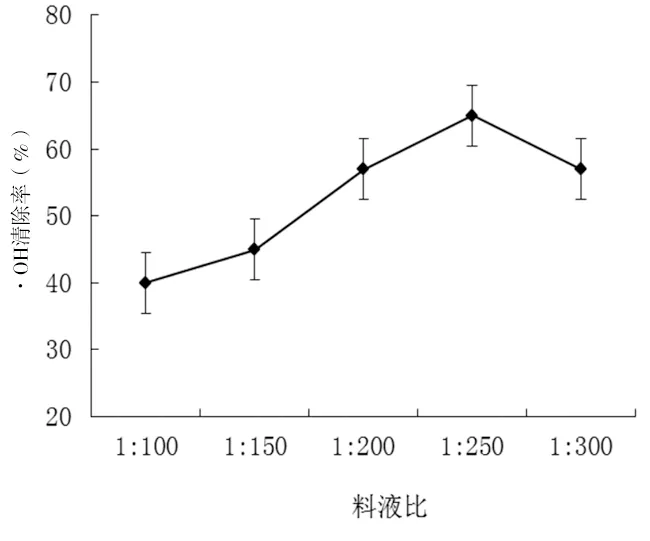
圖1 (c)不同料液比對阿拉伯半乳聚糖·OH清除率的影響
2.1.1.4 超聲功率對阿拉伯半乳聚糖·OH清除率的影響

圖1 (d)不同超聲功率對阿拉伯半乳聚糖·OH清除率的影響
由圖1(d)可以看出:隨著超聲功率增大,對·OH清除率呈先升高后降低的趨勢;當超聲功率達到150W時,對·OH清除率達到最高值為60.07%,而后緩慢降低。其原因可能是超聲功率的增加能強化空化效應,從而增加了斷裂生物大分子化學鍵的能量,引起降解作用加強[3]。而超聲功率超過150W時,隨著超聲功率的繼續增大,超聲的巨大能量可能會破壞多糖的活性部位,或者將有抗氧化活性的多糖鍵打斷變成較小分子而使得活性降低,從而引起降解作用的減弱[21]。
2.1.2 正交試驗
由于提取效果受到降解溫度、降解時間、降解功率、料液比四個因素的影響,為確定更適宜的提取條件,采用4因素3水平正交試驗L9(34)對超聲降解落葉松中阿拉伯半乳聚糖的工藝條件進行優化,具體結果見表2。
根據極差R的大小,進行因素的主次排列:極差越大,說明該因子水平變動時,實驗結果的變動越大,即該因子對實驗結果的影響越大。因此,在本實驗中,這個因素就越重要;反之,R越小,這個因素就越不重要。由表2 可知,本實驗各因素對降解效果的影響主次順序為:B>D>C>A,即降解溫度>料液比>降解時間>降解功率。
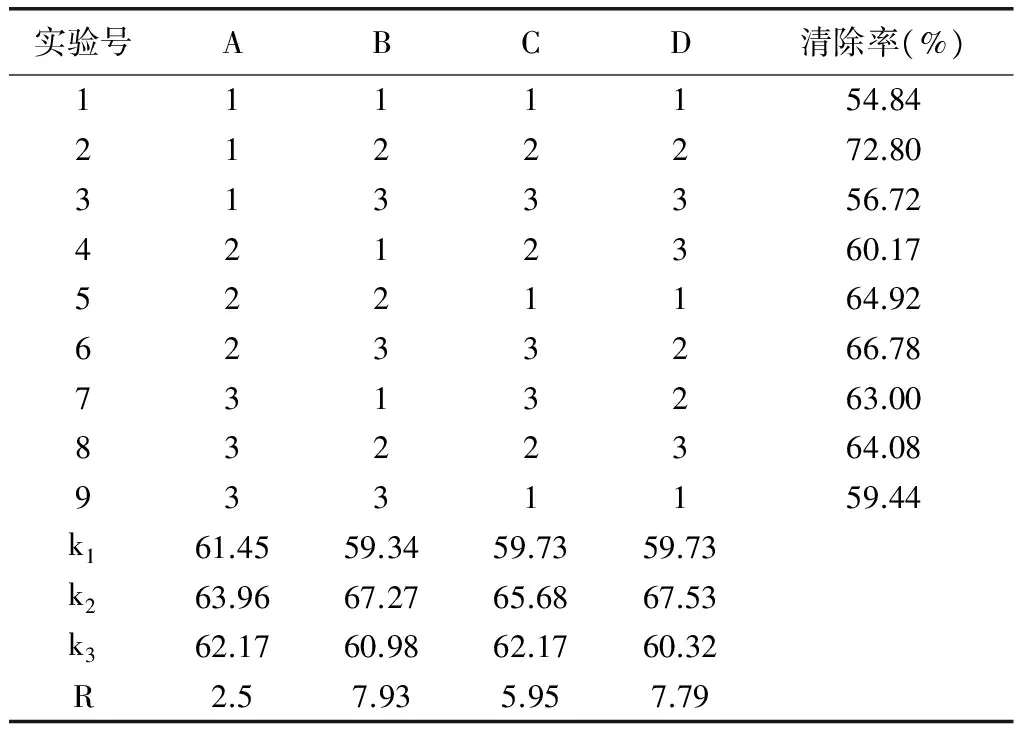
表2 L9(34)正交試驗設計分析結果表
K1、K2、K3反映了試驗因子各水平對實驗結果的影響,因而最大的K值對應于最好的水平,通過表2正交試驗結果分析,可以看出本實驗最適宜的降解條件為B2D2C2A2,即料液比1∶250、降解溫度70℃、降解時間2.0h、降解功率150W。
2.2 降解前后阿拉伯半乳聚糖抗氧化活性的比較
2.2.1 清除羥自由基
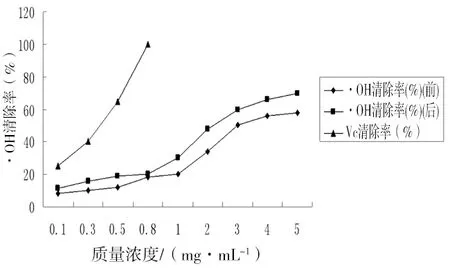
圖2 不同質量濃度的阿拉伯半乳聚糖降解前后對·OH清除效果比較
羥自由基的化學性質極為活潑,也是毒性最大的自由基,可以與多種有機物或無機物反應[5]。由圖2可知,超聲法降解前后阿拉伯半乳聚糖對·OH都有一定清除作用,降解后清除·OH能力明顯增強,而且均呈隨質量濃度提高而增強的趨勢,且增速先慢后快。通過與VC進行比較,當VC濃度達到0.8mg/mL時,清除率達到100%;而超聲法降解前后清除率均低于VC清除率,當質量濃度達到5mg/mL時,超聲法降解后多糖對·OH清除率達到70.32%。
2.2.2 清除DPPH
DPPH是一種穩定的有機自由基,通過檢測抗氧化劑對DPPH的清除能力,可以表示其抗氧化性的強弱[6]。由圖3可知,超聲法降解前后對DPPH都有一定清除作用,降解后阿拉伯半乳聚糖清除DPPH能力明顯增強,而且均呈隨質量濃度提高而增強的趨勢,增速先慢后快。通過與VC進行比較,當VC濃度達到0.8mg/mL時,清除率達到100%;而超聲法降解前后清除率均低于VC清除率,當質量濃度達到5mg/mL,超聲法降解后多糖對DPPH清除率達到80.16%。
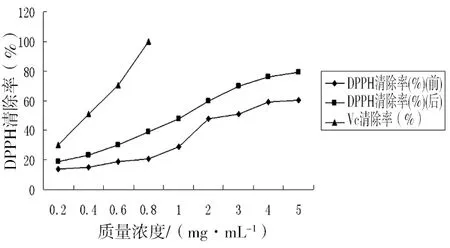
圖3 不同質量濃度阿拉伯半乳聚糖降解前后對DPPH清除效果比較
由以上分析可知,在實驗質量濃度范圍內,降解前后的阿拉伯半乳聚糖都有一定的抗氧化活性。經回歸分析可知,抗氧化活性順序為降解前<降解后,即超聲法有利于提高阿拉伯半乳聚糖的抗氧化活性。
3 結論
用物理法中的超聲降解法來降解阿拉伯半乳聚糖,以降解松針多糖對自由基清除率為檢測指標,通過單因素試驗考察超聲功率、降解溫度、降解時間、料液比對松針多糖體外抗氧化活性的影響,利用正交試驗確定最佳降解條件為降解溫度70℃、降解時間2.0h、料液比1∶250、超聲功率150W。在抗氧化活性方面,降解后的阿拉伯半乳聚糖較未降解前在清除·OH和DPPH上都有一定提高。
本試驗對超聲降解最佳工藝和抗氧化活性變化做了初步研究,但是其作用機制還有待進一步深入探討,今后應著重微觀機理的研究,探明超聲降解多糖生物大分子鍵斷裂機制和自由基反應機理,建立相應的物理數學模型,從根本上解決該技術產業化的科技問題[20]。
[1]Hauer J, Anderer F A. Mechanism of stimulation of human natural killer cytotoxicity by arabinogalactan from Larix occidentalis[J].Cancer Immunology,Immunotherapy,1993,36(4):237-244.
[2]Chandrasekaran R, Janaswamy S. Mophology of Western larch arabinogalactan[J].Carbohydrate Research,2002,337(21-23):2211-2222.
[3]任瑞,馬海樂,劉斌,等.超聲降解香菇多糖及其體外抗氧化活性的研究[J].安徽農業科學,2008,36(17):7061-7062,7065.
[4]高玉杰,呂海濤. 酸法降解滸苔多糖及其清除羥自由基活性研究[J].食品科學,2013,34(16):62-66.
[5]魏濤,何培新,鄭俊麗. 鐵棍山藥水溶性多糖的超聲波提取工藝及體外抗氧化活性的研究[J].河南工業大學學報(自然科學版),2010,31(6):25-28.
[6]阿吉姑·阿布都熱西提,買爾旦·馬合木提,馬合木提·烏斯滿,等.維生素C清除自由基能力3種檢測方法的比較[J]. 新疆醫科大學學報,2008,31(5):578-579,582.
[7]李堅斌,李琳,李冰,等.超聲降解多糖研究進展[J].食品工業科技,2006,27(9):181-184.
[8]馬艷麗,方桂珍,等.超聲波法提取木材中阿拉伯半乳聚糖的工藝參數優化[J].林產化工通訊,2004,38(5):6-7.
[9]方桂珍,馬艷麗,徐鳳英.等超聲波法提取木材中的阿拉伯半乳聚糖的研究[J]. 林產化學與工業,2004,24(4):104-106.
[10]Thompson L H, Doraiswamy L K.Sonochemistry:science and engineering[J] .Industrial & Engineering Chemistry Research,1999,38(4):1215-1249.
[11]方桂珍,黃占華,李淑君.微波法提取木材中阿拉伯半乳聚糖[J].林產化學與工業,2003,23(3):81-84.
[12]馮若,趙逸云,李化茂.超聲在生物技術中應用的研究進展[J].生物化學與生物物理進展,1994,21(6):500-503,562.
[13]DORAISWAMYLKTH.Science and engineering industrial &engineering chemistry research[J] .Sonochemistry ,1999,38(4):1215.
[14]茍勁.超聲波在化學化工中的應用研究[J] .重慶工學院學報,2002,16(3):76.
[16]GOELLNER E M, UTERMOEHLEN J, KRAMER R, et al.Structure of arabinogalactan from Larix laricina and its reactivitywith antibodies directed against type-Ⅱ-arabinogalactans[J].Carbohydrate Polymers,2011,86(4):1739-1744.
[17]黃桂東,鐘先鋒.阿拉伯半乳聚糖的研究進展[J].食品與機械,2006,22(4):141-144.
[18]任瑞,馬海樂,劉斌,等.超聲降解香菇多糖及其體外抗氧化活性的研究[J].安徽農業科學,Journal of Anhui Agri. Sci. 2008,36 (17):7061- 7062,7065.
[19]龔淑俐,鄧放明.真菌多糖的生物活性研究進展 [J].食物與營養,2006 (1) :27- 28.
[20]閔婷,孫杰,黃菲,等.超聲處理對龍眼果肉多糖理化特征及免疫調節活性的影響[J] .現代食品科技,2016,32 (5):125-125.
[21]王小梅,薛慧君,孫潤廣,等.超聲提取功率對麥冬多糖體外清除羥自由基作用影響的研究[J] .食品工業科技,2011,32(04):73-74.

