“物質構成的奧妙”考點歸納和題型透視
洪茲田+陳女婷


摘 要:“物質構成的奧秘”蘊涵很多初中重要的知識點、化學思想和化學方法,一直在中考化學用語考查中備受青睞.分析2017年全國各地市中考化學試題中關于“物質構成的奧秘”的相關考題,從考點歸納和題型透視等方面進行歸納和總結,以期為中考化學復習提供教學參考.
關鍵詞:物質構成的奧妙;化學用語;考點歸納;題型透視
原子、分子、離子及元素是初中化學重點要掌握內容和中考熱點.微觀知識較為抽象,但中考對本部分內容的考查一般難度不大,以選擇題和填空題為主.學習該部分知識,要求學生能從微觀上解釋一些宏觀現象,認識原子結構,知道原子、分子、離子及元素的聯系及區別,學習元素符號和元素周期表[1].
一、考點歸納
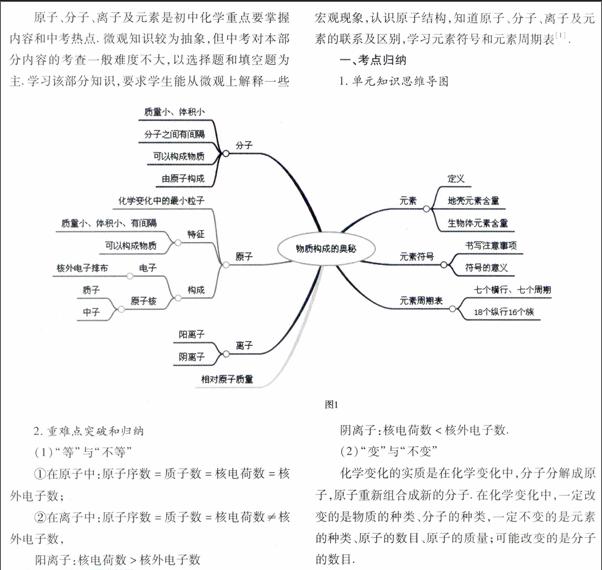
1.單元知識思維導圖
2.重難點突破和歸納
(1)“等”與“不等”
①在原子中:原子序數=質子數=核電荷數=核外電子數;
②在離子中:原子序數=質子數=核電荷數≠核外電子數,
陽離子:核電荷數>核外電子數
陰離子:核電荷數<核外電子數.
(2)“變”與“不變”
化學變化的實質是在化學變化中,分子分解成原子,原子重新組合成新的分子.在化學變化中,一定改變的是物質的種類、分子的種類,一定不變的是元素的種類、原子的數目、原子的質量;可能改變的是分子的數目.
(3)兩個“最小”
由分子構成的物質,分子是保持物質化學性質的最小粒子;原子化學變化中的最小粒子.
(4)兩個“圖”
①原子(或離子)結構示意圖
②周期表的“單元格”
(5)四個“決定”
①元素的種類是由核電荷數(或質子數)決定;
②原子的種類是由質子數和中子數決定;
③元素的化學性質主要由最外層電子數決定(一般來說,元素的最外層電子數相同,則元素的化性質相同).
i稀有氣體元素的最外層電子數為8(He為2),不易得失電子;
ii金屬元素的最外層電子數<4,易失去電子形成陽離子;
iii非金屬元素的最外層電子數>4,易得到電子形成陰離子.
④物質的化學性質是由“分子”決定,分子不能決定物理性質.
二、題型透視
考點1 構成物質的基本微粒
例1【2017年江蘇省揚州市】下列物質由離子構成的是( )
A.A1 B.H2O C.CO2 D.NaCl
解析 構成物質的微粒有分子、原子、離子等;根據金屬、大多數固態非金屬單質、稀有氣體等由原子構成;有些物質是由分子構成的,氣態的非金屬單質和一般由非金屬元素組成的化合物,如氫氣、水等;有些物質是由離子構成的,一般是含有金屬元素和非金屬元素的化合物,如氯化鈉.金屬鋁是由原子直接構成的;水是由分子直接構成的;二氧化碳是由分子直接構成的;氯化鈉是由鈉離子和氯離子構成的.故答案選D
答案 D
考點2 分子和分子的性質
例2【2017年江蘇省蘇州市】下列有關分子的說法中,不正確的是( )
A.分子的質量和體積都很小
B.溫度升高,分子的體積變大
C.分子在不停地運動
D.溫度越高,分子運動速率越快
解析 本題考查分子的基本性質.溫度升高,分子的體積不變,但分子間的間隔變大,故B錯誤.
答案 B
例3【2017年湖南省邵陽市】圖4中“●”和“○”分別表示氫原子和氮原子,能保持氨氣(NH3)化學性質的微粒是( )
解析 本題考查微粒觀點及模型圖的應用.構成物質的微粒就是保持物質化學性質的微粒.氨氣由氨分子構成,1個氨氣分子由1個氮原子和3個氫原子構成,故選A
答案 A
考點3 原子和原子結構示意圖
例4【2017年山東省威海市】學習完“原子的構成”之后,萍萍同學形成了以下認識,其中錯誤的是( )
A.原子由居于中心的原子核和核外電子構成
B.核外電子在離核遠近不同的區域中運動
C.原子核的質量和電子的質量相差不大
D.原子核的體積與整個原子的體積相比要小很多
解析 本題考查原子的定義構成.原子由居于中心的原子核和核外電子構成,故A正確;核外電子是分層排布的,核外電子在離核遠近不同的區域中運動,故B正確;電子的質量很小可以忽略不計,原子的質量主要集中在原子核上,故C錯誤;原子核的體積很小,原子核的體積與整個原子的體積相比要小很多,故D正確.
答案 C
例5【2017年浙江省杭州市】右圖5是 X、Y 兩種微粒的結構示意圖.下列說法正確的是( )
A.X 為原子,Y 為離子
B.X、Y 均屬于非金屬元素
C.X 在反應中可失去 6 個電子
D.X 與 Y 形成化合物的化學式為YX
解析 本題考查原子結構示意圖、離子結構示意圖的識別;元素的化學性質、元素化合價與最外層電子數的關系.X中滿足核電荷數=質子數=核外電子數=8,X為原子; Y中滿足核電荷數=質子數=核外電子數=12,Y為原子;故A錯誤;X的質子數為8,為氧元素,屬于非金屬元素,Y的質子數為12,為鎂元素,屬于金屬元素,故B錯誤;X最外層電子數為6個,在反應中易得到2個電子,形成-2價的陰離子,故C錯誤;Y最外層電子數為2個,在反應中易失去2個電子,形成+2價的陽離子,所以X與Y形成化合物的化學式為YX,故D正確.endprint
答案 D
考點4 離子和離子結構示意圖
例6【2017廣州市】圖6是元素X的一種粒子結構示意圖,下列說法正確的是( )
A.X是非金屬元素
B.X的最外層電子數為8
C.該粒子最外層電子層已達到相對穩定結構
D.該粒子可表示為X-
解析 本題考查離子結構示意圖,元素的化學性質、元素化合價與最外層電子數的關系.X是金屬元素,故A錯誤;元素X的最外層電子數為1,故B錯誤;最外層電子數是8個的結構是相對穩定結構,故C正確;該粒子可表示為X+,故D錯誤.
答案 C
考點5 元素和元素周期表
例7【2017年天津市】地殼中含量最多的元素是( )
A.Si B.Fe C.O D.Al
解析 本題考查地殼中的元素之最.地殼中元素的含量,按由多到少的順序是:氧、硅、鋁、鐵、鈣.
答案 C
例8【2017浙江省杭州市】2017年5月,中科院、國家語委和全國科技名詞委正式定名118號元素為“”,其部分信息圖7所示.則下列有關氮的說法正確的是( )
A.元素符號為Og
B.相對原子質量為118
C.原子的核電荷數為179
D.原子的核外電子數為297
解析 本題考查元素、原子的相對原子質量,原子符號的含義以及粒子數目的關系.根據元素周期表的圖,可知Og為元素符號,原子序數為118,相對原子質量為297,故A正確、B錯誤;根據核電荷數=質子數=核外電子數=原子序數,核電荷數、核外電子數為118,故C、D錯誤.
答案 A
考點6 綜合運用
例9【2017年天津市】根據下列粒子結構示意圖8,回答問題.
(1)A、B、C、D所示粒子共表示種元素(填數字).
(2)D所示粒子在化學反應中容易電子(填“得到”或“失去” ).
(3)若E中x=10 時,則該粒子屬于(填“原子”或“離子” ).
解析 本題綜合考查微粒的結構示意圖及原子判斷、元素種類的判斷、元素化學性質與最外層電子數的關系的知識.(1)質子數決定元素的類別,A、B、C、D所示粒子共表示三種元素;(2)D所示粒子,最外層電子數大于4,在化學反應中容易得到電子;(3)若E中x=10 時,則該粒子呈電中性,屬于原子.
答案 (1)3 (2)得到 (3)原子
例10 用“”和“”分別代表兩種不同的單質分子A2和B2,它們在一定條件下能發生化學反應,其反應的微觀示意圖如圖9:
請回答下列問題:
(1)每個生成物分子由個原子構成;
(2)反應物B2與生成物的分子個數比為;
(3)該反應屬于反應(填寫基本反應類型).
(4)從圖中你還能獲得的信息是(答兩條即可):①②.
解析 (1)最后一圖中有兩種分子,其中“”是該反應的剩余反應物之一,另一種分子即為生成物的分子,每個生成物分子由4個原子構成;(2)由圖示可知有2個B2分子參加反應,生成了4個生成物分子,所以分子個數比是2:4(即1∶2);(3)該反應是由兩種物質生成一種物質,屬于化合反應;(4)該圖示利用微觀變化反映物質的化學變化,因此可從物質的變化、元素的變化、分子的構成、分子和原子的變化等方面獲得相應的信息.
答案 (1)4 (2)1:2(或2:4) (3)化合 (4)①化學變化中分子可分;②原子是化學變化中的最小粒子;③化學反應前后元素的種類不變;④化學反應前后原子的種類不變;⑤化學反應前后原子個數不變等(任寫兩點即可,其他合理答案亦可).
三、同步練習
1.保持氫氣化學性質的最小粒子是( )
A.H2 B.H2O C.H D.H+
2.從圖10所示的兩種微粒結構示意圖中,所獲信息錯誤的是( )
A.它們屬于同種元素
B.它們的核外電子層數相同
C.它們的核外電子數相同
D.①表示陰離子,②表示原子
3.某密閉容器中,物質變化過程的微觀示意圖如圖11,圖示中“●”代表碳原子,“○”代表氧原子,下列說法正確的是( )
A.過程Ⅰ反應類型是化合反應
B.過程Ⅱ發生了化學變化
C.示意圖中所有物質均為氧化物
D.參加反應的CO與O2分子個數比為1:1
4.“見著知微,見微知著”是化學思維方法.
(1)從宏觀知微觀.
50mL水與50mL乙醇混合后,溶液體積小于100mL,微觀解釋為;
(2)從微觀知宏觀.
①微粒A最外層電子數是,在化學反應中容易 (填“得”或“失”)電子;
②如圖12所示,微粒A、B、C、D、E中,對應單質化學性質最穩定的是(填編號,下同),屬于同一種元素的是和;
③甲和乙在催化劑、高溫高壓條件下反應生成丙,三種物質微觀結構示意圖如圖13所示,該反應的化學方程式:.
5.模型是聯系宏觀與微觀的橋梁.
(1)圖14是鈉原子結構示意圖.
①x的數值為.
②“11”指的是.
③鈉原子在化學反應中易失去1個電子,形成(填離子符號).
(2)圖15是氫分子和氧分子運動的示意圖.
①在A、B和C中,能比較得出“溫度越高,分子運動速率越快”的是(填標號).
②從圖中可見,影響分子運動速率的因素除溫度外,還與有關.
③舉一個能說明“溫度升高,分子運動速率加快”的生活事例:.
【參考答案】1.A 2.D 3.A
4.(1)分子間有間隔
(2)①7 得 ②B C和E
③CO + H2催化劑高溫高壓CH3OH
5.(1)①8 ②鈉原子的質子數為11(或其他合理答案) ③Na+
(2)①BC ②分子種類(或其他合理答案)
③濕衣服在陽光下比在陰涼處干得快(或其他合理答案)
參考文獻:
[1]劉海燕.“物質構成的奧秘”考點掃描[J].中學生數理化:中考版,2017(9).endprint

