二甲雙胍聯合克羅米芬治療多囊卵巢綜合征并不孕癥的臨床療效及其對患者內分泌的影響
孫培培,王桂花,高丹
(鄭州市第二人民醫院,河南 鄭州 450000)
多囊卵巢綜合征(PCOS)是育齡女性常見的一種婦科內分泌代謝異常疾病,在生育期女性中的發病率約占5%~15%左右[1]。臨床以卵巢多囊性改變,排卵功能紊亂或喪失,胰島素抵抗以及高雄性激素血癥為主要特征,這一疾病通常呈現出進行性的發展趨勢,容易引發女性功能障礙,是引起女性月經紊亂以及無排卵性不孕癥的主要原因之一[2-3]。PCOS的發病原因目前尚不明確,臨床表現也呈現多種多樣性,因此目前有關這一疾病的治療方案主要是采用對癥治療,通過降低患者血漿胰島素的水平,減輕患者高雄性激素的癥狀,改善其內分泌的代謝,最終達到治療的目的[4]。
二甲雙胍是一種胰島素受體增敏劑,能夠通過對糖代謝的調節增強周圍組織對葡萄糖的攝入量,進而抑制肝糖原的產生,減少餐后胰島素的分泌,改善胰島素抵抗,預防代謝綜合征的產生[5]。克羅米芬作為一種誘導排卵藥物,在結構上與雌激素相似,能夠通過抑制雌激素對下丘腦的負反饋作用來增加循環中的卵泡雌激素與黃體生成素的水平,進而刺激卵泡的生長。本文通過采用二甲雙胍聯合克羅米芬對PCOS引起的不孕癥患者進行治療,取得了一定的臨床療效,現將結果報道如下。
1 資料與方法
1.1 一般資料 選取2015年1月—2016年1月鄭州市第二人民醫院婦產科收治的PCOS合并不孕的患者60例作為研究對象,依據入院的編號,按隨機數字表法將患者分為觀察組與對照組,每組30例。觀察組采用二甲雙胍聯合克羅米芬進行治療,對照組采用克羅米芬進行治療。
1.2 診斷標準 參照鹿特丹會議提出的診斷標準[6]:(1)排卵稀發甚至無排卵:初潮2~3年內不能建立規律的月經周期,閉經(停經的周期超過3個以往的月經周期或者≥6個月);(2)高雄激素血癥或者出現其它相關臨床表現;(3)超聲檢查提示多囊卵巢(一側或雙側的卵巢中直徑在2~9 mm的卵泡超過12個,或者卵巢的體積≥10 mL),以上條件符合2條且符合排除其他原因引起的高雄性激素血癥(如:先天腎上腺皮質增生、分泌雄性激素的腫瘤以及柯興綜合征等)或其他引起排卵異常的疾病(如:卵巢早衰、甲狀腺功能異常、高泌乳素血癥等)即可做出診斷。
不孕癥的診斷標準:已婚1年以上,在未采用任何避孕措施的情況下,性生活正常卻沒有成功妊娠的患者。
1.3 納入標準[5](1)鹿特丹會議提出的診斷標準;(2)年齡22~35歲,體質量40~70 kg,精神狀態良好;(3)肝、腎功能正常的患者;(4)無其他婦產科疾病及嚴重的全身性疾病;(5)3個月內未使用激素類、促排卵類以及對胰島素代謝產生影響的藥物;(6)符合不孕癥的診斷,并且排除由于輸卵管因素以及男方因素造成不孕的患者;(7)各項檢查資料完整,患者簽署知情同意書,能夠遵醫囑理解并配合治療。
1.4 排除標準 (1)不符合診斷標準的患者;(2)肝、腎功能異常的患者;(3)其他原因引起的高雄性激素血癥(如:先天腎上腺皮質增生、分泌雄性激素的腫瘤以及柯興綜合征等)或其他引起排卵異常的疾病(如:卵巢早衰、甲狀腺功能異常、高泌乳素血癥等);(4)對試驗藥物存在著嚴重不良反應以及禁忌證的患者。
1.5 治療方法與觀察指標
1.5.1 治療方法 對照組患者的第1個月經周期的第5天開始口服枸櫞酸氯米芬膠囊(廣州康和藥業有限公司)50 mg·d-1,連續服用5 d,連續服用3個月經周期,觀察組患者服用鹽酸二甲雙胍緩釋片(江蘇天士力帝益藥業有限公司)每次500 mg,3次/天,連續服用3個月經周期,第4個周期開始服用枸櫞酸氯米芬膠囊,服用方式與對照組相同,在患者停藥2~3 d后采用B超每天進行卵泡大小以及子宮內膜厚度的監測,當發現卵泡的直徑≥19 mm時進行人絨毛膜促性腺激素(HCG,上海上藥第一生化藥業有限公司)注射6 000~8 000 U,與此同時指導患者進行同房。在治療的過程中囑咐患者進行適度飲食結構的調整并進行適當鍛煉。
1.5.2 觀察指標 觀察比較兩組患者治療前后體質量、體質量指數(BMI)以及腰臀比(WHR);治療前及治療后第4個月經周期的第4天左右進行空腹采血,檢測血清中的促卵泡刺激素(FSH)、黃體生成素(LH)、垂體泌乳素(PRL)、睪酮(T)、雌二醇(E2)、空腹胰島素(FIN)、空腹血糖(FPG)以及胰島素抵抗指數(HOME-IR)水平變化情況;治療后排卵率、妊娠率、早孕流產率以及子宮內膜厚度。患者同房36 h 后采用B超觀察患者是否排卵,超聲顯示優勢卵泡出現明顯消失或者體積縮小,卵泡壁出現塌陷就表明已排卵[7]。并在治療后對患者進行3個月左右的隨訪,觀察患者是否妊娠(以是否超聲監測到胎心搏動作為判斷臨床妊娠的標準)。
BMI=體質量(kg)/身高(m2),患者BMI>25 kg·m-2為超重,患者BMI>28 kg·m-2為肥胖[8]。WHR=腰圍(cm)/臀圍(cm),女性理想的腰臀比范圍在0.67~0.8之間[8]。HOMA-IR=空腹血糖×空腹胰島素/22.5[9]。

2 結果
2.1 兩組患者治療前一般資料的比較 兩組患者年齡、體質量、BMI、腰臀比、病程以及不孕年限等各項一般資料的比較差異無統計學意義(P>0.05),說明兩組具有可比性,見表1。
2.2 兩組患者治療后體質量、BMI、腰臀比及子宮內膜厚度比較 兩組患者治療后體質量、BMI及子宮內膜厚度與治療前比較均有所下降,差異有統計學意義(P<0.05);WHR與治療前比較有所下降,但差異無統計學意義(P>0.05),見表2。
2.3 兩組患者治療前后血清中的FSH、LH、PRL、T、E2、FIN、FPG水平以及HOMA-IR的變化 與治療前相比:觀察組患者血清中LH、PRL、T、E2、FIN、FPG水平及HOMA-IR均顯著改善,差異有統計學意義(P<0.05);對照組患者血清中LH、PRL、T、E2水平顯著改善,差異有統計學意義(P<0.05),FIN、FPG水平及HOMA-IR值差異無統計學意義(P>0.05);兩組患者FSH水平與治療前比較均差異無計學意義(P>0.05);治療后與對照組相比,觀察組患者LH、PRL、T、FIN水平顯著降低、E2水平顯著升高,差異有統計學意義(P<0.05),見表3。
2.4 兩組患者治療后妊娠率、排卵率及早孕流產率比較 治療后觀察組患者妊娠率、排卵率均顯著優于對照組,差異有統計學意義(P<0.05);兩組患者早孕流產率比較差異無統計學意義(P>0.05),見表4。
2.5 兩組不良反應比較 兩組患者在治療過程中均未出現顯著不良反應。
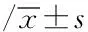
表1 兩組患者治療前一般資料比較
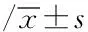
表2 兩組患者治療前后體質量、BMI、腰臀比及子宮內膜厚度比較
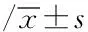
表3 兩組患者治療前后血清中的FSH、LH、PRL、T、E2、FIN、FPG以及HOMA-IR水平的變化

表4 兩組患者治療后妊娠率、排卵率以及早孕流產率比較/例(%)
3 討論
PCOS是目前婦科較為常見的一種內分泌代謝性疾病,其具體的發病機制尚不明確,發病過程涉及到了眾多因素,如環境、遺傳、免疫、神經以及內分泌代謝等[10-11]。該病的產生多是由于生殖內分泌紊亂所致,臨床多表現為閉經、肥胖、多毛、痤瘡以及排卵障礙等高雄性激素癥狀,并且常常伴有代謝異常如胰島素抵抗及高胰島素血癥等[12-13]。目前認為這一疾病的產生可能是由于內分泌功能的紊亂以及丘腦下部的垂體平衡失調所造成的,在精神或藥物的作用下或是某些疾病的影響下,丘腦下部所分泌的促性腺激素在釋放激素的過程中失去了周期性,導致垂體分泌的促性腺激素比例失調,卵泡雖然在發育但卻不成熟、不排卵,最終形成了囊狀的卵泡[14]。由于卵巢沒有定期排卵,因此無法分泌孕激素,只能分泌出雌激素與雄激素,這就成為了導致PCOS合并不孕癥的重要原因,PCOS不僅影響到患者的生殖功能,同時也會引起相關的代謝疾病,甚至會影響到患者的遠期健康,患者容易出現糖尿病、高血壓、冠心病以及子宮內膜癌等疾病[15]。這些疾病嚴重影響到了患者的健康,因此一旦發現就需要進行及時有效的治療。
目前由于對PCOS的發病原因尚無有效定論,因此在治療方面,所采用的治療方式主要集中在減少或者抑制雄性激素的產生,例如腹腔鏡卵巢打孔、芳香酶抑制劑、口服抗雄性激素藥物、避孕藥等等。近年來相關研究表明胰島素抵抗以及胰島素血癥是導致PCOS患者生殖功能以及糖代謝異常產生的病理學基礎,而胰島素抵抗的產生與高雄性激素血癥密切相關[14]。血清LH、PRL、T 偏高是PCOS內分泌異常的表現,高胰島素會導致LH-卵泡膜細胞分泌激素的作用增強,抑制肝臟合成性激素結合蛋白,促使游離的T水平增加,高水平的LH則會刺激卵巢中的卵泡膜細胞合成過多的雄性激素,FSH的分泌相對不足,卵泡顆粒細胞的芳香化作用減弱,也導致雄性激素的分泌過多,卵泡成熟出現障礙[16]。雄性激素的持續升高亦導致游離的T含量增加,有研究表明PCOS患者血清中的總睪酮含量是正常人群的1.5~1.7倍[17]。睪酮含量的增加促進脂肪細胞的生長,同時還能夠抑制α-腎上腺能受體,進而抑制脂肪分解,最終導致脂肪堆積,過度的脂肪堆積又會導致脂質代謝的異常,促使胰島素的敏感度下降,因此PCOS患者多伴有肥胖,其中多數為中心性肥胖,且肥胖患者與非肥胖患者比較更加容易加重PCOS的胰島素抵抗程度。本次研究結果顯示經過藥物的治療、鍛煉以及飲食控制,兩組患者的體質量及BMI均有所改善,這在一定程度上有利于改善胰島素抵抗程度,達到治療的目的。
關于PCOS的治療方案主要是改善胰島素的抵抗、糾正治療高雄性激素血癥,促進卵巢功能的恢復,實現患者有效排卵。克羅米芬作為一種常用的PCOS促排卵藥物,能夠通過對下丘腦雌激素受體的作用來阻斷中樞神經對外周的雌激素產生的調節反饋,進而促進外周雌激素的釋放,引起宮頸黏液變厚,達到促進排卵的作用,但是其在促排卵的過程中會導致妊娠率較低[18],對于胰島素抵抗的患者,也容易產生排卵障礙,本次研究結果顯示觀察組患者治療后LH、PRL、T、E2水平以及妊娠率、排卵率、子宮內膜厚度均顯著優于單純使用克羅米芬的對照組(P<0.05),這一結果說明二甲雙胍與克羅米芬聯合使用不僅能夠有效改善單純使用克羅米芬所造成的妊娠率相對較低的問題,增強了克羅米芬的促排卵作用,提高了妊娠率,降低了LH、PRL、T、FIN水平,增加了E2水平,促進了激素的分泌,對生殖內分泌作用也較為明顯;二甲雙胍作為一種雙胍類的降糖藥,不僅能夠有效地改善糖代謝降低體質量,降低血LH及游離T水平,破壞并糾正多囊卵巢狀態下的高雄性激素血癥,還能夠增加胰島素的敏感性,糾正胰島素抵抗,最終是雄性激素水平下降達到治療的目的[19-20]。二甲雙胍還能有效改善患者的宮頸評分、排卵情況以及妊娠率[21]。本次研究結果顯示觀察組患者治療后的排卵率、妊娠率以及子宮內膜厚度均顯著優于對照組(P<0.05),且FIN、FPG水平及HOMA-IR與治療前比較差異有統計學意義(P<0.05),這一結果進一步說明聯合用藥能夠有效改善胰島素抵抗,改善患者的臨床癥狀。本研究結果顯示:治療后觀察組患者T和LH等性激素水平以及FINS均顯著低于對照組(P<0.05),這一研究結果與既往的研究報道基本一致[22],這一結果表明兩藥聯用較單獨使用克羅米芬能夠更加有效降低PCOS并不孕患者的性激素和血糖水平,原因可能在于患者體內存在著胰島素,單獨使用克羅米芬治療雖然可提高患者的排卵率,但妊娠率卻較低下[22-23]。在治療的過程中加入雙胍類降糖藥二甲雙胍,可以抑制小腸內細胞葡萄糖的吸收率,提高外周組織中胰島素受體的酪氨酸激酶活性,降低患者的胰島素水平。患者血清中的FSH、T及LH水平均會隨胰島素水平的降低而下降,改善下丘腦-垂體-卵巢軸,促進患者促排卵反應,最終達到排卵受精妊娠的目的。
綜上所述,二甲雙胍聯合克羅米芬用于治療PCOS合并的不孕癥能夠有效調節患者的內分泌水平,改善胰島素抵抗,彌補了單純使用克羅米芬所存在的不足之處,有效地改善了患者的排卵率,提高了妊娠率,值得臨床進行推廣。
[1] 豐有吉,沈鏗.婦產科學[M].北京:人民衛生出版社,2005:8.
[2] 王卉.二甲雙胍聯合克羅米芬治療多囊卵巢綜合征合并不孕的療效[J].中國醫藥指南,2016,14(11):55.
[3] 張建偉,何泓.多囊卵巢綜合征導致不孕的危險因素及治療方案探討[J].海南醫學,2014,25(12):1750-1753.
[4] 蘇丹,張晉峰,侯麗輝,等.多囊卵巢綜合癥治療研究進展[J].中國中西醫結合雜志,2013,33(2):286-288.
[5] 梁遜瑩,黃武炎,許慧芳,等.達英-35與二甲雙胍聯合治療對多囊卵巢綜合征患者內分泌系統的影響及其效果分析[J].中國醫藥導報,2014,11(9):104-106.
[6] Rotterdam ESHRE/ASRM-Sponsored PCOS Consensus Workshop Group.Revised 2003 consensus on diagnostic criteria and long-term health risks related to polycystic ovary syndrome[J].Fertil Steril,2004,81(1):19-25.
[7] 毓星,吳乃森.計劃生育超聲診斷學[M].2版.北京:科學技術文獻出版社,2005:207-208.
[8] 李楊,劉春田,謝鈞,等.腰臀比與血管彈性及體脂肪率的相關性分析[J].檢驗醫學與臨床,2017,14(6):851-853.
[9] INVESTIGATORS OT,GILBERT RE,MANN JF,et al.Basal insulin glargine and microvascular outcomes indysglycaemic individuals:results of the Outcome Reductionwith an Initial Glargine Intervention(ORIGIN) trial[J].Diabetologia,2014,57(7):1325-1331.
[10] 田玄玄,阮祥燕,王娟,等.437例多囊卵巢綜合征相關因素調查分析[J].首都醫科大學學報,2014,35(4):414-418.

[12] 許良智,單丹.多囊卵巢綜合征:一種代謝障礙性全身性疾病在卵巢的表現[J/CD].中華婦幼臨床醫學雜志(電子版),2011,7(5):407-411.
[13] MARCH WA,MOORE VM,WILLSON KJ,et al.The prevalence of polycystic ovary syndrome in a community sample assessed under contrasting diagnostic criteria[J].Hum Reprod,2010,25(2):544-551.
[14] 杜鵬.論92例多囊卵巢綜合征患者內分泌變化和臨床治療分析[J].中外醫療,2014,33(5):41-42.
[15] 冉愛冬.炔雌醇環丙孕酮片、二甲雙胍緩釋片聯合克羅米芬治療多囊卵巢綜合征不孕患者的臨床療效[J].中國婦幼保健,2011,26(22):3443-3445.
[16] 母義明,劉敏.胰島素抵抗和多囊卵巢綜合征[J].中華內分泌代謝雜志,2013,29(3):185-188.
[17] HUANG A,BRENNAN K,AZZIZ R.Prevalence of hyperandrogenemia in the polycystic ovary syndrome diagnosed by the National Institutes of Health 1990 criteria[J].Fertil Steril,2010,93(6):1938-1941.
[18] GHASEMI M,ASHRAF H,KOUSHYAR H,et al.The cycle characteristics of clomiphene with clomiphene and menotropins in polycystic ovary syndrome and non polycystic ovary syndrome infertile patients[J].Minerva Ginecol,2013,65(3):311-317.
[19] DIAMANTI-KANDARAKIS E,CHRISTAKOU CD,KANDARAKI E,et al.Metformin:an old medication of new fashion:evolving new molecular mechanisms and clinical implications in polycystic ovary syndrome[J].Eur J Endocrinol,2010,162(2):193-212.
[20] VIOLLET B,GUIGAS B,SANZ GARCIA N,et al.Cellular and molecular mechanisms of metformin:an overview[J].Clin Sci,2012,122(6):253-270.
[21] FRUZZETTI F,PERINI D,LAZZARINI V,et al.Comparison of effects of 3 mg drospirenone plus 20 mug ethinyl estradiol alone or combined with metformin or cyproterone acetate on classic metabolic cardiovascular risk factors in nonobese women with polycystic ovary syndrome[J].Fertil Steril,2010,94(5):1793-1798.
[22] 王艷改.二甲雙胍聯合克羅米芬治療多囊卵巢綜合征合并不孕的效果分析[J].中國社區醫師,2014,30(21):78-79.
[23] 劉奎泉.二甲雙胍聯合克羅米芬治療多囊卵巢綜合征合并不孕癥的臨床療效觀察[J].中國衛生產業,2013,10(27):96-97.

