基于DWI的肝癌栓塞早期療效定量評估軟件的設計及應用
任芳,常英娟,潘奇,王珂,王虹,任靜
1.第四軍醫大學第一附屬醫院 放射科,陜西 西安 710032;2.西安醫學院第二附屬醫院 影像科,陜西 西安 710038
引言
磁共振彌散加權成像(Magnetic Resonance Diffusion Weighted Imaging,MR-DWI)是目前能在活體上進行水分子擴散測量與成像的唯一方法,可以反映組織微觀結構和功能的改變,在一定程度上可分析肝癌的細胞密度、核漿比及癌周浸潤情況,在肝癌診斷和療效評估上已經獲得越來越多的認可[1-2]。由DWI計算出的表觀擴散系數(Apparent Diffusion Coeffcient,ADC)表示水分子移動的自由度,肝癌組織在DWI多呈高信號,ADC值明顯降低,且肝癌惡性程度與其ADC值相關,栓塞治療后ADC值的升高在一定程度上反映了肝癌細胞的壞死[3-4]。
對于肝癌栓塞治療前后的DWI圖像和ADC值,臨床上只能進行主觀分析,很大程度上依賴醫生的臨床經驗,缺乏客觀的定量評估方法。DWI圖像提供了可供進一步分析的豐富信息和數據,因此臨床迫切需要可靠的圖像后處理技術來彌補影像設備和成像中的不足,從而獲得常規方法無法得到的深層信息。
MATLAB是美國MathWorks公司出品的主要用于算法開發、數據分析以及數值計算的高級技術計算語言和交互式環境。經過不斷地改進和完善,MATLAB已經具備了超強的數據計算、圖像處理和用戶界面制作的功能。同時,它擁有對DICOM格式圖像進行讀取、分析和存儲的函數,從而大大簡化對醫學圖像處理的難度和復雜度。在MATLAB環境下開發的醫學功能成像分析軟件(Medical Functional Imaging Analysis,MedFIA)可以對比治療前后的肝癌組織內每個像素的ADC值,還可以繪制治療前后ADC值直方圖和療效彩色圖譜,從而客觀地反映腫瘤組織治療前后的改變,及時準確地評估療效,為臨床提供更加直觀、全面的分析信息;對患者下一步治療方案的選擇和預后評估具有至關重要的意義[5-6]。而且,軟件界面友好和操作方便等優點便于臨床工作者在日常工作中使用。
1 軟件設計
1.1 MedFIA評估軟件界面設計
MedFIA評估軟件界面設計原則:主界面及子界面在排版樣式上統一,與傳統風格一致,對所有控件的位置和大小進行合理布局,保證清晰、簡單地體現出界面的功能和特征。使用用戶所熟悉的格式及標志,使用戶自學入門,盡快掌握操作方法[7]。
1.2 系統構架設計
MedFIA評估軟件分析流程圖,見圖1。首先,分別獲取治療前后的高低b值彌散圖像;第二步,對治療前后圖像進行剛性配準以及病變分割[8];第三步,分別計算病變治療前ADC值和治療后ADC值并繪制其ADC值直方圖;第四步,計算病變中每個像素在治療前后的ADC變化值,同時繪制其直方圖;第五步,根據用戶輸入的上下限閾值,將直方圖分類并計算分類統計數據。
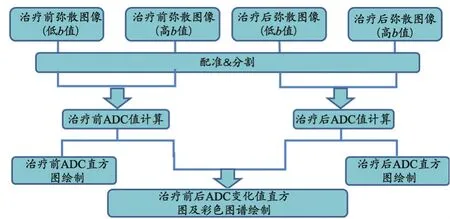
圖1 MedFIA評估軟件分析流程圖
2 MedFIA評估軟件功能
該軟件主要實現的功能包括:圖像讀取、病變的配準和分割、ADC值計算、直方圖繪制、治療前后對比、療效彩圖顯示、定量數據計算以及數據保存。各功能具體介紹如下:
(1)病變配準。盡管同一病人術前術后磁共振檢查選擇同樣的視野(Filed of View,FOV),但是病人位置的不同以及呼吸帶來的病變位移會導致病變在術前術后圖像中位置不同。位置的不同又會導致結果分析的不準確。因此,圖像預處理的第一步為圖像配準。由于病變不存在變形和旋轉,所以配準只需校正位置的變化[9]。
(2)病變分割。該軟件的分割方式為半自動分割,分為以下3步。第一步:手動選取感興趣區域(Region of Interest,ROI),進行病變的粗略選取;第二步:閾值分割,選擇合適的閾值區分病變與正常組織[10];第三步:形態學分割,去除正常組織并且保留完整的病變[10]。
(3)ADC值計算。輸入b值后,利用公式計算病變每個像素的ADC值[11],其中S代表DWI信號強度,b代表選取的b值,high為高b值,low為低b值。

(4)直方圖繪制。計算病變內每個ADC值的頻率,分別繪制治療前后的ADC值直方圖。直方圖可以直觀的顯示ADC值的范圍和分布情況。
(5)治療前后對比。對比病變內的每一個像素在治療前后的ADC值變化,量化治療效果[12-13]。
(6)療效彩圖顯示。將ADC變化值轉化成色階并覆蓋在解剖圖像上,更加直觀地顯示治療效果[12-13]。
(7)定量數據計算。根據用戶輸入的閾值計算并顯示ADC變化值分類統計數據[14]。
3 臨床應用
目前,針對采取動脈內栓塞治療的肝癌患者,預測其治療效果常用的方法是觀察腫瘤體積大小、組織密度的變化[15-16]。但是,肝癌組織密度在治療前后變化一般不明顯,而要出現明顯的體積大小變化一般需要數月或者更長時間,時間對于此類病人至關重要,早期的療效評估對后期治療方案的選擇及預后判斷有重要意義[15-16]。
磁共振彌散成像相對快速、無創、敏感等特點使之成為大部分肝癌患者優先選擇的檢查項目,也是MedFIA評估軟件用于早期治療效果分析的基礎數據。我們開發的MedFIA評估軟件已經通過兩名有經驗的放射科醫生對20例肝癌栓塞治療的患者進行了臨床驗證:首先通過西門子工作站在肝癌栓塞治療前后的腫瘤最大層面圖像上畫出圓形或類圓形ROI,使其盡量包括全部病灶。然后再將獲取的平均ADC值與該軟件計算出的腫瘤區域平均ADC值進行比較,兩者的平均ADC值相似程度超過95%。初步證明該軟件計算所得結果準確可信,可用于肝癌栓塞治療患者的早期療效評估。依據DWI即可對每位患者治療前后的ADC值進行對比分析,并繪制出ADC變化值直方圖,便于觀察其整體變化趨勢[5-6]。圖2和圖3可以看到基于像素分析的ADC值栓塞治療后明顯升高,按照預先設定的色階分類ADC變化閾值(±160×10-6mm2/s)計算,紅色代表治療后ADC值明顯升高的肝癌組織所占比例(67.92%),綠色代表ADC值無明顯變化(22.73%),藍色代表ADC值明顯降低(9.35%)。ADC變化值直方圖,見圖2。圖中顯示肝癌栓塞治療后ADC值整體升高,提示肝癌組織有明顯壞死,治療可能有效。ADC變化值彩色圖譜及分類統計結果,見圖3。圖片根據彩色圖譜還可以分析肝癌組織內每個像素點對治療的反應情況:哪些部分ADC升高明顯,提示該部位肝癌組織壞死明顯,對治療敏感程度也就一目了然。臨床醫生可以參考這些結果,擬定更為科學的后續治療措施,做到有的放矢。分類統計數據將ADC值變化按升高、未變化、降低進行分類統計,進一步對治療效果進行量化表示,更加直觀地顯示治療前后肝癌組織ADC值的變化[5-6]。

圖2 ADC變化值直方圖

圖3 ADC變化值彩色圖譜及分類統計結果
4 結論
隨著計算機及圖像后處理技術的迅速發展,使得該技術廣泛的應用于醫學領域,為數字醫療開創了新時代。借助數字圖像處理技術,可以獲得更清晰、更準確的診斷結果。我們自主開發的MedFIA評估軟件,主要基于二維磁共振彌散圖像計算肝癌患者栓塞治療前后ADC值的變化,量化評估其早期栓塞治療的效果,通過臨床驗證和與相關文獻報道比對,其重復性、穩定性和準確率均較高,完全能滿足臨床需求[14-16]。當然與國外售價高昂的同類軟件相比,尚存在一定差距:比如病變的三維數據分析和顯示,更多定量參數的獲取等。另外該軟件也需要在更多肝癌栓塞治療病例中去應用,并結合組織病理變化和最終臨床療效進行深入驗證與評估。總之,以肝癌為代表的腫瘤患者的DWI圖像分析與后處理技術具有很大的應用優勢和前景,不僅有利于提高臨床診斷的準確性,也能快速、準確地判斷臨床療效和預后,值得我們進一步去探索。
[1]段宏偉,張振勇,劉學平.磁共振擴散加權成像對肝癌的診斷價值[J].中國實用醫藥,2012,7(18):85-86.
[2]Gluskin JS,Chegai F,Monti S,et al.Hepatocellular carcinoma and diffusion-weighted MRI: detection and evaluation of treatment response[J].J Cancer,2016,7(11):1565-1570.
[3]武麗芳,顏竹蕓,徐鵬舉,等.ADC值變化率早期預測肝細胞癌(≤5.0 cm) TACE療效的價值[J].放射學實踐,2016,31(3):245-251.
[4]高回青,郁義星,胡春洪,等.彌散加權成像聯合普美顯磁共振成像在肝癌TACE術后療效評估中的應用[J].介入放射學雜志,2016,25(9):774-778.
[5]Bonekamp S,Jolepalem P,Lazo M,et al.Hepatocellular carcinoma: response to TACE assessed with semiautomated volumetric and functional analysis of diffusion-weighted and contrast-enhanced MR imaging data[J].Radiology,2011,260(3):752-761.
[6]Li Z,Bonekamp S,Halappa VG,et al.Islet cell liver metastases:assessment of volumetric early response with functional MR imaging after transarterial chemoembolization[J].Radiology,2012,264(1):97-109.
[7]趙彩云,張永壽,趙曉辰.醫學圖像處理系統的設計與實現[J].中國醫學裝備,2014,11(2):45-47.
[8]Chapiro J,Lin M,Duran R,et al.Assessing tumor response after loco-regional liver cancer therapies: the role of 3D MRI[J].Expert Rev Anticancer Ther,2015,15(2):199-205.
[9]鄧兵華,張明.Matlab環境下圖像配準方法[J].電子科技,2014,27(1):139-141.
[10]李越.MATLAB在醫學圖像分割處理中的應用[J].價值工程,2015,34(28):191-194.
[11]Bharwani N,Koh DM.Diffusion-weighted imaging of the liver:an update[J].Cancer Imaging,2013,13(2):171-185.
[12]Corona-Villalobos CP,Halappa VG,Bonekamp S,et al.Functional magnetic resonance imaging response of targeted tumor burden and its impact on survival in patients with hepatocellular carcinoma[J].Invest Radiol,2015,50(4):283-289.
[13]Sobhani F,Xu C,Murano E,et al.Hypo-vascular liver metastases treated with transarterial chemoembolization: assessment of early response by volumetric contrast-enhanced and diffusion-weighted magnetic resonance imaging[J].Transl Oncol,2016,9(4):287-294.
[14]Bonekamp S,Li Z,Geschwind JF,et al.Unresectable hepatocellular carcinoma: MR imaging after intraarterial therapy. Part Ⅰ. Identification and validation of volumetric functional response criteria[J].Radiology,2013,268(2):420-430.
[15]Chapiro J,Wood LD,Lin M,et al.Radiologic-pathologic analysis of contrast-enhanced and diffusion-weighted MR imaging in patients with HCC after TACE: diagnostic accuracy of 3D quantitative image analysis[J].Radiology,2014,273(3):746-758.
[16]Bonekamp S,Halappa VG,Geschwind JF,et al.Unresectable hepatocellular carcinoma: MR imaging after intra-arterial therapy. Part Ⅱ. Response stratification using volumetric functional criteria after intraarterial therapy[J].Radiology,2013,268(2):431-439.

