紫外線和熱力對55型腺病毒的滅活效果
劉 媛,王文博,鄒自英,邱 薇,范泉水,馮子良,熊 杰
人腺病毒(human adenovirus,HAdV)是一類無包膜的雙鏈DNA病毒,分為A~G 7個血清學組,60多個血清型。其中B組腺病毒感染目前已成為急性呼吸系統疾病的重要病原,其中引起軍隊新兵呼吸道感染流行的主要是腺病毒3型、7型和55型[1-5]。其中55型腺病毒(HAdV-55)是基于HAdV-B14型基因組骨架嵌合HAdV-B11型Hexon部分片段的重組新病毒,屬于B組的B2亞組。該病毒第一次在我國引起感染疫情發生在2006年3~4月陜西岐山縣[3]。近年來,HAdV-B55在成人特別是在學校和軍隊特殊人群中,引起日益頻繁的急性呼吸道傳染病流行[4-5]。另外也有研究表明,HAdV-55感染是成人社區獲得性肺炎的重要病因之一,成人腺病毒肺炎流行有明顯季節性,多在每年的2~3月份流感流行后期發生[6]。
由于腺病毒屬于DNA病毒,且沒有包膜,病毒本身比較穩定,能夠在環境中存活時間相對較長。為了解紫外線和熱力對HAdV-55的滅活效果,本研究開展了相關實驗,現將結果報告如下。
1 材料與方法
1.1 細胞和試劑 人喉癌上皮細胞HEp-2購自中國科學院上海細胞庫,由本實驗室保存培養;GIBCO胎牛血清、DMEM、青/鏈霉素、Invitrogen PureLinkTMViral RNA/DNA Mini Kit購自賽默飛世爾科技(中國)有限公司;引物和PCR試劑購自成都擎科梓熙生物技術有限公司;生化試劑購自上海生工生物工程有限公司。
1.2 HAdV-55毒株 病毒毒株SF04/SC/2016為本實驗室前期從HAdV-55感染者咽拭子標本中分離獲得,按照Reed-Muench公式計算病毒滴度為2.5×105,具體信息見參考文獻[7]。
1.3 紫外線對HAdV-55的滅活試驗 取100μl病毒液(滴度為2.5×105)平鋪于48孔板底部,均勻涂布孔底,形成一層薄層,隨機分為紫外照射30min組、1 h組和2 h組及對照組。紫外照射組置于超凈臺紫外燈下,紫外線波長254 nm,功率20瓦(W),距離60 cm,分別照射30min、1 h和2 h;對照組不進行紫外線照射。紫外線照射組照射完成后,采用實時定量PCR(RT-PCR)法檢測病毒液中HAdV-55 DNA水平。然后將4組分別接種HEp-2細胞,1×105個/孔,置于37℃、5%CO2飽和濕度培養箱中培養。培養24 h后,檢測細胞內病毒DNA水平;培養72 h后,收集細胞上清,采用Reed-Muench法檢測上清液中病毒滴度。
1.4 熱力對HAdV-55的滅活試驗 將100μl病毒(滴度為2.5×105)加入1.5 ml離心管中,隨機分為熱力滅活30min組、1 h組和2 h組及對照組。熱力滅活組置于恒溫水浴鍋內,溫度設置為65℃,時間分別為30 min、1 h和2 h,對照組不進行熱力滅活,置于4℃暫存。熱力處理完成后,采用RT-PCR法檢測病毒液中HAdV-55 DNA水平。然后將4組病毒液各100μl分別置于48孔板中,接種HEp-2細胞,細胞密度 1×105個/孔,于 37℃、5%CO2飽和濕度培養箱中培養。此后,細胞內和細胞培養上清中病毒的檢測方法和步驟同1.3。
1.5 RT-PCR方法 采用Invitrogen PureLinkTMViral RNA/DNA Mini Kit提取上述病毒分離液的腺病毒DNA,具體操作參照說明書進行。建立HAdV-55DNA檢測的標準曲線,對提取的腺病毒DNA水平進行定量檢測。相對定量以GAPDH作為內參基因,采用ΔΔCt法分析各組HAdV水平。所用引物如下,HAdV-F:5'-AGATGAAGAAAGTAAACCGATTT-3';HAdV-R:5'-CCATCAAGGTCAGTCCAA-3',預期產物86 bp;GAPDH-F:5'-TGGGCTACACTGAGCACCA G-3',GAPDH-R:5'-AAGTGGTCGTTGAGGGCAAT-3',預期產物 100 bp。
1.6 統計學方法 應用 SPSS 15.0軟件分析,計量數據以x±s表示,多組間差異采用單因素方差分析,兩組間比較采用Tukey檢驗,假設檢驗水準α=0.05。
2 結果
2.1 紫外線對HAdV-55的滅活效果 紫外線照射30min、1 h和2 h后,紫外線照射組HAdV-55 DNA水平與對照組相比無顯著差異(P>0.05,圖1A)。但紫外線照射組病毒感染HEp-2細胞水平降低,與對照組相比,紫外線照射30 min組細胞內病毒DNA水平降低約50%;紫外線照射1 h和2 h組細降低約 2個數量級(P<0.05,圖1B)。
進一步檢測細胞培養上清中子代病毒滴度,結果顯示,對照組子代病毒滴度為(2.5±0.10)×105,紫外線照射30min組、1 h組和2 h組分別為(1.9±0.08)×103、(5.7±0.08)×10 和(2.3±0.05)×10。見圖 2。

圖2 各組子代病毒滴度比較
2.2 熱力對HAdV-55的滅活效果 65℃熱力滅活30min、1 h和2 h后,熱力滅活組HAdV-55 DNA水平與對照組相比顯著降低(P<0.05,圖3A)。熱力滅活組病毒感染HEp-2細胞水平也降低,65℃處理30 min、1 h和2 h,病毒感染HEp-2水平降低>104個數量級(P< 0.05,圖 3B)。
熱力滅活病毒感染細胞產生子代病毒的滴度也顯著降低。65℃處理30min病毒組感染細胞產生的子代病毒滴度為(2.04±0.06)×101;而 1 h 組和 2 h組產生的子代病毒,不能再次感染細胞。
3 討論
人腺病毒屬腺病毒科,是無包膜的DNA病毒,病毒的核心由雙鏈DNA及蛋白質組成,病毒的衣殼呈規則的20面體結構,直徑80~110 nm。人腺病毒無類脂質包膜,耐乙醚和氯仿等脂溶性消毒劑,耐酸,在環境中穩定性相對較高。由于病毒的有效滅活涉及到病毒的傳播和控制、生物安全等多個方面,因此,探討紫外線和熱力對腺病毒的滅活效果具有重要意義。
目前腺病毒的滅活主要使用含氯消毒劑。李杰等[8]研究了常用消毒劑對HAdV-55的滅活效果,發現用含有效氯400 mg/L的次氯酸鈉和600mg/L的過氧乙酸作用20min,或含有效碘1000mg/L的碘伏溶液作用40min,對HAdV-55的滅活對數值可≥4.00;而醋酸氯己定和苯扎氯銨等低效消毒劑對該病毒的滅活作用稍弱。
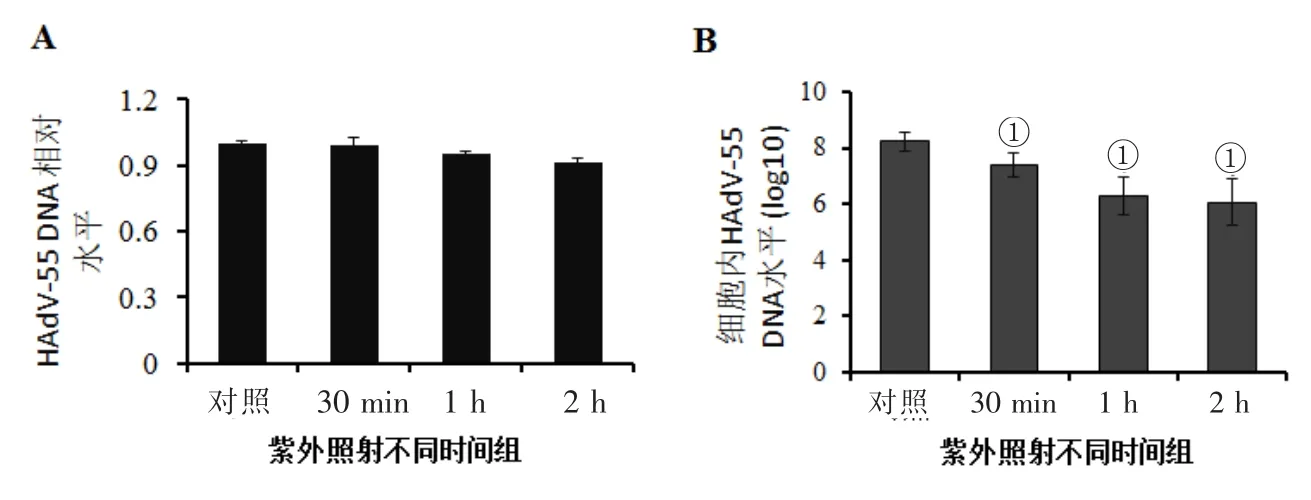
圖1 紫外照射對HAdV-55活力的影響

圖3 熱力滅活對HAdV-55病毒活力的影響
楊玲等[9]報道了紫外線照射對腺病毒氣溶膠活力和粒級分布的影響,采用HEK293包裝細胞制備綠色熒光蛋白標記的重組腺病毒,通過在熒光顯微鏡計數帶綠色熒光的PKl5細胞數以檢測病毒的感染力及活力,發現波長為254 nm的紫外線照射5 min時,細胞內感染的病毒數即明顯減少;254 nm紫外線照射30min時,感染細胞內不能檢測到綠色熒光。該研究還發現波長為254 nm的紫外線比365 nm的紫外線照射滅活腺病毒氣溶膠的效果更顯著。
本研究發現,波長254 nm的紫外線照射HAdV-55,對病毒DNA水平影響不大,但顯著降低病毒的感染活力。紫外線照射30 min后,細胞內病毒DNA水平降低約50%;照射1 h和2 h,細胞內病毒DNA水平降低約2個數量級,而且病毒感染細胞產生子代病毒的滴度也顯著降低,均證明紫外線照射可在一定程度上滅活腺病毒,采用紫外線照射能在一定程度上控制腺病毒的傳播。但由于實驗條件所限,本研究采用的紫外燈功率為20W,照射距離為60 cm,僅設置了照射時間一個變量。此外,由于紫外滅活的效果與時間、距離、功率、環境溫度、濕度等都有關,因此,在實際工作中,可通過適當延長紫外照射時間、縮短照射距離、提高照射功率等方法,提高滅活效果。
文獻報道,不同溫度對病毒滅活強弱效果也有差異[10-11],65℃滅活病毒可作為篩選滅活疫苗株的一個條件。本研究結果顯示,熱力對HAdV-55的滅活作用較強,65℃處理30 min后,病毒感染水平的對數值降低4.0左右,產生子代病毒的滴度顯著降低;65℃處理1 h和2 h后,HAdV-55感染細胞產生的新病毒極少。因此,對腺病毒污染物品進行加熱消毒是可行且有效的。
254 nm紫外線和65℃熱力對HAdV-55均有不同程度的滅活作用,其中紫外線照射可作為實驗室空間整體消毒的一種方法,熱力滅活可作為篩選滅活疫苗株的一種手段,其中65℃熱力對HAdV-55處理1 h以上可使其不能產生子代病毒,為后續研究HAdV-55滅活疫苗提供參考。
【參考文獻】
[1]袁躍彬,趙京生,段新科,等.腺病毒3型急性呼吸道感染暴發流行的病原學診斷[J].第三軍醫大學學報,2010,32(22):2468-2469.
[2]王琳,陸海宇,劉其會,等.人類腺病毒B組7型致軍營聚集性感染的臨床特征[J].中華傳染病雜志,2015,33(2):79-82.
[3]楊朝輝.人腺病毒11a型的全基因序列測定及分析研究[D].蘭州:蘭州大學,2009.
[4]Lu Qingbin,Tong Yigang,Wo Y,et al.Epidemiology of human adenovirus and molecular characterization of human adenovirus 55 in China,2009-2012 [J].Influenza&Other Respiratory Viruses,2014,8(3):302-308.
[5]Li X,Mei K,Xu S,et al.An outbreak of acute respiratory disease in China caused by human adenovirus type B55 in a physical training facility[J].International Journal of Infectious Diseases,2014,28:117-122.
[6]Cao B,Huang GH,Pu ZH,et al.Emergence of communityacquired adenovirus type 55 as a cause of community-onset pneumonia[J].Chest,2014,145(1):79-86.
[7]劉媛,王文博,鄒自英,等.快速獲取 55型腺病毒基因組序列的方法[J].微生物學通報,2017,44(11):2708-2713
[8]李杰,魏秋華,饒林,等.常用消毒劑對新發現腺病毒55型滅活效果研究[J].中國消毒學雜志,2016,33(5):405-407.
[9]楊玲,李曉巖,畢新慧,等.紫外線照射對腺病毒氣溶膠活力和粒級分布的影響[J].中華生物醫學工程雜志,2007,13(5):286-289.
[10]饒林,王太星,蔣莉,等.紫外線和熱力滅活脊髓灰質炎病毒效果的試驗觀察[J].中國消毒學雜志,2001,18(2):69-74.
[11]李曉東,廖昊,劉妍,等.60℃加熱1 h滅活病毒方法對常規臨床檢測指標的影響研究[J].傳染病信息,2016,29(3):160-163.

