早期腸內、外聯合營養對食管癌術后的療效
丁紅霞,張 靜,王 勝,趙小梅
食管癌患者常因吞咽困難就診,術前患者多數已存在營養不良等情況,術中創傷造成血液和蛋白質丟失,術后因腸外營養使患者得不到有效的營養支持,使患者長期處于營養不良狀態[1]。食管癌手術患者分解代謝增加,常規腸外營養限制患者營養物質攝入,增加營養風險,以致患者能量的缺失不利于術后腸道功能恢復及身體康復[2]。早期腸內營養(early enteral nutrition,EEN) 聯合小劑量腸外營養支持,可滿足機體營養及各類代謝的需求。因此,術后早期進行腸內、外營養支持對食管癌手術患者具有重要意義[3]。本研究對早期腸內、外聯合營養對食管癌術后降低食管癌術后患者疲勞指數、改善術后營養狀況進行對比分析,旨在為改善食管癌術后營養狀況提供幫助。
1 對象與方法
1.1 對象 隨機選取2016-04至2017-04我院收治的食管癌183例,按是否進行早期腸內、外聯合營養分為受試組(91例)和對照組(92例)。入組標準:(1)首次確診原發食管癌患者;(2)對手術方式無禁忌證;(3)均為同組手術醫師進行手術;(4)無住院費用等壓力,能承擔各項費用。排除標準:(1)有精神障礙或心理疾病者;(2)合并慢性腸道疾病;(3)腫瘤遠處轉移者;(4)因各類因素中斷研究者。兩組患者的年齡、性別、教育程度、預計病理分型等一般資料進行比較,差異無統計學意義,具有可比性(表1)。
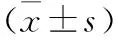
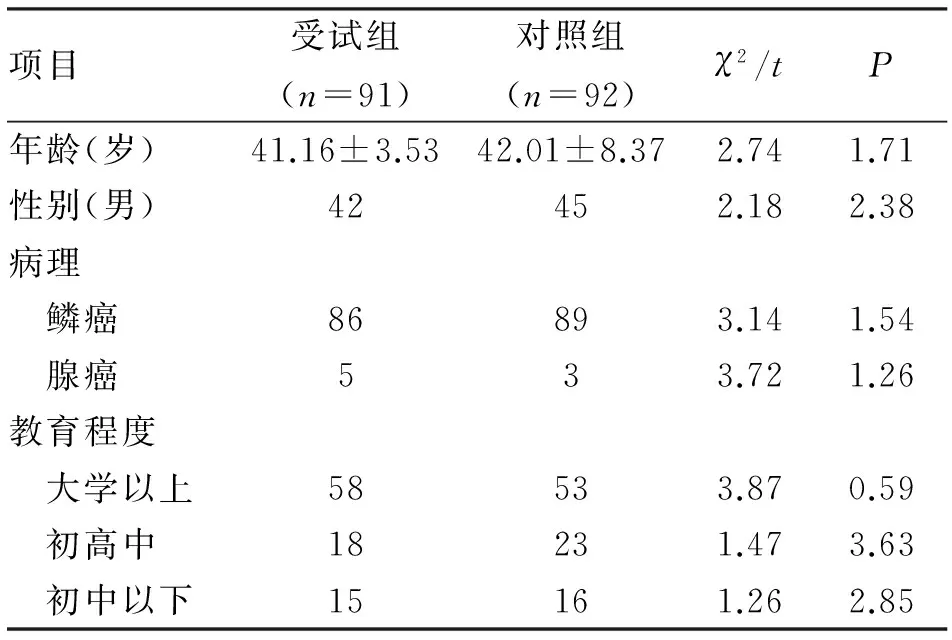
項目受試組(n=91)對照組(n=92)χ2/tP年齡(歲)41.16±3.5342.01±8.372.741.71性別(男)42452.182.38病理 鱗癌86893.141.54 腺癌533.721.26教育程度 大學以上58533.870.59 初高中18231.473.63 初中以下15161.262.85
1.2 方法
1.2.1 受試組 經術中放置的鼻腸管進行腸內、外聯合營養,術后24 h內常規靜脈液體輸注,術后1 d后應用限速營養泵滴入能全力的腸內營養劑,熱量為750 kcal,滴速為20 ml/h; 術后2 d根據患者耐受營養液情況將腸內營養混懸液加至800~1000 ml/d, 滴速增至40 ml/h;術后3 d將營養液加量至1500 ml/d,滴速增至60 ml/h,以后每天增加20 ml/h,夾控溫度在37~39 ℃。
1.2.2 對照組 術后給予TPN 83.6~104.6 kJ,20~25 kcal/(kg·d),術后3 d開始給予能全力750 ml,20~25 ml/h胃管泵入[4-6]。
1.3 觀察指標 分別對兩組術前、術后3 d、7 d進行歐洲營養風險篩查量表(nutritional risk screening 2002,NRS2002)分析,人體學測量、近期體重變化、膳食攝入情況,并對調查結果進行統計學分析。測定患者的前白蛋白、血漿白蛋白、血紅蛋白結果,對兩組患者進行營養評估。
NRS2002總評分——營養狀況評分+疾病嚴重程度評分(年齡大于70歲者加1分),總分0~7分。總評分≥3分說明存在營養風險,需給予營養支持[7];兩組應用CHristensens 法測評疲勞指數,評分標準:(1)1~2分健康,劇烈活動才引起疲勞,睡眠時間正常;(2)3~5分輕度疲勞,輕度體力活動即出現疲勞感,睡眠時間未見明顯增多;(3)6~8分困乏,全身肌肉無力較明顯,睡眠需要時間顯著增多;(4)9~10分疲勞,不能進行任何日常活動。

2 結 果
2.1 NRS2002對比 術前對兩組患者NRS2002評分進行統計分析,兩組差異無統計學意義;術后3 d、7 d,受試組的營養風險評估分數小于3分例數均高于對照組,差異有統計學意義(P<0.05,表2)。
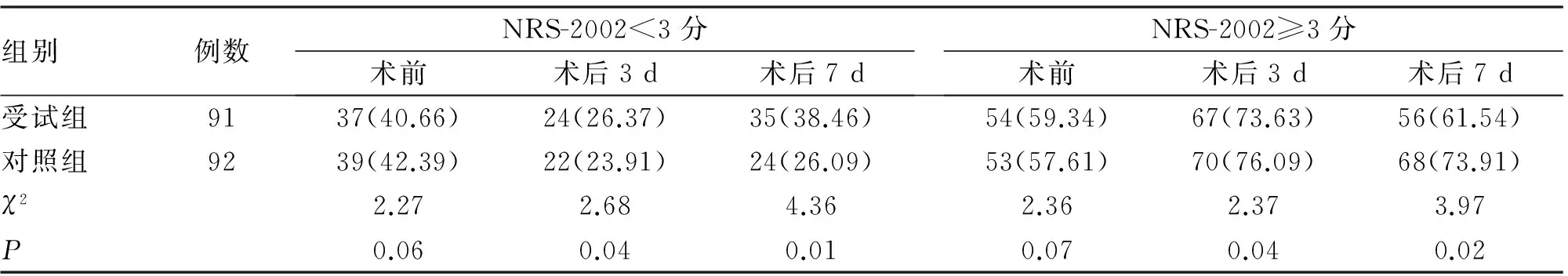
表2 食管癌兩組患者NRS-2002量表比較 (n;%)
2.2 疲勞指數 術前兩組經CHristensens 法進行疲勞指數評估,差異無統計學意義;術后兩組疲勞指數評估,兩組間疲勞指數差異有統計學意義(P<0.05);術后3 d、7 d,受試組的疲勞指數均低于對照組,差異具有統計學意義(P<0.05,表3)。
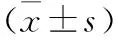

組別術前術后3d術后7d受試組7.97±0.376.21±0.37①3.37±0.63①②對照組7.29±0.267.36±0.52①6.81±0.29①
注:與術前比較,①P<0.05;與術后3 d比較,②P<0.05
2.3 血清蛋白等比較 兩組患者術前、術后3 d、7 d前白蛋白、血漿白蛋白結果進行對比,術前兩組前白蛋白、血漿白蛋白差異無統計學意義;術后受試組的前白蛋白、血漿白蛋白均高于對照組,差異有統計學意義(P<0.05,表4)。
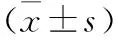
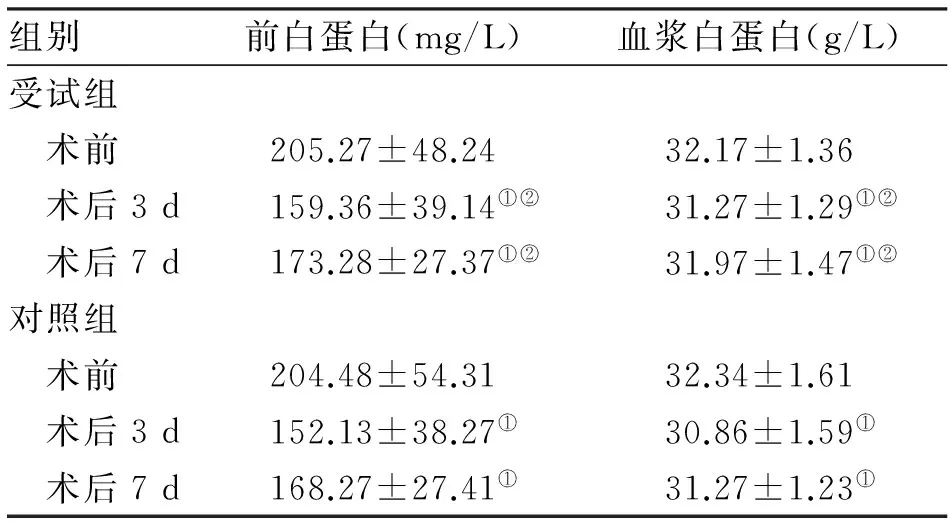
組別前白蛋白(mg/L)血漿白蛋白(g/L)受試組 術前205.27±48.2432.17±1.36 術后3d159.36±39.14①②31.27±1.29①② 術后7d173.28±27.37①②31.97±1.47①②對照組 術前204.48±54.3132.34±1.61 術后3d152.13±38.27①30.86±1.59① 術后7d168.27±27.41①31.27±1.23①
注:與術前比較,①P<0.05;與對照組比較,②P<0.05
3 討 論
食管癌患者因吞咽功能障礙,多在術前已存在營養不良狀況。既往認為,術后單一進行腸外營養,能更有效地減少消化系統負擔。但近年來研究發現,術后早期進行腸內營養可有效改善營養狀況降低進一步惡化的風險,且聯合腸外營養可進一步補充腸內營養的不足。據報道,腸內營養具有以下優勢:(1)更符合胃腸道生理,全面系統,營養均衡;(2)有利于維持腸黏膜細胞的結構與組織功能完整,降低內毒素釋放與細菌易位發生率;(3)促進胃腸道功能的恢復,構建腸道黏膜的屏障;(4)有助于改善肝膽功能,控制血糖,改善免疫功能,抑制代謝激素釋放,減少腸源性高代謝反應;(5)糾正腸下黏膜缺血狀態,改善內臟血流;(6)補充蛋白質和熱量比腸外營養更有效,減少炎癥與感染;(7)營養支持效果好,并發癥少[9]。本研究發現,術前兩組患者的營養風險篩查表評分,差異無統計學意義;術后兩組的營養風險篩查表評分經統計學分析,差異有統計學意義;術后3 d、7 d,受試組的營養風險評估分數小于3分患者均多于對照組,表明對食管癌患者早期進行腸內、外聯合營養可明顯降低營養風險。
疲勞指數可以相對反映患者術后恢復情況。術后疲勞綜合征是消化道手術后的常見表現,也是引起消化道術后各種并發癥的常見原因[9]。本研究發現,術前兩組患者疲勞指數,差異無統計學意義;術后3 d、7 d,受試組的疲勞指數均低于對照組,差異具有統計學意義。說明受試患者疲勞程度低于對照組,表明患者早期進行腸內、外聯合營養對減低患者疲勞指數有積極效果。
文獻[10]發現,一般患者手術后6 h內小腸能恢復自身的消化吸收、蠕動等功能, 24 h后能恢復收縮分泌等功能,整體代謝水平及內環境已趨于穩定,可給予腸內營養。長時間采用腸外營養,特別是手術后禁食期間,因為缺少食物刺激,會使腸道黏膜萎縮,損害腸道黏膜屏障,因此近年來主張在術后早期使用腸內營養[11]。本研究表明,經早期腸內、外聯合營養后患者的各類蛋白指數均得到顯著提高。因腸內營養通過食物對腸道黏膜的刺激,可以使腸道黏膜的纖毛系統正常運動,使腸道的菌群正常生長,保持腸黏膜的內環境穩定,增強了腸黏膜的抗毒素能力,減少細菌移位的可能性[12,13]。
綜上所述,早期腸內、外營養可降低患者的營養風險指數,降低食管癌患者術后的疲勞指數,有效提高患者術后前白蛋白、血漿白蛋白指標。下一步研究將擴大樣本量,對早期腸內、外營養降低術后各種并發癥的可能機制等進行更深入地研究。
【參考文獻】
[4]Grabe,W.(1991).Current Development in Second Language Reading Research.TESOL Quarterly,25(3).375-406.
[1] 姚紅兵,曾榮城,文明波,等,早期腸內營養與延遲腸內營養治療重癥急性胰腺炎的臨床療效比較[J]. 實用醫學雜志,2014,30(14) :2231-2233.
[2] Shang Y,Mu L,Gun X,etal.Clinical significance of interleuking,tumor necrosis factor-α and high-sensitivity Creactive protein in neonates with hypoxic.ischemic encephalopathy[J].Exp Ther Med,2014,8(4):1259.1262.
[3] 黎介壽.首選腸內營養的合理性[J].腸外與腸內營養,2013,20(6):321-323.
[4] 許穎玲. 早期腸內營養對食管癌手術療效的影響研究[J].國際醫藥衛生導報, 2011, 21 (6): 503-504.
[5] 侯亞紅,施月仙,邸紅軍,等. 腸內營養單用與聯合針灸治療顱腦損傷合并胃癱患者的療效比較:一項前瞻性研究[J].武警醫學, 2017,28(2):140-142.
[6] 高紅梅,姚俊利,路 玲,等.急性胃腸損傷分級在重癥監護病房 患者早期腸內營養支持中應用的臨床研究[J].中華危重病急救醫學,2014,26(4):214-218.
[7] 楊倩蓉,楊明瑩,王劍松,等.我國延續護理的應用研究現狀[J].護理學報.2014,21(9):17-18.
[8] 任 寧.肺癌患者癌因性疲乏與生活質量的相關性研究[J].中華現代護理雜志,2012,18(7):751-755.
[9] Osland E J,Memon M A,Early postoperative feeding in resectional gastrointestinal surgical cancer patients[J].World J Oncology,2010,2(4):187.
[10] Daniela T,Nelson S A,Bo H M,etal.High energy particleinduced tumorigenesis throughout the gastroin testinal tract[J].Radiat Res,2014,181(2):162-171.
[11] 郭華鑫. 腸內營養干預對胃腸道腫瘤患者術后炎性反應和預后的影響[J].武警醫學, 2016,27(6): 597-600.
[12] Sun J K,Mu X W,Li W Q,etal.Effects of early enteral nutrition on immune function of severe acute pancreatitis patients [J]. World J gastroenterology,2013,19(6):917-923.
[13] 沈 玨,趙擎宇,顧葆春,等. 腫瘤重癥患者的營養狀況評估及營養 支持現狀分析[J]. 熱帶醫學雜志,2014(1):52-55.

