低分子肝素鈣皮下注射治療慢性阻塞性肺疾病急性加重期合并肺心病的療效
徐婕 曾龍飛 龔建祖 葛德海
南京梅山醫院呼吸科(南京210041)
慢性阻塞性肺疾病急性加重(acute exacerbation of chronic obstructive pulmonary disease,AECOPD)是臨床上常見的呼吸系統疾病,AECOPD患者隨著病程的延長,肺心病、肺動脈高壓等不良心血管并發癥的發生率在增加,進而影響預后。文獻顯示年齡>45歲的患者中,AECOPD合并肺心病患者的發生率逐漸上升,而抗感染、糖皮質激素、支氣管擴張劑等常規綜合性治療措施的總體有效率不足45%,且治療后患者的病情緩解率較低[1-2]。在COPD急性期中,機體存在較強的炎癥反應,血液呈高凝狀態[3],而低分子肝素鈣(molecular weight heparin calcium,MvH)可以抑制患者體內的高凝狀態,改善血流動力學指標,進而恢復患者通氣/血流比值,改善肺通氣或者肺換氣功能[4-5],同時MvH具有比肝素更好的抗炎癥作用[6]。有鑒于此本研究選取2016年1月至2017年12月我院收治的AECOPD合并肺心病患者128例,通過皮下注射MvH聯合常規治療措施,探討MvH對AECOPD肺心病患者的影響機制和臨床效果。
1 資料與方法
1.1 一般資料 選取2016年1月至2017年12月我院收治的AECOPD合并肺心病患者128例,采用EXCEL 2007生成隨機數字表分為觀察組和對照組各64例。觀察組64例,男41例、女23例,年齡56~79歲,平均(65.7± 9.2)歲,病程6~18年,平均病程(12.6±5.9)年,紐約心臟病協會(NYHA)心功能分級:Ⅲ級48例、Ⅳ級16例。對照組64例,男43例、女21例,年齡58~79歲,平均(67.4±8.6)歲,病程6~21年,平均病程(13.0±5.5)年,NYHA心功能分級:Ⅲ級50例、Ⅳ級14例。兩組患者的年齡、性別、病程、NYHA心功能分級差異均無統計學意義(P>0.05)。
1.2 納入排除標準
1.2.1 納入標準 (1)AECOPD患者的診斷標準參考2007年中華醫學會呼吸病學分會制定COPD診療指南(修訂版)中的標準[7];(2)肺心病診斷符合內科學第七版肺心病診斷標準[8];(3)NYHA心功能分級Ⅲ~Ⅳ級;(4)年齡 ≤ 79歲;(5)本觀察研究獲得患者及醫學倫理委員會的批準。
1.2.2 排除標準 (1)近6個月應用華法林、肝素、阿司匹林藥物;(2)肝腎功能不全;(3)具有腦血管出血病史、上消化道出血病史、消化道活動性出血疾病;(4)合并冠心病、瓣膜性心臟病的患者。
1.3 治療方法 對照組:給予常規抗感染、吸氧、祛痰、維持水電解質平衡、強心利尿等基礎治療;觀察組在對照組的基礎上聯合皮下注射低分子肝素鈣(速碧林,葛蘭素史克公司生產),4 100 U/次,每日2次,連續治療1周。
1.4 觀察指標 檢測并對比兩組患者治療前后的舒張末期心室容積(EDV)、收縮末期心室容積(ESV)、右心室射血分數(RVEF)、肺動脈加速時間(AT)、動脈血氧分壓(PaO2)、動脈血二氧化碳分壓(PaCO2)、pH值、全血黏度低切、全血黏度高切、血漿黏度、紅細胞壓積、血漿D-二聚體(D-D)。
清晨采集空腹靜脈血,分離血清后,-20℃保存待測,采集標本后1周內檢測、全血黏度低切、全血黏度高切、血漿黏度、紅細胞壓積、血漿D-二聚體(D-D),相關指標測定采用酶聯免疫吸附測定試驗,檢測試劑盒購自福建新大陸生物技術有限公司;pH值的檢測采用電化學發光法,具體檢測方法參照試劑盒說明書,試劑盒內配有質控血清或質控標準品,所有操作嚴格按照操作說明完成。
1.5 統計學方法 數據統計分析采用SPSS 20.0進行處理,所有計量指標均采用均數±標準差進行統計描述,干預前后組內比較應用配對t檢驗,組間比較采用兩組獨立樣本的t檢驗;P<0.05表示差異具有統計學意義。
2 結果
2.1 兩組患者的心功能變化 治療前,觀察組和對照組的EDV、ESV、RVEF、AT差異無統計學意義(P>0.05);治療后,觀察組的EDV、ESV均低于對照組(P<0.05),RVEF、AT均高于對照組(P<0.05)。見表1。
表1 兩組患者的心功能變化Tab.1 Changes of heart function index in two groups ±s
注:與治療前比較,*P<0.05,與對照組比較,△P<0.05
時間治療前治療后組別研究組對照組研究組對照組EDV(mL)88.4±5.9 86.0±6.2 63.0±5.5*△69.6±7.3*ESV(mL)62.8±5.9 64.3±7.4 38.0±6.7*△43.0±7.5*RVEF(%)28.9±6.4 29.5±6.8 45.2±6.0*△41.6±7.3*AT(s)0.11±0.03 0.12±0.04 0.17±0.04*△0.14±0.05*
2.2 兩組患者的血氣指標比較 治療前,觀察組和對照組的PaO2、PaCO2、pH值差異無統計學意義(P>0.05);治療后,觀察組的PaCO2值低于對照組(P<0.05),PaO2、pH值均高于對照組(P<0.05)。見表2。
表2 兩組患者的血氣指標比較Tab.2 Changes of blood gas index in two groups ±s
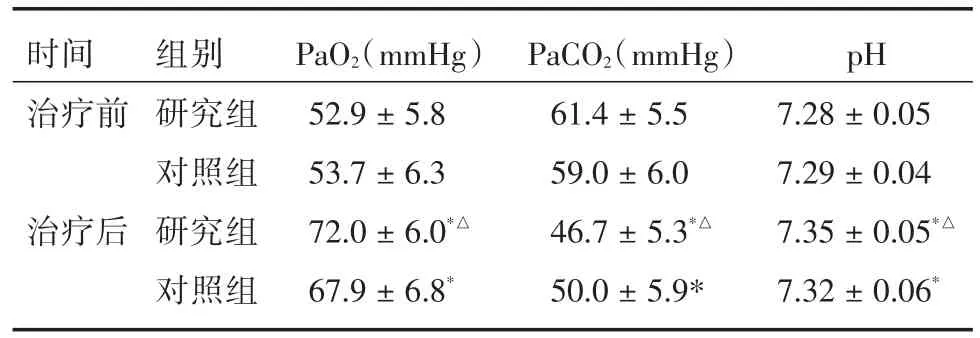
表2 兩組患者的血氣指標比較Tab.2 Changes of blood gas index in two groups ±s
注:與治療前比較,*P<0.05,與對照組比較,△P<0.05
時間治療前治療后組別研究組對照組研究組對照組PaO2(mmHg)52.9±5.8 53.7±6.3 72.0±6.0*△67.9±6.8*PaCO2(mmHg)61.4±5.5 59.0±6.0 46.7±5.3*△50.0±5.9*pH 7.28±0.05 7.29±0.04 7.35±0.05*△7.32±0.06*
2.3 兩組患者的血液流變學指標比較 治療前,觀察組和對照組的全血黏度低切、全血黏度高切、血漿黏度、紅細胞壓積、血漿D-D值差異無統計學意義(P>0.05);治療后,觀察組的全血黏度低切、全血黏度高切、血漿黏度、紅細胞壓積、血漿D-D值低于對照組(P<0.05)。見表3。
表3 兩組患者的血液流變學指標比較Tab.3 Changes of the blood rheology index in two groups ±s

表3 兩組患者的血液流變學指標比較Tab.3 Changes of the blood rheology index in two groups ±s
注:與治療前比較,*P<0.05,與對照組比較,△P<0.05
時間治療前治療后D-D(mg/dL)2.87±0.36 2.91±0.44 1.95±0.35*△2.52±0.41*組別研究組對照組研究組對照組全血黏度低切(mPa·s)12.41±2.15 12.05±2.36 8.73±1.89*△10.14±1.96*全血黏度高切(mPa·s)7.89±1.38 7.74±1.33 6.52±1.14*△7.50±1.07*血漿黏度(mPa·s)1.83±0.31 1.81±0.28 1.63±0.30*△1.79±0.26*紅細胞壓積(%)0.522±0.031 0.528±0.029 0.461±0.043*△0.498±0.036*
2.4 不良發應 觀察組有4例患者出現注射部位皮下瘀斑、1例出現痰中帶血、1例出現消化道不適,對照組有3例出現消化道不適,兩組患者的不良發應發生率比較差異無統計學意義(P>0.05)。
3 討論
COPD患者隨著病情的反復和進展,可出現肺心病、肺動脈高壓等嚴重并發癥,導致病死率的上升[9-10]。一項匯集了172例樣本量的研究顯示,AECOPD合并肺心病患者的臨床綜合治療效果有限,治療后患者的阻塞性通氣功能障礙或者呼吸系統炎癥表現仍然無明顯改善[11]。我們已經認識到AECOPD患者肺部異常炎癥反應會導致患者氣道周圍聚集大量的浸潤性炎細胞,并不斷釋放TNFa、IL-6、白三烯B4等炎癥介質,研究證實:TNFα、IL-6等因子能導致局部肺泡組織及毛細血管的過氧化應激損傷,促進肺動靜脈的內皮損傷;能激活凝血系統、抑制纖維蛋白降解、血液粘稠度增高、肺微小動脈栓塞的形成等,繼而促進了肺動脈壓力的增高、心臟代償功能的障礙和增加AECOPD合并肺心病患者心肌梗死、急性心力衰竭或失代償性心功能不全等的發生[12-13]。因此尋求針對AECOPD患者并發肺心病、肺動脈高壓發生機理的治療措施,可能有利于控制病情的進展。
低分子肝素鈣在AECOPD患者并發肺心病患者的應用研究中顯示低分子肝素可以有效治療AECOPD患者,促進綜合治療效果的顯著增強[14-15],而低分子肝素鈣改善AECOPD合并肺心病的機制可能與下列因素有關:(1)低分子肝素改善了局部肺泡毛細血管血流動力學的紊亂,降低了心臟泵血負荷,改善了心臟功能;(2)低分子肝素對于血小板性微血栓或者局部氧化應激性損傷的抑制作用,可以保護心肌細胞膜完整性免受損傷,改善心臟舒張功能[16];本組研究資料顯示反應肺心病患者心臟收縮或者舒張功能的影像學指標EDV或ESV,在觀察組患者中明顯下降,提示患者收縮或者舒張末期的心室壁容積明顯減小,心臟舒張或者收縮功能明顯改善。同時本研究發現治療后右心室射血分數(RVEF)、肺動脈加速時間(AT)等指標明顯上升,高于對照組,提示心臟代償功能的進一步改善。結果與周凌等回顧性分析的低分子肝素鈣治療AECOPD合并肺心病患者的心臟射血分數可平均上升15%以上,且左側心房及左側心室壁舒張末期容積明顯下降臨床結果基本一致[17]。因此筆者認為低分子肝素鈣對于肺心病患者心功能改善作用的機制可能與下列因素有關:(1)低分子肝素鈣可以通過改善冠狀動脈或者肺動脈的血流動力學指標,促進局部血流微循環,降低心臟收縮的前負荷[17];(2)低分子肝素鈣治療后,可以通過降低肺栓塞或者冠狀動脈血栓形成導致的心臟舒張或者收縮功能的障礙,改善心臟代償功能;(3)低分子肝素鈣對于肺靜脈壓力的改善或者低于右側心室壁回心血流動力學的保護;(4)比肝素更好的抗炎癥作用[6],進而保護內皮細胞功能,重建機體免疫系統內穩狀態等。
本組研究資料還顯示:低分子肝素鈣治療后觀察組患者的血氣代謝指標明顯改善,血壓飽和度及動脈血氧含量上升,而二氧化碳分壓持續下降,血氣分析指標的改善,考慮可能與低分子肝素鈣治療后對于肺泡局部氧氣彌散功能的改觀有關,同時也可能與低分子肝素鈣治療后對于肺部血小板性血栓形成的抑制,進而提高局部有效通氣有關。血流動力學指標的分析也可以發現,低分子肝素鈣治療后的觀察組患者的全血黏度低切、全血黏度高切、血漿黏度、紅細胞壓積等均明顯改善,D-二聚體也明顯下降,患者的纖維蛋白溶解系統亢進表現得到了顯著的抑制,進一步提示了低分子肝素鈣治療AECOPD合并肺心病的臨床效果。
綜上所述,MvH皮下注射治療AECOPD合并肺心病患者能改善患者的血液流變學水平、改善心功能及血氣水平,且治療后并未出現明顯的副反應,臨床安全性較為可靠,值得推廣應用。但本研究仍有許多不足,如MvH治療AECOPD合并肺心病患者遠期生存預后指標、MvH治療的最佳劑量和療程等,有待進一步的研究探討。
參考文獻
[1]GARCIA RIO F.Enfermedad pulmonar obstructiva crónica y cardiopatía isquémica:una asociación no tan infrecuente[J].Revista Clínica Espa?ola,2014,214(5):281-282.
[2]GRIFFO R,SPANEVELLO A,TEMPORELLI P L,et al.Frequent coexistence of chronic heart failure and chronic obstructive pulmonary disease in respiratory and cardiac outpatients:Evidence from SUSPIRIUM,a multicentre Italian survey[J].Euro J Prevent Cardiol,2017,25(6):170-173.
[3]李廣生,李月川.血小板平均體積及中性粒細胞/淋巴細胞比率聯合檢測在老年AECOPD近期預后中的臨床價值[J].實用醫學雜志,2017,33(6):928-931.
[4]VAN DER PLAS A G,OOSTERVELD-VLUG M G,PASMAN H R W,et al.Relating cause of death with place of care and healthcare costs in the last year of life for patients who died from cancer,chronic obstructive pulmonary disease,heart failure and dementia:A descriptive study using registry data[J].Palliat Med,2017,26(06):56-58.
[5]丁明霞,盧丹,常媛媛,等.低分子肝素治療老年慢性阻塞性肺疾病合并肺心病急性發作期效果[J].臨床肺科雜志,2015,20(3):487-489.
[6]吳志雄,馮坤好,譚家余,等.小劑量肝素鈉與低分子肝素鈣對膿毒癥治療作用的對比研究[J].臨床和實驗醫學雜志,2016,15(4):359-361.
[7]王琴,王巖,王玉宏.APACHEⅢ評分對無創通氣治療慢性阻塞性肺疾病急性加重患者的預后評估[J].中華臨床醫師雜志(電子版),2014,22(8):1585-1587.
[8]陸再英,鐘南山.內科學[M].北京:人民衛生出版社,2008:167.
[9]QIAN Y,X IE H,TIAN R,et al.Efficacy of low molecular weight heparin in patients with acute exacerbation of chronic obstructive pulmonary disease receiving ventilatory support[J].COPD,2014,11(2):171-176.
[10]姚婉貞.慢性阻塞性肺疾病病情和預后評估指標新認識[J].中華醫學雜志,2015,95(8):561-563.
[11]PARKER D R,LIU J,ROBERT M B,et al.Is inflammatory chronic obstructive pulmonary disease a coronary heart disease risk equivalent?A longitudinal analysis of the third National Health and Nutrition Examination Survey(NHANES III),1988-1994[J].BMC Pulm Med,2014,14(1):90-92.
[12]毛小青,馬文江.COPD患者實施抗栓預防治療應用低分子肝素的效果分析及纖維蛋白原的改變情況分析[J].中國醫院藥學雜志,2015,22(15):1414-1417.
[13]史靈芝.抗凝治療對慢性阻塞性肺疾病穩定期患者合并血栓前狀態的影響[J].江蘇醫藥,2014,42(23):2845-2847.
[14]王玉春.低分子肝素鈣皮下注射治療慢性阻塞性肺疾病急性加重期合并肺心病療效觀察[J].中西醫結合心血管病雜志,2016,4(36):38.
[15]朱瑞航,余艷芳,屠春林.低分子肝素鈉治療慢性阻塞性肺疾病急性加重期的療效分析[J].貴州醫藥雜志,2016,40(5):484-486.
[16]衛小紅,王軍輝,Asmitanand Thakur,等.低分子肝素、N-乙酰半胱氨酸干預對COPD大鼠氣道重塑的影響[J].西安交通大學學報(醫學版),2014,25(02):196-199.
[17]周凌,席家寧.低分子肝素對慢性阻塞性肺疾病急性加重治療效果的Meta分析[J].軍事醫學,2015,22(08):621-625.

