溫針灸對膝骨關節炎SD大鼠軟骨中TNF-α和MMP-3的影響
宋昳星,郭冬梅
(新疆醫科大學附屬中醫醫院,新疆 烏魯木齊 830000)
膝骨關節炎是一種以疼痛為早期表現,隨著時間的延長,可以出現關節僵硬、腫脹以及屈伸功能異常,并最終導致關節變形、行走功能喪失的慢性退行性疾病。該病的發病機制尚不明確,其中年齡、運動習慣、體質量以及遺傳等因素均與其發生和發展有關[1],而軟骨的退行性改變是該病發生的核心所在,且炎癥細胞因子損傷機制逐漸受到重視[2]。炎癥細胞因子主要包括腫瘤壞死因子、基質金屬蛋白酶、白細胞介素以及一氧化氮等,目前對腫瘤壞死因子-α(TNF-α)和基質金屬蛋白酶-3(MMP-3)的研究最多,前者主要由單核吞噬細胞產生,對軟骨細胞具有較強的分解作用,可抑制軟骨基質合成[3];后者在正常生理狀態下主要以基質蛋白酶原的形式存在,但在膝骨關節炎患者中,其被過度激活,導致軟骨細胞外基質蛋白分解酶過度激活,從而加速了軟骨的分解和代謝,加速軟骨損傷[4]。目前西醫多以對癥治療為主,早期主要以患者教育、功能鍛煉為主,中期主要以鎮痛、消炎為主,后期則主要以關節腔注射藥物、腔鏡手術為主[5-6]。中醫將本病歸為“痹證”“筋痹”“骨痹”的范疇,治療上有方藥內治、方藥外治以及針灸治療等方法,其中針灸療法作為中醫外治的主要方法,具有操作簡單、療效確切、價廉的特點,非常適合本病的早期治療[7],但作用機制不明確。本研究通過動物實驗,觀察了溫針灸對膝骨關節炎SD大鼠行為學以及軟骨中TNF-α和MMP-3的影響,旨在為該病的臨床治療提供依據。
1 實驗資料
1.1實驗動物 清潔級雄性SD大鼠90只,體質量200~250 g,由山東中醫藥大學動物實驗室提供,合格證號:SCXK(魯)2014-0025。所有動物飼養于我院實驗動物實驗室,飼養溫度保持在(22±2)℃,濕度(60±10)%,敏感周期為12 h。自由攝水,標準飼料適應性喂養1周。
1.2主要試劑和儀器 水合氯醛(廣州化學試劑廠,批號:20160223-3);蘇木精染料(天津化學試劑廠,批號:20160305-6);甲醛(北京普博欣科技有限公司,批號:20150105-6);二甲苯(天津化學試劑廠,批號:20160316-1);TNF-α試劑盒(美國Sigma公司生產,購自北京定國化學生物技術有限公司,批號:LOT#035M1523V);MMP-3試劑盒(美國Sigma公司生產,購自北京定國化學生物技術有限公司,批號:LOT#113M3652V);離心機(德國制造,型號:5810R);石蠟包埋機(浙江金華益迪制造,型號:YD62);切片機(美國制造,型號:RM2235);760日立全自動生化儀(日本制造);放射免疫測量儀(中國制造,型號:SN-682)。
1.3分組、造模及干預 將喂養1周后SD大鼠隨機分為正常組、模型組和針灸組,每組30只。模型組和針灸組大鼠參照文獻[8]采取關節腔注射木瓜酶法復制右膝關節炎模型,并于造模后第4周測量左右膝關節厚度,若右膝關節較左側腫脹大于20%,則視為造模成功。本實驗中大鼠全部造模成功。然后針灸組給予溫針灸治療,選取血海、陽陵泉、內膝眼為主穴,穴位位置參照《實驗針灸學》[9]。血海位于右后肢髕骨底與髕骨內側連線上方約0.8 cm處;陽陵泉位于腓骨頭下方凹陷處;內膝眼位于后肢髕骨下方,髕骨韌帶內側凹陷處。針刺前,大鼠板固定后進行穴位定位,采用太和牌0.22 mm×0.25 mm一次性針灸針,每穴刺入3~5 mm,采用平補平瀉手法上下提插5次后,于針柄處粘貼一蠶豆大艾柱后點燃,持續10 min,連續針灸2周。正常組和模型組大鼠不給予任何干預。
1.4觀察指標
1.4.1大鼠行為學表現 干預前后采用改良版Lequesne MG量表評估大鼠行為學表現,主要評估內容包括大鼠局部疼痛度、步態、關節腫脹情況以及關節活動范圍。疼痛程度:無疼痛記0分;患肢出現收縮記1分;患肢收縮同時伴有輕度全身反應記2分;患肢聚類收縮,伴有全身顫抖甚至掙扎記3分。步態:大鼠正常行走記0分;輕度跛行,觸地有力記1分;患肢參與行走,但跛行明顯記2分;患肢不能參與行走記3分。關節腫脹程度:無腫脹記0分;輕度腫脹,骨性標記線變淺記1分;重度腫脹,骨性標記線消失記2分。關節活動范圍:90°以上且無明顯疼痛反應記0分;45°~90°且無明顯疼痛反應記1分;15°~45°且無明顯疼痛反應記2分;<15°且無明顯疼痛反應記3分。
1.4.2大鼠軟骨組織中TNF-α和MMP-3含量實驗結束時采用空氣栓塞法將所有大鼠處死后固定于手術臺,將右后肢伸直以固定膝關節,備皮后剝離皮膚及皮下組織,暴露膝關節后,使用眼科剪與小刀片切取膝關節面軟骨約20 mg,生理鹽水沖洗干凈后分為2份,一份標本放置于4%的甲醛中固定進行HE染色切片;另一份放置于1.5 mL試管中加入5 mL生理鹽水,離心取上層清液,按照TNF-α和MMP-3試劑盒說明書,采用放射免疫法檢測TNF-α和MMP-3含量。

2 結 果
2.13組大鼠干預前后Lequesne MG評分比較干預前,模型組和針灸組Lequesne MG評分均顯著高于正常組(P均<0.05)。干預結束后,模型組和針灸組評分均顯著下降(P均<0.05),且針灸組評分明顯低于模型組(P<0.05)。見表1。
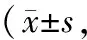
表1 3組大鼠干預前后Lequesne MG評分比較分)
注:①與正常組比較,P<0.05;②與干預前比較,P<0.05;③與模型組比較,P<0.05。
2.23組大鼠膝關節組織病理學表現 正常組大鼠膝關節組織未發現病理改變,關節軟骨表面光滑完整,各層軟骨細胞排列緊密有序,見圖1;模型組大鼠膝關節面粗糙不平,部分地方出現病理性裂隙,中間可見壞死性軟骨組織,周圍可見增生細胞及炎癥細胞,見圖2;針灸組大鼠膝關節病變范圍小于模型組,其水腫程度、炎癥浸潤及壞死程度均輕于模型組,少數壞死組織區內可見新生的軟骨細胞和纖維組織,見圖3。

圖1 正常組大鼠膝關節組織鏡下表現

圖2 模型組大鼠膝關節組織鏡下表現

圖3 針灸組大鼠膝關節組織鏡下表現
2.33組大鼠膝關節組織中TNF-α、MMP-3含量比較 模型組及針灸組大鼠膝關節組織中TNF-α、MMP-3含量均明顯高于正常組(P均<0.05),但針灸組TNF-α、MMP-3含量均明顯低于模型組(P均<0.05)。見表2。

表2 3組大鼠膝關節組織中TNF-α、MMP-3含量比較
注:①與正常組比較,P<0.05;②與模型組比較,P<0.05。
3 討 論
目前膝骨關節炎的動物模型有很多,然而由于膝骨關節炎的發病機制十分復雜,多種因素均參與其中,故現有的動物模型均很難模擬膝骨關節炎的發病全過程,只是模擬了其中的一點或者一段過程[10]。木瓜蛋白酶可以使軟骨基質中的多種蛋白進行分解,使蛋白多糖從軟骨基質中丟失,激活骨關節的炎癥反應,造成類骨關節炎的病理狀態,故木瓜蛋白酶造模是目前常用的膝骨關節炎造模法之一,且成功率較高[11-12]。本研究也采用該法造模,結果均造模成功。
中醫認為膝骨關節炎病因主要為肝腎不足,氣血虧虛,適逢外感風寒或跌打損傷等,導致局部經絡不通,不通則痛,故在治療上宜滋補肝腎、溫經通絡[13]。《黃帝內經》中有云“腧穴所在,主治所及”,故本研究中取血海、陽陵泉、內膝眼三穴以疏通局部經絡,恢復關節內環境平衡。血海為足太陰脾經之穴,具有滋補脾腎、益氣活血之功效,為“治血要穴”,臨床上常用來疏通局部經絡,濡養關節,達到通則不痛、榮則不痛的目的;陽陵泉屬于足少陽膽經,為八會穴之一的“筋會”,“膝為筋之府”,故選取此治筋穴以治骨病;內膝眼為治療骨痹之經驗用穴,常配合外膝眼進行透刺,但因大鼠膝關節較小難以操作,故單用此穴以促進膝關節周圍氣血的運行。《素問·痹論》中有“痛者,寒氣多也”,提示疼痛的發生多與寒氣侵蝕有關。而溫針灸是一種將針刺和艾灸結合的治療方法,具有溫經散寒、通絡止痛的雙重作用,因此常被用來治療膝骨關節炎[14-16]。本研究結果顯示,干預結束后,模型組和針灸組Lequesne MG評分顯著下降,且針灸組明顯低于模型組。進一步病理觀察發現,正常組大鼠膝關節組織未發現病理改變;模型組大鼠膝關節中可見廣泛的病理性改變;針灸組大鼠膝關節病變范圍少于模型組,且水腫程度、炎癥浸潤及壞死程度均輕于模型組,少數壞死組織區內可見新生的軟骨細胞和纖維組織。上述結果提示溫針灸不僅可改善膝骨關節炎的臨床癥狀,而且可減輕骨關節病理改變,這與文獻[17]報道相一致。
細胞因子在人體中是一種免疫調節因子,在人體各項功能中發揮著重要作用。在膝骨關節炎中,軟骨細胞異常分泌了多種細胞炎癥因子,這些因子被釋放至細胞外基質,導致基質細胞內代謝平衡被打破,抑制軟骨細胞生成的同時加速了軟骨細胞的凋亡。本研究結果顯示,模型組及針灸組軟骨組織中TNF-α、MMP-3含量均明顯高于正常組,但針灸組TNF-α、MMP-3含量均明顯低于模型組。提示溫針灸可能通過降低軟骨細胞中TNF-α、MMP-3含量,從而起到治療本病的作用。
綜上所述,溫針灸可以改善膝骨關節炎SD大鼠軟骨形態,具有改善軟骨退變和保護軟骨的作用,可能是通過降低軟骨細胞中炎癥因子TNF-α、MMP-3含量來實現的。然而本次實驗僅僅測定了實驗結束后的TNF-α、MMP-3含量,未能對上述指標進行動態監測,溫針灸治療膝骨關節炎的作用機制有待進一步探討。
[]
[1] 申延清,劉風霞,曹紅,等. 膝骨關節炎患者的臨床表現及相關影響因素[J]. 中國組織工程研究與臨床康復,2011,15(9):1643-1646
[2] Johnson VL,Hunter DJ. The epidemiology of osteoarthritis[J]. Best Pract Res Clin Rheumatol,2014,28 (1):5-15
[3] 陳益丹,邱華平,金肖青,等. 針刺對膝骨關節炎模型兔血清白介素-1β、腫瘤壞死因子-α的影響[J]. 上海針灸雜志,2010,29(7):468-470
[4] 周景輝,李石勝,吳耀持,等. 長針透刺膝骨關節炎模型大鼠滑膜組織中基質金屬蛋白酶3的變化[J]. 中國組織工程研究與臨床康復,2011,15(50):9415-9418
[5] Spaans AJ,van Minnen LP,Kon M,et al. Conservative treatment of thumb base osteoarthritis: A systematic review[J]. J Hand Surg Am,2015,40(1):16-21
[6] 張軍,杜海軍,陳軍,等. 玻璃酸鈉注射治療膝關節退行性骨關節病的療效觀察[J]. 吉林醫學,2013,34(23):4734-4735
[7] 王麗紅,何英. 中西醫治療骨關節炎的研究進展[J]. 中國老年學雜志,2011,31(10):1923-1926
[8] Kopp S,Mejersjo C,Clemenssson E. Induction of osteoarthritis in the guinea pig knee by papain[J]. Oral Surg Oral Med Oral Pathol,1983,55(3):259-266
[9] 李忠仁. 實驗針灸學[M]. 北京:中國中醫藥出版社,2013:327
[10] 謝希,高潔生. 骨關節炎動物模型研究進展[J]. 醫學綜述,2005,11(1):67-69
[11] Havdrup T,Telhag H. Papain-induced changes in the knee joints of adult rabbits[J]. Acta Orthop Scand,1977,48(2):143-149
[12] 韓冠英,凌沛學,王鳳山,等. 不同濃度木瓜蛋白酶建立兔膝骨關節炎模型的比較研究[J]. 中國骨傷,2012,25(5):424-429
[13] 王建國,何麗娟. 溫針灸治療膝骨關節炎療效觀察[J]. 中國針灸,2007,27(3):191-192
[14] 劉立安,馬春燕,姜文. 溫針灸治療老年性膝骨關節病的臨床觀察[J]. 中國針灸,2003,23(10):579-580
[15] 李俐,洪昆達,吳明霞,等. 溫針灸治療陽虛寒凝型膝骨性關節炎40例[J]. 福建中醫藥,2010,41(5):36-37
[16] 丁明暉,張宏,李燕. 溫針灸治療膝關節骨性關節炎:隨機對照研究[J]. 中國針灸,2009,29(8):603-607
[17] Nelson AE,Allen KD,Golightly YM,et al. A systematic review of recommendations and guidelines for the management of osteoarthritis:The chronic osteoarthritis management initiative of the U.S.bone and joint initiative[J]. Semin Arthritis Rheum,2014,43(6):701-712

