血清肌酐正常的2型糖尿病患者腎小球濾過率水平與危險因素分析
李愛琴,何泱,湯正義,王衛慶,寧光
(1.上海交通大學醫學院附屬瑞金醫院內分泌代謝病科、上海市內分泌代謝病臨床醫學中心上海市內分泌代謝病研究所,上海 200025;2.開封市中心醫院內分泌科,河南 開封 475000)
慢性腎臟病變嚴重性的判斷,是根據腎小球濾過率(glomerular filtration rate,GFR)確定的[1]。在糖尿病微血管并發癥的臨床工作中,檢查與估算GFR并不作為常規項目,尿微量白蛋白與血肌酐檢測值才是最常用的指標。尿微量白蛋白受飲食等因素影響,可能變化較大;血肌酐若超過正常上限,說明患者的病情已經比較嚴重。如何在臨床簡單判斷,仍是不斷在討論的問題。影響GFR的因素很多[2-3],在糖尿病患者,血糖、血壓作為傳統的致病因素倍受重視,但以同位素GRF作為其腎病病變判斷指標的研究資料較少。本研究以同位素GFR作為腎臟病變的指標,觀察臨床上糖尿病相關指標變化與腎臟病變的危險因素。
1 資料與方法
1.1一般資料連續收集2012年9月至2014年3月在上海交通大學醫學院附屬瑞金醫院內分泌代謝病科住院的2型糖尿病(T2DM)患者381例(符合WHO1999標準[4]),年齡范圍18~86歲,其中男性257例,女性124例,其一般資料見表1。排除有以下情況的患者:(1)入院時有危及生命的急性代謝紊亂,如糖尿病酮癥酸中毒及高血糖性高滲狀態等;(2)血清肌酐測定值超過本院正常范圍(53~103 μmol·L-1);(3)合并有嚴重的肝、心等臟器疾病(轉氨酶增高、心衰等);(4)中、重高血壓(血壓>160/100 mmHg);(5)妊娠期以及哺乳期婦女。本研究經過上海交通大學醫學院附屬瑞金醫院醫學倫理委員會批準,所有患者均簽署知情同意書。
1.2方法
1.2.1一般情況與糖尿病病情資料 對入選者收集病史(包括人口學資料、發病診治情況、血糖變化等)、體格檢查(身高、體質量、血壓測定)、生化檢查(見表1)。糖尿病病程從確立診斷時計算。
1.2.2研究方法 99mTc標記的二乙三胺五乙酸(99mTc-DTPA)腎動脈顯像檢測GFR:患者仰臥位,肘靜脈“彈丸”注射,動態采集。應用專用軟件,按照Gates公式[5],編出計算程序,自動算出總腎GFR及分腎GFR。根據GFR分組,GFR≥90 mL·min-1腎功能正常的納入正常組,GFR≥60~90 mL·min-1腎功能輕度異常納入輕度組,GFR≥30~60 mL·min-1腎功能中度異常納入中度組。同時應用Cockcroft-Gault公式[6]評估eGFR:男性:Cr(mL·min-1) =(140-年齡)×體質量(kg)/72×血肌酐(mg·dL-1);女性:Cr(mL·min-1)=(140-年齡)×體質量(kg)/85×血肌酐(mg·dL-1)。應用CKD-EPI公式[7]評估eGFR:女性Scr≤0.7,則eGFR=144×(Scr/0.7)-0.329×0.993年齡,女性Scr>0.7,則eGFR=144×(Scr/0.7)-1.209×0.993年齡;男性Scr≤0.9,則eGFR=141×(Scr/0.9)-0.411×0.993年齡,男性Scr>0.9,則eGFR=141×(Scr/0.9)-1.209×0.993年齡。上述公式中eGFR為GFR的估算值,Cr為內生肌酐清除率(臨床常以肌酐為基礎估算eGFR),Scr(血肌酐)單位為mg·dL-1。

2 結果
2.1一般臨床資料在研究對象中,隨著GFR減少,年齡、糖尿病病程、收縮壓,糖化血紅蛋白、低密度脂蛋白膽固醇逐漸增加,血漿白蛋白不斷下降,組間比較(F=7.261、10.286、5.273、4.347、6.281、4.962,均P<0.05),差異有統計學意義。體質量指數(BMI)、舒張壓、總蛋白、膽固醇、三酰甘油及高密度脂蛋白膽固醇組間比較(F=0.861、0.793、1.247、0.913、0.591、0.734,均P>0.05),差異無統計學意義(見表1)。
2.2糖尿病患者GFR水平與臨床常用腎臟指標間的關系糖尿病患者中,血清肌酐的數值,都在正常范圍內(見表2);尿免疫球蛋白、尿轉鐵蛋白、尿微量白蛋白、尿α1微球蛋白、尿肌酐、尿蛋白與尿肌酐比值隨GFR的減少而增加,其中,正常組的尿白蛋白值僅稍高于正常值,輕度組的為正常值2倍以上,中度組的基本在4倍以上;而胱抑素在3組間比較差異無統計學意義(F=0.983,P>0.05)。
2.3GFR與CG-eGFR、CKD-EPI-eGFR相關性分析
糖尿病患者,在肌酐正常的情況下,正常組CG-eGFR(121.51±11.26) mL·min-1·(1.73m2)-1高于GFR(114.25±10.73) mL·min-1,中度組CG-eGFR(37.21±8.64) mL·min-1·(1.73m2)-1低于GFR(45.25±8.27) mL·min-1[組間比較,t=3.217、4.328,P<0.01],而輕度組CG-eGFR(76.56±9.34) mL·min-1·(1.73m2)-1低于GFR(78.43±10.92) mL·min-1,組間比較,t=-1.231,P>0.05);CG-eGFR隨著GFR的下降而下降,兩者呈正相關關系(r=0.79,P<0.05)。CKD-EPI-eGFR正常組(118.19±10.65) mL·min-1·(1.73m2)-1及中度組(48.32±8.57)均高于GFR正常組(114.25±10.73) mL·min-1及中度組(45.25±8.27) mL·min-1,組間比較,t=2.973、3.124,P<0.05,而輕度組CKD-EPI-eGFR(77.24±9.73) mL·min-1·(1.73m2)-1與GFR(78.43±10.92) mL·min-1組間比較,t=-1.361,P>0.05,差異無統計學意義;CKD-EPI-eGFR隨著GFR的下降而下降,兩者呈正相關關系(r=0.80,P<0.05)。正常組、輕度下降組、中度下降組尿微量白蛋白超過正常上限(3 mg·dL-1)者所占比例分別為14.2%(26/183)、19.5%(31/159)、43.6%(17/39),三組間尿微量白蛋白升高者所占比例呈升高趨勢(P=0.000 2)。

表1 糖尿病381例一般臨床資料比較
注:BMI為體質量指數;SBP為收縮壓;DBP為舒張壓;HbA1c為糖化血紅蛋白;TG為三酰甘油;TC為膽固醇;LDL-C為低密度脂蛋白膽固醇;HDL-C為高密度脂蛋白膽固醇。與正常組相比,aP<0.01,cP<0.05; 與輕度組相比,bP<0.05
2.4篩查影響GFR的因素
2.4.1ordinal回歸結果 以年齡、病程及糖尿病相關指標為自變量,以GFR3個等級為因變量,對因變量頻數分析后選擇logit作為連接函數進行ordinal等級回歸,結果顯示性別、年齡、糖尿病病程、HbAlc、血肌酐、尿α1微球蛋白、尿肌酐、尿白蛋白與尿肌酐比值是GFR顯著影響因素(β值分別為0.072、0.044、0.022、0.051、0.452、-0.059、0.324、-0.902,P<0.05),而血壓、膽固醇、三酰甘油、高密度脂蛋白膽固醇及低密度脂蛋白膽固醇并沒有成為危險因素(P>0.05)。見表3。
2.4.2影響GFR的因素調整后結果 將初步回歸中P值較大(P﹥0.05)的變量剔除,使有顯著影響的危險相關因素的作用和程度更突出。改進后的血肌酐及年齡與GFR仍顯著相關(β值分別為0.051、0.076,P<0.000),糖尿病病程、HbAlC,尿α1微球蛋白、尿肌酐、尿白蛋白/尿肌酐、性別 (β值分別為0.048、0.023、0.454、-0.072、0.324、-0.911,P<0.05) 較改進前相關性更加明顯。見表3。
3 討論
臨床實踐中,常以血肌酐為基礎并考慮年齡、性別、種族等因素來估算eGFR。Bjornstad等[8]對1型糖尿病患者研究顯示,高血糖影響以肌酐為基礎的eGFR的評估,本研究也發現:對血肌酐正常的糖尿病患者來說,CG-eGFR及CKD-EPI-eGFR可能估高或估低腎臟功能,因此,以肌酐為基礎的eGFR在評估糖尿病患者的腎臟功能方面存在一定的局限性。本研究應用99mTc-DTPA腎動脈顯像檢測糖尿病患者GFR,該方法被認為是測定腎臟功能的金標準[9],減小了GFR估算的誤差。
本研究發現,對比GFR正常的糖尿病患者,GFR輕中度降低與年齡、性別、糖尿病病程、血清肌酐、血糖、蛋白尿及尿肌酐等因素相關,因此,對血肌酐正常的T2DM患者腎臟病變程度進行判斷時,除了考慮血清肌酐值,還應注意年齡、性別、糖尿病病程、血糖、尿蛋白、尿肌酐等多種因素,例如尿蛋白的輕度升高提示GFR可能下降到輕度異常,如果升高超過數倍,腎功能可能已經中等程度下降了。因而本研究的結果對臨床腎臟功能的判斷具有一定的參考意義。另外,本研究結果還能為腎臟損傷的預防提供參考,在眾多與GFR降低相關的因素中,年齡、性別、糖尿病病程等因素可能引起GFR的下降,但這些是不可控制因素,血清肌酐、蛋白尿、尿肌酐等指標是從不同的側面反應了腎臟功能的降低,難以說明這些指標是GFR下降的因或果,而糖化血紅蛋白與GFR呈負相關,即高血糖可能引起GFR的下降,提示對糖尿病患者,血糖控制是預防腎臟損傷的關鍵因素。
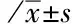
表2 糖尿病381例中GFR異常與臨床常用腎臟指標間的關系比較
注:GFR為腎小球濾過率;CG-eGFR 為經Cockcroft-Gault formula估算的腎小球濾過率;CKD-EPI-eGFR為經CKD-EPI formula估算的腎小球濾過率;Scr為血肌酐;Cystatin為胱抑素;URBP為尿視黃醇結合蛋白;NAIGG為尿免疫球蛋白G ;UTFP為尿轉鐵蛋白;UMA為尿微量白蛋白;α1-UMG為尿α1微球蛋白;UCR為尿肌酐;UACR為尿白蛋白/尿肌酐。與輕度組相比,aP<0.01,dP<0.05;與正常組相比,bP<0.01,cP<0.05

表3 糖尿病381例中影響GFR的因素等級回歸結果
注:性別為男=0,女=1;BMI為體質量指數;SBP為收縮壓;DBP為舒張壓; HbA1c為糖化血紅蛋白;TG為三酰甘油;TC為膽固醇;LDL-C為低密度脂蛋白膽固醇;HDL-C為高密度脂蛋白膽固醇
既往對GFR輕中度異常的糖尿病患者臨床資料分析,其結果之間互有差別。與本研究結果類似,陳燕等[10]的研究是根據尿蛋白的值進行分組,有的已存在血清肌酐升高,分析尿蛋白及GFR的影響因素,也發現年齡、糖化血紅蛋白、糖尿病病程、肌酐等因素與糖尿病患者腎臟功能相關,而本研究選取血清肌酐正常的糖尿病患者,根據GFR進行分組,分析影響GFR的因素。Rodriguez-Poncelas等[11]應用CKD-EPI公式評估eGFR研究中,與研究類似的發現年齡、糖尿病病程、血肌酐及尿蛋白排泄是eGFR的影響因素,但其SBP、HbAlC不隨eGFR的減少而增加,與本研究不符,可能與患者人群、GFR的計算方法及糖尿病治療方案等不同有關。本研究發現血清肌酐正常的糖尿病患者GFR與胱抑素之間無顯著相關性,與Zhang、 Suzuki及李明等研究結果不符[12-14],可能與早期糖尿病患者高濾過有關。另外,根據本研究的統計結果發現男性對GFR的下降有輕微的保護作用,與既往研究[15]有差異,可能因為本研究中主要收集住院患者,與實際人群有偏差。
本研究入選者總體血糖控制稍差,沒有納入血糖控制良好與血糖控制非常差的患者,這些對結果的分析,尤其是血糖對GFR的影響會形成一定的誤差。本研究中的研究對象在入選時血壓控制良好,但未追蹤其過去血壓控制情況和入院時高血壓藥物應用情況,此外,本研究資料來自出院后的病史資料總結,病史中部分患者吸煙資料不全,故統計時未將吸煙的因素納入。降壓藥物的應用、吸煙等因素可能都與GFR有關,這是本研究的不足。
本研究提示,對血清肌酐正常的糖尿病患者,判斷腎臟病變時應綜合考慮尿蛋白、糖尿病病程、糖化血紅蛋白等多種因素,加強糖尿病腎臟病變的篩查[16];微量白蛋白尿的出現,意味著腎功能開始異常,需要引起高度關注;預防糖尿病患者腎臟損傷,最主要的還是控制血糖。
[1] KDOQI.Clinical Practice Guidelines and Clinical Practice Recommendations for Diabetes and Chronic Kidney Disease[J].Am J Kidney Dis,2007,49(2 Suppl 2):S12-154.
[2] INKER LA,SCHMID CH,TIGHIOUART H,et al.Estimating glomerular filtration rate from serum creatinine and cystatin C[J].N Engl J Med,2012,367(1):20-29.
[3] ZHANG QL,ROTHENBACHER D.Prevalence of chronic kidney disease in population-based studies:systematic review[J].BMC Public Health,2008,8:117.
[4] GABIR MM,HANSON RL,DABELEA D,et al.Plasma glucose and prediction of microvascular disease and mortality:evaluation of 1997 American Diabetes Association and 1999 World Health Organization criteria for diagnosis of diabetes[J].Diabetes Care,2000,23(8):1113-1118.
[5] GATES GF.Split renal function testing using Tc-99m DTPA.A rapid technique for determining differential glomerular filtration[J].Clin Nucl Med,1983,8(9):400-407.
[6] COCKCROFT DW,GAULT MH.Prediction of creatinine clearance from serum creatinine[J].Nephron,1976,16(1):31-41.
[7] LIU X,WANG Y,WANG C,et al.A new equation to estimate glomerular filtration rate in Chinese elderly population[J].PLoS One,2013,8(11):e79675.DOI:10.1371/journal.pone.0079675.
[8] BJORNSTAD P,MCQUEEN R B,SNELL-BERGEON J K,et al.Fasting blood glucose-A missing variable for GFR-estimation in type 1 diabetes?[J].PLoS One,2014,9(4):e96264.DOI:10.1371/journal.pone.0096264.
[9] MAIOLI C,COZZOLINO M,GALLIENI M,et al.Evaluation of renal function in elderly patients:performance of creatinine-based formulae versus the isotopic method using 99mTc-diethylene triamine pentaacetic acid[J].Nucl Med Commun,2014,35(4):416-422.
[10] 陳燕,葉山東,金小毛,等.2型糖尿病患者白蛋白尿與腎動態顯像GFR的關系及影響因素[J].中華疾病控制雜志,2014,18(2):143-146.
[11] RODRIGUEZ-PONCELAS A,COLL-DE TUERO G,TURRO-GARRIGA O,et al.Impact of chronic kidney disease on the prevalence of cardiovascular disease in patients with type 2 diabetes in Spain:percedime2 study[J].BMC Nephrol,2014,15(1):150.
[12] ZHANG PP,ZHAN JF,XIE HL,et al.Evaluation of glomerular filtration rate using cystatin C in diabetic patients analysed by multiple factors including tubular function[J].J Int Med Res,2010,38(2):473-483.
[13] SUZUKI Y,MATSUSHITA K,SEIMIYA M,et al.Serum cystatin C as a marker for early detection of chronic kidney disease and grade 2 nephropathy in Japanese patients with type 2 diabetes[J].Clin Chem Lab Med,2012,50(10):1833-1839.
[14] 李明,陳慧卿,劉迅,等.臨床常用腎小球濾過率評估方程在2型糖尿病患者中的效能比較[J].中華糖尿病雜志,2012,4(6):334-339.
[15] VEJAKAMA P,INGSATHIT A,ATTIA J,et al.Epidemiological study of chronic kidney disease progression:a large-scale population-based cohort study[J].Medicine (Baltimore),2015,94(4):e475.DOI:10.1097/MD.0000000000000475.
[16] 胡仁明.加強糖尿病腎臟病變的篩查和防治[J].中華糖尿病雜志,2014,6(10):709-711.

