去甲基化酶JMJD6調控雌激素受體依賴的增強子和編碼基因轉錄激活的分子機制
乳腺癌中大約2/3為雌激素受體陽性,其發生發展的主要原因之一是由于雌激素水平紊亂導致細胞內雌激素/雌激素受體介導的基因轉錄異常激活[1].對于這類乳腺癌的常見治療方式為內分泌治療,但耐藥和腫瘤復發是臨床上亟待解決的問題.因此,尋找這類乳腺癌新的藥物治療靶點,并對其作用機制進行研究具有重要的意義.已有研究表明,在雌激素受體陽性的乳腺癌細胞中,雌激素受體通過和基因組中的增強子結合并激活相應區域產生一種新型非編碼RNA(增強子RNA)[2].增強子的激活對于鄰近雌激素靶基因的轉錄激活至關重要,然而可供靶向的“分子開關”鮮有報道,制約了相關研究的開展.
廈門大學藥學院劉文教授課題組在早期研究中,揭示了去甲基化酶JMJD6和其相互作用的溴結構域蛋白BRD4通過與特定增強子結合,遠程調控轉錄蛋白復合體的活性,進而調控鄰近編碼基因轉錄延伸的轉錄調控新模式[3];隨后還發現JMJD6蛋白的另一個功能,即其直接和RNA發生相互作用,作為一個RNA結合蛋白參與調控基因的可變剪接[4].在此基礎上,該課題組進一步對JMJD6蛋白在乳腺癌細胞中調控基因轉錄的功能和分子機制展開了深入研究.
2018年4月5日,劉文教授課題組在《Molecular Cell》上在線發表研究論文[5],報道了JMJD6蛋白調控雌激素受體依賴的增強子和編碼基因轉錄激活的相關分子機制的最新成果.研究發現在雌激素受體陽性的乳腺癌細胞中,JMJD6蛋白在雌激素誘導下能被特異性地招募到雌激素受體結合的活性增強子區域,并對增強子RNA及其鄰近的編碼基因轉錄激活起決定性作用;進一步的機制研究表明JMJD6和Mediator復合物中的MED12相互作用,并對MED12結合到活性增強子區域起調控作用(圖1).該研究證實了JMJD6蛋白對乳腺癌細胞生長和小鼠體內移植瘤形成起重要作用,并且這些功能與其酶活性密切相關,為乳腺癌防治提供了潛在的藥物靶點.
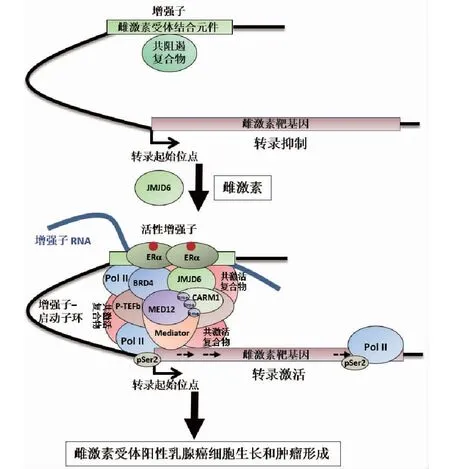
圖1 JMJD6蛋白調控雌激素誘導的增強子RNA及其鄰近靶基因轉錄激活
[1] YAGER J D,DAVIDSON N E.Estrogen carcinogenesis in breast cancer[J].N Engl J Med,2006,354(3):270-282.
[2] HERVOUET E,CARTRON P F,JOUVENOT M,et al.Epigenetic regulation of estrogen signaling in breast cancer[J].Epigenetics,2013,8(3):237-245.
[3] LIU W,MA Q,WONG K,et al.Brd4 and JMJD6-associated anti-pause enhancers in regulation of transcriptional pause release[J].Cell,2013,155(7):1581-1595.
[4] YI J,SHEN H F,QIU J S,et al.JMJD6 and U2AF65 co-regulate alternative splicing in both JMJD6 enzymatic activity dependent and independent manner[J].Nucleic Acids Res,2017,45(6):3503-3518.
[5] GAO W W,XIAO R Q,ZHANG W J,et al.JMJD6 licenses ERα-dependent enhancer and coding gene activation by modulating the recruitment of the CARM1/MED12 co-activator complex[J].Mol Cell,2018,70(2):340-357.

