右美托咪定對創傷應激障礙大鼠疼痛行為及認知功能的影響
張慶洪 馮宇峰 張麗娟
(廈門大學附屬第一醫院麻醉科,福建 廈門 361003)
創傷后應激障礙(PTSD)核心癥狀包括創傷性再體驗、回避與警覺性增高等〔1〕。經歷過創傷事件的人群有5%~15%發展為 PTSD,手術患者PTSD的發生率高達71%〔2〕。如何預防及降低手術患者PTSD一直是臨床探討的話題。右美托咪定是臨床常用的麻醉藥物,具有鎮靜、鎮痛、抗焦慮作用,還可減少術后躁動。右美托咪定可以通過減輕術中疼痛程度來降低PTSD的發生〔3〕。本研究通過建立PTSD動物模型的方法,觀察右美托咪定對創傷應激障礙大鼠疼痛行為及認知功能的影響。
1 材料與方法
1.1動物選擇及分組 雄性SD大鼠32只,購自廈門大學動物實驗中心(許可證號20160215),8~10周齡,體重250~350 g,本研究報請醫院動物倫理委員會批準。隨機分為對照組、PTSD組、20 μg右美托咪定組、40 μg右美托咪定組各8只。對照組、PTSD組按1 ml/kg腹腔注射生理鹽水,20 μg右美托咪組、40 μg右美托咪定組分別按20 μg/kg和40 μg/kg腹腔給予右美托咪定。生理鹽水和右美托咪定在PTSD模型建立后立即給予,連續用藥3 d。
1.2PTSD模型建立 應用條件性恐懼實驗分析系統建立PTSD模型,通過聲音、環境、電刺激來促使大鼠產生恐懼記憶,使條件性刺激控制恐懼反應,并通過僵直行為來檢測評定動物恐懼記憶是否形成及其嚴重程度〔4〕。對照組于第0、1、3天僅給予聲音刺激,PTSD組、右美托咪定組于第0、1、3天將大鼠放入斯金納箱(30 cm×26 cm×22 cm)中,適應5 min后給予30 s、5 kHz、75 db的聲音刺激,隨后在15 min內給予5次2 mA、2 s的電刺激,并在第7、14、21天將大鼠再次暴露于相同的環境中。
1.3觀察指標
1.3.1疼痛行為 分別于干預前、干預后1、3、7、14 d測定各組大鼠熱痛閾、機械痛閾值。熱縮足反射潛伏期(TWL):采用PL-200測痛儀,以Hargreaves 法記錄,將裝有大鼠的有機玻璃箱至于6 mm的玻璃板下,適應10 min后,用可移動光束、40%點光強度刺激照射足底中部,從照射開始至大鼠出現抬腿、舔足的時間為TWL。每只大鼠測定3次,間隔5 min,取其平均值。機械性縮足反射閾值(MWT):采用von Frey儀器測定機械痛,用單纖維絲探針在大鼠后爪趾面給予連續增加的壓力,大鼠出現抬足或舔足行為時測痛儀上顯示的數值為MWT,每只動物測定3次,每次刺激間隔5 min,取其平均值。
1.3.2認知功能 第27天進行水迷宮實驗,評估大鼠的空間學習記憶能力。水迷宮實驗在120 cm長、50 cm高的圓形水池中進行。將水池分為4個象限,在左上象限中放置直徑為10 cm、位于水面下1 cm的平臺。實驗過程中控制水溫在(25±1)℃,將大鼠面向池壁隨機從4個不同的象限放入水中,記錄大鼠找到平臺的潛伏期。若大鼠在60 s內未找到平臺,則將其放置在平臺上停留15 s。連續訓練4 d,第5天撤去平臺,記錄各組大鼠在目標象限探索時間百分比。
1.4統計學方法 采用SPSS20.0軟件進行方差分析及配對t檢驗。
2 結 果
2.1各組TWL比較 干預前各組大鼠TWL比較差異無統計學意義(P>0.05);干預后1、3、7、14 d,PTSD組、右美托咪定組TWL均明顯低于對照組(P<0.05),且40 μg右美托咪組>20 μg右美托咪定組>PTSD組,各組間差異有統計學意義(P<0.05),見表1。
2.2各組MWT比較 干預前各組MWT比較差異無統計學意義(P>0.05);干預后1、3、7、14 d,PTSD組、右美托咪定組MWT均明顯低于對照組(P<0.05),且40 μg右美托咪定組>20 μg右美托咪定組>PTSD組,各組間差異有統計學意義(P<0.05),見表2。

表1 各組TWL比較
與對照組比較:1)P<0.05;與PTSD組比較:2)P<0.05;與20 μg右美托咪定組比較:3)P<0.05

表2 各組MWT比較
2.3各組認知功能比較 與對照組比較,其余各組尋找平臺潛伏期時間延長,探索時間百分比明顯下降(P<0.05);且40 μg右美托咪組<20 μg右美托咪定組
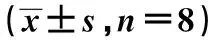
表3 各組認知功能比較
3 討 論
PTSD的特征為對創傷相關記憶增強產生的過度恐懼〔5〕。PTSD病程慢、治療效果差,藥物治療只能部分緩解PTSD癥狀〔6〕。PTSD的發生與創傷性事件密切相關,手術是一種創傷性事件,因此手術患者是PTSD的高發人群。右美托咪定通過抑制交感神經活性發揮鎮靜、鎮痛作用,可使患者血流動力學更穩定,降低術后躁動發生率〔7〕。
疼痛刺激是引起PTSD的原因之一。曹銘輝等〔8〕研究認為,右美托咪定能抑制背根神經節內p-ERK信號通路的激活,有效緩解神經病理性疼痛大鼠的痛覺過敏。張曉燕等〔9〕研究報道,幼鼠結腸降鈣素基因相關肽表達與內臟痛敏具有相關性;而湯翠菊等〔10〕則指出,右美托咪定能降低前炎性細胞因子表達,改善乳腺癌骨轉移大鼠疼痛行為。本研究結果表明,右美托咪定能有效緩解PTSD大鼠疼痛行為,且大劑量右美托咪定效果更明顯。
PTSD的顯著特征之一就是恐懼記憶的增強,當患者暴露于急性應激環境中時,出現交感-去甲腎上腺素系統的高反應性,增加PTSD的發生風險〔11〕。右美托咪定主要通過激動α2腎上腺素受體影響腦干藍斑核而干擾恐懼記憶的獲得〔12〕。陳丹丹等〔13〕文獻報道,右美托咪啶能夠有效緩解ICU患者鎮靜期應激反應,錢寶民等〔14〕認為,右美托咪定能減緩氯胺酮麻醉致幼齡大鼠海馬神經元凋亡。本研究與類似文獻報道〔15〕,結果一致提示右美托咪定能改善創傷應激大鼠的認知功能。
4 參考文獻
1Allen JP,Crawford EF,Kudler H.Nature and treatment of comorbid alcohol problems and post traumatic stress disorder among American Military Personnel and Veterans〔J〕.Alcohol Res,2016;38(1):133-40.
2詹 惟,潘鐵成,李建波,等.中老年創傷后應激障礙的相關因素〔J〕.中國老年學雜志,2012;32(21):4729-31.
3楊嬌嬌,孫曉茹,張 慧,等.右美托咪定對創傷后應激障礙大鼠焦慮狀態和認知功能的影響〔J〕.臨床麻醉學雜志,2015;31(8):797-800.
4Verma M,Bali A,Singh N,etal.Investigating the role of nisoldipine in foot-shock-induced post-traumatic stress disorder in mice〔J〕.Fundam Clin pharmacol,2016;30(2):128-36.
5Carletto S,Borghi M,Bertino G,etal.Treating post-traumatic stress disorder in patients with multiple sclerosis:a randomized controlled trial comparing the efficacy of eye movement desensitization and reprocessing and relaxation therapy〔J〕.Front Psychol,2016;7(1):526.
6康延海,蔣湘玲,郭 敏,等.海南省熱帶地區黎族與漢族PTSD患者血小板5-HT濃度的比較研究〔J〕.海南醫學院學報,2013;19(10):1345-8.
7張滿和,周秀敏,邢彥杰,等.右美托咪定對創傷性腦損傷大鼠海馬神經元自噬的影響〔J〕.中華麻醉學雜志,2015;35(3):373-6.
8曹銘輝,何惠燕,紀風濤,等.右美托咪定緩解神經病理性疼痛大鼠的痛覺過敏并抑制背根神經節內p-ERK信號通路的激活〔J〕.中華實驗外科雜志,2011;28(5):789-91,封4.
9張曉燕,吳 斌,楊燕珍,等.幼鼠結腸降鈣素基因相關肽表達與內臟痛敏的相關性〔J〕.中國疼痛醫學雜志,2011;17(4):237-41.
10湯翠菊,于世英,張 敏.鞘內注射p38MAPK抑制劑對乳腺癌骨轉移大鼠疼痛行為及前炎性細胞因子表達的影響〔J〕.中華實驗外科雜志,2008;25(1):27-9.
11Angel CM.Resilience,post-traumatic stress,and posttraumatic growth:Veterans′ and active duty military members′ coping trajectories following traumatic event exposure〔J〕.Nurse Educ Today,2016;47:57-60.
12丁旭東,鄭寧寧,曹巖巖,等.右美托咪啶預處理對大鼠缺氧缺血性腦損傷的影響〔J〕.中國現代神經疾病雜志,2014;14(5):427-32.
13陳丹丹,王 偉.右美托咪定聯合瑞芬太尼TCI對ICU患者鎮靜期應激反應的影響〔J〕.海南醫學院學報,2016;22(8):819-21.
14錢寶民,高清麗,房立峰,等.右美托咪定對創傷性腦損傷大鼠認知功能和海馬CA1區氧化應激的影響〔J〕.臨床麻醉學雜志,2015;31(8):801-5.
15Bentefour Y,Rakibi Y,Bennis M,etal.Paroxetine treatment,following behavioral suppression of PTSD-like symptoms in mice,prevents relapse by activating the infralimbic cortex〔J〕.Eur Neuropsyychopharmacol,2016;26(2):195-207.

