應用6σ方法評價河北省17家三級甲等醫院血細胞分析項目室內質量控制室間比對性能
王會茹, 李貴霞, 黃 晶, 吳 昊, 邸 陽
(1.河北省兒童醫院檢驗科,河北 石家莊 050031;
2.河北省臨床檢驗質量管理與控制中心,河北 石家莊 050031)
六西格瑪(six sigma,6σ)質量管理方法被用于客觀、定量地評價檢測質量時,可反映質量水平的高低,較高的西格瑪(sigma,σ)值意味著較低的分析誤差和較少的可疑檢測結果,能避免漏報可接受的檢測結果[1]。6σ的含義是檢測的缺陷率為百萬分之三點四,一般σ>4為“優”,3≤σ≤4為“良”,2≤σ<3為 “中”,σ<2為“差”[2]。室內質量控制(internal quality control,IQC)數據室間比對是臨床實驗室IQC的深入發展,參加比對的臨床實驗室使用同批號質控品 ,在相互比較中可了解自己和其他臨床實驗室的差距。本研究應用6σ方法對河北省17家三級甲等醫院血細胞分析項目IQC室間比對數據進行評價,以了解臨床實驗室血細胞分析項目的檢測性能,探討IQC室間比對的新方法,進而改進檢驗質量。
1 材料和方法
1.1 研究對象
收集河北省參加IQC室間比對的17家三級甲等醫院的臨床實驗室上報到河北省臨床檢驗質量管理與控制中心(簡稱質控中心)的數據。質控中心每月按照方法學分組的結果進行比對。血細胞分析項目包括:白細胞(white blood cell,WBC)計數、紅細胞(red blood cell,RBC)計數、血紅蛋白(hemoglobin,Hb)、血小板(platelet,PLT)計數。
1.2 儀器
XE 2100 血液分析儀和XE 5000血液分析儀(日本希森美康公司,9家); XN 9000血液分析儀(日本希森美康公司,2家); XT 4000i血液分析儀(日本希森美康公司,1家); LH 750血液分析儀和DXH 800血液分析儀(美國貝克曼公司,4家)。所用試劑均為原廠配套試劑。
1.3 方法
1.3.1 數據采集 2016年6—8月使用批號為77062和77063的質控品,2016年9—11月使用批號為77082和77083的質控品。17家三級甲等醫院的臨床實驗室使用同批號中值及高值2個水平的Bio-Rad血細胞分析質控品進行每日常規IQC并上報到質控中心,質控中心每月按照方法學分組的結果進行比對并及時反饋給臨床實驗室。WBC計數、RBC計數、PLT計數采用電阻抗法,Hb采用比色法。統計2個批次中值及高值2個水平質控品的質控數據。
1.3.2 不精密度估計 應用伯樂unity質控軟件,分別統計參加比對的臨床實驗室2個批次質控品的質控數據,計算和變異系數(coefficient of variation,CV)。2個批次中值和高值2個水平質控品分別得到2個CV,使用CV合并作為同水平質控品不精密度的估計值[3],公式為:
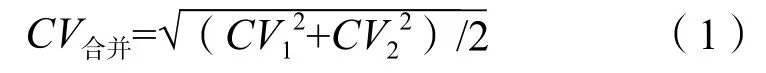
式中CV1和CV2分別代表同水平2個批次累積在控CV。
1.3.3 偏移(bias,Bias)的估計 用Excel軟件分別計算2個批次中值和高值質控品的Bias,公式為:
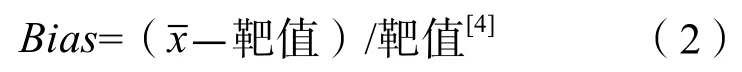
式中靶值為伯樂質控全球實驗室同儀器組對應批次累積2個批次中值和高值質控品分別得到2個Bias,使用Bias合并作為同水平Bias的估計值,公式為:
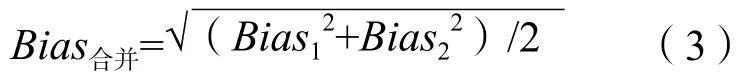
式中Bias1和Bias2分別代表同水平2個批次的Bias。
1.3.4 計算σ值 選用我國衛生行業標準 WS/T 406—2012《臨床血液學檢驗常規項目分析質量要求》[5]的允許總誤差(allowable total error,TEa)(WBC計數為15%,RBC計數為6%,Hb為6%,PLT計數為20%)分別計算2個水平的σ值,公式為:
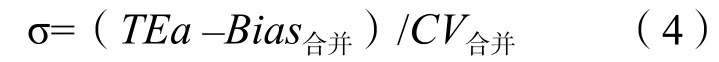
1.3.5 計算質量目標指數(quality goal index,QGI) 分別計算2個水平的QGI,公式為:
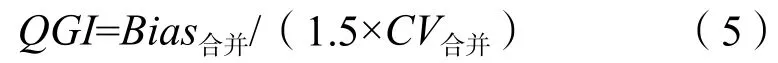
根據QGI查找性能不佳的主要原因。QGI<0.8,精密度超出范圍;0.8≤QGI≤1.2,提示準確度、精密度都不符合要求;QGI>1.2,準確度較差[6]。
2 結果
2.1 各臨床實驗室血細胞分析項目的σ值和QGI
各臨床實驗室血細胞分析項目中值和高值2個水平質控品的σ值和QGI見表1、表2。
2.2 各臨床實驗室血細胞分析項目中值和高值質控品σ值分布情況
各臨床實驗室血細胞分析項目中值和高值2個水平質控品≥6σ的實驗室分別占52.94%、47.06%,17.65%、17.65%,35.30%、23.53%和52.94%、58.82%;4≤σ<6的實驗室分別占35.30%、47.06%,29.41%、29.41%,47.05%、47.06%和35.30%、35.30%。見表3。
2.3 各臨床實驗室中值和高值質控品QGI分布情況
各臨床實驗室中值和高值質控品QGI分布情況見表4。
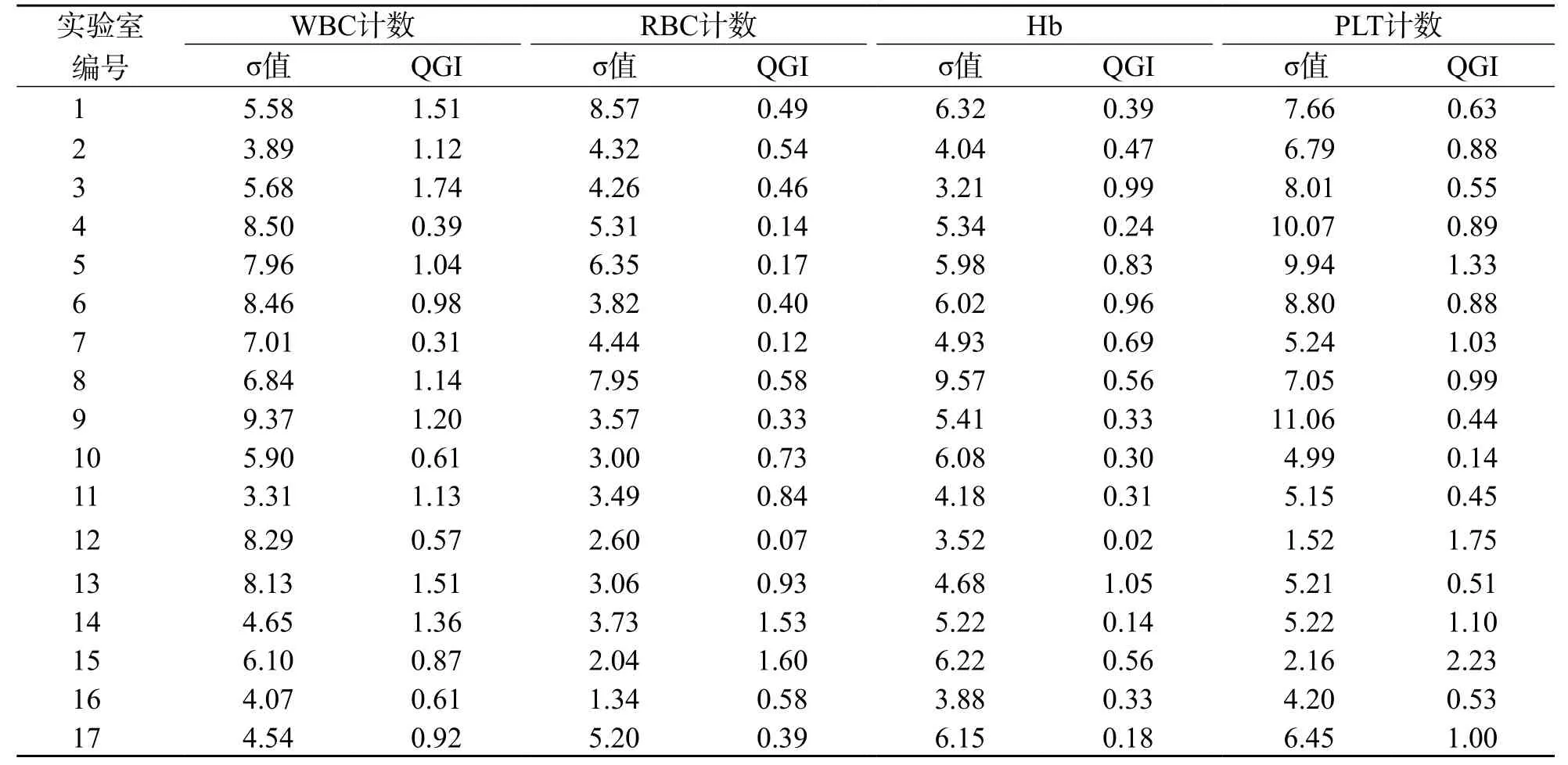
表1 各臨床實驗室血細胞分析項目中值質控品σ值和QGI
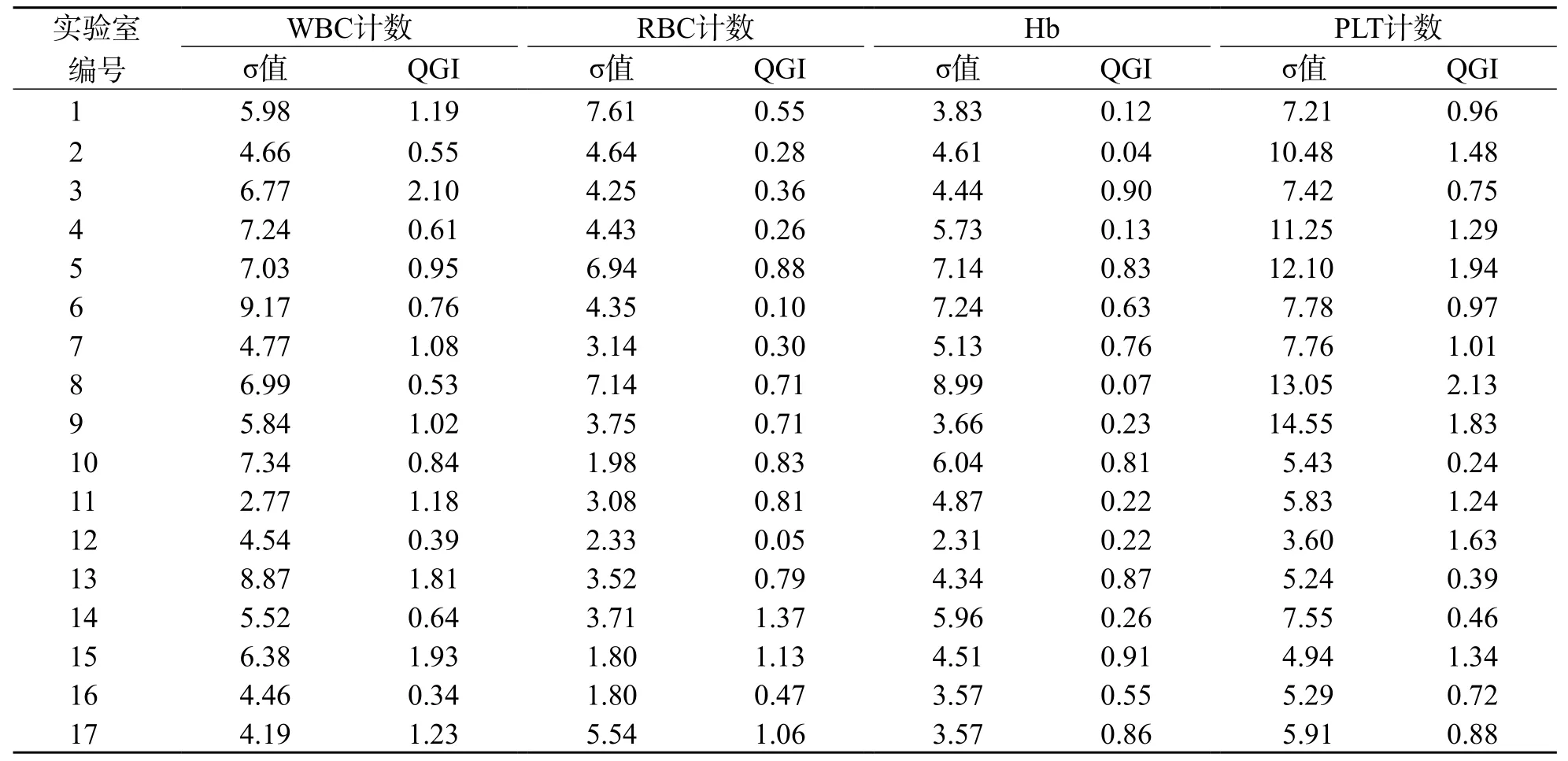
表2 各臨床實驗室血細胞分析項目高值質控品σ值和QGI
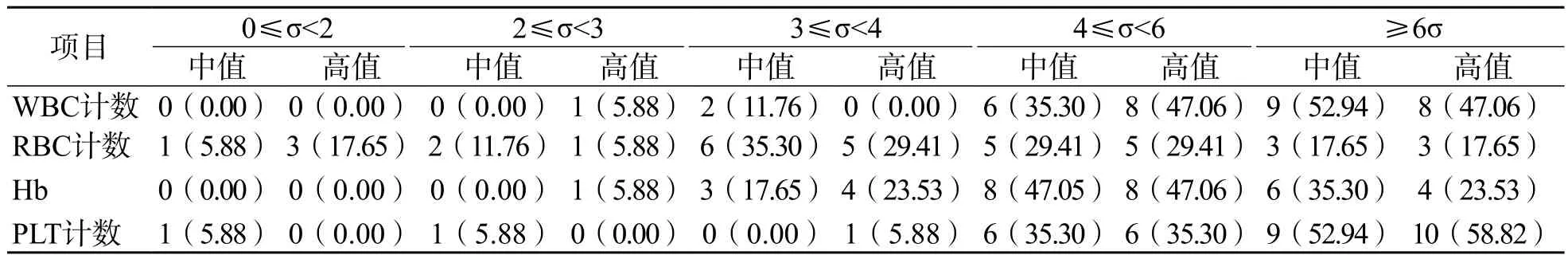
表3 各臨床實驗室中值及高值質控品σ值分布情況 [家(%)]

表4 各臨床實驗室中值及高值質控品QGI分布情況 [家(%)]
3 討論
6σ適用于任何一個可測量的數據結果,近年來在國際上發展迅速。6σ質量管理方法應用于臨床檢驗領域尚處于初級階段。在σ質量管理水平中,6σ被認為是“世界級水平”, 3σ被認為是日常性能的最低可接受水平[7]。6σ 可用于檢驗全過程的質量管理。檢驗中階段可通過測量變異的方法,利用公式σ=(TEa-Bias)/CV來評價實驗室檢測性能[8]。長期的質控數據可以確保更加穩定的不精密度估計值,如超過6個月或1年,其CV可代表更典型的長期分析質量[9],本研究收集2個批次的質控數據并統計CV合并,保證了不精密度估計結果具有代表性;Bias是由公式Bias=(-靶值)/靶值計算所得[4],靶值為伯樂質控全球實驗室同儀器組對應批次累積雖然有局限,但反映了臨床實驗室日常的真實情況;我國衛生行業標準 WS/T 406—2012《臨床血液學檢驗常規項目分析質量要求》基于個體內和個體間生物學變異,同時考慮我國當前可實現的分析質量水平而設定,適合于大部分臨床實驗室,選擇其作為TEa計算σ值具有統計意義。本研究統計各參加比對的臨床實驗室σ值的分布情況,各臨床實驗室血細胞分析項目中值和高值2個水平質控品≥6σ的實驗室分別占52.94%、47.06%,17.65%、17.65%,35.30%、23.53%和52.94%、58.82%;4≤σ<6的實驗室分別占35.30%、47.06%,29.41%、29.41%,47.05%、47.06%和35.30%、35.30%,說明按照我國衛生行業標準 WS/T 406—2012《臨床血液學檢驗常規項目分析質量要求》,河北省17家三級甲等醫院的臨床實驗室WBC計數、RBC計數、Hb、PLT計數項目的檢驗性能優良。
QGI應用于指導臨床實驗室決策優先改進精密度或準確度,從客觀上為臨床實驗室提供了質量改進的方向。QGI<0.8,提示精密度超出范圍,需優先改進;QGI>1.2,提示準確度較差,需優先改進;0.8≤QGI≤1.2,提示精密度和準確度均需改進[6]。本研究統計各臨床實驗室的QGI,WBC計數、RBC計數、Hb、PLT計數項目中值和高值2個水平質控品中 ,需優先改進精密度的實驗室分別占29.41%、41.18%,76.48%、64.71%,76.48%、64.71%和41.18%、29.41%;需優先改進準確度的實驗室分別占29.41%、23.53%,11.76%、5.88%,0.00%、0.00%和17.65%、47.06%。影響精密度和準確度的因素很多,包括儀器的校準及定期維護、試劑的保存及穩定性、質控品的穩定性、規范的操作流程、科學的管理制度等。臨床實驗室應使用配套檢測系統,制定標準化操作流程并對實驗室人員進行定期的規范化培訓。
6σ質量管理方法可用于檢驗全過程,提供統一而簡單的評價標準,便于臨床實驗室客觀、準確地評價自身的質量水平,及時發現問題,制定解決方案,實現質量改進[10]。目前,質控中心對臨床實驗室血細胞分析項目每月進行性能評價,缺乏長期質量性能觀察指標。本研究統計長期IQC數據并進行6σ、QGI分析,提出了長期質量評價的新思路。
[1] KINNS H,PITKIN S,HOUSLEY D,et al. Internal quality control:best practice [J]. J Clin Pathol,2013,66(12):1027-1032.
[2] WESTGARD J O, WESTGARD S A. The quality of laboratory testing today:an assessment of sigma metrics for analytic quality using performance data from prof i ciency testing surveys and the CLIA criteria for acceptable performance [J]. Am J Clin Pathol,2006,125(3):343-354.
[3] 中華人民共和國衛生部. WS/T 407—2012 醫療機構內定量檢驗結果的可比性驗證指南[S]. 北京:中國標準出版社,2013.
[4] 蔣敏,吳瑞珊,龐韜,等. 應用西格瑪進行血清ALT,Cr,Glu檢測項目的性能驗證[J]. 現代檢驗醫學雜志,2014,29(4):163-165.
[5] 中華人民共和國衛生部. WS/T 406—2012 臨床血液學檢驗常規項目分析質量要求[S]. 北京:中國標準出版社,2013.
[6] 陳先戀,何月娟,鄢仁晴,等. 應用6σ質量管理理論評價腫瘤標志物性能及質控方案選擇 [J]. 國際檢驗醫學雜志,2016,37(12):1607-1609.
[7] SINGH B, GOSWAMI B, GUPTA V K, et al.Application of sigma metrics for the assessment of quality assurance in clinical biochemistry laboratory in India:a pilot study [J] . Indian J Clin Biochem,2011,26(2):131-135.
[8] 王治國. 臨床檢驗質量控制技術[M]. 3版. 北京:人民衛生出版社,2014:554-567.
[9] 張路,王薇,王治國. 允許總誤差在西格瑪度量用于評價臨床化學檢測項目分析質量上的應用研究[J]. 檢驗醫學,2015,30(9):953-957.
[10] 張莉,張健,陸銀華. 不同允許總誤差在腫瘤標志物檢測性能評價與質量控制規則選擇中的應用[J].檢驗醫學,2010,25(5):382-384.

