調強放療聯合紫杉醇及奈達鉑同步化療治療食管癌的臨床療效分析
楊金旗,谷存銀
(陽谷縣人民醫院腫瘤科,山東 陽谷 252300)
食管癌是指發生在食管上皮組織的惡性腫瘤。放射治療屬于局部治療,通過放射能對癌腫部位進行照射,是食管癌的主要治療方法之一。調強放療是三維適形放療的一種特例,在這種放療中用計算機輔助的優化程序來計算出非均勻的強度分布,以便達到某種特殊的臨床目的[1-2]。紫杉醇是目前已發現的最優秀的天然抗癌藥物,是一個具有抗癌活性的二萜生物堿類化合物,生物活性廣泛,可用于治療多種癌癥[3]。奈達鉑是繼順鉑、卡鉑后第三代鉑類抗腫瘤藥物,抗癌譜廣[4]。本文聯合調強放療與紫杉醇、奈達鉑治療食管癌,現將結果報告如下。
1 資料與方法
1.1一般資料:選擇2015年1月~2016年8月在我院診斷治療的食管癌患者80例的臨床資料進行回顧性分析。納入標準:病理學證實為食管癌;有區域外淋巴結轉移或腫瘤侵及周圍組織,不能手術切除治療,無其他臟器轉移;功能評分≥70分;無嚴重其他系統疾病;臨床資料完整。排除標準:手術治療,完全梗阻,惡病質,有穿孔前征象或已經發生食管穿孔、縱隔炎等,中度以上貧血,發生遠處轉移。80例患者中40例采用調強治療設為對照組,40例采用調強放療聯合紫杉醇及奈達鉑同步化療設為觀察組。兩組患者一般資料比較,差異無統計學意義(P>0.05),具有可比性。見表1。本研究經過醫院醫學倫理委員會同意。
1.2治療方法:對照組采用調強放療治療。MIC動態調強,利用多葉準直器相對應的一對葉片的相對運動來實現對照射野內強度的調節,在每個照射野的照射過程中,由計算機系統按照調強計劃給出的數據進行控制,在各對葉片作變速運動時,加速器不停地以變化的劑量率出束,由此得到所要求的強度分布。患者體位固定,CT掃描,勾畫輪廓和靶區,確定照射中心,逆向計劃設計,計劃確認,QA驗證,輸入網絡,傳輸至加速器,執行治療。1次/d,5次/周。觀察組調強放療治療聯合紫杉醇及奈達鉑同步化療治療。調強放療同對照組。在化療第9天開始化療周期:第1天、第8天,紫杉醇80 mg/m2加入500 ml生理鹽水中,靜脈滴注,每次用藥前12小時及6小時口服地塞米松10 mg,治療前30分鐘給予20 mg苯海拉明肌內注射,100 mg雷尼替丁加250 ml生理鹽水靜脈滴注,預防并發癥。第2~4天奈達鉑40 mg/m2加入500 ml生理鹽水靜脈滴注。上述化療方案每4周重復1次。
表1兩組患者一般資料比較(n=40)

組別性別男 女平均年齡(x±s,歲)組織學(例)鱗癌 腺癌位置(例)頸段 胸上段 胸中段 胸下段觀察組381256.1±7.33915111212對照組361455.8±7.6382691312t/χ2值0.0520.1800.3460.331P值>0.05>0.05>0.05>0.05
1.3臨床療效及并發癥觀察:2個化療周期完成后評價臨床療效,根據情況分為完全緩解、部分緩解、穩定、進展、完全緩解加部分緩解為有效。每周復查1次血常規,每個療程結束后評估不良反應。放療相關不良反應包括急性放射性肺炎、放射性食管炎。化療毒性反應根據WHO抗腫瘤藥物不良反應分度標準進行。放療結束后6個月病變部位未出現病灶為局部控制,放療6個月后局部出現病灶為腫瘤復發。隨訪期間未發生局部未控制或復發為局部控制,比較兩組1年、2年及3年局部控制率,計算隨訪期間復發率及平均復發時間。比較兩組1年、2年及3年生存率。
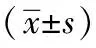
2 結果
2.1兩組近期臨床療效比較:見表2。觀察組治療結束后CR率及總有效率顯著高于對照組,差異有統計學意義(P<0.05)。
2.2兩組隨訪期間局部控制情況比較:見表3。隨訪1年時兩組局部控制率比較差異無統計學意義(P>0.05)。隨訪2年及3年時,觀察組局部控制率顯著高于對照組,差異有統計學意義(P<0.05)。隨訪3年,觀察組有27例復發,對照組33例復發,觀察組平均復發時間顯著較對照組長,差異有統計學意義(P<0.05)。
2.3兩組隨訪期間生存情況比較:見表4。隨訪1年及2年時兩組生存率比較差異無統計學意義(P>0.05)。隨訪3年,觀察組生存率高于對照組,差異有統計學意義(P<0.05)。
表2兩組近期臨床療效比較[例(%)]

組別例數CRPRSDPD總有效觀察組4026(65.0)10(25.0)3(7.5)1(2.5)36(90.0)對照組4015(37.5)12(30.0)9(22.5)4(10.0)27(67.5)χ2值5.0030.0632.4510.8534.781P值<0.05>0.05>0.05>0.05<0.05
表3兩組隨訪期間局部控制情況(n=40)

組別1年[例(%)]2年[例(%)]3年[例(%)]復發[例(%)]平均復發時間(x±s,月)觀察組33(82.5)28(70.0)15(37.5)27(67.5)18.9±5.5對照組27(67.5)17(42.5)5(12.5)33(82.5)15.1±4.8t/χ2值1.3745.0795.4005.4003.292P值>0.05<0.05<0.05<0.05<0.05
表4兩組生存率比較[例(%)]

組別例數第1年第2年第3年觀察組4035(87.5)31(77.5)18(45.0)對照組4031(77.5)25(62.5)6(15.0)χ2值0.2061.4887.202P值>0.05>0.05<0.05
2.4兩組不良反應比較:觀察組Ⅰ~Ⅱ級放射性食管炎33例,Ⅲ級7例,對照組Ⅰ~Ⅱ級為31例,Ⅲ級9例,兩組比較差異無統計學意義(P>0.05)。觀察組的化療相關并發癥主要表現為血細胞減少及惡心、嘔吐,以Ⅰ~Ⅱ級為主,無Ⅳ級不良反應發生。Ⅰ~Ⅱ度白細胞減少33例,Ⅲ度7例,Ⅰ~Ⅱ度血小板減少9例,Ⅲ度2例,Ⅰ~Ⅱ度惡心、嘔吐25例,Ⅲ度4例。
3 討論
食管癌是指原發于食管黏膜上皮的惡性腫瘤,男性好發,高發年齡為50~65歲。食管癌有明顯的地域性分布,是我國常見的惡性腫瘤之一。食管癌的病因包括不良的飲食及生活習慣、營養缺乏、亞硝胺類化合物、真菌毒素、食管慢性炎性反應、遺傳等因素。食管癌的治療一般采用綜合治療,早期食管癌首選手術治療,因內科疾病不能手術或患者拒絕手術時,可行根治性放射治療,對部分局部晚期,單純手術切除困難者可先行術前放射治療。中晚期患者應選擇以放射治療為主的綜合治療。頸段及胸上段食管癌首選根治性放射治療,胸中段食管癌根據患者具體情況選擇手術或放射治療,胸下段食管癌應首選手術,輔以術后綜合治療。根治性放射治療的適應證包括全身情況中等以上,KPS評分≥70分,可進流食或半流食,無聲帶麻痹或遠處轉移,病變長度不超過8 cm,無明顯的外侵征象,無嚴重內科相關疾病,拒絕手術者,食管癌術后局部復發或縱隔淋巴結轉移,術后有腫瘤殘余者。本次納入研究的患者均符合根治性放射治療的適應證。
放射治療是治療惡性腫瘤的三大重要手段之一,大約有60%~70%的惡性腫瘤患者需要接受放射治療。放射治療使用的都是強度幾乎一致的射線,而腫瘤本身的厚度是不均一的,因此造成腫瘤內部劑量分布不均。為了實現腫瘤內部劑量均勻,就必須對射野內的射線強度進行調整,因此調強概念被提出。它是一種思維放射治療技術,在三維放療技術基礎上加入了時間因數的概念[5-6]。這個技術要求把一束射線分解為幾百束細小的射線,分別調節每一束射線的強度,射線以一種在時間和空間上變化的復雜形式進行照射。調強放療通過改變靶區內的射線強度,使靶區內的任何一點都能得到理想均勻的劑量,同時將要害器官所受劑量限制在可耐受范圍內,使緊鄰靶區的正常組織受量降到最低。調強放療能夠減少正常組織15%~20%的劑量,同時增加靶區腫瘤劑量20%~40%[7-8]。在本次研究中,兩組均進行了調強放療,對照組單純采用調強放療治療,其近期有效率也達到了67.5%。并且兩組與放療有關的不良反應主要是Ⅰ~Ⅱ級食管炎,無其他嚴重放射相關不良反應發生,說明調強放療的照射相關不良反應相對較輕,患者可耐受。
紫杉醇是紅豆杉屬植物中的一種復雜的次生代謝產物,是一種新型的抗微管藥物,通過促進微管蛋白聚合抑制解聚,保持微管蛋白穩定,抑制細胞有絲分裂[9]。體外試驗證明紫杉醇具有顯著的放射增敏作用,可能是使細胞中止于對放療敏感的G2和M期有關。研究顯示,紫杉微管上,不與未結合的微管蛋白二聚體反應。細胞接觸紫杉醇后在細胞內積累大量的微管,這些微管的積累干擾了細胞的各種功能,特別是使細胞分裂停止于有絲分裂期,阻斷了細胞的正常分裂。奈達鉑是第二代鉑類抗腫瘤藥物[10-11]。在常見腫瘤中,奈達鉑對食管癌、頭頸部癌癥、小細胞肺癌和子宮頸癌的緩解率超過40%。目前證實對食管癌有效的化療藥物不多,多數藥物都是建立在對鱗癌有效的基礎上。順鉑是療效最確切的藥物之一,單藥有效率在20%以上,老藥包括5-FU、絲裂霉素、順鉑、博來霉素、甲氨蝶呤、米多蒽醌、阿霉素和長春地辛等,新藥包括紫杉醇、多西他賽、長春瑞濱、奈達鉑等。奈達鉑寫入中國抗癌協會食管癌專業委員會《食管癌規范化診治指南》(2010版)。鉑類抗癌藥物的抗癌機制可分為4個步驟:跨膜轉運,水合解離,靶向遷移,作用于DNA,引起DNA復制障礙,從而抑制癌細胞的分裂[12-13]。目前國內常用的鉑類抗癌藥物共有5種,第一代順鉑、第二代卡波及奈達鉑、第三代奧沙利鉑、洛鉑,以上五種藥物作用機制類似。奈達鉑的溶解度大約是順鉑的10倍,作用比順鉑好,腎毒性較低,其不良反應主要表現在血液毒性[14-15]。本次研究中,觀察組采用調強放療聯合紫杉醇及奈達鉑同步化療治療食管癌,患者近期療效、遠期療效、局部控制率均優于單純調強化療患者。觀察組患者化療相關不良反應主要是血細胞減少,惡心、嘔吐,主要表現在Ⅰ~Ⅱ度,少部分患者為Ⅲ度,無Ⅳ度不良反應發生,在患者可耐受范圍內。
綜上所述,食管癌患者采用調強放療聯合紫杉醇及奈達鉑同步化療治療能夠顯著提高近期、遠期臨床療效,延長生存率。

