睪酮對慢性腎功能衰竭大鼠腎性貧血的影響及其作用機制
謝萬祥,黃金平
(湖北醫藥學院附屬隨州醫院腎內科,湖北 隨州 441300)
腎性貧血是慢性腎臟病(chronic kidney disease,CKD)最常見的并發癥之一,幾乎所有CKD 5期的患者均伴有不同程度的貧血。腎性貧血不僅嚴重影響尿毒癥患者生存質量,而且增加心腦血管事件的發病率,進而影響CKD患者預后[1]。腎性貧血的主要原因是腎臟促紅細胞生成素(EPO)不足和造血原料缺乏[2]。隨著重組人促紅細胞生成素(rh EPO)的問世,大大改善了腎性貧血的糾正效果,幾乎終結了腎性貧血患者需要依賴異體輸血維持正常生理機能需求的治療方案。
但隨著rhEPO的普及,相關研究表明:約25%的透析患者使用常規劑量的EPO難以糾正貧血或需加大EPO的使用劑量(>200 IU·kg-1·week-1)才能維持目標血紅蛋白值,這一類患者稱為EPO抵抗[3]。發生EPO抵抗的原因復雜且至今未明,自身體內EPO抗體的形成、骨髓紅系祖細胞表面的 EPO 受體(EPO receptor)功能紊亂,以及體內微炎癥狀態、鐵劑的缺乏均參與其中。而睪酮作為雄激素的主要成分,其受體廣泛分布于生殖系統、肌肉、皮膚、骨骼、心血管系統等。就造血而言,睪酮可通過刺激特定的核受體單元提高紅細胞增殖和集落形成單位刺激紅細胞的生成[4],對再障性貧血,頑固性貧血具有一定療效,但國內外尚未見睪酮對腎性貧血影響及其作用機制的研究。基于此,本研究自2015年10月至2016年10月觀察睪酮干預慢性腎功能衰竭大鼠后貧血糾正的療效,旨在發現治療腎性貧血的新途徑。
1 材料與方法
1.1材料
1.1.1儀器 Olympus公司雙量程電子天平(北京賽多利斯有限公司),電子恒溫水浴鍋(金壇市恒磊實驗儀器廠),低溫超速離心機(美國Beckman公司),垂直電泳槽(北京六一儀器廠),移液器(德國Eppendorf Easypet公司),全自動血液分析儀(美國Beckman公司)。
1.1.2藥品與試劑 丙酸睪酮注射液(上海通用藥業股份有限公司),蛋白裂解液(美國BD, Biosciences),聚丙烯酰胺(SDS-PAGE)預制膠(Novex,san diego,CA),EPO抗體(美國R&D Systems公司),Marker(美國Fermentas公司),anti-hepcidin(美國Bioss公司),Hepcidin-Elisa(瑞士Bachen公司)。
1.1.3細胞與動物 24只SPF級Wistar雄性大鼠,質量200~220 g,購于武漢大學實驗動物中心,動物許可證:HBDW 201504-3。
1.2方法
1.2.1模型制備及分組 24只雄性大鼠經適應性飼養1周后,隨機單位組設計組法分為對照組(NC)、正常大鼠睪酮干預組(NT)、慢性腎功能衰竭大鼠組(CD)、慢性腎功能衰竭大鼠睪酮治療組(CT)。每組6只。CD組、CT組大鼠給予腺嘌呤飼料(腺嘌呤含量0.75%),NC組、NT組給予標準顆粒飼料。4周后CD組,CT組大鼠尾靜脈采血檢測血肌酐、血尿素氮判斷是否造模成功。造模成功后,NT組、CT組大鼠給予皮下注射丙酸睪酮(1 mg/100 μL芝麻油,每周2次),NC組、CK組給予皮下注射芝麻油100 μL,每周2次,治療4周。
1.2.2標本收集及研究方法 干預4周后麻醉處死大鼠,心臟采血,留取血標本,留取腎臟、肝臟及十二指腸保存于-80 ℃冰箱用于下一步檢測。
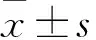
2 結果
2.1大鼠一般情況及貧血相關指標比較四組大鼠體質量的基線水平差異無統計學意義,使用嘌呤飼料造模后,CD組、CT組大鼠生長較NC組NT組遲緩,出現體質量減輕,活動減少,精神萎靡,動作遲緩,毛發粗糙進食飲水及尿量明顯增多等癥狀,所有大鼠均未見死亡。處死大鼠血液檢測顯示:與正常組大鼠相比, CD組大鼠血紅蛋白(Hb)紅細胞計數(RBC),血清鐵(SI),總鐵蛋白結合力(TIBC)明顯下降,呈現小細胞低色素貧血,缺鐵性貧血,使用睪酮治療后,上述指標均顯著提升,大鼠貧血狀態糾正。見表1。
2.2大鼠腎臟病理NC組、NT組腎臟病理未見明顯異常,CD組可見輕到中度腎臟損害,表現為較正常組相比可見腎小管上皮細胞肥大、炎性細胞浸潤、腎小管管腔擴張且不規則等表現,而CT組病變表現輕于CD組,僅見炎癥細胞浸潤。見圖1。
2.3大鼠腎臟組織中EPO表達NC組、 NT組、 CD組、CT組大鼠腎臟中EPO的水平分別為(184.321±27.679)、(188.582±15.374)、(142.701±12.249)、(166.322±21.580) μg·g-1,CD組大鼠腎臟EPO表達顯著低于正常大鼠,經丙酸睪酮治療后EPO表達明顯增加(P=0.013),差異有統計學意義。免疫蛋白印跡顯示:與對照組大鼠相比,CD組大鼠腎臟組織中EPO表達顯著減少,使用睪酮干預后,NT組較NC組相比EPO表達變化不顯著,但CT組較CD組大鼠腎臟內EPO表達水平明顯增多。見圖2。

組別鼠數Hb/g·L-1RBC/106·mm-2HTC/%SI/mg·L-1TIBC/mg·L-1NC組6131.2±15.56.23±1.2241.33±5.724.82±1.038.27±2.33NT組6142.5±21.76.98±1.3747.23±5.895.36±1.228.50±3.21CD組6106.1±23.44.95±2.1426.31±6.283.57±1.145.87±3.04CT組6121.9±19.6a5.33±2.26a32.30±7.64a4.13±1.60a6.62±3.36aF值678.20266.53178.62156.23231.54P值0.000.000.000.000.00
注:與CD組比較,aP<0.05
2.4大鼠肝臟組織中鐵調素的表達免疫蛋白印跡顯示:與對照組大鼠相比,CD組大鼠肝臟組織中鐵調素表達顯著顯著增多,使用睪酮干預后,NT組較NC組,CT組較CD組大鼠肝臟內鐵調素表達水平明顯下調。見圖3。

圖3 免疫蛋白印跡顯示4組大鼠肝臟組織中鐵調素表達情況
3 討論
腎性貧血是慢性腎衰竭患者最常見的并發癥,隨著慢性腎衰竭的進展,貧血發生率,嚴重程度逐步上升。一項納入12 077例成年慢性腎臟病患者的研究[5]表明,在美國CKD1期患者腎性貧血的發病率為8.4%,而同人群CKD5期患者腎性貧血的發病率達53.4%。腎性貧血不僅嚴重影響患者生活質量,而且增加心血管疾病的發生率和死亡率。
腎性貧血的主要原因是EPO不足和造血原料(鐵)缺乏[5]。EPO是哺乳動物調節紅細胞生成的主要因子,90%由腎臟合成,促進骨髓紅系祖細胞生長、增殖、分化和成熟[6]。隨著慢性腎衰竭的進展,腎單位逐漸減少導致EPO合成減少。于此同時腎衰竭患者體內鐵代謝發生紊亂,相關研究表明,透析患者每年經慢性出血、透析丟失等途徑損失的鐵達1~3 g[7]。維持全身鐵平衡最主要的激素是鐵調素(hepcidin),鐵調素由肝臟合成入血,通過結合鐵輸出細胞上膜鐵轉運蛋白,進而導致鐵既不能從小腸上皮細胞轉運入血,也不能從網狀內皮系統中釋放而被再利用,最終抑制鐵劑的吸收[8]。
正常人體內睪酮主要由男性睪丸或女性卵巢分泌,全身多器官組織均存在雄激素受體。Jill等[9]研究表明,在老年貧血患者中,血紅蛋白水平下降與睪酮下降水平相一致。而對于腎性貧血的患者,即使調整EPO達相同水平,低睪酮水平狀態下腎性貧血仍不能糾正。近年來雄激素及其相關衍生物如司坦唑醇、十一酸睪酮已經開始用于治療慢性再生障礙性貧血等一些血液系統疾病,并取得了較好的療效。那么不由假設,提升慢性腎衰竭患者體內睪酮水平是否可以糾正腎性貧血?由此我們課題組設計了該實驗。
本次實驗結果證實:睪酮可提升慢性腎臟病腎性貧血大鼠體內血清鐵含量,升高血紅蛋白值,糾正貧血。同時可降低大鼠肝臟內鐵調素水平,升高腎臟內EPO水平。睪酮糾正貧血的機制可能與降低鐵調素進而增加腸道鐵的吸收與利用,同時升高EPO增加紅細胞合成相關。
迄今為止國內外尚未見睪酮對腎性貧血影響及其作用機制的研究,因此本研究使用腺嘌呤誘導CRF大鼠模型,研究睪酮對腎性貧血的影響,并對肝腎組織中鐵調素,EPO表達水平進行測定,旨在闡明睪酮治療腎性貧血的可能機制,具備一定創新性,為腎性貧血的治療打開新的思路。但本研究尚未研究不同性別大鼠對睪酮干預的影響,及使用睪酮治療后相關副作用等一些重要的問題,擬在今后的實驗中進一步研究。

注:NC為對照組;NT為正常大鼠睪酮干預組;CD為慢性腎功能衰竭大鼠組;CT為慢性腎功能衰竭大鼠睪酮治療組
圖1四組大鼠腎臟病理典型圖片(HE×400)

