江蘇省學業水平測試“實驗計算綜合題”試題評析
王建華
江蘇
江蘇省化學學業水平測試中實驗計算綜合題模塊(第26題),題型傳統,但考查角度靈活,有創新,近年來主要以實驗流程為載體考查實驗技能、信息素養、數據處理和運用化學原理解決實際問題的能力。本文僅對該題近九年的分析和歸納,從中能發現一些命題規律,找出一些答題方法,提出對此題的復習方向。
一、2009年至2017年實驗計算綜合題考查統計
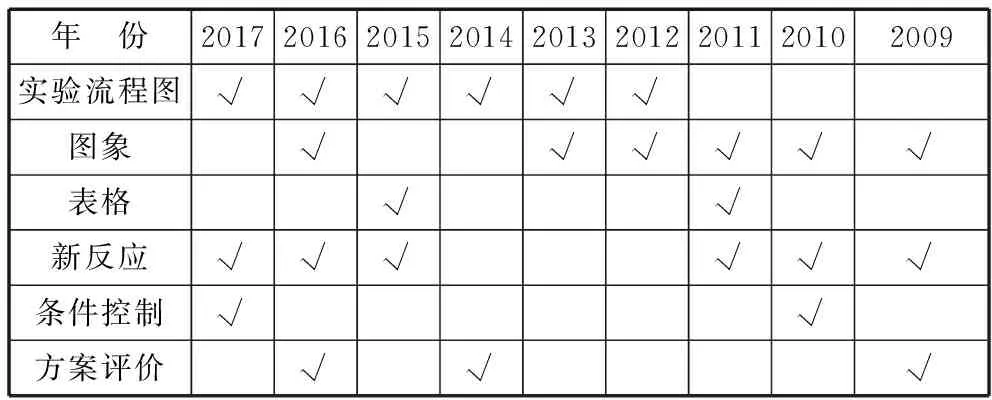
年 份201720162015201420132012201120102009實驗流程圖√√√√√√圖象√√√√√√表格√√新反應√√√√√√條件控制√√方案評價√√√
基于以上分析,教師應著力培養學生以下基本能力:
(1)信息加工能力:流程解讀,化學曲線解讀,實驗數據解讀,陌生轉化關系解讀;
(2)實驗探究能力:實驗目的分析,實驗條件控制,實驗方案評價;
(3)證據推理能力:依據反應規律推理,依據化學圖表推理,依據實驗數據推理。
二、實驗條件控制
從近幾年試題考查來看,實驗條件的控制多數為溫度、pH和投料控制,答題的一般思路如下:
1.溫度控制
溫度可以影響反應速率,反應程度(浸出率),副反應,溶解度、揮發等方面,答題時多數從下面幾個方面入手。
(1)溫度控制在××℃以下。答題一般為溫度過高,會××。
(2)溫度控制在××℃以上。答題一般為溫度過低,會××。
(3)溫度控制在××℃~××℃。答題一般為溫度過高,會××,溫度過低,會××。
(4)溫度控制的方法:反應體系插入溫度計,水浴[熱水浴、沸水浴、冰(冷)水浴],試劑加入速率(放熱顯著的反應)。
2.pH控制
pH一般影響反應速率,副反應,沉淀,促進或抑制物質的溶解(吸收)等方面,答題時多數從下面幾個方面入手。
(1)加入××(試劑),調節pH至××。答題一般為使××離子完全沉淀。
(2)加入××(試劑),調節pH至××~××。答題一般為使××離子完全沉淀,同時保證××離子不沉淀。
(3)pH控制的方法:加入酸、堿、氧化物、碳酸鹽等。
3.投料控制
(1)試劑過量。答題一般為使××充分反應;充分吸收××(氣體)、充分溶解××(固體);提高××(物質或元素)浸出率。
(2)固體粉碎/液體噴霧。答題一般為增大接觸面積,加快反應速率;增大接觸面積,使××充分反應(溶解、轉化)。
(3)氣體流量/流向。控制流量,答題一般為使××充分反應(溶解、吸收);采用逆流,答題一般為延長××與××接觸時間,使××反應(溶解、吸收、冷卻)。


分析:由信息可知,反應溫度不能高,所以要采用控制溫度較低的方法,用冷水浴較好。
答案:將丙裝置浸在盛有冷水的水槽中
三、物質的除雜、分離
1.關鍵詞——沉淀
沉淀是否完全的判斷:靜置,往上層清液中滴加××(沉淀劑),若沒有沉淀生成,則已沉淀完全。
沉淀洗滌的方法:向沉淀中加水至浸沒沉淀,等水流出后,重復2~3次。
冰水洗滌的作用:降低沉淀或晶體在水中的溶解量。
揮發性的有機溶劑(例如酒精、乙醚)洗滌的作用:既能降低沉淀或晶體在水中的溶解量,又能快速干燥。
檢驗沉淀是否洗凈的方法:取最后一次洗滌液少許于試管中,加入××溶液,若無沉淀生成,說明沉淀已洗滌干凈。
2.關鍵詞——結晶
緩升型(NaCl)——蒸發結晶,趁熱過濾,洗滌,干燥;
陡升型(KNO3)——蒸發濃縮,冷卻結晶,過濾,洗滌,干燥;
結晶水合物——蒸發濃縮,冷卻結晶,過濾,洗滌,干燥。
3.關鍵詞——檢驗
答題順序為操作→現象→結論。
答題一般為取待檢液少許于試管中,滴加××,產生××現象,說明試樣中含××。
例2某硫酸廠產生的燒渣(主要含Fe2O3、FeO,還有一定量的SiO2)可用于制備FeCO3,其流程如下:
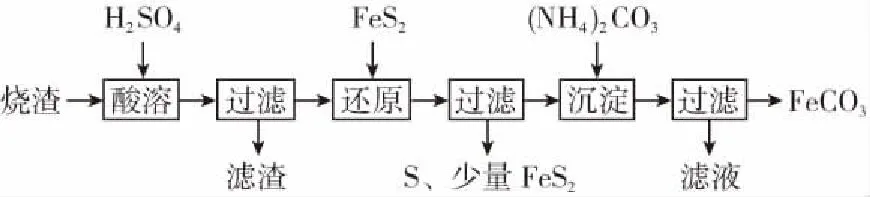
已知:“還原”時,FeS2與H2SO4不反應,Fe3+通過反應Ⅰ、Ⅱ被還原,其中反應Ⅰ如下:

(1)加入FeS2還原后,檢驗Fe3+是否反應完全的試劑為________。
(2)所得FeCO3需充分洗滌,檢驗是否洗凈的方法是___________________。“沉淀”時,pH不宜過高,否則制備的FeCO3中可能混有的雜質是 ________。

答案:(1)KSCN溶液 (2)取最后一次洗滌液少許放入試管中,滴加稀鹽酸,待無明顯現象后,再滴加BaCl2溶液,若無白色沉淀生成,表明已洗滌干凈,反之,則說明沒洗干凈 Fe(OH)3
四、陌生方程式的書寫
一般書寫步驟如下:
(1)根據流程信息寫出關鍵性的反應物或生成物的化學式;
(2)根據守恒(電子、電荷、原子)完成方程式配平;
(3)完善書寫細節(如反應條件、物質狀態等)。
例3鐵黑(Fe3O4)是常見的鐵系顏料。一種制取鐵黑的實驗流程如下圖所示:

制取鐵黑的反應原理可表示為

(1)加入氨水調節pH至7~9時,發生反應的離子方程式為___________________。
分析:在“調節pH至7~9”這個環節注意物質的流入(FeSO4、NH3·H2O),所以反應物自然就確定了。

五、化學計算類型歸納
1.定量的反應物與變量的混合物計算(讀表格)
例4某氮肥硫酸銨中混有硫酸氫銨。為測定該氮肥的含氮量,一化學研究性學習小組取一定量氮肥樣品,研磨使其混合均勻,備用。已知:


稱取不同質量的上述樣品分別與40.00mL相同濃度的氫氧化鈉溶液混合,完全溶解后,加熱充分反應(此溫度下銨鹽不分解),并使生成的氨氣全部被稀硫酸吸收,測得氨氣的質量。部分實驗數據如下:

氫氧化鈉溶液體積/mL40.00樣品質量/g7.75015.5023.25氨氣質量/g1.8701.8701.700
請計算(計算結果保留兩位小數):
①樣品中氮元素的質量分數是___________%。
②所用氫氧化鈉溶液的物質的量濃度為___________mol/L。
③若樣品質量為31.00 g,則生成氨氣的質量為___________g。
分析:由表中數據可知,第一組實驗中NaOH明顯過量,第三組實驗中NaOH明顯不足。要計算樣品中的有關組成,則要讓樣品完全反應,故以第一組實驗計算;要計算有關NaOH,則要讓NaOH完全反應,故以第三組實驗計算。

②以第一組實驗,計算出樣品中NH4HSO4和(NH4)2SO4的組成比例。設樣品中NH4HSO4物質的量為xmol、(NH4)2SO4物質的量為ymol,根據關系式:NH4HSO4~NH3和(NH4)2SO4~2NH3,列方程組:
解得:x=0.01 moly=0.05 mol
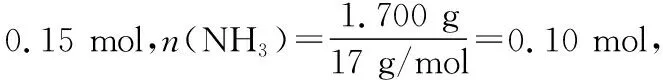
先發生:

0.03 mol 0.03 mol 0.015 mol

0.10 mol 0.10 mol

③若樣品質量為31.00 g(正好是第一組的4倍),可知NH4HSO4物質的量為0.04 mol,(NH4)2SO4物質的量為0.20 mol,NaOH量更不足了。據下列兩個反應:
先發生:

0.04 mol 0.04 mol 0.002 mol
后發生:

(0.13-0.04) mol 0.09 mol
所以m(NH3)=0.09 mol×17 g/mol=1.53 g
答案:①19.87%;②3.25 mol/L;③1.53 g
點評:解答這種類型題目時要讀懂表格上的數據,確定哪一組實驗數據中哪一反應物是否過量。若要求某一反應物的組成時,一定要讓該反應物全部反應完,才能計算。
2.方案評價類計算(含滴定)
例5國家標準規定產品中Na2SO3的質量分數≥97.0%為優等品,質量分數≥93.0%為一等品。為了確定實驗所得產品的等級,研究小組采用了兩種方法進行測定。
①方法Ⅰ:稱取2.570 g產品,用蒸餾水溶解,加入足量的雙氧水使Na2SO3完全氧化生成Na2SO4,再加入過量的BaCl2溶液,所得沉淀經過濾、洗滌、干燥后稱重,質量為4.660 g,通過計算確定產品中Na2SO3的質量分數(寫出計算過程)。
②方法Ⅱ:稱取1.326 g產品,配成100 mL溶液。取25.00 mL該溶液,滴加0.125 0 mol·L-1I2溶液,恰好使Na2SO3完全氧化生成Na2SO4時,消耗I2溶液20.00 mL。通過計算確定產品中Na2SO3的質量分數(寫出計算過程)。
③判斷Na2SO3產品的等級,并說明理由。

答案:①據比例Na2SO3~Na2SO4~BaSO4,2.570 g產品中
m(Na2SO3)=2.000×10-2mol×126 g/mol=2.520 g

②據比例Na2SO3~I2,25.00 mL溶液中
n(Na2SO3)=n(I2)=0.125 0 mol·L-1×0.020 L=2.500×10-3mol
1.326 g產品中Na2SO3的質量
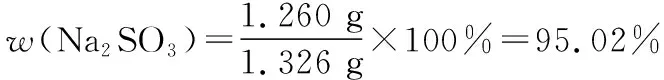

點評:這種類型題目的特點是方案評價,解題的特點是理解題意,結合滴定反應方程式,列出反應比例,進而計算。類似的方案評價還有2014年的學測最后一題。


