Ag/Cu3(BTC)2復合催化劑的制備及其NH3-SCR催化性能
石 勇,牛丹陽,武卓敏,劉震震,肇啟東,熊 巍,李新勇 (大連理工大學環境學院工業生態與環境工程教育部重點實驗室和精細化工國家重點實驗室,遼寧 大連 116024)
大氣中的 NOx主要來源于煤、石油、天然氣等化石燃料的燃燒[1],其過量排放會對生態環境及人類健康帶來巨大的影響和危害.因此氮氧化物的脫硝處理問題成為環境保護領域關注的重點[2-3].以 NH3為還原劑的選擇性催化還原法(Selective Catalytic Reduction by NH3, NH3-SCR)以其處理效率高、無二次污染等優點[4-5]成為目前工業上治理氮氧化物污染廣泛采用的方法.其中在商業上應用廣泛的脫硝催化劑為 V2O5-WO3/TiO2[6-7],但該種催化劑運行中存在反應溫度高,溫度窗口窄,釩具有毒性等諸多不足[8-9].因此尋求高催化活性、多活性位點及無毒的催化劑成為脫硝領域的研究熱點.
金屬框架化合物(MOF)是近年來新興的納米多孔功能材料,其具有豐富的孔道結構及巨大的比表面積等特征,成為熱門的吸附和催化劑載體材料.Cu3(BTC)2是目前研究較為廣泛的一種MOF材料,其具有比表面積大,孔道結構排列規則有序,可調控尺寸且物化性質穩定等優點,并且在其骨架結構中分布大量配位不飽和金屬活性位點,非常有利于氣體小分子的吸附.這些特殊的優點使 Cu3(BTC)2被廣泛應用到氣體儲存、分離和催化等領域[10-13].在本課題組先前的研究報導中,證明該材料對低溫 NH3-SCR反應中有較好的催化效果[14].
此外,有關MOFs材料負載貴金屬納米顆粒的催化性能研究日益得到關注,已有報導將 Ru/MOF[15-16]、Pd/MOF[17-18]、Pt/MOF[19-20]和 Au/MOF[21-22]等負載金屬納米粒的MOFs催化劑,均表現出增強的催化活性.這是由于MOFs材料可以提供有效的封閉空孔道間從而促成金屬納米顆粒的成核過程,從而將貴金屬納米顆粒高度分散到其表面或孔道中,成功實現貴金屬納米顆粒的負載,從而進一步提高MOFs材料的吸附和催化效率.這是由于MOFs材料有限的孔道尺寸可以限制金屬顆粒的大小,能有效地避免貴金屬納米顆粒的團聚現象,效果如圖1所示.
針對 Cu3(BTC)2的晶體結構分析表明,其軸向的兩個銅離子距離為 0.8nm,這個距離有利于納米銀顆粒在 Cu3(BTC)2上的分散[23].Zhao等[24]利用濕含浸法合成出了 5%Ag/Cu3(BTC)2復合催化劑并將其應用在CO氧化過程中,與Cu3(BTC)2催化劑相比,不僅降低了催化劑的起活溫度同時提高了催化效率.夏卓英等[25]通過絡合浸漬法成功將 Ag納米顆粒負載在氧化亞銅上并將其應用在生物抗菌領域,取得明顯的抑菌效果.此外,相比于金、鉑等貴金屬來講,銀的價格相對較低,因此其具有較好的經濟性.而目前尚未發現將負載Ag納米顆粒的Ag/Cu3(BTC)2復合催化劑應用在脫硝催化方面的報導.
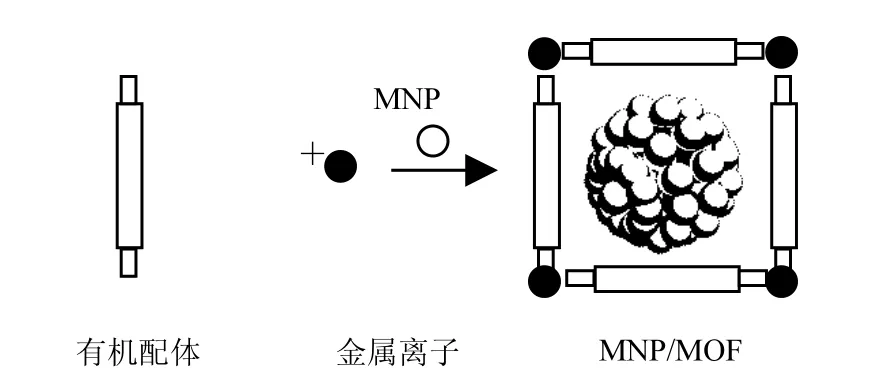
圖1 用MOFs做載體負載金屬納米顆粒的示意Fig.1 Schematic representation of MOFs carries loaded with metal nanoparticles
本文采用Cu3(BTC)2作為Ag納米金屬顆粒的載體,采用紫外還原法成功制備了分散程度較好的Ag/Cu3(BTC)2復合催化劑,通過各種表征手段分析其結構與物化性能,并應用于 NH3-SCR催化反應,系統研究了其脫硝效率和反應機理.
1 實驗方法
1.1 Ag/Cu3(BTC)2復合催化劑的制備
通過紫外還原法制備Ag/Cu3(BTC)2復合催化劑的實驗過程如下所示:
首先按照文獻報道[26]制備Cu3(BTC)2晶體,然后稱取質量比例為1:13的AgNO3與Cu3(BTC)2催化劑分別置于30mL的無水乙醇中進行超聲處理至其溶解,并將反應物混合轉移至燒杯中,磁力攪拌 3h;接著將混合反應物轉移到帶有紫外燈的密閉容器中,在紫外暗態條件下照射2h并攪拌,在紫外光的作用下,硝酸銀被還原為金屬Ag納米顆粒負載于Cu3(BTC)2催化劑結構的表面;反應完全后,采用離心機以8000r/min的轉速使用無水乙醇多次清洗,以去除殘留在催化劑表面的雜質,最后在恒溫干燥箱中干燥得到負載量為 5wt%的Ag/Cu3(BTC)2催化劑.通過改變 AgNO3與 Cu3(BTC)2質量比例,采用同樣的方法制備出Ag納米顆粒負載量為10wt%和15wt%的Ag/Cu3(BTC)2催化劑.制備催化劑的實驗裝置圖如圖2所示.
1.2 性能表征
采用全自動 shimadzuXD-3A型衍射儀(日本SHIMADZU公司)對 Ag/Cu3(BTC)2復合催化劑進行X 射線衍射(XRD)分析;比表面積、孔容、孔徑測定由NOVA 4200e型自動比表面和孔徑分布分析儀進行;采用TECNAI G20-STWIN型透射電子電子顯微鏡(美國FEI公司)進行TEM表征;原位傅里葉變換紅外光譜分析在布魯克VERTEX 70型傅里葉變換紅外光譜儀上進行.
1.3 脫硝活性測試
測試采用自制固定床反應裝置評價催化劑的NH3-SCR反應活性.此裝置由配氣系統,固定床反應系統和煙氣測試系統三部分組成.模擬煙氣由純度均為 0.25%的氨氣和一氧化氮,純度為 25%的氧氣和高純氮氣組成,各組成成分的流量由質量流量計控制,氣體總流量為 100mL/min,其中[NO] = [NH3] =0.05%,[O2] = 5% (volume fraction, φ),剩余以 N2作為補充氣.反應裝置中的U型石英反應管內徑為5mm,催化劑用量為 0.1g,催化劑的體積為 0.2cm3,空速比為 30000h-1.用溫控加熱儀進行升溫控制,反應溫度為100~280℃.用testo350煙氣分析儀對NOx進行實時在線濃度的檢測并用相關軟件中記錄數據.反應裝置圖如圖3所示.目的是利用NO的轉化率對催化劑的脫硝性性能進行表征,其計算公式如下:

圖2 紫外還原法制備Ag/Cu3(BTC)2催化劑的實驗裝置Fig.2 Schematic diagram of experimental setup of Ag/Cu3(BTC)2 by UV reduction
2 結果討論
2.1 Ag/Cu3(BTC)2復合催化劑的脫硝性能
首先對Ag/Cu3(BTC)2復合催化劑進行前期處理,將3種不同Ag納米顆粒負載量的復合催化劑在N2保護下在 230℃高溫活化處理 2h,目的是脫除 MOFs催化劑上的溶劑分子,從而暴露出更多的金屬催化活性位點.圖 4給出了活化后不同 Ag負載量的Ag/Cu3(BTC)2材料的催化活性測試結果.從圖中可以看出,3種催化劑的脫硝效率均隨著反應溫度的升高而增大.Ag/Cu3(BTC)2復合催化劑的起活溫度發生在100℃,明顯低于先前報導的Cu3(BTC)2材料140℃的起活溫度,且表現出更高的低溫活性[27].此外,隨著 Ag負載量的增多,Ag/ Cu3(BTC)2復合催化劑的催化效率呈上升趨勢.負載量為15wt%的Ag/Cu3(BTC)2催
化劑表現最佳催化效率,在220℃~260℃時達到了100%的NO脫除效率,溫度窗口寬度約為40℃.這一測試結果說明Ag納米顆粒的引入明顯提高了Cu3(BTC)2催化劑的低溫催化活性.
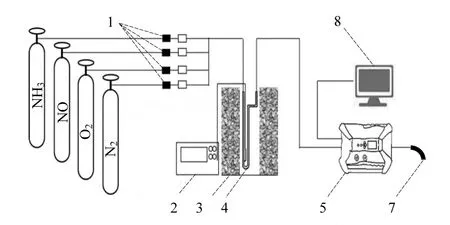
圖3 NH3-SCR 反應裝置示意Fig.3 Schematic diagram of experimental apparatus for NH3-SCR reaction
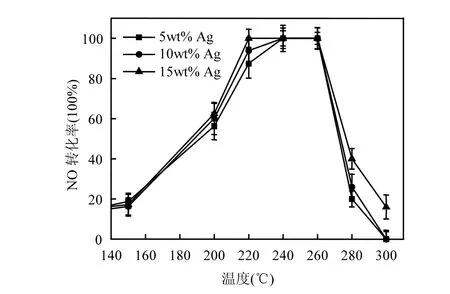
圖4 負載量不同的Ag/Cu3(BTC)2催化劑的NO轉化率Fig.4 NO conversion on various xAg/Cu3(BTC)2 catalysts
2.2 催化劑的物理化學性質表征
2.2.1 XRD表征 為觀測確定Ag納米顆粒的負載情況,采用XRD研究了Ag/Cu3(BTC)2復合催化劑的晶體結構,所得譜圖如圖5所示.與Cu3(BTC)2的譜圖(a)相比,可以看出在 Cu3(BTC)2骨架結構上負載 Ag納米顆粒之后,XRD譜圖(b,c,d)的衍射峰強度均明顯增強,說明復合催化劑的晶型結構更為完善.而負載不同量的Ag納米顆粒的Ag/Cu3(BTC)2復合催化劑的特征峰強度基本一致.參考標準卡片(JCPDS 48-1548)可知,位于 2θ = 38.7°,44.3°處的 2 個峰分別歸屬于金屬Ag的(111)、(200) 2個晶面的衍射峰,這證明了 Ag納米粒子已經成功負載在 Cu3(BTC)2晶體表面[24-25,28].
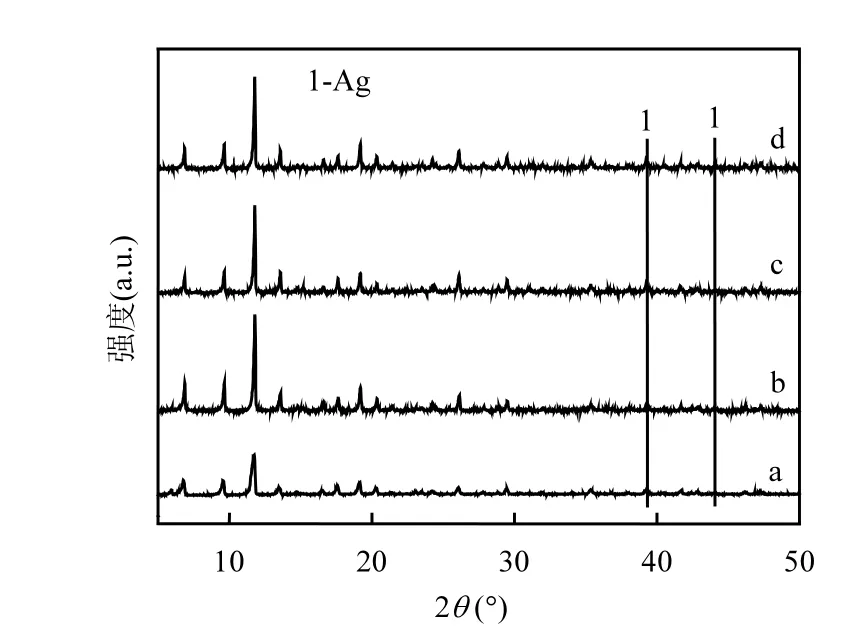
圖5 Cu3(BTC)2和負載量不同的Ag/Cu3(BTC)2催化劑的XRD譜Fig.5 XRD patterns of (a)Cu3(BTC)2;(b) 5wt% Ag/Cu3(BTC)2;(c) 10wt% Ag/Cu3(BTC)2 and (d)15wt% Ag/Cu3(BTC)2
2.2.2 TEM表征 為進一步研究Ag納米顆粒的分布和結構信息,對 Ag/Cu3(BTC)2復合催化劑進行TEM表征.圖6為負載量為15wt%的Ag/Cu3(BTC)2催化劑的透射電鏡圖,從圖中可以看出Ag納米顆粒成功負載到Cu3(BTC)2骨架結構的表面,其呈現出均一的球狀結構,且分布較為均勻.透射電鏡觀察到的Ag納米顆粒粒徑尺寸約為 5nm,并能通過高倍透射電鏡表征清晰觀察出晶格條紋,可以測出相鄰晶格的距離為0.234nm,這與立方晶相Ag的(111)理論晶面間距0.236nm一致,說明Ag納米顆粒沿著(111)面生長.
2.2.3 XPS表征 通過 XPS表征對 Ag/Cu3(BTC)2催化劑表面的元素組成以及金屬元素價態,結果如下圖 7所示.圖 7(a)的全譜圖出峰位置在 932.9eV、531.8eV、368.4eV、284.8eV,分別代表Cu2p、Ag3d、O1s、C1s軌道的特征峰.說明了 Ag/Cu3(BTC)2催化劑的表面元素組成.圖7(b)中934.4eV和954.3eV兩個峰分別歸屬于 Cu 2p3/2和Cu 2p1/2軌道,代表Cu2+的兩個特征峰;932.9eV和 952.8eV兩個峰分別歸屬于 Cu2p3/2和 Cu 2p1/2軌道,代表 Cu+的兩個特征峰
[29-30].同時,在 940~945eV 區域出現了強烈的雙伴峰(shake-up satellites),這表示有絡合的雙銅離子Cu(Ⅱ)存在[31],這個結果與 Cu-BTC晶體結構相吻合.圖 7(c)為催化劑Ag3d的XPS譜圖,其中374.4eV和368.4eV特征峰與Ag3d3/2和Ag3d5/2軌道的特征峰相對應,分別代表有Ag+和Ag單質的存在.圖7(d)為催化劑O1s軌道的XPS譜圖,結合能為531.8eV的特征峰歸屬于催化劑的晶格氧 O2-.催化劑中氧空位的存在可產生表面氧空位協同效應,對反應起促進作用[32].

圖6 負載量為15wt%的Ag/Cu3(BTC)2催化劑的透射電鏡Fig.6 TEM images of 15wt% Ag/Cu3(BTC)2 catalyst(a)15wt%;(b)15wt%;(c)HRTEM image of 15wt% Ag/Cu3(BTC)2
2.2.4 N2吸脫附表征 為研究負載Ag納米顆粒對復合Ag/Cu3(BTC)2復合催化劑孔結構的影響,對負載量15wt%的Ag/Cu3(BTC)2和Cu3(BTC)2材料進行了N2吸脫附表征,其比表面積、孔體積和孔徑等物理性質參數列于表 1.可以看出,負載 Ag納米顆粒后,Ag/Cu3(BTC)2催化劑的比表面積相比 Cu3(BTC)2明顯減小,由 800.4m2·g-1變為 604.0m2·g-1,說明金屬 Ag成功填充到Cu3(BTC)2催化劑孔道內部.此外,根據前面的催化活性測試數據可知,復合催化劑比表面積的減小并沒有降低其脫硝性能,相反,NO的轉化率隨Ag的加入明顯提高.這一方面可以歸因于Ag/Cu3(BTC)2催化劑的孔體積和孔徑出現增加,如表1所示,分別達到0.577cm3·g-1和3.818nm,這說明負載Ag后的孔結構更有利于反應氣體在催化劑中的吸附和參與反應;另一方面也證明了貴金屬Ag納米顆粒和Cu3(BTC)2中的 Cu活性位存在良好的協同催化作用,可大幅提高材料的催化活性,使NO轉化效率在比表面積下降的情況下仍然得以提高.
2.2.5 原位 FTRI表征及反應機理研究 根據 NH3和NOx在脫硝反應中的相態,氨法催化脫硝反應機理可以分為 Eley-Rideall(E-R)和 Langmuir-Hinshelood(L-H)機理.為了闡明在 Ag/Cu3(BTC)2復合催化劑表面的脫硝反應機理通過原位紅外光譜技術對吸附和反應過程進行了原位測試.圖 8為催化劑在 240℃吸附NH3飽和后通入NO + O2后表面吸附物種隨時間變化的原位紅外譜圖.在Ag/Cu3(BTC)2復合催化劑吸附氨氣40分鐘后,由圖可以觀察到3個明顯的特征峰.其中,1689cm-1處的特征峰歸屬于 NH3吸附在Br?nsted酸性位上形成的NH4+,1622cm-1處的特征峰歸屬于氣相或弱吸附的NH3吸附峰,而1510cm-1處的特征峰歸屬于-NH2物種.-NH2被認為是E-R反應機理中一種重要的中間產物, 主要是 NH3被氧化脫氫而形成的,該中間體可以與氣相的NO迅速反應生成NH2NO,并進一步分解為N2和H2O[33].

表1 不同樣品的N2吸脫附物理性質參數Table 1 Structural parameters of various xAg/Cu3(BTC)2 catalysts derived from N2physisorption results
經 He氣吹掃后,1622cm-1處的弱吸附或氣相的NH3特征峰消失,Br?nsted酸中心吸附形成的 NH4+物種(1689cm-1)以及-NH2物種(1510cm-1)穩定存在催化劑表面.當通入NO和O2后,在1548、1600、1628、1840、1901cm-1等處生成硝酸鹽物種的特征峰, 酸性位上的NH3物種和 Br?nsted酸中心吸附形成的 NH4+物種(1689cm-1)消失,說明 NO、O2與 NH3發生了反應.其中,1548cm-1處的特征峰歸屬于雙齒硝酸鹽, 1600cm-1處的特征峰歸屬于單齒硝酸鹽[34],1628cm-1處的特征峰歸屬于橋聯硝酸鹽[35],1840和1901cm-1處的特征峰歸屬于氣相 NO或弱吸附的硝酸鹽物種[36].因此可得出結論,表面吸附NH3參與SCR反應中且具有較高活性,吸附NH3和NH4+物種峰的消失說明Lewis酸性位和Br?nsted酸性位都參與到反應中,-NH2是SCR反應中的重要中間產物,其遵循 E-R反應機理和氣態 NO反應生成N2和H2O,反應過程推測如下:
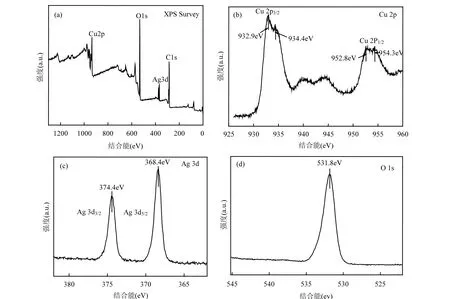
圖7 負載量為15wt%的Ag/Cu3(BTC)2催化劑的XPS表征Fig.7 XPS spectra of 15wt%Ag/Cu3(BTC)2 catalyst
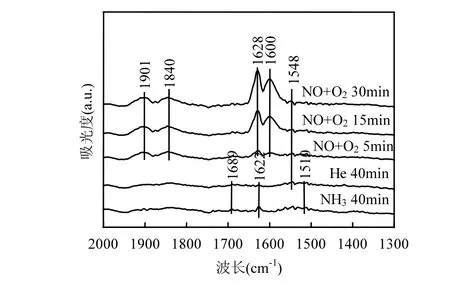
圖8 Ag/Cu3(BTC)2催化劑在240℃下表面NH3預吸附物種與500ppmNO,5% O2的反應的原位FTIR譜Fig.8 In situ FTIR spectra of Ag/Cu3(BTC)2 at 240℃ upon passing 500ppm NO + 5 %O2 over the NH3 pre-adsorbed
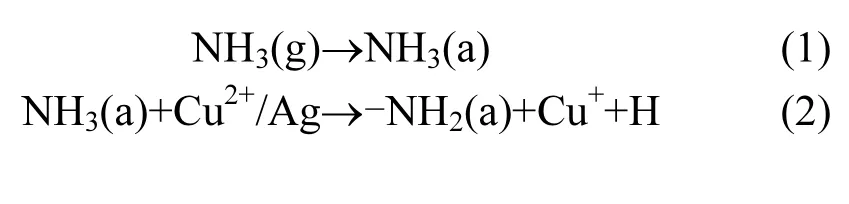

總反應方程:4NO + 4NH3+ O2→ 4N2+ 6H2O
3 結論
本文采用紫外還原方法首次成功地將貴金屬Ag納米顆粒負載 Cu3(BTC)2骨架結構表面上,制備了三種 Ag納米顆粒負載量的不同的復合 Ag/Cu3(BTC)2催化劑,透射電鏡顯示 Ag納米顆粒以較完整的球狀結構負載到 Cu3(BTC)2骨架結構的表面,粒徑大小約在5nm左右;催化劑有明顯的金屬銀的晶格條紋存在.對催化劑的脫硝性能進行了研究,發現Ag/Cu3(BTC)2催化劑在NH3-SCR反應中具有優于Cu3(BTC)2催化劑的脫硝效率,其在 220~260℃的溫度區間內達到100%的 NO轉化率,說明負載的 Ag納米顆粒與 Cu金屬活性位點之間具有較強的協同催化作用.并利用原位紅外技術推測出其反應遵循E-R反應機理.

