核酸檢測(cè)與酶免檢測(cè)平行篩查血液在基層血站的應(yīng)用效果評(píng)價(jià)
陳艷萍
(安陽市中心血站檢驗(yàn)科,河南 安陽 455000)
輸血傳播病原體篩查是為確保血液及血液制品的安全,對(duì)輸血相關(guān)傳染病進(jìn)行預(yù)防和控制的一種保障血液安全的重要手段,且一直以來備受世界各國(guó)關(guān)注[1]。目前,國(guó)內(nèi)對(duì)獻(xiàn)血者往往常規(guī)采用酶聯(lián)免疫法(enzyme linked immunosorbent assay,ELISA)開展梅毒螺旋體血清學(xué)及HIV、HBV、HCV檢測(cè),雖然此種篩查模式能夠使輸血傳播疾病的風(fēng)險(xiǎn)得到極大地降低,有較高的敏感度,但對(duì)血液的準(zhǔn)確篩查仍存在一定的局限性[2]。而近年來發(fā)展的核酸擴(kuò)增技術(shù) (nucleic acid amplification techniques,NAT),具有高度敏感及特異性,可明顯縮短梅毒螺旋體血清學(xué)及HIV、HBV、HCV病毒的檢測(cè)窗口期,保障血液制品的安全性[3]。為了進(jìn)一步提高篩查血液的敏感度,為此,本文探討核酸檢測(cè)與酶免檢測(cè)平行篩查血液在基層血站的應(yīng)用效果評(píng)價(jià)。
1 資料與方法
1.1 標(biāo)本來源 選取2016年1月-2017年7月本基層血站無償獻(xiàn)血者標(biāo)本34680例,獻(xiàn)血者均符合國(guó)家《獻(xiàn)血者健康檢查要求》中相應(yīng)的要求。均對(duì)每位獻(xiàn)血者進(jìn)行血液采集的同時(shí)留取ELISA和NAT兩種樣管,所有血液標(biāo)本采集后保存于2~8℃冰箱,采樣后4h內(nèi)進(jìn)行1500g室溫離心20min低溫離心,離心后臨時(shí)保存于2~8℃,并在24h內(nèi)進(jìn)行NAT檢測(cè)。
1.2 方法
1.2.1 儀器 ELISA檢測(cè)使用 (瑞士HAMILTON公司)Hamilton Star全自動(dòng)加樣儀和FAME酶免分析儀)。核酸檢測(cè)使用 (瑞士HAMILTON公司)的Hamilton Star全自動(dòng)混樣儀,Cobas Taq Man Analyzer核酸擴(kuò)增檢測(cè)儀,其通過混樣和數(shù)據(jù)管理服務(wù)器(PDM)連接組成羅氏診斷Cobas's 201血液核酸血篩平臺(tái)(CAP/CTM),Cobas Amp Li Prep核酸提取儀,(美國(guó)ABI公司)ABI 7500實(shí)時(shí)熒光定量PCR儀,(日本KUBOTA公司)低溫大容量離心機(jī)KUBOTA 8730。
1.2.2 試劑 上海科華生物工程股份有限公司批號(hào)200909051、200912011、201003041 的 HBsAg 檢測(cè)試劑;北京萬泰生物藥業(yè)有限公司批號(hào):C20121221、C20130305、C20130406 等 抗-HCV 檢測(cè)試劑盒;上海科華生物工程股份有限公司,批號(hào):201212031、201303021、201304011 等) 等 抗-HIV1/2檢測(cè)試劑盒;美國(guó)羅氏診斷公司批號(hào)P011692、R01529、R01528 等 NAT 試劑),配套耗材均由各試劑公司提供,(美國(guó)雅培公司)乙肝血清學(xué)補(bǔ)充試驗(yàn)試劑。
1.3 觀察指標(biāo)
1.3.1 對(duì)獻(xiàn)血者標(biāo)本進(jìn)行核酸檢測(cè)與酶免檢測(cè)平行檢測(cè),按試劑盒說明書嚴(yán)格操作,結(jié)果判定:標(biāo)本HBsAg/抗-HCV/抗-HIV1/2對(duì)2種試劑反應(yīng)為陽性則判為陽性,反應(yīng)均為陰性則判為陰性,對(duì)于反應(yīng)陰性或只有1種試劑反應(yīng)陽性的標(biāo)本均進(jìn)行NAT。
1.3.2 NAT檢測(cè) 實(shí)驗(yàn)嚴(yán)格按照操作儀器及試劑盒說明書步驟,若單個(gè)Pool結(jié)果為陽性的再對(duì)其進(jìn)行拆分,結(jié)果判定:NAT陰性:混樣有陽性而拆分陰性的標(biāo)本;NAT陽性:混樣有陽性拆分也有陽性的標(biāo)本。
1.3.3 將核酸檢測(cè)陽性標(biāo)本進(jìn)行分項(xiàng)定量檢測(cè)和乙肝血清學(xué)補(bǔ)充試驗(yàn),檢測(cè)出的陽性標(biāo)本作HBV DNA、HCVRNA和HIV RNA分項(xiàng)定量檢測(cè)和乙肝5項(xiàng)檢測(cè)。
1.4 統(tǒng)計(jì)學(xué)方法 采用SPSS 19.0軟件分析本研究的所有數(shù)據(jù),采用χ2檢驗(yàn)計(jì)數(shù)資料,以P<0.05為差異有統(tǒng)計(jì)學(xué)意義。
2 結(jié)果
2.1 核酸檢測(cè)結(jié)果 經(jīng)ELISA篩查HBsAg、抗-HCV和抗-HIV-1/2無反應(yīng)性及僅1種試劑為反應(yīng)性的標(biāo)本共32456例,經(jīng)核酸NAT檢測(cè)陽性標(biāo)本72例,陽性檢出率為0.21%;如表1所示。

表1 核酸檢測(cè)結(jié)果
2.2 分項(xiàng)定量檢測(cè)篩查結(jié)果 72例NAT檢測(cè)陽性標(biāo)本進(jìn)行分項(xiàng)定量檢測(cè),定量檢測(cè)HBV DNA陽性36例,陽性率為75.00%(36/48),未檢測(cè)出HIV RNA陽性和HCV RNA陽性。
2.3 乙肝血清學(xué)補(bǔ)充試驗(yàn) 72例NAT檢測(cè)陽性標(biāo)本 ELISA 篩查 HBsAg,抗-HBs,抗-HBe,HBeAg,抗-HBc,最終確認(rèn)陽性標(biāo)本48例,確認(rèn)陽性率為66.67%(66/72)(陽性率比較 χ2=239.68,P<0.05),見表2。
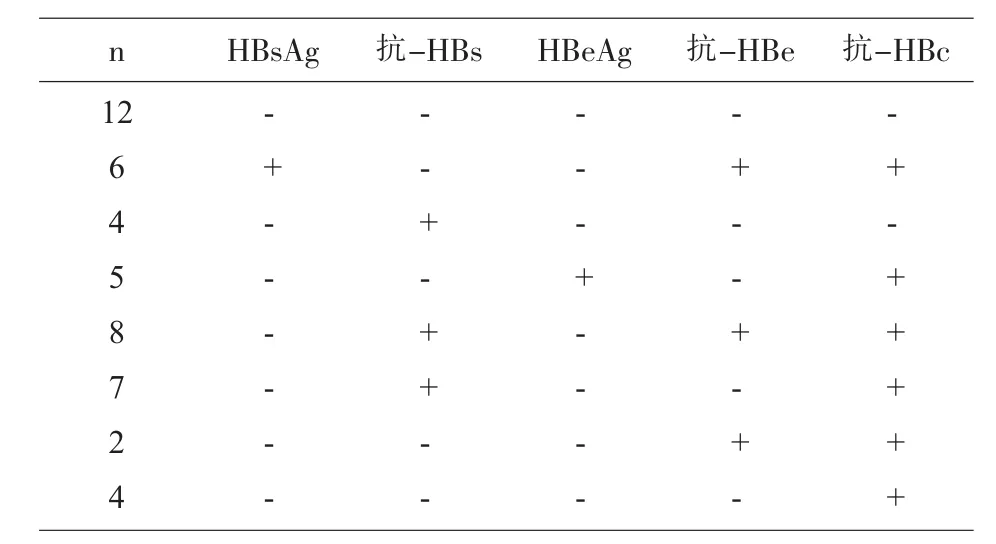
表2 48例標(biāo)本乙肝“兩對(duì)半”血清學(xué)模式
3 討論
核酸擴(kuò)增檢測(cè)技術(shù)(NAT)是直接通過采用分子診斷技術(shù)對(duì)病原體核酸進(jìn)行檢測(cè)的一系列技術(shù)的方法的總稱,包括核酸提取、擴(kuò)增和檢測(cè)三種基本步驟[4]。因?yàn)椴《究乖翱贵w蛋白結(jié)構(gòu)的變異,易導(dǎo)致“窗口期”漏檢,而NAT具有較高的敏感性、特異性和自動(dòng)化的特點(diǎn),在病毒感染后數(shù)天便可檢測(cè)出標(biāo)本中極微量的病毒核酸,從而使 “窗口期”縮短,減少漏檢導(dǎo)致的輸血后病毒感染[5-7]。
本研究探討核酸檢測(cè)與酶免檢測(cè)平行篩查血液在基層血站的應(yīng)用效果評(píng)價(jià),結(jié)果發(fā)現(xiàn),經(jīng)ELISA篩查HBsAg、抗-HCV和抗-HIV-1/2無反應(yīng)性及僅1種試劑為反應(yīng)性的標(biāo)本共32456例,經(jīng)核酸NAT檢測(cè)陽性標(biāo)本72例,陽性檢出率為0.21%,遠(yuǎn)低于東莞(0.9%)[7],而高于我國(guó)其他地區(qū)報(bào)道的數(shù)據(jù)0.06%、0.081%,分析原因可能是人群分布的區(qū)域差異所致[8,9]。
本研究還發(fā)現(xiàn)72例NAT檢測(cè)陽性標(biāo)本進(jìn)行定量檢測(cè),ELISA 篩查 HB-sAg,抗-HBs,抗-HBe,HBeAg,抗-HBc,最終確認(rèn)陽性標(biāo)本48例。可見該NAT的靈敏度是很高的,可使病毒檢測(cè)的 “窗口期”縮短,有利于篩出隱匿性HBV感染的[10-12]。對(duì)75例標(biāo)本通過補(bǔ)充實(shí)驗(yàn)和追蹤檢測(cè)進(jìn)行確認(rèn),確認(rèn)HBV感染36例,確認(rèn)陽性率75.00%,未能確認(rèn)HBV感染12例,可能原因包括:由于工作人員不當(dāng)?shù)牟僮髟斐蓹z測(cè)結(jié)果顯示假陽性;或送往確認(rèn)標(biāo)本時(shí)對(duì)血樣的運(yùn)輸、保存不當(dāng)造成,如過長(zhǎng)的運(yùn)輸時(shí)間、過高的環(huán)境溫度等使核酸物質(zhì)分解;或在留存確認(rèn)血樣時(shí)因?yàn)樵谘獫{中病毒顆粒的泊松分布使病毒濃度分布不均,致使留取血樣病毒濃度降低,使確認(rèn)時(shí)未能檢出[13-15]。
綜上所述,核酸檢測(cè)與酶免檢測(cè)平行篩查,兩種手段相互補(bǔ)充,可使輸血傳播疾病殘余風(fēng)險(xiǎn)極大得到降低,預(yù)防經(jīng)輸血傳播的病毒性疾病,從可有效地保障血液安全。
 實(shí)驗(yàn)與檢驗(yàn)醫(yī)學(xué)2018年4期
實(shí)驗(yàn)與檢驗(yàn)醫(yī)學(xué)2018年4期
- 實(shí)驗(yàn)與檢驗(yàn)醫(yī)學(xué)的其它文章
- 病毒滅活血漿與普通冰凍血漿臨床應(yīng)用價(jià)值對(duì)比探討
- 在微柱凝膠血小板血型配型實(shí)驗(yàn)中紅細(xì)胞血型不規(guī)則抗體的影響因素觀察及處理措施
- 國(guó)產(chǎn)和進(jìn)口ELISA試劑HIV初篩結(jié)果與確證結(jié)果對(duì)比分析
- 基層醫(yī)院孕婦血型鑒定與抗體檢測(cè)分析
- 采用凝聚胺法及微柱凝膠法檢測(cè)不規(guī)則抗體的應(yīng)用比較
- 結(jié)直腸癌錯(cuò)配修復(fù)蛋白MLH1,PMS2,MSH2和MSH6及P16的表達(dá)及意義
