雙能CT聯合血清IL?1β檢測在痛風診斷中的應用價值
吳春葉,龔寶琪,屈瑾,李巍
痛風是一種晶體相關性關節病,尿酸鹽結晶在關節周圍的沉積是發病的主要因素,嚴重者可出現殘疾,影響患者生活質量。隨著生活水平的提高,人們飲食結構發生變化,飲酒、高嘌呤、高蛋白飲食大量攝入,痛風的發病年齡越來越年輕化,發病率逐年升高[1]。目前偏振光顯微鏡或痛風結節活檢發現尿酸鹽結晶是痛風診斷的金標準,但其為有創性檢查,易受穿刺部位、操作熟練程度及尿酸鹽結晶數量的影響,還有穿刺部位局部出血、感染等并發癥,亦有可能假陰性。有報道稱雙能CT(duel?energy computer tomography,DECT)在顯示尿酸鹽結晶沉積方面具有重要價值,目前在早期痛風的診斷中應用較廣,但其特異度較低[2]。白細胞介素(IL)?1在人體存在IL?1α和IL?1β兩種亞型,但以IL?1β為主,外源性刺激或病理狀態可刺激活化的巨噬細胞分泌IL?1β的水平明顯升高。而痛風急性發作患者血清IL?1β明顯升高,被認為是導致其急性發作和慢性遷延的重要致炎因子[3]。本文旨在觀察痛風患者DECT及血清IL?1β水平的變化,探討兩者聯合檢測在痛風診斷中的應用價值。
1 對象與方法
1.1 研究對象 選取2015年6月—2016年6月在天津市第一中心醫院風濕免疫科門診及住院就診,明確診斷為痛風的患者76例。疾病符合美國風濕病學會的痛風診斷與治療專家共識中制定的診斷標準[4]。具體如下:(1)關節液中有特征性尿酸鹽結晶。(2)用化學方法或偏振光顯微鏡證實痛風結節中含尿酸鹽結晶。(3)具備以下12條中6條或6條以上者。這12條分別為:①急性關節炎發作多于1次;②炎癥反應在1 d內達到高峰;③急性單關節炎發作;④患病關節可見皮膚呈暗紅色;⑤第1跖趾關節疼痛或腫脹;⑥單側關節炎發作,累及第1跖趾關節;⑦單側關節炎發作,累及跗骨關節;⑧有可疑痛風結節;⑨高尿酸血癥;⑩X線攝片檢查顯示不對稱關節內腫脹;?X線攝片檢查顯示不伴侵蝕的骨皮質下囊腫;?關節炎發作期間關節液微生物培養陰性。符合以上(1)~(3)條中任何1個條件者即可診斷為痛風。76例患者中男60例,女16例,平均年齡(52.1±1.8)歲。血尿酸濃度為(452.4±23.4)μmol/L。選取同時期就診臨床有關節腫痛的40例非痛風患者做為對照組,其中33例為類風濕關節炎,7例為骨關節炎。男31例,女9例,平均年齡(55.6±1.7)歲,血尿酸濃度為(234.1±17.5)μmol/L,2組間性別(χ2=0.032)、年齡(t=0.421)比較差異均無統計學意義(P>0.05)。所有入組患者均簽定知情同意書,操作流程符合我院人體試驗委員會倫理審核標準。
1.2 方法
1.2.1 DECT檢查 運用德國Siemens Somatom Definition DECT掃描儀,對治療前2組患者雙腕關節、膝關節、踝關節、跖趾關節進行掃描,數據傳輸至MMVP工作站,調入Gout軟件后進行圖像處理。根據不同物質衰減系數的不同,將檢測到的尿酸鹽結晶標記為綠色,骨性結構標記為藍色,鈣質沉積標記為紫色,由2位經驗豐富的骨骼肌方向的放射診斷醫生采用雙盲法進行數據分析,記錄是否存在綠色結晶沉積、沉積部位及數量,結果不一致時協商決定。偽影的標準依據參考文獻[5],具體如下。指甲偽影:綠色偽彩影局限于指甲區域;皮膚偽影:綠色偽彩影局限于皮膚區域;亞毫米偽影:單個綠色偽彩影<1 mm;金屬偽影:綠色偽彩影局限于射線硬化偽影層面;運動偽影:綠色偽彩影局限于運動層面的骨皮質;血管鈣化偽影:綠色偽彩影局限于血管鈣化區域。
1.2.2 血清IL?1β測定 2組患者分別于治療前取空腹靜脈血5 mL,分離血清后保存于?20℃低溫箱中待測。采用酶聯免疫吸附法(ELISA)檢測血清IL?1β水平,嚴格按照說明書步驟進行。試劑盒購自西門子醫學診斷產品(上海)有限公司,試劑盒提供的陽性參考值為≥5 ng/L。
1.3 臨床查體 臨床醫生對初次就診的患者進行關節查體,檢查關節局部有無紅腫熱痛、功能有無障礙及痛風石形成,尿酸鹽沉積病灶陽性為肉眼可見痛風石形成或關節局部紅腫熱痛。
1.4 統計學方法 采用SPSS 15.0統計軟件對數據進行分析和處理,符合正態分布的計量資料以均數±標準差(±s)表示,2組間比較采用獨立樣本t檢驗,計數資料以例(%)表示。計算DECT、血清IL?1β以及聯合檢查結果相對于金標準的敏感度、特異度、預測值、約登指數、Kappa值等指標,采用受試者工作特征(ROC)曲線分析IL?1β的診斷價值,計算曲線下面積(AUC),確定最佳的診斷界值。聯合檢測陽性定義為聯合檢測中任意一項檢測陽性,聯合檢測陰性定義為聯合檢測中所有檢測均為陰性。以P<0.05為差異有統計學意義。
2 結果
2.1 DECT檢查結果 DECT陽性者可在肌腱、韌帶、皮下、關節周圍及關節囊內可見綠色高密度尿酸鹽結晶影,伴有周圍軟組織腫脹或關節腔積液。76例痛風患者中臨床查體共發現尿酸鹽沉積病灶158處,DECT共發現尿酸鹽沉積病灶349處,其中第1跖趾關節為245處(64.5%),見圖1A。對照組5例患者出現假陽性,3例為甲周偽影(圖1B),2例為足底皮膚(足墊)偽影(圖1C),關節均未見尿酸鹽沉積病灶。
2.2 3 種檢查方法診斷痛風的臨床價值 DECT、IL?1β、DECT+IL?1β對痛風的診斷價值見表1、2。DECT在診斷痛風性關節炎的敏感度較高,特異度尚可。IL?1β在診斷痛風性關節炎的敏感度一般,特異度較高;兩者聯合檢測敏感度和特異度均較好。
2.3 血清IL?1β的ROC曲線 如圖2所示,血清IL?1β的曲線下面積(AUC)為0.929(0.882~0.977),最佳診斷值為5 ng/L,與試劑盒提供的陽性參考值一致。
3 討論
目前,痛風發病呈年輕化趨勢,嚴重影響患者生活質量,因此早期診斷是治療的關鍵。IL?1β是一種炎性因子,可促進前列腺素、基質金屬蛋白酶的合成和釋放,促進滑膜細胞和淋巴細胞的增殖,導致炎癥因子表達增加,細胞凋亡受阻,滑膜細胞增生,在軟骨破壞和骨侵蝕中起著重要作用[6]。Terkeitaub等[7]研究發現痛風組患者血清IL?1β水平明顯高于非痛風組,故降低痛風患者IL?1β水平可能成為痛風潛在的治療靶點。
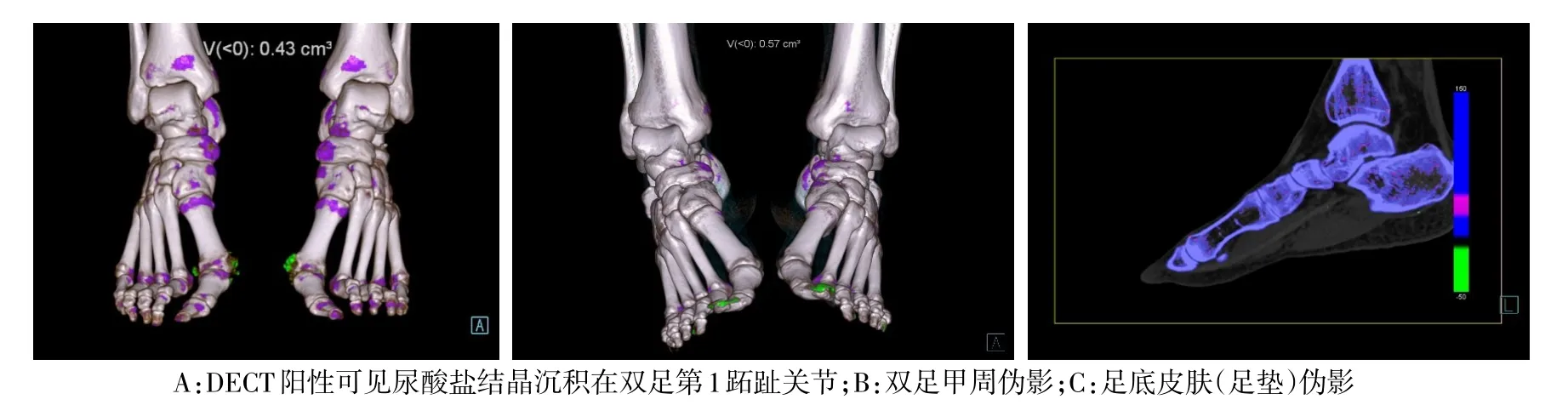
Fig.1 The results of DECT圖1 DECT檢查結果
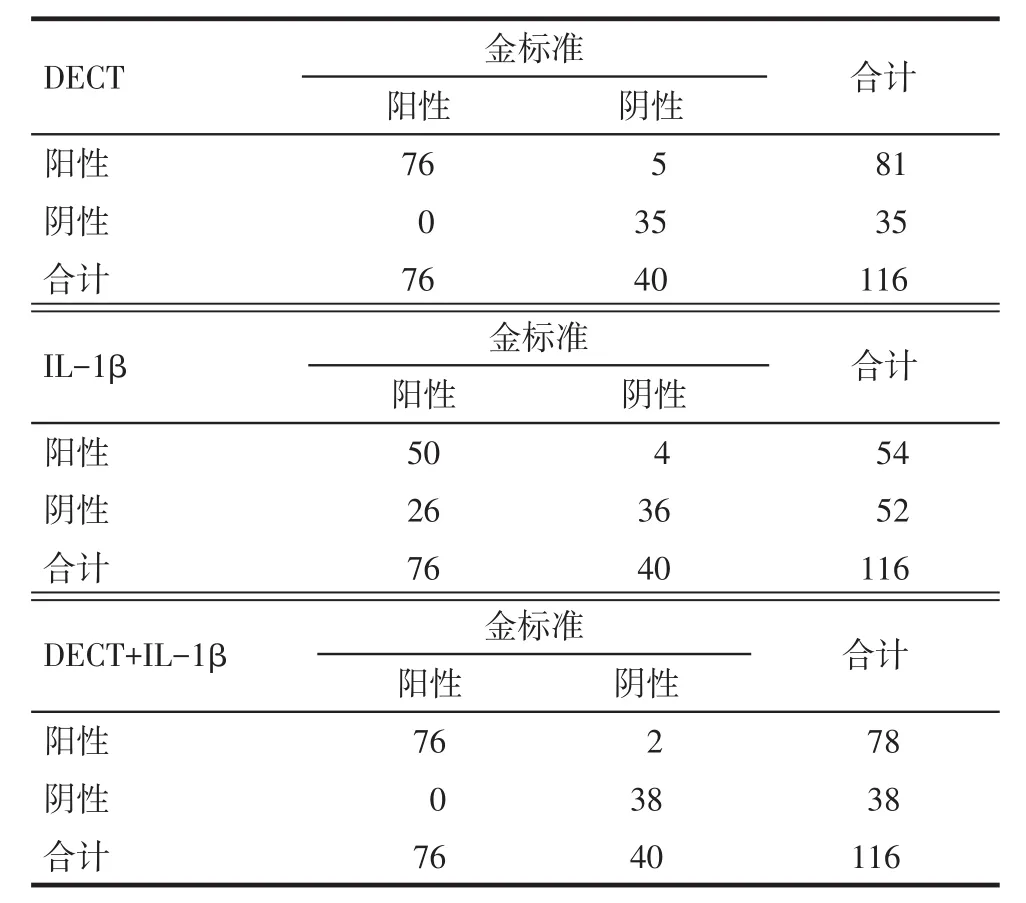
Tab.1 Comparison of the diagnostic results between three groups表1 3種診斷方法與金標準的診斷結果 例

Tab.2 Comparison of the clinical diagnosis for gout between three methods表2 3種診斷方法對痛風的診斷效能
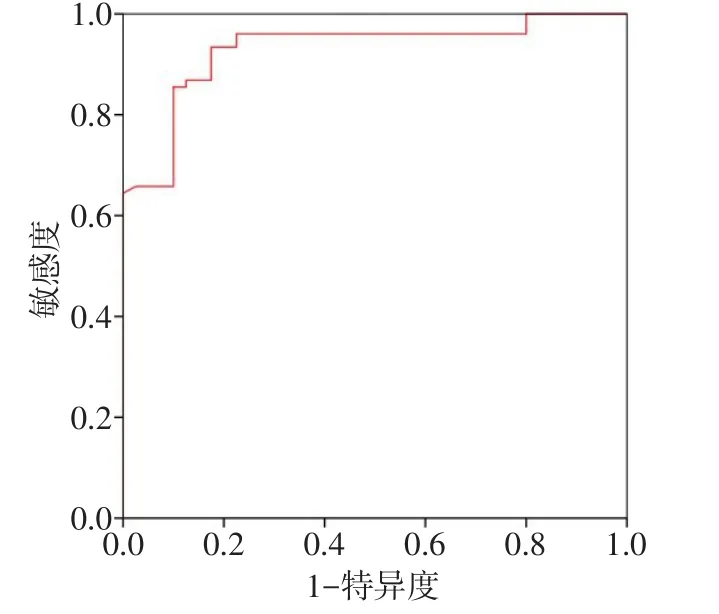
Fig.2 The ROC curve of IL?1β圖2 IL?1β的ROC曲線
目前,臨床常用于痛風檢查的影像學手段為X線、CT、MRI及超聲檢查。普通X線片僅能顯示明顯骨侵蝕,不能顯示早期病變;普通CT檢查可顯示痛風石,還可顯示骨質及軟組織改變,但在鑒別痛風結節和骨質增生、軟組織內鈣化灶時有一定困難;MRI為評價滑膜炎的首選,可顯示痛風石受累關節周邊軟組織情況,但對骨構造顯示欠佳,不能準確評價痛風石的骨質浸潤情況。超聲檢查無創且相對特異,但依賴于操作者經驗且存在視野局限,僅適用于四肢大關節[8]。DECT掃描是利用各種物質的密度不同,能量衰減曲線不同的原理,將采集到的不同能量的衰減信息進行分析匯總的成像辦法,可檢測掃描部位尿酸鹽化學成分,顯示尿酸鹽的堆積情況,進而評估尿酸鹽結晶體積[9]。患者在DECT檢查時必然會遭受輻射,但由于輻射區域為外周關節,且這些區域對放射線并不敏感,因此危險性非常小。檢查時患者外周關節輻射總量為2~3 mSV,這接近于中國平均自然輻射本底(2.3 mSV),故其輻射劑量是在可接受范圍內[10]。值得注意是,DECT檢查時血尿酸升高的患者檢測到尿酸鹽結晶的可能大,但血尿酸不高者亦可檢測到尿酸鹽綠色結晶[11]。本研究5例對照組患者出現假陽性,3例為甲周偽影,2例為足底皮膚(足墊)偽影。有報道指出局部偽彩可能是偽影,包括指甲、皮膚及血管鈣化的偽影等;指甲偽影通常位于甲溝處,而皮膚偽影多存在于角質化較為嚴重的皮膚處,如足跟等,且皮膚偽影多為層狀順皮膚方向走形[12]。當出現局部偽影時應注意識別并更改重建算法,調整后處理參數,避免出現假陽性。另外掃描部位有金屬內固定的患者不宜行DECT,易產生假陽性;金屬內固定偽影導致的綠色標記呈放射狀分布,部分甚至位于體外,且偽影均位于有金屬內固定一側,對側無顯示,臨床工作中需仔細詢問病史,認真識別[13]。
本研究中DECT檢查顯示的尿酸鹽結晶沉積病灶數明顯多于體表檢查,且DECT可顯示深部肌腱中的尿酸鹽結晶堆積,彌補了臨床診斷的缺陷,尤其是少見部位的沉積病灶,可協助發現亞臨床狀態的痛風,幫助對患者病情更精準地評價。第1跖趾關節為急性痛風性關節炎典型發病部位,本研究中該部位出現尿酸鹽結晶沉積的比例也較高(64.5%)。上述結果均表明DECT可直觀、準確地顯示痛風石的部位、范圍及骨質的破壞情況,為痛風的診療提供可靠的影像依據[14]。
本研究中DECT診斷痛風的敏感度為100%,特異度為87.5%,IL?1β檢測的敏感度為65.7%,特異度為90.0%,兩者聯合檢測敏感性、特異性均顯著高于其單獨檢測,且兩者聯合檢測對痛風的診斷陽性預測值與現通用的痛風診斷金標準無明顯差異,兩者診斷效能相當,但更簡便易行。作為非侵入性的診斷方法,本研究認為聯合應用DECT及血清IL?1β水平的檢測可以提高痛風的早期診斷率,明確尿酸鹽沉積部位,彌補了傳統診斷方法的不足,為痛風的診斷提供新的方法及治療靶點,使痛風患者得到及時正規的治療,有一定臨床推廣價值。

