新生兒危重先天性心臟病的超聲心動圖診斷及外科治療經驗
孟紅,逄坤靜,王浩,徐楠,李守軍,閆軍,花中東,王強
方法:回顧2012-01至2017-01來中國醫學科學院阜外醫院就診的160例危重先心病新生兒資料,總結并分析這類患者的超聲心動圖診斷及外科治療經驗。危重先心病指:患有嚴重心內或大血管結構異常,容易導致難以糾正的低氧血癥、酸中毒、呼吸道感染、心力衰竭等,只有通過外科或介入治療才能生存。
結果:患兒術前超聲心動圖診斷包括完全性大動脈轉位(50%)、室間隔完整型肺動脈閉鎖或重度肺動脈瓣狹窄(17.5%)、單純主動脈離斷或弓縮窄(15%)、完全型肺靜脈異位回流(10.6%)、共同動脈干或右肺動脈起源于升主動脈(3.8%)、合并室間隔缺損的肺動脈閉鎖或重度法樂四聯癥(1.9%)、巨大室間隔缺損并發嚴重左心衰竭(0.6%)、右心房占位(0.6%)。共140例患兒接受手術治療,其中134例接受一期根治手術,4例接受姑息手術,2例接受分期根治手術。院內死亡率為7.9%。129例患兒接受術后隨診,平均隨訪時間(16.8±18.2)個月。僅2例患兒接受二次手術,其余患兒均康復良好。
結論:有八類先心病需在新生兒期進行外科干預,既有紫紺型又有肺血多型。大部分危重先心病患兒經手術治療可獲得良好效果。
危重先天性心臟病(先心病)是指心臟大血管的嚴重解剖畸形,從而造成血液動力學嚴重異常,導致患兒出現難以糾正的低氧血癥、酸中毒并呈進行性惡化,或反復出現呼吸道感染、心力衰竭,內科治療難見成效。新生兒期危重先心病患兒表現尤其明顯,只有通過外科或介入治療才能生存[1]。新生兒期需要救治的危重先心病包括不同病種,其病理解剖、臨床癥狀、手術方式也各有不同[2]。準確進行術前評估是制定最優手術方案、把握最佳治療時機的前提[3]。本研究旨在回顧中國醫學科學院阜外醫院近5年救治的新生兒期危重先心病患兒資料,總結其病種分布、術前超聲診斷要點及手術治療情況。
1 資料與方法
本研究自2012-01至2017-01期間連續收集來中國醫學科學院阜外醫院就診的新生兒期危重先心病患兒160例。危重先心病指:患有嚴重心內或大血管結構異常,容易導致難以糾正的低氧血癥、酸中毒、呼吸道感染、心力衰竭等,只有通過外科或介入治療才能生存。所有患兒在我院救治的臨床資料齊全,均通過超聲心動圖明確診斷,其中28例行心血管造影或計算機斷層攝影術(CT)補充或肯定超聲心動圖診斷。所有手術患兒于術后一周復查超聲心動圖。出院后患兒在門診接受臨床和超聲心動圖隨訪以及電話隨訪。
統計學方法:采用SPSS 19.0統計學分析軟件處理所有數據,正態分布計量資料以均數±標準差表示,非正態分布計量資料以中位數及范圍表示,計數資料以例(%)表示。
2 結果
160例患兒中,男113例,女47例,就診時平均年齡(14.1±8.8)d。24例患兒術前經歷搶救(表1)。
160例患兒涉及的先心病病種(圖1):80例(50%)完全性大動脈轉位(TGA);28例(17.5%)室間隔完整型肺動脈閉鎖或重度肺動脈瓣狹窄;24例(15%)單純主動脈弓離斷或弓縮窄;17例(10.6%)完全型肺靜脈異位回流(TAPVC);6例(3.8%)共同動脈干或右肺動脈起源于升主動脈;3例(1.9%)合并室間隔缺損(室缺)的肺動脈閉鎖或重度法樂四聯癥;1例(0.6%)巨大室缺并發嚴重左心衰竭;1例(0.6%)右心房占位,梗阻三尖瓣口。
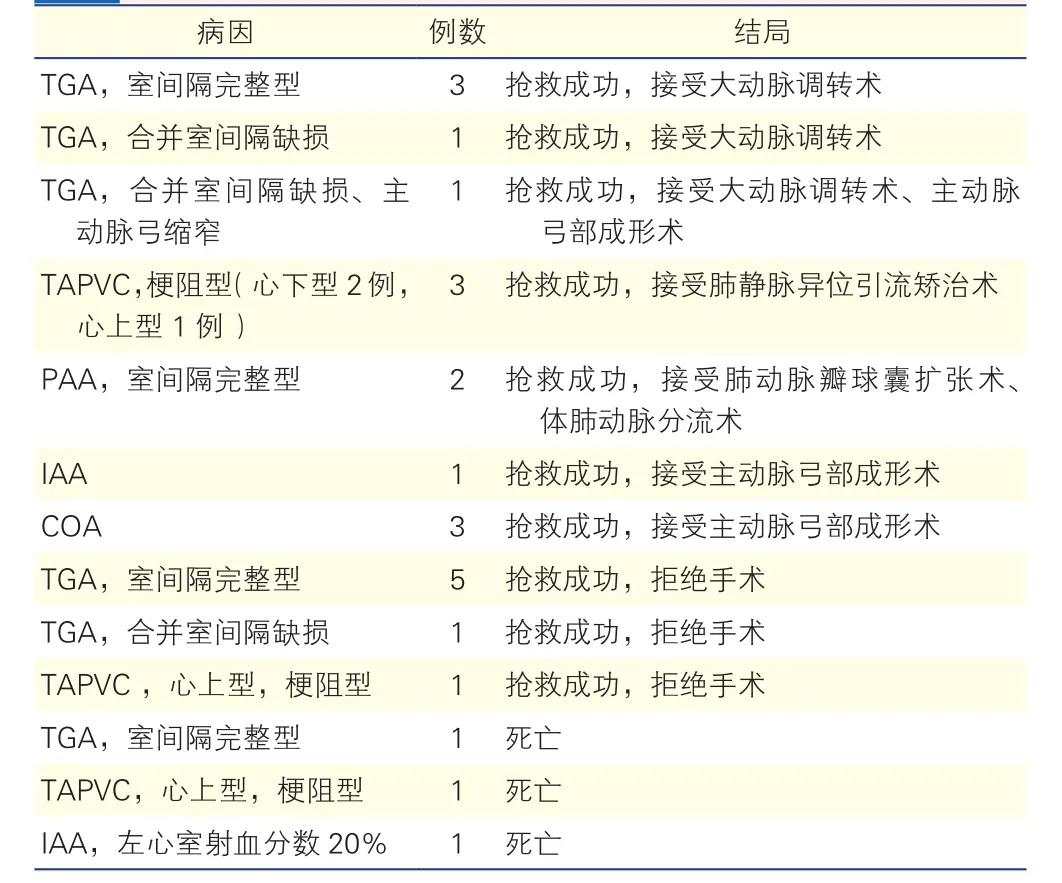
表1 住院期間術前經歷搶救的24例先天性心臟病患兒情況
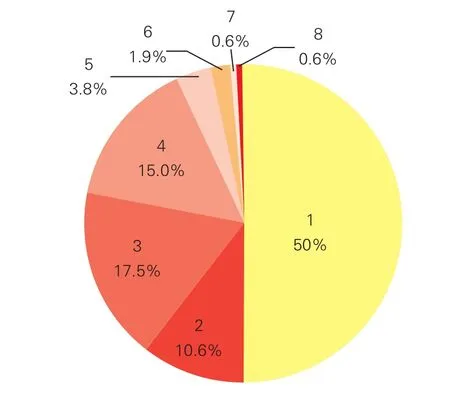
圖1 160例新生兒期危重先天性心臟病病種分布
80例TGA患兒中,52例為室間隔完整型,平均經皮氧飽和度為67%(25%~90%);26例合并室缺,平均經皮氧飽和度為72%(45%~97%)。2例TGA患兒同時合并嚴重主動脈弓部病變(A型主動脈弓離斷和重度主動脈弓縮窄),術前行CT檢查肯定超聲心動圖對主動脈弓部病變的診斷。
17例TAPVC患兒中,8例心上型,5例心內型,3例心下型,1例混合型;12例共同肺靜脈干回流途徑存在梗阻或合并小房間隔缺損(≤4 mm),甚至僅為卵圓孔未閉(圖2)。TAPVC患兒的平均經皮氧飽和度為77%(38%~89%)。術前7例患兒行CT檢查明確肺靜脈異常回流途徑,與超聲心動圖檢查結果均一致,無肺內靜脈狹窄。
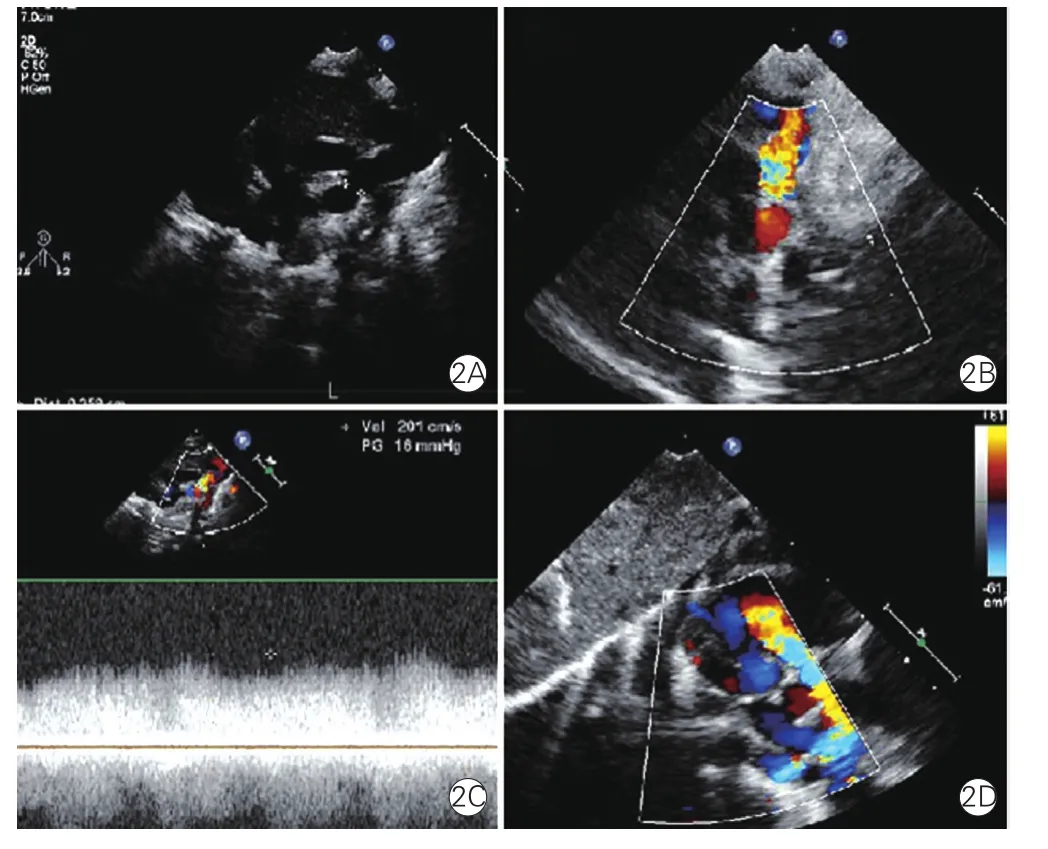
圖2 完全型心上型肺靜脈異位回流病例超聲心動圖結果
15例室間隔完整型肺動脈閉鎖的患兒中,5例出現右心室發育不良;13例重度肺動脈瓣狹窄的患兒中,1例合并右心室發育不良(圖3)。所有患兒均合并三尖瓣中度或以上程度反流,其中2例合并瓣葉發育不良、瓣葉狹窄或無啟閉功能。患兒的平均經皮氧飽和度為73%(45%~94%)。
9例單純主動脈弓離斷患兒中,6例為A型,3例為B型[4],均合并室缺及動脈導管未閉;15例重度主動脈弓縮窄患兒,降主動脈最窄處內徑2~4 mm,其中2例合并二尖瓣病變(傘型二尖瓣或瓣上狹窄)。患兒的平均經皮氧飽和度為93%(54%~100%)。14例患兒(5例主動脈弓離斷,9例主動脈弓縮窄)術前行CT檢查,與超聲心動圖檢查結果一致。
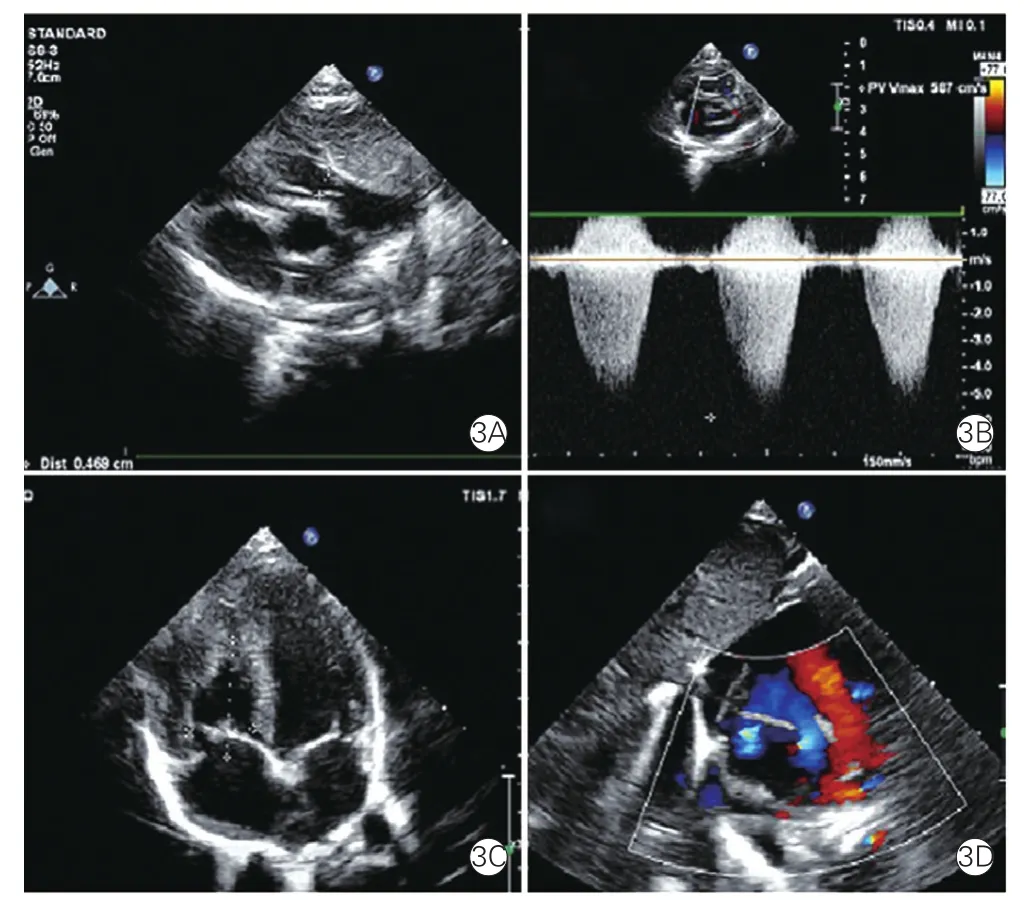
圖3 重度肺動脈瓣狹窄病例超聲心動圖結果
2例共同動脈干患兒,均為主肺動脈發自動脈干(Van Praaph A1型)[5],合并較大室缺(9 mm),均行CT檢查肯定超聲心動圖診斷;4例右肺動脈起源于升主動脈,室間隔均完整且合并動脈導管未閉。患兒的平均經皮氧飽和度為92%(80%~92%)。
2例肺動脈閉鎖和1例重度法樂四聯癥患兒,合并較大室缺,肺動脈發育極差。術前均行心血管造影,肯定超聲心動圖對肺動脈發育情況的診斷,左、右肺動脈內徑 2~4 mm(Z值 -3~-7.2),患兒發育滯后,紫紺嚴重,平均經皮氧飽和度為78%(65%~86%)。
最終共140例患兒接受手術治療(表2),其中非體外循環下手術26例,體外循環下手術114例。134例接受一期根治手術,4例接受姑息手術,2例接受分期根治手術。患兒手術時的平均年齡為(20.6±7.8)d(3~30 d),平均體重(3.5±0.6)kg(1.8~5.1 kg)。
11例(7.9%)接受手術的患兒院內死亡。129例(92.1%)患兒出院后接受臨床及超聲心動圖隨診。平均隨診時間(16.8±18.2)個月(1~62個月)。僅2例患兒接受二次手術:一例主動脈弓縮窄成形術后患兒3個月超聲心動圖復查顯示主動脈弓部再次狹窄,二次行主動脈弓部成形手術,術后隨診主動脈弓降部恢復通暢;另一例室間隔完整型TGA行大動脈調轉術及肺動脈瓣成形術,術后18個月超聲心動圖復查發現肺動脈瓣再次狹窄,二次行肺動脈瓣球囊擴張術,術后肺動脈瓣口峰值壓差下降。其余患兒康復良好。
表2 140例患兒術前診斷及手術情況(±s)

表2 140例患兒術前診斷及手術情況(±s)
術前診斷 例數 年齡(d) 體重(kg) 身高(cm) 手術類型完全性大動脈轉位(室間隔完整型51例,室間隔缺損型14例)65 19.4±7.3 3.5±0.5 51.2±2.8 大動脈調轉術完全性大動脈轉位,室間隔完整型 1 28 4.0 50 分期手術(一期行肺動脈環縮術及體肺動脈分流術,二期行大動脈調轉術)完全性大動脈轉位,室間隔缺損,主動脈弓縮窄 1 13 2.1 50 大動脈調轉術和主動脈弓部成形術完全性大動脈轉位,室間隔缺損,主動脈弓離斷 1 26 3.3 55 分期手術(一期行主動脈弓成形術及動脈導管縫合術,二期行大動脈調轉術及室缺修補術)完全型肺靜脈異位回流(12例回流途徑梗阻) 14 23.9±5.9 3.5±0.6 51.1±3.3 異位引流矯治術肺動脈閉鎖,室間隔完整型 14 14.3±7.7 3.4±0.5 50.6±2.5 單純肺動脈瓣球囊擴張術2例,肺動脈瓣球囊擴張術和改良體肺動脈分流術11例,姑息手術(改良體肺動脈分流術)1例重度肺動脈狹窄,室間隔完整型 11 19.3±7.1 3.7±0.5 47.1±7.8 單純肺動脈瓣球囊擴張術9例,肺動脈瓣球囊擴張術和改良體肺動脈分流術2例主動弓離斷或重度主動脈弓縮窄(主動脈弓離斷7例,主動脈弓縮窄14例)21 22.8±8.8 3.5±0.6 52.0±4.0 主動脈弓部成形術右肺動脈起源升主動脈 4 20.5±5.1 3.5±0.5 51.8±1.7 肺動脈異常起源矯治術共同動脈干 2 29.0±0.0 3.7±0.1 51.5±2.1 完全動脈干矯正術巨大室間隔缺損 1 30 3.8 54 單純室間隔缺損修補術右心房占位(三尖瓣口梗阻) 1 30 4.4 53 右心房腫物切除術肺動脈閉鎖,室間隔缺損 2 29.3±0.6 3.8±1.2 51.0±2.6 姑息手術(改良體肺動脈分流術)重度法樂四聯癥 1 30 3.3 50 姑息手術(改良體肺動脈分流術)
3 討論
新生兒出生后動脈導管日趨變細、閉合,使部分先心病在新生兒期成為致死性疾病。雖然近50年來先心病的診療及圍手術期管理水平顯著提高,但新生兒各個臟器未完全發育成熟,復雜的心外科手術以及暴露于體外循環下激發的炎性反應均會導致新生兒期心外科手術風險增高。所以術前更需通過超聲心動圖鑒別出新生兒期危重先心病,準確把握診斷要點,選擇手術時期,避免過早治療,也避免延誤治療而危及生命。
本研究中,TGA占據新生兒期危重先心病的一半,是最常見的在新生兒期需要緊急救治的先心病。該疾病因心室、動脈連接不一致,患兒全身器官處于缺氧狀態,所以動、靜脈血液混合越多,患兒越安全。但動脈導管在新生兒期趨于閉合,雖靜脈泵入前列腺素E1,但有時依然難以維持導管開放。當合并較大的室缺時,較多氧合血可以通過室水平分流進入主動脈,提高患兒混合血的氧合度;反之當室間隔完整時,患兒更危重。在本研究中,需要術前搶救的11例TGA患兒中,9例為室間隔完整型。所以術前超聲診斷TGA時,尤其需要關注室間隔情況,完整型或僅合并小房室間隔缺損的TGA更危重,更需要及早救治。此外,室間隔完整型TGA患兒在出生后隨著肺動脈阻力下降,與肺動脈相連的左心室內壓力也下降,導致左心室無法承擔動脈調轉術后的體循環壓,這種現象稱為解剖左心室退化[6]。超聲心動圖表現為收縮期室間隔明顯向左心室側偏移,呈壓低狀態,提示解剖左心室內壓力下降,還可測量二、三尖瓣反流速度,估算及比較解剖左、右心室收縮壓,當雙心室收縮壓比值<60%時,需通過手術環縮主肺動脈,增加解剖左心室后負荷,糾正左心室退化,一般術后一周再次行超聲心動圖評估,當雙心室收縮壓比值>60%時,室間隔運動基本恢復正常,再行大動脈調轉術。
排在新生兒期危重先心病第二位的為室間隔完整型肺動脈閉鎖或重度肺動脈瓣狹窄,約占總病例數的17.5%。因為經肺動脈瓣口無或極少血流入肺氧合,所以患兒嚴重缺氧、紫紺,應盡早實施球囊擴張術,解除瓣膜閉鎖或狹窄才是根本救治方法[7]。如果患兒合并右心室發育不良,單純瓣膜成形術后氧飽和度多不滿意,需加做改良體肺分流術,改善氧和[8]。術前超聲心動圖評估要點:(1)右心室的三部分腔室大小(流入部、流出部、心尖小梁部),心尖小梁部及流出部最易被異常肌束填充,嚴重發育不良病例超聲心動圖四腔心切面可觀察到右心室長徑遠小于左心室長徑,流入部變小,流出腔甚至呈縫隙樣;(2)三尖瓣瓣環大小,超聲心動圖測量二、三尖瓣瓣環直徑,同時計算Z值。正常情況三尖瓣瓣環應大于或至少等于二尖瓣瓣環,若所測值遠小于二尖瓣環,則證明三尖瓣瓣環發育不良;(3)三尖瓣瓣葉發育情況,預測術后三尖瓣反流情況;(4)冠狀動脈病變,尤其右心室依賴型冠狀動脈循環,這種情況多發生在嚴重右心室發育不良,三尖瓣瓣環發育差(Z值大多<-5)的病例。合并室缺的肺動脈閉鎖或法樂四聯癥多不在新生兒期行根治手術,只有在患兒頻繁缺氧發作時,才實施改良體肺動脈分流術,以避免缺氧意外發生。
本研究中處于第三位的新生兒期危重先心病為主動脈弓離斷或縮窄,約占患兒總數的15%。嚴重降主動脈病變會引發下肢及內臟缺血。所以本研究中2例主動脈弓離斷和3例主動脈弓縮窄患兒術前出現呼吸急促、嚴重酸中毒而接受搶救。此外,嚴重主動脈弓部病變會引發左心功能減低、重度肺動脈高壓,增加圍手術期死亡風險。Kreutzer等[9]指出,主動脈弓離斷患者合并發育小的主動脈瓣環或瓣葉畸形(如二瓣化)時,術后易出現左心室流出道狹窄,這與圓錐間隔病理性向后移位有關。所以術前超聲診斷主動脈弓離斷或縮窄時,觀察重點包括主動脈弓部病變位置及累及長度、分支動脈是否在病變部位發出、心臟功能及主動脈瓣發育情況。術前可行CT檢查明確主動脈弓部病變累及長度以及分支動脈情況。
另一種在新生兒期容易導致猝死、需急救的先心病為TAPVC,約占所有患兒的10.6%,回流途徑存在梗阻時尤為危重。梗阻部位包括肺靜脈總干、垂直引導靜脈或限制性房水平分流(小缺損甚至卵圓孔未閉)。所以本研究中術前搶救的5例患兒都是梗阻型TAPVC。Seale等[10]指出,術前嚴重的肺靜脈梗阻是術后肺靜脈狹窄發生及死亡的獨立危險因素,這可能和長時間的回流途徑梗阻導致肺靜脈分支發育不良有關。所以術前超聲心動圖需仔細追蹤檢查回流途徑中是否存在梗阻,房水平分流情況,術前可行CT檢查明確肺內靜脈發育情況。
其他類型先心病包括共同動脈干、右肺動脈起源于升主動脈、巨大室間隔缺損等會誘發少數患兒出現藥物難以糾正的心力衰竭,所以可選擇在新生兒期手術矯治。在行超聲心動圖檢查時,需結合臨床表現找出心力衰竭的病因,為臨床治療提供及時、準確的信息。
本研究中提到的八種先心病均為新生兒期致死性先心病,必須予以及時、準確的救治。術前超聲心動圖診斷至關重要,明確每一種危重先心病的術前診斷要點,才能提供合理的術前建議,制定最優的手術方式,從而提高新生兒期危重先心病的救治效果。
特別感謝盤錦市中心醫院李劍白醫師參與電話隨訪工作。

