不同發育階段湖羊生殖器官脂聯素受體與睪酮分泌關鍵基因表達模式及相關性研究
姚曉磊,黃欣愛,肖慎華,鄭臨楓,范麗潔,金宇月,劉孜斐,張艷麗,王 潔,王 鋒*
(1. 南京農業大學動物科技學院,南京210095; 2. 南京農業大學羊業科學研究所,南京 210095;3. 江蘇農牧科技職業學院,泰州 225300)
脂聯素(adiponectin,Adp)是由脂肪細胞特異分泌的因子,具有調節機體新陳代謝[1]、炎癥[2]和免疫應答[3]等生物學作用。Adp生物學功能的發揮是通過脂聯素受體 (adiponectin receptor,AdpR)介導完成的。迄今為止,已克隆出3種AdpR:AdpR1、AdpR2 和T-鈣粘蛋白(T-cadherin)。AdpR1和AdpR2在下丘腦[4]、垂體[5]、睪丸[6-7]、卵巢[8]中均有表達,提示下丘腦-垂體-性腺軸(hypothalamus-pituitary-gonad axis,HPG)可能是Adp發揮作用的重要靶器官。Ocon等[6]研究發現,AdpR1主要存在于公雞睪丸間質細胞、曲精細管管壁肌樣細胞,而AdpR2主要表達于間質細胞、支持細胞、精子細胞、精子中。同時,研究者也發現,AdpR1和AdpR2存在于牛精子中[9]。
睪丸間質細胞中存在AdpR1和AdpR2。提示Adp可能與睪酮(testosterone,T)分泌有關。人注射T后,血漿中Adp水平下降[10]。Tsou等[11]證實隨著男性青春期發育和T水平的增加,血漿中的Adp水平下降,說明T水平可能與Adp水平呈負相關,這一結論被Adamczak等[12]研究證實。但是,后來Landry等[13]研究發現,Adp能夠促進T的合成。這一結論也得到國內外相關研究證實[14-15]。關于血漿中Adp水平與T含量之間相關性仍然是個有爭議的問題。因此,明確Adp水平與機體T含量之間的關系具有重要的意義。
T合成與分泌受HPG的調節。這是由于下丘腦通過分泌促性腺激素釋放激素(gonadotropin releasing hormone,GnRH),最終作用于睪丸分泌T,促進睪丸的發育。AdpR1和AdpR2存在于下丘腦中,提示Adp可能通過介導下丘腦功能的發揮對HPG進行調節[16]。同時下丘腦分泌的促性腺激素抑制激素(gonadotropin inhibitory hormone,GnIH)負反饋抑制GnRH的分泌。據此推測,Adp可能與GnRH和GnIH之間存在一定的相關性。
目前關于AdpR1和AdpR2在生殖器官中的表達主要集中在嚙齒類和哺乳動物上,雖然已有研究表明,AdpR1和AdpR2在綿羊繁殖器官中表達[17],但二者在綿羊不同發育階段生殖器官中如何變化,還未見報道。因此,本研究以不同發育階段的湖羊為研究對象,采用qRT-PCR技術從mRNA水平探究AdpR1、AdpR2及T合成關鍵基因在不同發育階段湖羊生殖器官中的表達規律;采用ELISA技術測定不同發育階段湖羊血清中Adp、T、GnRH和GnIH含量,分析Adp與GnRH、GnIH、T及T合成關鍵基因的相關性;應用免疫組化技術將AdpR1在湖羊生殖器官中進行定位,為進一步研究AdpR1在性腺發育過程中如何發揮作用提供理論依據。
1 材料與方法
1.1 試驗動物及樣品采集
本試驗所需湖羊由江蘇省泰州市海倫羊業有限公司提供。選取3月齡((16.07±0.20)kg)、9月齡((40.07±2.75)kg)、24月齡((76.65±4.38)kg)發育正常的健康湖羊各5只,共15只,進行常規飼養管理。屠宰前禁食12 h,給予正常飲水,頸靜脈采血,3 000 r·min-1離心15 min,吸取上清,-20 ℃保存;屠宰后,采集下丘腦、垂體、睪丸、附睪頭、體、尾組織,迅速置于液氮中,-80 ℃保存;從每只羊的睪丸、附睪頭、體、尾的相同部位采集組織樣品,約0.5 cm×0.5 cm×0.2 cm,4.0%多聚甲醛固定。
1.2 試驗方法
1.2.1 ELISA檢測 嚴格按照綿羊脂聯素(Adp)、睪酮(T)、促性腺激素釋放激素(GnRH)、促性腺激素抑制激素(GnIH)ELISA試劑盒 (Kmals,上海)說明書分別測定不同發育階段湖羊血清中Adp、T、GnRH和GnIH濃度。
1.2.2 總RNA提取及反轉錄 按照Trizol Reagent試劑盒(Invitrogen公司,美國)說明書分別提取不同發育階段(n=5)湖羊下丘腦、垂體、睪丸、附睪頭、體、尾總RNA,DEPC水(Invitrogen,美國)溶解,核酸蛋白測定儀ND-2000(NanoDrop Technologies,美國)測定總RNA濃度和純度,同時采用1.5% 凝膠電泳檢測RNA質量。調整其濃度為1 μg·μL-1左右,反轉錄體系為40 μL,按照PrimeScript?RT reagent Kit With gDNA Eraser試劑盒(TaKaRa,大連)說明書進行操作。反轉錄產物cDNA -20 ℃保存。
1.2.3 引物設計與合成 根據NCBI上綿羊(Ovisaries)的相關基因序列,利用Primer 5.0軟件設計引物(表1),由南京擎科生物有限公司合成引物序列。

表1 用于qRT-PCR引物序列
1.2.4 qRT-PCR 以反轉錄的cDNA為模板,對AdpR1、AdpR2、LHR、StAR、3β-HSD、GAPDH基因進行qRT-PCR擴增。反應體系為20 μL:SYBR Green Master mix (Roche,德國)10 μL,上下游引物(10 μmol·L-1)各0.6 μL,cDNA 1 μL,ddH2O 7.8 μL。反應條件及步驟嚴格按照試劑盒說明書進行。
1.2.5 免疫組化 采用石蠟對已固定好的組織進行包埋,切片厚度為6 μm,37 ℃烤片24 h,常規脫蠟流程按照SABC試劑盒操作說明進行。其中,Rabbit anti-AdpR1(華安生物,杭州;1∶100),4 ℃過夜,PBS每5 min洗3次;Goat anti-Rabbit(博士德,武漢;1∶100),37 ℃ 30 min,用PBS每5 min洗3次;SABC(博士德,武漢;1∶100),37 ℃ 30 min,PBS每5 min洗3次。同時設置陰性對照,用PBS代替一抗,并用Nikon生物顯微鏡觀察。
1.3 數據分析
各目的基因相對表達量采用△△CT法計算,相對表達水平為2-△△CT,各目的基因相對表達量均應經GAPDH校正。其中各目的基因mRNA表達量分別以3月齡表達量均值為對照,其余(9和24月齡)以相對于對照的倍數作圖。比較AdpR1、AdpR2 mRNA 表達量時,以AdpR1 3月齡表達量為對照。其余月齡相對于其倍數作圖。數據采用SPSS 24.0 統計軟件進行分析,結果表示為“平均值±標準誤”。差異顯著性采用One-way ANOVA 和T-test分析,相關性分析采用Bivariate correlation進行,顯著水平為P<0.05。
2 結 果
2.1 AdpR1 在9月齡湖羊生殖器官中的定位
如圖1A所示,AdpR1 定位于湖羊睪丸間質細胞、精母細胞、精子細胞和曲精細管管壁肌樣細胞。在附睪頭、體、尾上皮細胞中均檢測到AdpR1陽性信號,即細胞核被DAB染成深色(圖1B~D);陰性對照未檢測到任何陽性信號,即細胞核沒有被DAB染色,因此細胞核為淺色(圖1E)。

A~D.睪丸、附睪頭、附睪體、附睪尾;E.陰性對照(A~C和E 400×;D 200×)。PMC.曲精細管管壁肌樣細胞;LC.間質細胞;Sc.精母細胞;St.精子細胞;PC.主細胞(上皮細胞)A-D.Testis, caput, corpus and cauda, respectively;E. Negative control (A-C,E 400×;D 200×). PMC. Peritubular myoid cells; LC. Leydig cells; Sc. Spermatocyte; St. Spermatid, PC.Principal cells圖1 9月齡湖羊生殖器官中AdpR1蛋白表達Fig.1 Immunohistochemical location of AdpR1 protein in the reproductive tracts of 9 month Hu sheep
2.2 不同發育階段湖羊血清中Adp、T、GnRH、GnIH含量的變化
由圖2可知,湖羊血清中Adp和T(結果已另文發表)含量呈先上升后下降趨勢,表現為性成熟后(9和24月齡)血清中Adp和T濃度顯著高于性成熟前(3月齡)(P<0.05),但9與24月齡間差異不顯著(P>0.05); 血清GnRH含量同樣呈先上升后下降趨勢,3和 24月齡差異不顯著(P>0.05);血清GnIH含量在湖羊9月齡時達到最高,24月齡時最低,其中3與9月齡差異不顯著(P>0.05),但顯著高于24月齡 (P<0.05)。

不同小寫字母表示不同月齡之間差異顯著(P<0.05)Values with different small letter superscripts mean significant difference among different ages (P<0.05)圖2 不同月齡湖羊血清中Adp、GnRH 和GnIH濃度的變化Fig.2 The concentrations of Adp, GnRH and GnIH in serum at different developmental ages of Hu sheep
2.3 AdpR1和AdpR2在不同發育階段湖羊性腺軸中mRNA 表達模式
采用qRT-PCR技術對不同發育階段湖羊性腺軸中AdpR1和AdpR2 mRNA表達規律的檢測結果如圖3所示。AdpR1和AdpR2 mRNA 在9月齡湖羊性腺軸組織中呈現不同的變化趨勢,二者在睪丸中的表達水平顯著高于其他組織(P<0.05,圖3A和3B);AdpR1 在睪丸和附睪尾中mRNA表達量隨月齡的增大而升高,均表現為性成熟后(9和24月齡) 顯著高于性成熟前(3月齡)(P<0.05,圖3C和3I),其中睪丸中AdpR1 mRNA表達量在9與24月齡 間差異不顯著(P>0.05,圖3C);AdpR1在不同月齡湖羊附睪頭和附睪體中mRNA表達量差異不顯著(P>0.05,圖3E和3G);AdpR2在不同月齡湖羊睪丸、附睪頭和附睪體中mRNA表達量差異不顯著(P>0.05,圖3D、3F和3H);AdpR2 mRNA在24月齡附睪尾中的表達量顯著高于3 和9月齡(P<0.05), 但3與9月齡差異不顯著(P>0.05,圖3J)。
2.4 AdpR1和AdpR2在不同發育階段湖羊睪丸中mRNA表達量比較分析
從圖4可知,各個月齡睪丸和附睪尾中AdpR1 mRNA表達量均顯著高于AdpR2 (P<0.05)(圖4A,D);雖然各個月齡附睪頭和附睪體中AdpR1 mRNA表達量均高于AdpR2,但差異不顯著(P>0.05)(圖4B,C)。
2.5 睪酮合成關鍵基因在不同發育階段湖羊睪丸中mRNA表達變化
由圖5可知,湖羊睪丸中LHR和StARmRNA的表現為先上升后下降趨勢,且各組之間存在顯著差異(P<0.05),二者都是以9月齡表達量最高,3月齡表達量最低;3β-HSDmRNA在不同發育階段湖羊睪丸中呈現出先上升后下降趨勢,且性成熟后(9和24月齡)顯著高于性成熟前(3月齡)(P<0.05),但9與24月齡之間差異不顯著(P>0.05)。
2.6 湖羊血清激素和相關基因的相關性分析
由表2可知,湖羊血清中T分別與Adp和GnRH水平顯著正相關(P<0.05);AdpR1 mRNA表達水平與StAR、3β-HSDmRNA表達水平顯著正相關(P<0.05)。雖然Adp含量與GnRH正相關,與GnIH負相關,但均差異不顯著(P>0.05)。
3 討 論
Adp作為一種具有多種生理功能的脂肪細胞因子,通過內分泌方式循環到血液中,繼而發揮各種功能。檢測血清Adp水平臨床上對胰島素抵抗[18]、卵巢綜合征[19]等疾病的發生進行預測。而且越來越多研究表明,脂聯素對動物的生殖功能具有重要影響[20-21]。本研究首先測定了不同發育階段湖羊血清Adp含量,結果發現,性成熟(9和24月齡)湖羊血清中Adp水平顯著高于性成熟前(3月齡)。李云等[22]研究發現,性成熟皖南花豬血清中Adp含量顯著高于性成熟前。這一現象與前人在公雞[6]上的報道一致。這說明Adp在動物機體發育過程中扮演著重要角色。
Adp功能的發揮需要通過其受體(AdpR1/2)介導來完成。前期研究表明,AdpR1和AdpR2在豬[14]、雞[6-7]、大鼠[23]睪丸中表達。本試驗首先利用免疫組化技術對AdpR1在睪丸和附睪中進行了定位,研究發現,AdpR1主要存在于睪丸間質細胞、精母細胞、精子細胞、曲精細管管壁肌樣細胞以及附睪頭、體、尾中的上皮細胞中。而Ocón-Grove等[6]研究發現,AdpR1主要表達于公雞睪丸間質細胞和曲精細管管壁肌樣細胞。這種差異可能與物種差異有關。附睪是精子成熟的場所,精子在附睪中的成熟不僅受到精子自身因素的作用,還受到附睪微環境的影響[24]。附睪上皮細胞能夠分泌種類不同的蛋白質及免疫抑制分子,以形成不斷變化的附睪微環境,精子在附睪內轉運過程中,附睪液與精子相互作用是精子逐步獲得成熟時所具備的功能[25]。已有研究發現,AdpR1 和AdpR2 在牛[9]和綿羊[26]精子中有表達。提示Adp可能對精子成熟有一定的影響,但具體機制還需要進一步研究。
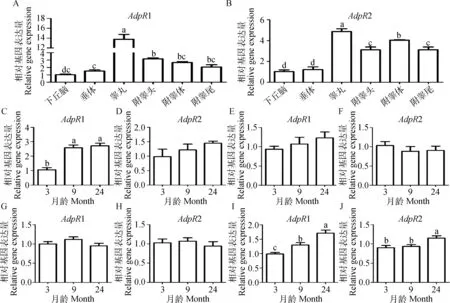
不同小寫字母表示不同組織或不同月齡之間差異顯著(P<0.05)。A、B.AdpR1和AdpR2在9月齡湖羊性腺軸中mRNA表達;C、E、G、I.AdpR1在不同月齡湖羊睪丸、附睪頭、體、尾中mRNA表達;D、F、H、J.AdpR2在不同月齡湖羊睪丸、附睪頭、體、尾中mRNA表達Values with different small letter superscripts mean significant different among different tissues or different ages (P<0.05)A, B.The mRNA expression of AdpR1 and AdpR2 in the gonadal-axis of 9 month Hu sheep, respectively. C, E, G, I.The mRNA expression of AdpR1 in the testis, epididymis caput, corpus and cauda at different developmental stages of Hu sheep, respectively; D, F, H, J.The mRNA expression of AdpR2 in the testis, epididymis caput, corpus and cauda at different developmental stages of Hu sheep, respectively圖3 AdpR1和AdpR2在不同月齡湖羊性腺軸中mRNA表達Fig.3 The mRNA expression of AdpR1 and AdpR2 in the gonadal-axis at different developmental stages of Hu sheep
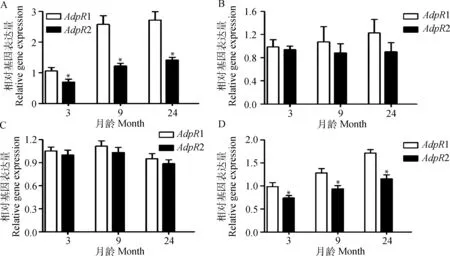
A~D.睪丸、附睪頭、體、尾。*.同一月齡AdpR1與AdpR2 mRNA間差異達顯著(P<0.05)A-D.Indicate testis, epididymis caput, corpus and cauda, respectively.*. Significant difference (P<0.05) between AdpR1 and AdpR2 mRNA abundance at the same ages圖4 AdpR1和AdpR2在不同月齡湖羊生殖器官中mRNA表達水平的比較Fig.4 Comparison of the mRNA expression levels between AdpR1 and AdpR2 in reproductive organs of Hu sheep at different developmental stages

不同小寫字母表示不同月齡之間差異顯著(P<0.05)Values with different small letter superscripts mean significant difference among different ages (P<0.05)圖5 LHR(A)、StAR(B)和3β-HSD(C)在不同月齡湖羊睪丸中mRNA表達水平Fig.5 The mRNA expression of LHR(A), StAR (B)and 3β-HSD (C) in the testis of Hu sheep at different ages

表2 不同月齡湖羊血清激素與相關基因的相關性分析
*表示縱向指標分別與橫向指標之間相比顯著相關 (P<0.05)
*indicate significant correlation between longitudinal indexes and horizontal indexes (P<0.05)
AdpR1 和AdpR2 mRNA 在綿羊睪丸和附睪有表達[17],但是二者在發育過程中是如何變化的,目前還未見報道。因此,本試驗進一步采用qRT-PCR技術探究了AdpR1和AdpR2 mRNA在不同發育階段湖羊睪丸和附睪中的表達模式。研究發現,AdpR1 mRNA在睪丸和附睪尾中表達量呈上升趨勢,且具有顯著的變化。這與前人發現的AdpR1 mRNA在不同發育階段雞[6]和皖南花豬[14]睪丸中變化趨勢一致。而AdpR2 mRNA在附睪尾中呈上升趨勢,而在其他生殖器官中無顯著變化。同時,筆者發現AdpR1 mRNA表達量在睪丸和附睪中表達量均高于AdpR2,其中AdpR1 mRNA在睪丸和附睪尾中具有顯著變化。提示Adp在睪丸和附睪中的作用主要通過AdpR1介導。
AdpR1在睪丸間質細胞中表達,推測Adp可能對T的生成有一定的影響。T的合成受HPG調節。而下丘腦是HPG的主要控制中心,通過分泌GnRH和GnIH對動物機體生殖功能進行調節。筆者進一步檢測了不同發育階段血清中T[27]、GnRH和GnIH含量發現,血清中T含量表現為性成熟后(9月齡)顯著高于性成熟前(3月齡),而GnRH和GnIH均表現為9月齡最高。這可能是由于湖羊在性成熟過程中,隨著血清中GnRH含量的增加,經過一系列內分泌調節,導致T含量升高,進而促進睪丸發育,當T含量積累到一定程度,就會反饋抑制GnRH的釋放,進而導致GnIH升高。而當湖羊達到24月齡后,睪丸已經發育完全,對T的依賴性有所減弱,進而導致GnRH和GnIH降低。前期研究表明,隨著男性青春期的發育和T水平的增加,血漿Adp水平下降[11]。這說明Adp與T含量之間有一定的相關性。但也有研究卻得出相反結論,Adp對T的生成有促進作用[13,15]。本研究發現,在特定的發育階段,血清中Adp和T含量顯著正相關,說明Adp能夠促進T生成,這一發現與邵康等[14]在皖南花豬上研究一致。前期研究已證實,Adp能夠抑制下丘腦GT1-7神經細胞GnRH的分泌[28]。李云等[22]研究表明,Adp與GnRH顯著負相關。但是,本研究發現,Adp與GnRH呈正相關。這可能與本研究選取的湖羊發育階段跨度太大有關。因此,二者相互作用關系還需要進一步研究證實。
T合成途徑中也受多種類固醇合成酶的調控。StAR和3β-HSD是睪丸間質細胞中類固醇激素合成途徑的2個最重要的限速酶[29]。StAR和3β-HSDmRNA表達量的高低直接影響T的生成[30]。本研究發現,StAR和3β-HSDmRNA在9月齡 表達量最高,表明此階段是T快速合成時期。StARmRNA顯著變化與邵康等[14]發現在皖南花豬性成熟前后表達趨勢一致。如前所述,AdpR1 mRNA 在睪丸中有顯著的變化,表現為性成熟后(9和24月齡)顯著高于性成熟前(3月齡)。且AdpR1分別與StAR和3β-HSDmRNA 表達量顯著正相關。在特定的發育階段,AdpR1與T合成限速酶有類似的表達量上升模式,提示它們有協同升高T的相互作用。
4 結 論
AdpR1 mRNA表達量在不同發育階段湖羊生殖器官中具有顯著性變化,且在各個階段睪丸和附睪尾中均顯著高于AdpR2,提示Adp在湖羊生殖器官中的作用主要由AdpR1介導。同時,AdpR1與StAR和3β-HSDmRNA 表達量顯著正相關,提示AdpR1介導Adp在湖羊睪丸發育過程中促進T生成。

