基于GC-MS代謝組學技術對葉酸調控雞原代肝細胞代謝的研究
劉艷利,孫文強,韓 迪,段玉蘭,楊 欣,楊小軍
(西北農林科技大學動物科技學院,楊凌 712100)
家禽通過肉、蛋為人類提供了大量的蛋白來源,近些年來,家禽育種工作一直在進步,但關于家禽的營養需要標準過于陳舊,使得日糧配制所參考的營養需要標準與目前動物機體真正所需要的標準之間在某種程度上存在一定偏差,再加上高度集約化養殖中不可避免的存在的環境管理問題等,導致現階段家禽養殖中面臨很多諸如動物抗應激能力差、免疫功能低下、出現未知代謝性疾病等問題。
肝是機體重要的代謝器官,在營養物質合成、轉運和儲存,以及外源物質的代謝解毒等方面均發揮重要作用[1]。因此,原代肝細胞體外培養是動物代謝、藥理和毒理學研究的良好模型,小鼠原代肝細胞被用來研究納米金屬氧化物對其脂代謝的影響[2],魚的肝細胞被分離培養用來進行藥物毒理學研究[3],雞的原代肝細胞也被用來進行研究藥物代謝、毒物耐受等[4-6]。葉酸是水溶性的B族維生素,有研究表明,胚胎期注射葉酸可通過改變表觀遺傳修飾來影響基因表達,促進胚胎發育[7],改善免疫功能,進而促進肉雞生產性能的提高[8]。Allah和Badary[9]研究指出,葉酸可通過降低炎癥因子的表達和脂質的過氧化來緩解乙酸鉛所誘導的肝細胞損傷。除此之外,葉酸也參與調控雞原代肝細胞脂質代謝相關基因的表達[10]。綜上可知,葉酸參與影響機體的很多代謝過程。
近些年來,組學技術的快速發展和應用為解析科學中的生物學本質進程提供了很多便捷,代謝組學可以檢測到一系列低分子量的代謝小分子,為明晰機體特定時間下具體發生的代謝變化指出精準的方向。本試驗以雞原代肝細胞為研究對象,通過給予不同葉酸含量的培養基進行處理,并借助GC-MS技術對細胞進行代謝組檢測,旨在探究葉酸對雞原代肝細胞代謝的影響,為葉酸參與細胞代謝的調控機制及其在家禽養殖中的合理有效應用提供理論基礎和科學依據。
1 材料與方法
1.1 主要試劑和儀器
葉酸和膠原酶IV購自Sigma公司;RPMI 1640無葉酸培養基以及青鏈霉素(雙抗)購自Gibco公司;胎牛血清購自南美BIOWEST公司;雞淋巴細胞分離液購自天津灝洋生物制品科技有限公司。試驗儀器主要有:細胞培養六孔板(美國康寧公司)、CO2培養箱、搖床、倒置顯微鏡等。
1.2 試驗設計及樣品收集
從陜西楊凌巨隆禽業有限公司購買1日齡剛出殼健康海蘭褐公雞,解剖獲取肝,并分離得到雞原代肝細胞,具體方法參照本團隊前期的報道[10],分離得到的細胞經形態和染色鑒定符合肝細胞的特性,可用于后續試驗,且本試驗中所用的葉酸添加劑量并未對細胞產生毒性作用[10]。待細胞長至鋪滿板底80%左右時,開始換處理培養基,分別為對照組(A組,無葉酸培養基)和葉酸添加組(C組,15 mg·L-1葉酸),每個處理6個重復,處理時間為12 h。處理完成后,吸除培養基,用PBS緩沖液清洗細胞3次,再加入 250 μL冰冷的甲醇,用細胞刮將細胞刮下來并移入 1.5 mL離心管中,再加入等體積的水清洗培養皿,并移入離心管,與甲醇溶液混合后超低溫冰箱凍存,以供代謝組學檢測。同樣的細胞培養處理方法,胰酶消化后清洗收集細胞沉淀,并凍存待測細胞內物質含量。
1.3 樣品預處理
將含有500 μL 50%甲醇的混合溶液在冰水浴中超聲15 min,然后-20 ℃靜置24 h,離心(12 000 r·min-1,4 ℃,15 min)。取180 μL上清液于GC衍生瓶中,加入10 μL內標(0.05 mg·mL-113C3-15N-L-alanine、13C5-15N-L-valine和13C6-15N-L-isoleucine),在溫和氮氣下干燥。向衍生瓶中加入30 μL 20 mg·mL-1的甲氧胺鹽酸鹽吡啶溶液,充分振蕩30 s,于37 ℃孵育90 min。向衍生瓶中加入30 μL的BSTFA(含1%TMCS),于70 ℃孵育60 min,室溫冷卻后,待GC-MS代謝組學分析。
1.4 GC-MS檢測及數據分析
氣相色譜和質譜分析委托上海譜領生物科技有限公司進行,具體設備型號、GC-MS檢測條件以及數據分析方法參照劉雪蓮等[11]的描述。
1.5 雞原代肝細胞差異代謝物的篩選與鑒定
在峰面積標準化的過程中,差異代謝物的篩選標準是OPLS-DA(VIP>1)和雙尾Student’sT檢驗(P<0.05)。差異代謝物的鑒定根據其已純化的質譜,通過比對儀器自帶的數據庫(NIST)以及商業的Golm Metabolome Database和Fiehn GC/MS Metabolomics RTL Library,最終確定其結構。
1.6 雞原代肝細胞脂類生化指標測定及數據分析
細胞內三酰甘油、游離脂肪酸及總膽固醇的含
量采用商品化的試劑盒測定,試劑盒購自南京建成生物有限公司。各指標數據用“mean±SEM”表示,用SPSS統計軟件進行分析。組間差異比較采用獨立樣本T檢驗,P<0.05表示差異顯著。
2 結 果
2.1 雞肝細胞GC-MS代謝組多元統計分析
采用SIMCA軟件(版本13.0)對兩組樣本進行多元統計分析,如圖1A所示,建立的含2個有效主成分的PCA模型累積解釋率R2X=0.573;圖1B建立的含2個有效主成分的PLS-DA模型中,R2Y=0.992,Q2=0.934(當前模型的參數值不看R2X值);圖1C建立的含1個主成分和2個正交成分的OPLS-DA模型中,模型主要質量參數為R2Y=0.998, Q2=0.857(當前模型的參數值不看R2X值)。各個模型中,兩組之間有明顯的分離,組內重復聚集緊湊,表明重復性較好。圖1D是對OPLS模型的置換檢驗結果,R2接近1,說明建立的模型符合樣本數據的真實情況,可以很好地解釋兩組樣本之間的顯著代謝差異,但對照組A中有一個樣品偏離其他組內樣品。
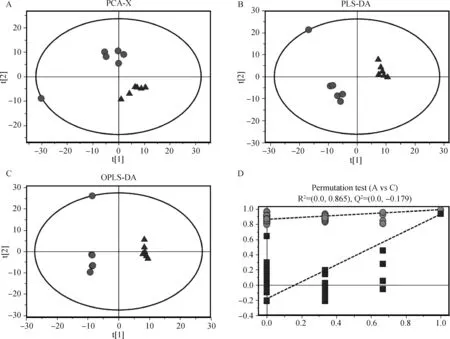
A、B、C分別代表樣本的PCA、PLS-DA和OPLS-DA得分圖:圓形代表對照組A組的6個樣本,三角形代表葉酸添加組C組的6個樣本;橫坐標表示第1主成分即PC1,用t[1]表示;縱坐標表示第2主成分即PC2,用t[2]表示。D圖是OPLS模型的置換檢驗:橫坐標表示置換檢驗的置換保留度(1處的點即為原模型的R2和Q2值),縱坐標表示R2或Q2的取值,圓點表示置換檢驗得到的R2值,方點表示置換檢驗得到的Q2值A, B, C show the samples score plots of PCA, PLS-DA and OPLS-DA, respectively: circles mean 6 samples in the control group and triangles mean 6 samples in folic acid addition group; X-axis show the first principal component, t[1], Y-axis show the second principal component, t[2]. D means the permutation test for OPLS-DA model: X-axis show the displacement retention (the point at 1 is R2 and Q2 values of OPLS-DA model), Y-axis mean the value of R2 or Q2, circles are on behalf of R2 value for permutation test and squares for Q2 value圖1 兩組樣本得分圖Fig.1 Samples score plots of two groups
2.2 雞肝細胞內差異代謝物篩選
采用OPLS-DA模型第一主成分的VIP值(閾值>1)并結合Student’sT檢驗(P<0.05),根據數據庫尋找差異性表達的代謝物。如表1所示,葉酸添加組與對照組相比,共檢測到32個差異代謝物,其中23個顯著上調,9個顯著下調。為了表征兩組差異代謝物之間的聚落關系,對這些差異性物質的定量信息進行熱圖分析,如圖2所示,每行表示差異性代謝物,每列表示樣本編號,從熱圖分析組內各重復的顏色也可看出樣品重復性較好,左側的樹狀結構表示差異性代謝物之間相似度聚類關系。
表1雞肝細胞葉酸組與對照組之間的差異代謝物
Table1Differentialmetabolitesbetweencontrolandfolicacidgroupsofchickenhepatocytes

差異代謝物Differential metabolite變量投影重要性1VIP1P值2P-value2變化趨勢3Change trend3α-酮戊二酸 2-ketoglutaric acid1.440.034 5↑葡萄糖Glucose1.610.014 2↑3磷酸甘油酸 3-phosphoglyceric acid1.370.047 4↑4磷酸赤蘚糖Erythrose-4-phosphate1.810.003 5↑天冬酰胺Asparagine1.850.002 4↑半胱氨酸Cysteine1.500.026 0↑腐胺Putrescine1.440.034 7↑天冬氨酸Aspartic acid1.630.011 9↑鳥氨酸Ornithine1.920.001 2↑蔗糖Sucrose1.550.019 5↑焦谷氨酸Pyroglutamic acid1.400.040 7↑賴氨酸Lysine1.370.045 9↑煙酰胺Nicotinamide1.720.006 5↑阿拉伯糖醇Arabitol1.800.003 5↑來蘇糖Lyxose1.680.009 2↑葡萄糖醛酸Glucuronic acid1.660.010 3↑次黃嘌呤核苷酸IMP1.370.045 8↑果糖Fructose1.380.044 2↑2羥谷氨酸 2-hydroxyglutaric acid2.310.000 0↑二甲基精氨酸ADMA1.360.048 4↑半乳糖醛酸Galacturonic acid1.420.037 5↑甘油醛Glyceraldehyde1.500.025 6↑蘇糖醇Threitol1.670.009 3↑乙醇胺Ethanolamine1.750.005 3↓3磷酸甘油Glycerol-3-phosphate1.430.035 8↓2磷酸甘油Glycerol-2-phosphate1.720.006 7↓蘇氨酸Threonine1.680.009 2↓丙氨酸Alanine1.570.017 7↓二甲基丁二酸Itaconic acid1.990.000 5↓絲氨酸Serine1.440.033 3↓甲基磷酸Methylphosphate1.450.032 2↓甲基琥珀酸Methylsuccinic acid1.680.086 0↓
1. VIP為變量投影重要性,從OPLS-DA模型獲得;2.P值由T檢驗得來;3.“↑”表示葉酸組的代謝物水平高于對照組,“↓”表示葉酸組的代謝物水平低于對照組
1. VIP is variable importance in the projection, is obtained from the OPLS-DA model;2. ThePvalue is calculated from Student’sTtest;3. “↑” means that metabolite level in folic acid group is higher than that in control group;“↓”means that metabolite level in folic acid group is lower than that in control group
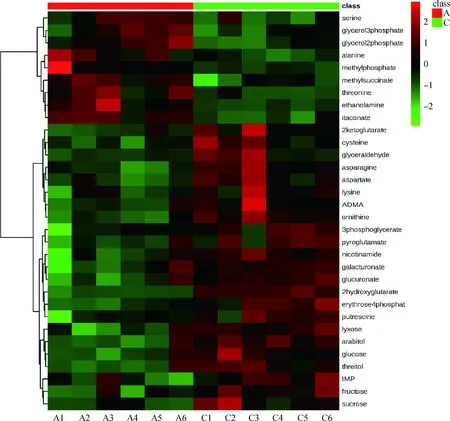
圖2 雞肝細胞對照組和葉酸組差異代謝物的熱圖Fig.2 Heatmap of differential metabolites between control and folic acid groups of chicken hepatocytes
2.3 雞肝細胞內差異代謝物相關性及通路分析
代謝物之間濃度的相關性和功能的相關性分別通過Pearson(圖3A)和Spearman(圖3B)相關進行分析,圖3A中的橫縱坐標為差異代謝物,綠色表示負相關,紅色表示正相關,顏色越深表明兩個代謝物在濃度上變化趨勢相似性越高。圖3B中粉色連線代表正相關,藍色代表負相關,同一彩色圓圈內的差異代謝物表示在功能上屬于同一分類。為了進一步解析葉酸對肝細胞代謝的影響,將差異代謝物輸入MetaboAnalyst軟件進行通路分析,結果顯示,共富集到31條通路,其中顯著的有19條,綜合分析圖3C顯示了通路的影響大小及相關P值,圓點越大表明該通路富集到的差異代謝物越多,顏色越深表明P值越小,離坐標圓點越遠表明該通路受到的影響越大。可見葉酸主要影響雞原代肝細胞代謝的氨基酸類通路、碳水化合物通路、甘油酯通路等。
2.4 葉酸對雞肝細胞內脂類物質含量的影響
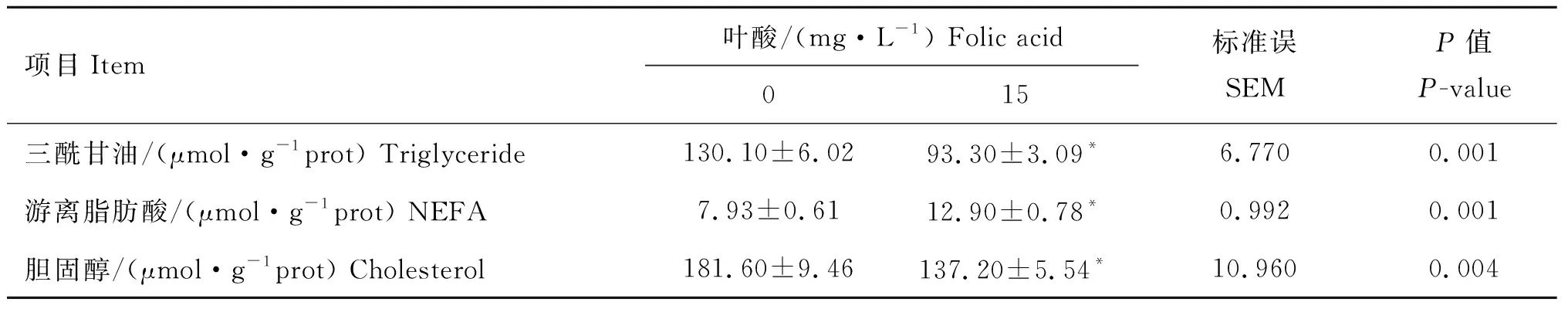
如表2所示,與對照組相比,培養基中添加葉酸能顯著降低雞原代肝細胞內的三酰甘油和膽固醇含量(P<0.05),除此之外,葉酸組游離脂肪酸的含量也顯著高于對照組(P<0.05)。
3 討 論
代謝組最接近機體的本質生物學過程,較基因組、轉錄組和蛋白組更能直接靈敏地反映機體真正的代謝變化,已被廣泛的應用于生命科學研究中。本試驗基于GC-MS技術,檢測了不同葉酸含量培養基下雞原代肝細胞內的代謝物變化,結果顯示,共有32種代謝物含量表現出了差異。根據差異代謝物本身所屬的分類及其所富集的通路分析,可以說明葉酸改變了細胞內的糖代謝、氨基酸代謝和脂類代謝,下面將逐一進行討論。

圖A表示各差異性代謝物之間的(濃度)相關性;圖B表示各差異性代謝物功能上的相關性;圖C是差異代謝物的富集通路分析Figure A is the correlation among differential metabolites in terms of concentration; Figure B is the correlation among differential metabolites in terms of functions; Figure C is the KEGG pathway analysis based on differential metabolites圖3 雞肝細胞差異代謝物的相關性分析與代謝通路分析Fig.3 Correlations and pathway analysis of differential metabolites between control and folic acid groups of chicken hepatocytes
表2葉酸對肝細胞內三酰甘油、游離脂肪酸和總膽固醇含量的影響
Table2Effectsoffolicacidontriglyceride,NEFAandcholesterolcontentsinchickenhepatocytes
項目Item葉酸/(mg·L-1) Folic acid015標準誤SEMP值P-value三酰甘油/(μmol·g-1prot) Triglyceride130.10±6.0293.30±3.09*6.7700.001游離脂肪酸/(μmol·g-1prot) NEFA7.93±0.6112.90±0.78*0.9920.001膽固醇/(μmol·g-1prot) Cholesterol181.60±9.46137.20±5.54*10.9600.004
*. 代表兩組之間差異顯著(P<0.05)
*. Means the significant difference between control and folic acid groups (P<0.05)
糖代謝是機體最重要的代謝之一,其中葡萄糖可氧化供能,糖酵解的終產物丙酮酸是連接三大營養物質糖、脂肪和蛋白質的重要樞紐,三羧酸循環的中間產物也可與氨基酸之間進行互相轉化[12]。本試驗中,葉酸添加組的α-酮戊二酸、葡萄糖、蔗糖、阿拉伯糖醇、來蘇糖、葡萄糖醛酸、半乳糖醛酸、果糖、蘇糖醇含量升高,通路分析中富集到了淀粉與蔗糖代謝、戊糖與葡萄糖醛酸酯互變、半乳糖代謝等碳水化合物類的代謝,表明葉酸影響了肝細胞內的糖類代謝過程。3-磷酸甘油酸是糖酵解中氧化放能過程的產物之一,其含量的升高與葡萄糖含量的升高相對應,揭示細胞內糖酵解過程的加強,但終產物丙酮酸的含量并沒有改變,這可能與其進入三羧酸循環代謝有關,因為α-酮戊二酸升高,表明細胞內檸檬酸循環過程也加強,兩者共同為細胞提供能量來源,代謝過程的中間產物也為糖醇、醛酸等小分子糖類物質的生成提供可能。
葉酸本身的生理代謝過程也涉及到很多氨基酸,甘氨酸和絲氨酸參與四氫葉酸與5,10亞甲基四氫葉酸的可逆轉化過程,蘇氨酸和甘氨酸參與5,10亞甲基四氫葉酸到5甲基四氫葉酸的非可逆轉化,5甲 基四氫葉酸為同型半胱氨酸提供甲基基團生成蛋氨酸[13]。本試驗中,葉酸添加組天冬酰胺、半胱氨酸、天冬氨酸和賴氨酸含量升高,蘇氨酸、丙氨酸和絲氨酸含量下降。丙氨酸可由丙酮酸轉化而來,糖酵解的加強并沒有改變丙酮酸的含量,反而丙氨酸的含量是下降的,進一步說明了糖酵解的終產物丙酮酸主要是進入三羧酸循環過程進行代謝。α-酮戊二酸和草酰乙酸分別是谷氨酸和天冬氨酸的前體物質,三羧酸循環加強但草酰乙酸濃度不變,可能是因為草酰乙酸用來轉化生成天冬氨酸和天冬酰胺。雖然細胞中谷氨酸的含量未受到影響,但葉酸組焦谷氨酸的含量增加,有研究指出,焦谷氨酸可能是甘氨酸和α-氨基丁酸的前體物質[14],參與碳水化合物和脂質代謝過程[15]。
通路分析顯示,氨酰轉移RNA生物合成是細胞受到影響最大的通路,并且差異代謝物也富集到了丙氨酸、天冬氨酸和谷氨酸代謝通路,甘氨酸、絲氨酸和蘇氨酸代謝通路,精氨酸和脯氨酸代謝通路,半胱氨酸和蛋氨酸代謝通路。半胱氨酸是谷胱甘肽的前體物[16],有研究指出,谷胱甘肽可清除自由基,有利于肝細胞損傷的修復[17]。葉酸本身也是一種抗氧化劑[18],可以清除自由基防止脂質的過氧化[19],因此,在該試驗中,葉酸有可能提高了細胞的抗氧化功能,也有研究表明,葉酸能降低動脈粥樣硬化鼠血液中的同型半胱氨酸含量,進而提高機體的抗氧化性能[20]。
另一方面,與哺乳動物不同,家禽的脂質代謝過程主要發生在肝中[21]。有學者基于甲基化作用從肉毒堿合成、磷脂酰膽堿合成、小RNA和脂代謝相關基因表達上闡述了葉酸調控肝脂質代謝的機制[22]。本試驗所鑒定到的差異代謝物3磷酸甘油酸、3磷酸甘油、2磷酸甘油、乙醇胺、甘油醛均參與脂代謝通路,甘油酯與甘油磷脂代謝也是通路分析所富集到的被顯著影響的通路。李呂木和Peebles[23]的研究指出,在雞胚發育的后1周,蛋中碳水化合物消化殆盡,卵黃囊被吸收入肝內,肝內的脂質含量持續增加,在出殼當天達到最高。并且在雛雞出殼后的第1周,采食量低但生長快,主要依靠肝的脂質代謝為機體提供營養和能量以供生長發育的需要[24]。因此雛雞1日齡肝本身脂質含量多、代謝旺盛。本研究結果顯示,葉酸添加組肝細胞中三酰甘油水解加強,膽固醇含量下降,游離脂肪酸含量增加,表明脂質分解代謝加強,脂肪酸氧化供能,甘油通過糖異生作用進入糖酵解和三羧酸過程。母鼠缺乏葉酸能影響子代胎鼠肝內的脂質代謝[25],與本試驗中葉酸改變肝細胞脂代謝的現象一致。
4 結 論
本研究基于GC-MS代謝組學技術分析葉酸對雞原代肝細胞代謝物變化及代謝通路的影響,共鑒定到32個差異代謝物,代謝通路分析及細胞內的脂類含量結果顯示,葉酸促進甘油三酯水解,改變了細胞內的糖代謝和氨基酸代謝,也一定程度上提高了細胞的抗氧化性能。研究結果為今后探究葉酸調控家禽肝代謝機制提供參考,也為葉酸在家禽上的合理有效應用提供理論基礎和科學依據。

