HCG在小鼠卵母細胞體外受精胚胎發育過程中的作用
邢雅欣,解其貴,楊志勇,劉玉兵,王玲,千日成*
(1.南通大學醫學院,南通 226000;2.上海市第十人民醫院生殖醫學中心,上海 200072)
在過去的十幾年中,胚胎培養體系得到了很大的改善,但它還是沒有完全模擬體內的環境條件,由此體外培養形成的胚胎質量還是不如體內形成的胚胎質量。然而體外條件下,種植前的胚胎會分泌一些因子來對抗不利的培養條件,因此很多研究在胚胎培養液中添加一些胚胎分泌的因子以改善培養條件,以提高體外培養胚胎質量[1]。
HCG是胚胎最早分泌的分子信號之一[2-3],受精后第2天即可檢測到HCG mRNA的表達以及分泌[4]。并且植入前胚胎分泌HCG的量與胚胎質量相關[5]。HCG和黃體生成素(LH)結構功能相近,同屬糖蛋白超家族,與相同的受體(LHCGR)結合引起下游反應。LHCGR是一種膜受體,屬于G蛋白偶聯受體超家族。Dinopoulou等[6]研究發現LHCGR表達于小鼠卵母細胞體外成熟(IVM)的各個階段以及體外受精之后合子、胚胎早期發育的各個時期。研究還發現除了在IVM培養液中添加HCG可以促進卵母細胞體外成熟之外,在受精和胚胎發育培養液中添加HCG對卵母細胞體外受精和胚胎發育有益。但是該研究未進行更深一步的分子生物學驗證,也未觀察HCG對常規體內成熟卵母細胞的體外受精及胚胎發育是否有影響。
本研究以小鼠體內成熟卵母細胞為研究對象,通過在體外受精及胚胎培養液中加入與Dinopoulou研究中相同濃度的HCG(1 500 U/L)進行體外受精和胚胎培養后,對其受精率、卵裂率和囊胚形成率以及囊胚內細胞團(ICM)、滋養層(TE)以及囊胚細胞總數,囊胚質量相關基因[基因多能性八聚體結合蛋白4(Oct4)、分化相關基因尾端型同源盒2(Cdx2)、氧化應激相關基因錳超氧化物歧化酶(MnSOD)、侵襲相關基因基質金屬蛋白酶9(Mmp9)]的表達情況進行了比較,為探討HCG在受精及胚胎發育過程中的作用,為進一步研究胚胎發育機制、優化胚胎體外培養體系提供理論和實驗依據。
材料和方法
一、材料
1.實驗動物:雌性4~6周、雄性8~10周ICR小鼠,SPF級,購自北京維通利華實驗動物技術有限公司。在穩定、標準化的實驗動物環境中飼養:溫度20~26℃,濕度40%~70%,光照/黑夜12/12 h,自由進食飲水。動物實驗通過上海市第十人民醫院實驗動物倫理委員會批準。
2.試劑和儀器:孕馬血清促性腺激素(PMSG,赤峰博恩藥業),HCG(珠海麗珠),受精液(HTF)、胚胎培養液(KSOM)、精子獲能液(TYH)(南京愛貝生物),胎牛血清(FBS)、M2操作液、礦物油(Sigma,美國),35 mm胚胎培養皿(Corning,美國),微量RNA抽提試劑盒、微量反轉錄試劑盒、Real time RT-PCR試劑盒(QIAGEN,美國),小鼠Cdx2抗體(Biogenex,美國),Alexa Fluor 488標記的兔抗小鼠二抗(Invitrogen,美國),DAPI染色液(上海碧云天),7900熒光定量PCR儀(ABI,Prism,美國),C2激光共聚焦顯微鏡(Nikon,日本)。
二、研究方法
1.實驗分組:依據培養液中HCG濃度分為對照組和HCG組,對照組的受精液HTF和胚胎培養液KSOM中HCG濃度為0 U/L,HCG組的受精液HTF和胚胎培養液KSOM中HCG濃度為1 500 U/L。配制的培養液需在培養箱(37℃、6% CO2、5%O2)中平衡過夜。
2.小鼠IVF:4~6周齡ICR雌性小鼠,每只腹腔注射10 U PMSG,48 h后注射10 U HCG,16~18 h后頸椎脫臼法處死小鼠,打開腹腔,無菌條件下取出雙側輸卵管于M2操作液中,體視顯微鏡下用1 ml無菌注射器針頭劃破輸卵管膨大處,使卵冠丘復合物(COCs)完全釋放出來,立即轉入HTF受精液中,加入提前在TYH獲能液中孵育1 h的精子。受精6 h后用HTF液洗滌受精卵,記錄受精情況,將形態正常的受精卵在KSOM液中繼續培養,在24 h和96 h觀察并計算2-細胞、囊胚的發育情況。
3.RT-qPCR檢測囊胚中相關基因的表達:采用RT-qPCR檢測HCG組和對照組囊胚相關基因mRNA表達水平,以GAPDH作為內參。各基因引物序列如表1所示。將HCG組、對照組囊胚吸出,PBS中洗滌后按照微量RNA提取試劑盒說明書提取各組總RNA后,立即用微量反轉錄試劑盒反轉錄成cDNA,用于RT-qPCR,體系如下:QuantiNova SYBR Green PCR Master Mix(2×)10 μl、QN ROX Reference Dye 2 μl、Primer Forward(10 μmol/L)1.4 μl、Primer Reverse(10 μmol/L)1.4 μl、cDNA 2 μl,余下用ddH2O補齊至20 μl。反應條件:兩步法PCR擴增標準程序:預變性95℃ 2 min,PCR反應95℃ 5 s、60℃ 30 s,共40個循環。待反應結束后確認擴增曲線和融解曲線。將目的基因與內參的所得結果相比,所得的比值為目的基因的相對表達量,結果以2-△△Ct表示。每20枚囊胚為一份樣本,每組各收集3份,共6份樣本。
4.囊胚免疫熒光標記:(1)在室溫條件下,將囊胚用1% BSA-PBS洗3次,每次10 min,然后移入4%多聚甲醛液中固定30 min;(2)固定完成后1% BSA-PBS中洗2次;(3)將固定后的囊胚移入含有 0.15%~0.25% Triton X100的1% BSA-PBS室溫1 h,1% BSA-PBS中洗滌2次;(4)將囊胚移入小鼠Cdx2抗體稀釋液中(稀釋比為1∶100),4℃過夜,1% BSA-PBS中洗滌2次;(5)將囊胚移入Alexa Fluor 488標記的二抗稀釋液(稀釋比為1∶500),室溫遮光1 h,1% BSA-PBS中洗滌2次;(6)將囊胚移入DAPI染色液滴中,室溫遮光孵育5 min,1% BSA-PBS中清洗;(7)在玻璃底的培養皿內做若干 1% BSA-PBS 的液滴,并用礦物油覆蓋,將染色完成的胚胎移入皿中,激光共聚焦顯微鏡下進行觀察計數并拍照。觀察囊胚ICM、TE數以及囊胚細胞總數。
5.觀察指標:受精率=雙原核1-細胞數/成熟卵母細胞數×100%,2-細胞率=2-細胞總數/1-細胞總數×100%,囊胚形成率=囊胚數/1-細胞總數×100%。
三、統計學分析
采用SPSS 20.0統計軟件對數據進行分析。目的基因mRNA表達以(±s)表示,采用單因素方差分析。P<0.05為差異有統計學意義,P<0.01為差異有極顯著統計學意義。
結 果
一、對照組和HCG組胚胎體外發育情況
對照組和HCG組小鼠卵母細胞體外受精6 h后去除周圍的顆粒細胞及精子,觀察雙原核細胞數量,24 h、96 h觀察胚胎發育情況,并計算受精率、2-細胞率、囊胚形成率。結果顯示,HCG組的受精率、2-細胞率以及囊胚形成率與對照組相比較,差異無統計學意義(P>0.05)(表2)。

表2 小鼠胚胎體外發育情況[n(%)]
二、兩組囊胚質量相關基因mRNA的表達相對水平比較
HCG組相關基因Cdx2、MnSODmRNA的表達水平顯著高于對照組(P<0.05);與對照組相比,HCG組Mmp9基因mRNA的表達水平上調,具有極顯著性差異(P<0.01);兩組的Oct4基因mRNA表達水平無顯著性差異(P>0.05)(圖1)。
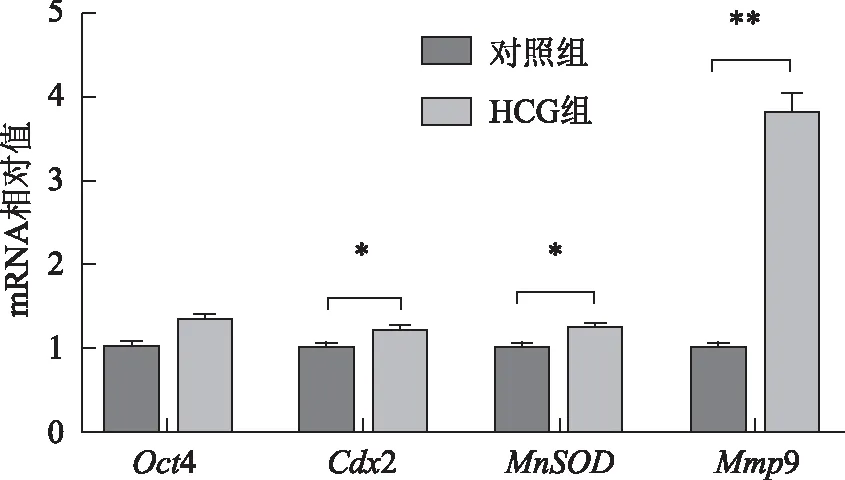
兩組相比較,*P<0.05,**P<0.01圖1 對照組和HCG組相關基因mRNA的表達
三、囊胚計數
采用免疫熒光法,對兩組囊胚進行Cdx2蛋白標記,以及DAPI染色。抗Cdx2蛋白抗體將囊胚TE標記為綠色,DAPI將囊胚細胞核染成藍色(圖2),ICM細胞數為兩者差值。結果顯示HCG組囊胚細胞總數顯著高于對照組(P<0.05),HCG組ICM細胞數及TE 細胞數多于對照組,但差異無統計學意義(P>0.05)。兩組ICM/TE值相比較,差異也無統計學意義(P>0.05)(表3)。
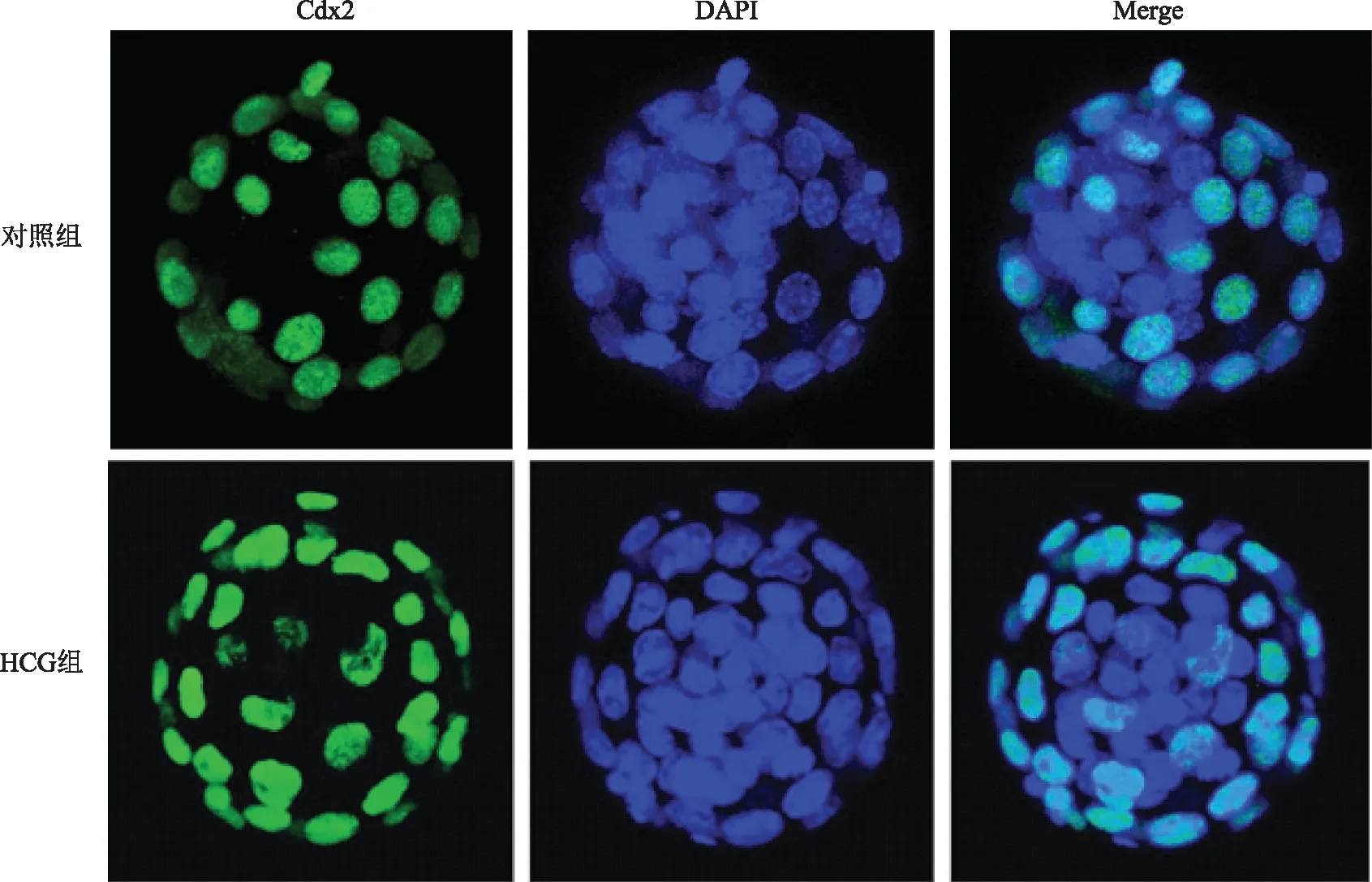
Cdx2標記的外滋養層細胞(綠色);DAPI標記的細胞總數(藍色);Merge為兩種標記的合圖圖2 小鼠囊胚差異性染色結果(免疫熒光染色,×200)

組 別囊胚細胞總數 ICM細胞數TE細胞數ICM/TE值對照組52.3±9.113.2±3.939.1±7.80.3HCG組61.7±16.3*15.4±3.846.2±13.10.3
注:與對照組比較,*P<0.05
討 論
HCG作用廣泛,被稱為當今科學界的奇跡[7]。HCG 作為糖蛋白激素家族中的一員,同 LH 都是通過 LH/HCG 受體發揮生物學作用[8-9]。LHCGR是一種跨膜G蛋白偶聯受體,主要通過 cAMP-磷脂酶 C/三磷酸肌醇途徑介導的信號通路發揮其生物學功能[10]。HCG 和卵巢細胞膜上的 LHCGR 相結合,激活腺氨酸環化酶系統刺激甾體激素的合成,進而介導受精卵著床、性腺發育及功能活動的調節等哺乳動物的生殖過程中:取卵前用HCG扳機提高卵母細胞成熟率、卵母細胞體外發育潛能及臨床妊娠率[11];HCG促進哺乳動物卵母細胞體外成熟、受精及早期胚胎發育[12-13];胚胎植入過程中,HCG是母胎界面分子交流最重要的信號分子[14],胚胎滋養層分泌的HCG以自分泌的形式刺激其侵入子宮內膜[15],改善子宮內膜容受性(ER)、延長種植窗口期,有利于胚胎著床,還可以調節子宮內膜的免疫耐受性;懷孕期間HCG通過卵巢黃體細胞合成孕激素,阻止月經來潮,維持妊娠等。
胚胎體外發育過程中,最早在2-細胞期即可檢測到HCG分泌;從卵母細胞到合子、各細胞期胚胎均有HCG mRNA及其受體的表達。之前很多研究分析了胚胎分泌的HCG對子宮內膜的作用,但很少研究胚胎分泌的HCG對胚胎本身的作用。而且,僅僅依靠形態學來評價胚胎質量是不夠的。本研究采用雙重染色方法分別計數ICM和TE,結果表明,胚胎培養液中加入HCG,雖然對小鼠囊胚ICM、TE細胞數增多作用并不明顯,但是小鼠囊胚細胞總數整體水平顯著提高,提示了HCG對改善小鼠囊胚質量的重要作用。
本研究不僅從形態學及囊胚細胞計數方面觀察到HCG對改善囊胚質量的作用,而且發現胚胎培養液中添加HCG刺激體外形成的小鼠胚胎發育質量相關的基因mRNA[16-19]的表達發生變化。
相關基因Cdx2蛋白是一個重要的轉錄因子,在哺乳動物囊胚中僅存在于外滋養層細胞。胚胎Cdx2基因在8細胞期開始表達,并逐漸開始在外滋養層表達上調,是外滋養層特異性表達因子[20],也是胚胎分化的重要相關基因[21]。本研究中,在胚胎培養液中加入HCG后,Cdx2基因表達明顯上調,可能預示著HCG促進體外囊胚細胞分化良好。Oct4特異性表達于ICM,與種植前胚胎發育和多能性相關[22]。本研究結果表明,HCG組Oct4基因表達上調不明顯,可能與胚胎體外發育過程中ICM增殖速度沒有TE快,與囊胚差異性染色結果相符[23]。通常認為胚胎培養過程中細胞內產生過度的活性氧對胚胎不利。氧化應激被認為是胚胎發育不良的原因之一。MnSOD存在于哺乳動物線粒體中,是體內重要的氧自由基清除劑[24]。Rizos等[25-26]研究發現,體內發育形成的胚胎MnSODmRNA表達水平比體外條件下更高。本研究中,HCG組MnSODmRNA表達水平比對照組顯著增高,說明在培養液中加入HCG使胚胎培養體系更接近體內環境。胚胎成功植入子宮內膜是輔助生殖技術中最重要的環節之一[27],基質金屬蛋白酶9(MMP9)被認為是著床過程中水解細胞外基質最重要的蛋白水解酶[28],在哺乳動物生殖過程中與胚胎遷移、侵襲和組織重建相關[29-30]。研究顯示胚胎分泌的MMP9的量與胚胎質量成正比。而胚胎分泌的HCG可以促進胚胎和子宮內膜MMP9的分泌[31-32]。本研究結果也顯示在胚胎培養液中添加HCG后Mmp9 mRNA表達量極顯著增加,有利于胚胎的植入。
綜上所述,在受精培養液中添加HCG對小鼠卵母細胞體外受精情況沒有影響,但是在胚胎培養液中添加HCG增加囊胚細胞總數,使胚胎質量相關基因表達上調,有潛力成為改善胚胎體外培養質量、優化胚胎體外培養體系的重要因子。至于HCG在此過程中的具體機制還有待進一步研究。

