卵泡液中游離線粒體DNA提取和定量方法的研究
劉宇,趙雪,鄒敏,邵淑敏,李嬌,張衷源,汪文諍,張玲,*
(1.華中科技大學同濟醫學院計劃生育研究所,2.華中科技大學同濟醫學院生殖醫學中心,武漢 430000)
游離DNA(circulating cell free DNA,cfDNA)是游離于細胞外的核酸,廣泛存在于血液[1-7]、卵泡液[8-9]、胚胎培養液[10-11]等液體中。血清和血漿中的cfDNA作為一種無創的檢測手段在腫瘤等疾病早期診斷及預后監測中表現出廣闊的應用前景。cfDNA包括游離核DNA(circulating cell free nuclear DNA,cfnDNA)和游離線粒體DNA(circulating cell free mitochondrial DNA,cfmtDNA)。線粒體DNA的結構比較簡單且數量多,因此,cfmtDNA具有成為無創檢測標志物的潛力。盡管有不少研究顯示了cfmtDNA與腫瘤的相關性[12-13],然而,對體液中cfmtDNA的研究尚處于起步階段,其檢測仍然存在很多問題,定量分析缺乏一個統一的標準,各實驗室的結果缺乏可比性。因此,本研究擬通過對卵泡液處理和冷凍儲存、不同Q-PCR引物和試劑盒進行分析比較,探索影響卵泡液中cfmtDNA提取和定量的因素,為后續實驗奠定基礎。
資料和方法
一、研究對象
收集2016年3月~10月在華中科技大學同濟醫學院生殖醫學中心進行IVF/ICSI的78名患者的1~2個大卵泡液。其中14名患者的卵泡液用于卵泡液處理、冷凍儲存和試劑盒選擇研究;剩余64名患者的卵泡液用于實時熒光定量PCR(Q-PCR)引物的比較研究。納入標準:(1)大卵泡(直徑>16 mm的卵泡)的卵泡液;(2)無明顯肉眼可見的血液污染。本研究通過本院倫理委員會批準([2017]倫審字(S206)號)。
二、主要試劑和儀器
1.主要試劑:DNase/RNase-Free Deionized water(北京天根生化科技)、 SYBR Green(Takara,日本)、50 bp DNA ladder(北京天根生化科技)
2.主要儀器和軟件:StepOne實時熒光定量PCR儀(ABI公司,美國);PCR產物凝膠電泳儀(JY200C,君意東方電泳設備,北京);臺式低溫離心機(Heofuge 15R,力康生物);凝膠成像系統:Biometra BDA Digital(Biometra,德國)
三、方法
1.卵泡液的處理:卵泡液用4種方法處理,分別為:(1)一步離心法即3 000g離心15 min;(2)兩步離心法即3 000g離心15 min后16 000g離心10 min;(3)在兩步離心法的基礎上用0.22 μm過濾器過濾;(4)在兩步離心法的基礎上用0.45 μm過濾器過濾;對cfmtDNA的提取量進行比較。
通過比較卵泡液4種處理方法對cfmtDNA提取量的影響實驗結果,在后續實驗中我們均用兩步離心法處理樣本。將IVF/ICSI患者的每人2 ml大卵泡液分成兩份:一份新鮮樣品直接提取cfmtDNA;另一份冷凍24 h后提取cfmtDNA。分別對新鮮及冷凍24 h后提取出來的cfmtDNA進行定量。
2.DNA提取:分別采用BeaverBeadsTMCirculating DNA 試劑盒和TIANamp Genomic DNA試劑盒進行樣本中cfmtDNA提取。提取方法完全按照試劑盒的說明書進行,用200 μl洗脫液洗脫DNA。
3.q-PCR:用線粒體編碼的基因ND1[11]和hmito3[15]為引物定量cfmtDNA,hmito3引物設計參考文獻,并進行驗證,合成委托上海生工生物工程公司,引物序列詳情見表1。
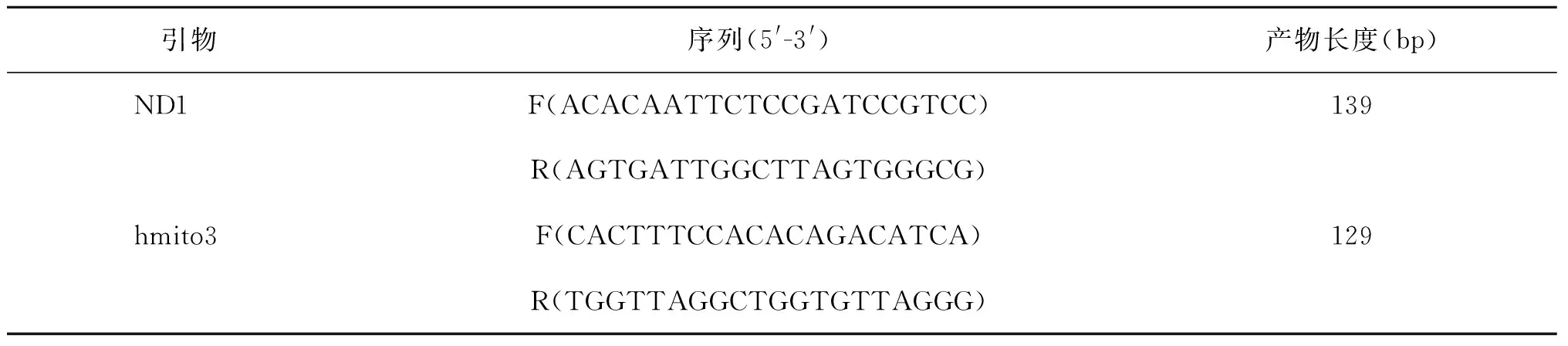
表1 線粒體編碼的基因ND1和hmito3引物序列
熒光定量PCR反應體系為20 μl,每個q-PCR反應包括2 μl cfmtDNA模板、2 μmol/L正向和反向引物和10 μl SYBR Green I的反應混合物。qPCR反應條件:在95℃孵育30 s,接著在95℃進行5 s的變性,以及60℃ 30 s的退火和72℃ 30 s的延伸,40個循環。實時定量PCR在StepOne Software v2.3中進行。每個樣本重復3次。
4.標準曲線繪制
(1)標準品的制備:通過普通PCR擴增線粒體編碼的ND1和hmito3基因,產物經2%瓊脂糖凝膠電泳進行鑒定并切膠回收測濃度,此時的瓊脂糖凝膠電泳產物即為標準品i。
(2)絕對定量標準曲線的制備:標準品i通過連續15次的5倍稀釋得到標準品ii-XVi,將標準品i-XVi分別進行熒光定量PCR分析。熒光定量PCR反應體系為20 μl: 2 μl標準品、2 μmol/L正向和反向引物和10 μl SYBR Green I的反應混合物;反應條件為:在95℃孵育30 s,接著在95℃進行5 s的變性,以及60℃ 30 s的退火和72℃ 30 s的延伸,40個循環。實時定量PCR在StepOne Software v 2.3中進行。
四、統計學處理
結 果
一、線粒體基因引物的特異性、相關性和絕對定量標準曲線
兩對引物用于熒光定量PCR以后,均顯示出良好的擴增效果,熔解曲線正常,無引物二聚體和非特異性擴增,引物的特異性好(圖1A、B,圖2A、B)。2%瓊脂糖凝膠電泳圖顯示,ND1和hmito3分別可見139 bp和129 bp的目的條帶(圖1C)。ND1絕對定量標準曲線方程為y=-3.78x+5.2715,其中R2=0.9979,擴增效率為83.89%(圖1D);hmito3絕對定量標準曲線方程為y=-3.5489x+0.8876,其中R2=0.999 4,擴增效率為91.33%(圖2C)。ND1和hmito3兩個基因的擴增效率好,適用于樣本分析。在同一熒光閾值下,ND1和hmito3引物擴增cfmtDNA所得的濃度平均值分別為(3.49±5.17)ng/L和(0.03±0.02)ng/L,兩對引物濃度平均值之間有顯著性差異(P<0.05),相關性分析顯示ND1與hmito3良好的相關性(r=0.63,P<0.000 1),因此在后面的研究中,我們只選擇了其中一種線粒體基因的引物ND1進行定量分析。
二、新鮮樣本中4種不同的處理方案對卵泡液中cfmtDNA提取量的影響
4種不同的處理方案下,用線粒體基因ND1去定量卵泡液中cfmtDNA濃度,結果依次為:(14.34±14.81)ng/L、(3.41±5.04)ng/L、(2.19±2.72)ng/L、(1.58±2.08)ng/L。一步離心法得到的cfmtDNA濃度最高,與其他三種方案相比較差異有統計學意義(P<0.05);其他3種方案之間cfmtDNA濃度差異無統計學意義(P>0.05)(圖3)。
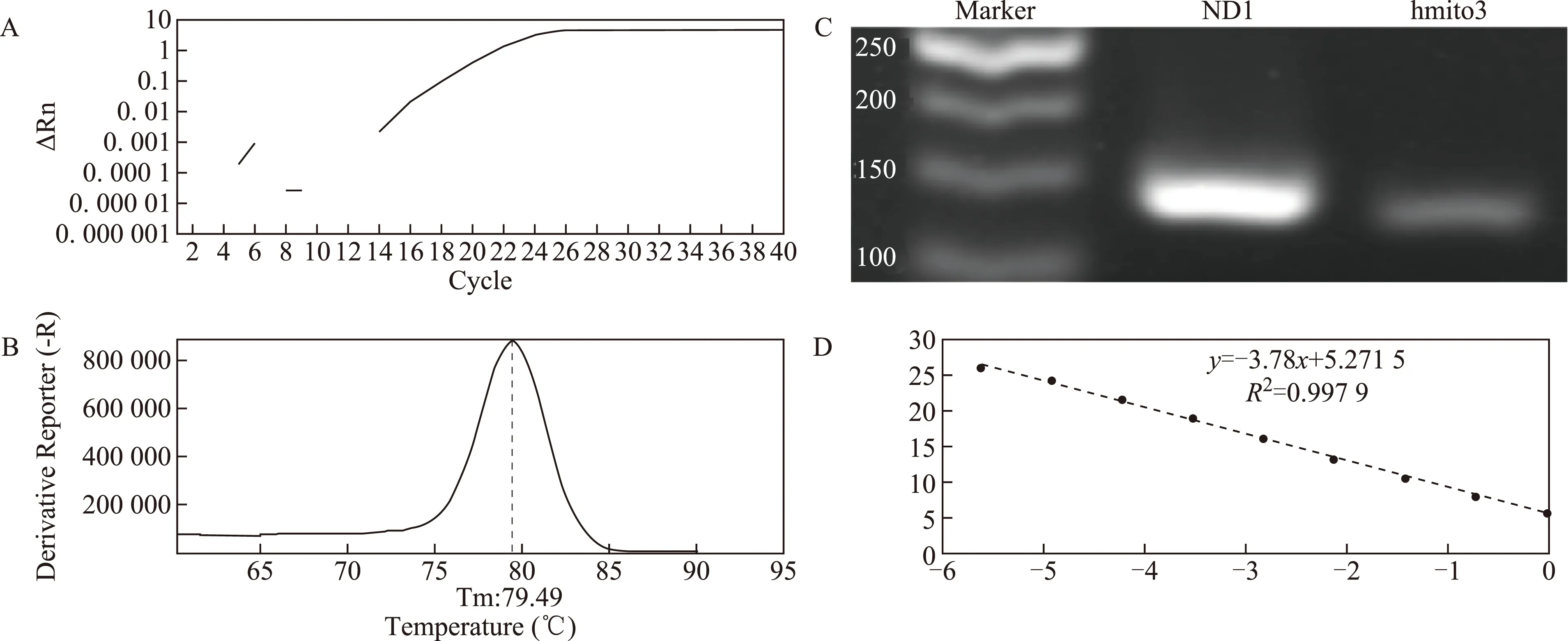
圖1 ND1引物的Q-PCR結果
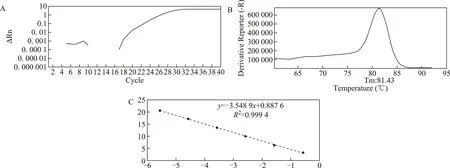
A:擴增曲線;B:熔解曲線;C:標準曲線;其中hmito3引物的凝膠電泳圖譜見圖1 C圖2 hmito3引物的Q-PCR結果
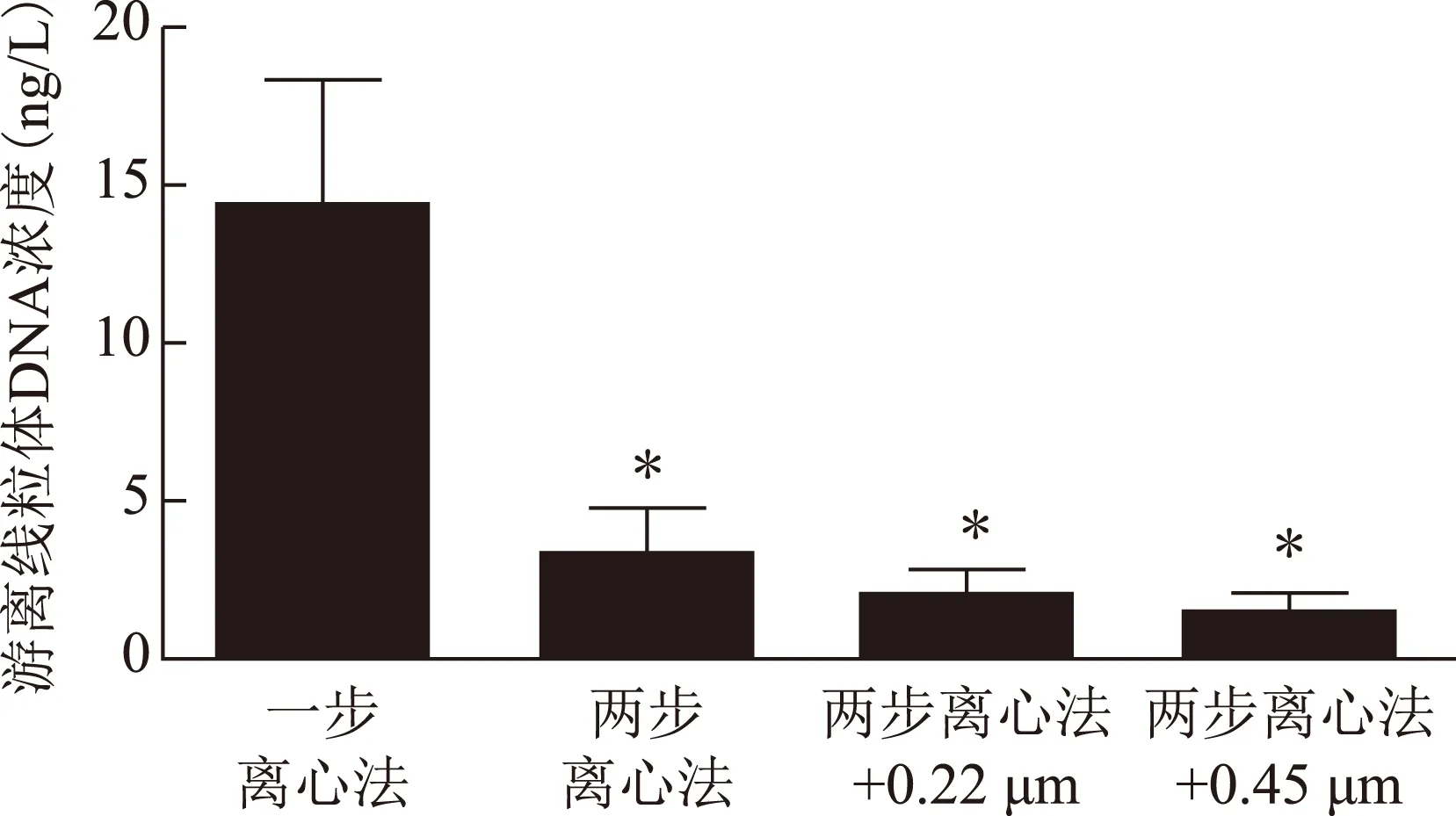
圖3 新鮮樣本中4種不同的處理方案對卵泡液中cfmtDNA提取量的影響與一步離心法相比,*P<0.05
三、儲存條件對卵泡液中cfmtDNA提取量的影響
以ND1為引物對cfmtDNA進行定量,冷凍前樣本中提取到的cfmtDNA濃度為(3.41±5.04)ng/L,冷凍后樣本中cfmtDNA為(2.82±2.40)ng/L,兩者cfmtDNA濃度差異無統計學意義(P>0.05)。
四、兩種不同試劑盒對卵泡液中cfmtDNA提取量的影響
用ND1定量兩種試劑盒提取卵泡液中cfmtDNA的濃度,BeaverBeadsTMCirculating DNA試劑盒提取卵泡液中cfmtDNA的濃度為(5.17±2.77)ng/L,而TIANamp Genomic DNA試劑盒提取的為(2.79±2.37)ng/L,前者比后者提取到卵泡液中cfmtDNA的量顯著增加(P<0.05)(圖4)。
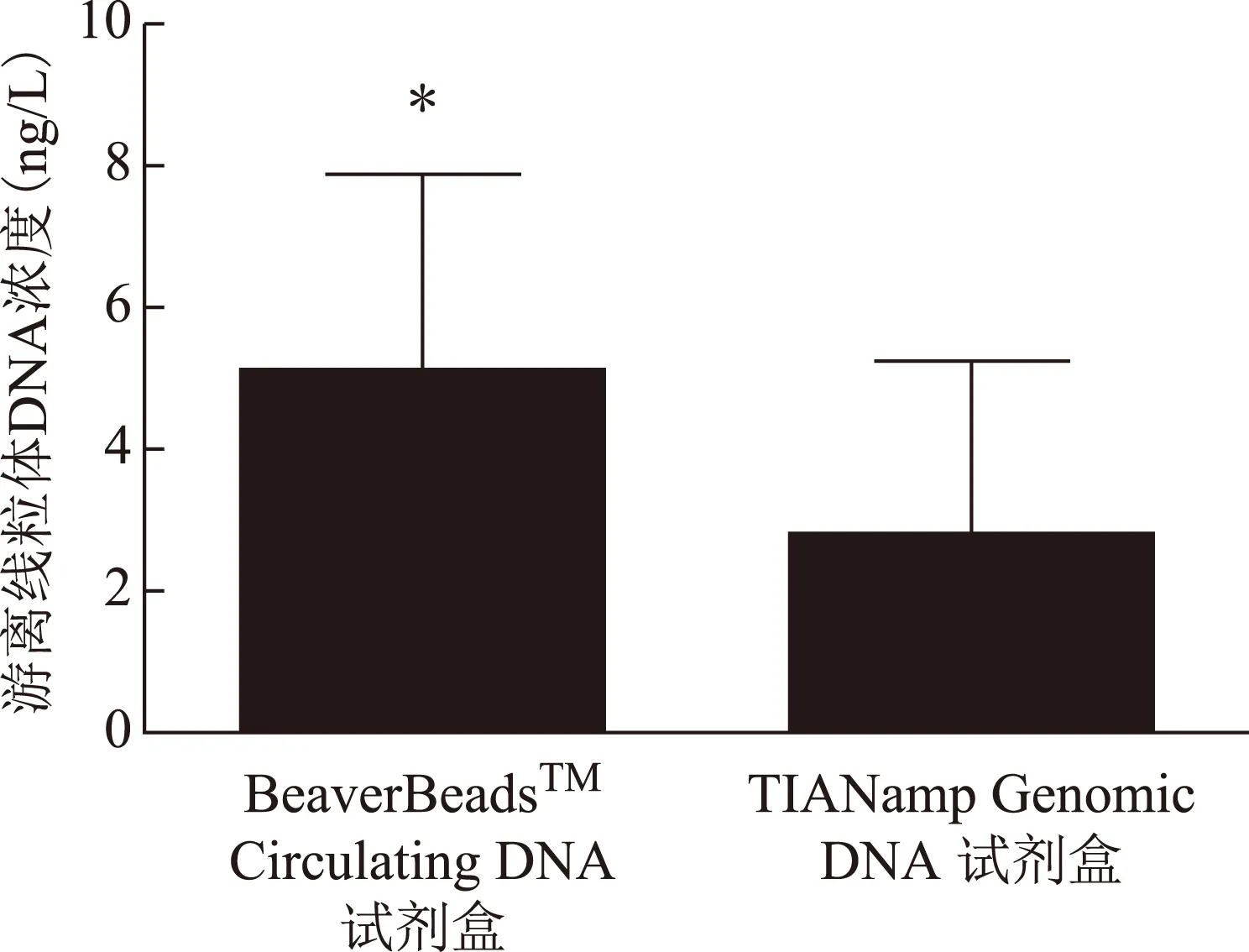
圖4 兩種不同的試劑盒提取卵泡液中cfmtDNA的比較與TIANamp Genomic DNA試劑盒相比較,*P<0.05
討 論
近年來由于分子生物學的飛躍發展,對體液中的cfDNA和cfmtDNA的研究有了長足的進展。線粒體為細胞活動提供所必需的能量,同時參與細胞內新陳代謝、鈣離子穩定[15]、細胞凋亡和信號傳遞等多種生物過程,能夠較為全面的反映細胞的功能狀態。線粒體DNA質與量的變化可導致氧化磷酸化異常等線粒體功能不良,在疾病的發生發展中起重要的作用。而且,線粒體DNA還具有基因長度短、分子結構簡單及拷貝數眾多等特點。因此,cfmtDNA具有成為信息量大、敏感性高的血清標志物潛力。目前關于cfmtDNA的研究主要針對血液及其他體液中cfmtDNA與腫瘤的關系,卵泡液中cfmtDNA的研究尚未見報道。
我們的研究結果顯示3 000g離心15 min的條件下卵泡液中cfmtDNA的濃度是最高的,而后3種處理方式下cfmtDNA的濃度差異沒有統計學意義(P>0.05)。這與Chiu等[16]人的研究結果是一致的。他們通過研究循環線粒體DNA的物理特征發現,不同的離心和過濾方案會影響健康個體血漿中線粒體DNA的定量,可能是由于血漿中存在顆粒相關(particle-associated)的線粒體DNA和非顆粒相關(non-particle-associated)的線粒體DNA。一步離心法獲得的卵泡液中cfmtDNA的濃度最高,推測是其中殘留的細胞碎屑所致。兩步離心法獲得的卵泡液則為一種幾乎無細胞或細胞碎屑的液體[17],這種離心方法可取得與過濾類似的效果,所以更建議用兩步離心法。-80℃冰箱冷凍卵泡液對cfmtDNA的提取量沒有影響,表明卵泡液樣本可先放于-80℃冰箱儲存,然后集中進行cfmtDNA的提取。這對于樣本的收集管理以及工作的安排提供了便利。
熒光定量PCR可以通過檢測熒光信號的變化來測定引物的特異性。在本研究中,線粒體的兩對引物ND1和hmito3用于熒光定量PCR以后,均顯示良好的擴增效果,熔解曲線正常,無引物二聚體和非特異性擴增,引物的特異性好,凝膠電泳也證實目的條帶明顯。ND1為引物所得到的cfmtDNA濃度平均值遠遠大于hmito3引物所得的濃度平均值。hmito3引物擴增cfmtDNA濃度較低可能推測與hmito3在mtDNA中獨特存在有關。Malik等人[18]研究證實了hmito3是mtDNA獨特的短區域設計出來的引物,其不會共擴增任何核假基因。本研究中相關性分析結果顯示ND1引物與hmito3引物良好的相關性(P<0.000 1),說明hmito3和ND1引物均可用于卵泡液中cfmtDNA的定量分析。
目前,提取cfmtDNA最常用的方法有磁珠法(例如:BeaverBeadsTMCirculating DNA 試劑盒)、硅膠膜離心柱吸附法(例如:TIANamp Genomic DNA試劑盒)等方法。磁珠法充分發揮了納米與生物技術的優點,利用磁場分離的原理,即磁珠可以特異性的吸附DNA,在外加磁場的作用下,能夠從液體中分離出DNA的方法;優點是提取DNA濃度高、純度好,同時省時、快速。硅膠模離心柱吸附法是利用一種特殊的硅基質膜吸附材料,選擇性的吸附DNA片段,而RNA、蛋白質等物質被過濾,最后用洗脫液將DNA片段從濾膜上洗脫下來的方法;優點是簡化了核酸的純化過程、操作簡便。我們的研究結果表明,與硅膠膜離心柱吸附法(TIANamp Genomic DNA試劑盒)相比,用磁珠法(BeaverBeadsTMCirculating DNA 試劑盒)可獲得較高濃度的cfmtDNA,快捷簡便。
綜上所述,在進行卵泡液中cfmtDNA的提取時,可選用兩步離心法來處理樣本;同時,可以將處理好的樣本凍于-80℃冰箱,待樣本量合適時統一處理。比較硅膠膜離心柱吸附法,磁珠法有助于減少提取過程中的損耗,獲得更多的cfDNA。線粒體編碼的基因ND1和hmito3均可用于cfmtDNA的定量分析,可根據需要選擇。

