裂殖壺菌制備二十二碳六烯酸油脂的研究歷程及發展前景
胡學超,任路靜,胡耀池,紀曉俊,黃和
(南京工業大學藥學院,南京工業大學生物與制藥工程學院,南京,211816)
二十二碳六烯酸(decosahexaeonic acid,DHA)是一種重要的ω-3長鏈多不飽和脂肪酸,具有促進腦細胞發育,降血脂,保護視力,抗癌,提高免疫力等重要生理功能[1],廣泛應用在嬰幼兒食品及醫藥行業。世界衛生組織早在1994年就規定嬰幼兒奶粉中必須添加DHA,市場需求量大。
傳統的DHA生產原料主要來源于魚油,但魚的種類、季節、地理位置等因素的差異造成了油含量和油中不飽和脂肪酸含量的不穩定;魚油提取獲得的DHA含有大量的EPA(eicosapetaenoic acid, 22∶5),腥味大,且DHA初始含量低,約為10%~20%左右,遠遠低于使用要求(35%),因此需要將魚油中的DHA純化以提高含量。天然的DHA為甘油三酯型,沸點較高,目前最常用的方法是利用甲醇或乙醇進行置換,形成甲酯或乙酯型DHA,沸點降低后提純[2],但甲酯或乙酯型DHA的人體吸收率相對于甘油酯型DHA低;再加上魚油來源日漸緊缺,難以實現此種高價值產品在食品和醫藥行業中的廣泛應用。為滿足DHA不斷增長的市場需求,近年來,科學工作者開展了利用海洋微生物發酵生產DHA的研究。常用的微生物包括隱甲藻 (Cryptheconidiumcohnii)、裂殖壺菌 (Schizochytriumsp.)、吾肯氏藻(Ulkeniaamoeboida)等,裂殖壺菌因其生長速度快、油含量高、DHA比例高,是當前DHA產業化的主要生產菌。本文主要針對生物制備DHA的過程進行綜述,以裂殖壺菌為重點,從菌種特性、安全性認證、發酵水平提升、油脂精煉技術的革新等角度論述生物法制備DHA油脂的研究歷程及發展前景。
1 DHA的生產菌
1.1 隱甲藻
隱甲藻是一種生活在海洋,沒有葉綠素,不能進行自養的雙鞭毛甲藻,在腐敗的大型褐藻及海藻上易于生長繁殖[3]。隱甲藻的分類地位屬于Eukaryota域,Protozoa界,Dinophyta門,Dinophyceae綱,Peridiniales目,Crypthecodiniaceae科,Crypthecodinium屬的一類橢球形單細胞海洋微生物。早在1968年HARRINGTON[4]首次發現隱甲藻產DHA的能力后,BEACH等進行了培養條件和環境方面的優化來提高其生產能力。1994年,KYLE等[5]取得了較好的結果,培養60~90 h生物量可達40 g/L,藻種含油量為15%~30%,DHA占總脂肪酸的20%~35%,隨后在美國Martek公司實現產業化,創建了Life’s DHA品牌,并在世界范圍內進行銷售。以de Swaaf代表的荷蘭農業研究所團隊在21世紀初開發了除葡萄糖外以乙酸[6]、乙醇[7]為底物對C.cohniiATCC 30772進行培養的研究,最高細胞干重達109 g/L,總脂含量61 g/L,DHA含量19 g/L,為至今為止隱甲藻生產DHA報道的最高產量。
1.2 裂殖壺菌
由于隱甲藻發酵生產DHA周期長,產率不高,且生產技術和應用被美國Martek公司壟斷,人們將目光轉向了海洋真菌——破囊壺菌和裂殖壺菌。裂殖壺菌又稱裂壺藻,屬于真菌門(Eumycota)、卵菌綱(Oomycetes)、水霉目(Saprolegniales)、破囊壺菌科(Thraustochytriaceae)的一類海洋真菌,單細胞、球形[8]。1964年,HASKINS等人[9]報道,破囊壺菌Traustochytriumaureum總脂中含有高達34%的DHA,揭示了破囊壺菌屬微生物產DHA的能力。隨后的研究多集中在不同海域中菌種的篩選和培養條件的改進方面。如1990年WILLIAM[10]等也在海水中篩選出一系列破囊壺菌菌屬的裂殖壺菌和破囊壺菌菌株,經工藝優化后被應用于Omega Tech公司的后續生產中;1996年NAKAHARA等[11]從日本Yap群島珊瑚礁附近海水分離到1株裂殖壺菌Schizochytriumsp. SR21,培養56 h,生物量即可達到21 g/L,DHA產量高達4.7 g/L,隨后為Sundory公司所用。我國研究者也陸續在中國海域篩選獲得了多株裂殖壺菌菌株等,如本團隊所篩選的Schizochytriumsp. HX-308[12],中國海洋大學的OUC88[13]等,為國內DHA產業的發展奠定了基礎。
1.3 不同DHA生產菌的生產能力差異
除隱甲藻和裂殖壺菌外,破囊壺菌、吾肯氏藻等菌株也可生產DHA。不同菌種生產的DHA其脂肪酸組分和生產能力不同。隱甲藻生產的DHA油脂中C14∶0(月桂酸)含量較高,但不含有DPA(二十二碳五烯酸,ω-6),而海洋真菌中C16∶0(軟脂酸)含量較高,含有DPA。
2 微生物來源DHA的安全性認證
2.1 安全性認證
作為嬰幼兒食品的DHA油脂,安全性至關重要。世界各國對于DHA油脂的安全性認證主要集中在3種菌,隱甲藻、裂殖壺菌和吾肯氏藻(Ulkeniasp.)。所有的認證都是以公司產品為主,在某個國家申請新資源認證,證明其可以通過安全性評價而作為食品添加劑應用在某些特定的領域。最早的安全認證來自美國馬泰克。2000年,其對2個主打產品DHASCO和ARASCO在美國提出GRAS認證,明確指明DHASCO由隱甲藻生產,ARASCO由高山被孢霉生產。而裂殖壺菌的安全認證經歷了漫長的歷史,直至2010年我國衛生部才頒布相關條文批準來源于雙鞭甲藻、裂殖壺菌、吾肯氏藻的DHA藻油可作為新資源食品,添加到食品中,此類規定的出臺是國內DHA產業的重要里程碑,促進了國內DHA產業的快速發展。隨后,2011年,GB24600—2011關于二十二碳六烯酸油脂(發酵法)的國家標準正式出臺,預示著發酵法生產DHA產業的規范化程度日漸成熟。此外,近年來國內也出現了多個DHA的行業標準,如《DHA藻油》、《DHA微囊粉》等,這些行標主要對產品某些特殊的指標又進行了限定。而對于吾肯氏藻的安全性認證,由Nutrinva公司2004年提出申請,最終也通過了美國GRAS認證。
2.2 DHA應用的法律法規
國內外權威部門對DHA的使用量做出了明確的規定。1994年,世界衛生組織推薦每天嬰幼兒每公斤體重應該補充20 mg DHA,早產嬰兒每天每公斤體重補充40 mg DHA;國際脂肪酸和類脂研究學會(ISSFAL)指出:妊娠和哺乳期婦女每天補充300 mg DHA,歐盟相關組織也做出類似規定,指出妊娠和哺乳期婦女每天至少補充200 mg DHA[14]。在我國,衛生部在2003年食品添加劑使用衛生標準增補品種中,首次將二十二碳六烯酸單細胞油(DHASCO)作為營養素強化劑添加到嬰幼兒食品中(添加量在0.09%~0.15%)。2004年在《食品添加劑使用衛生標準》(GB—2760)2004年增補內容中將添加量增加到10~126 mg/100g。2006年在衛生部公告第12號文件中將DHA的添加量增加到30~100 mg/100g,以上法規的出臺也使得DHA的使用更加規范。
3 裂殖壺菌發酵產DHA的研究概況
3.1 發酵水平
生產效率的提高是實現裂殖壺菌規模化制備DHA產業化的前提,評價DHA發酵的主要指標包括生物量、油脂產量、DHA占總油脂的百分比。圍繞裂殖壺菌發酵水平的提升,國內外研究主要集中在菌種性能提升、發酵過程調控和規模化放大3個方面。
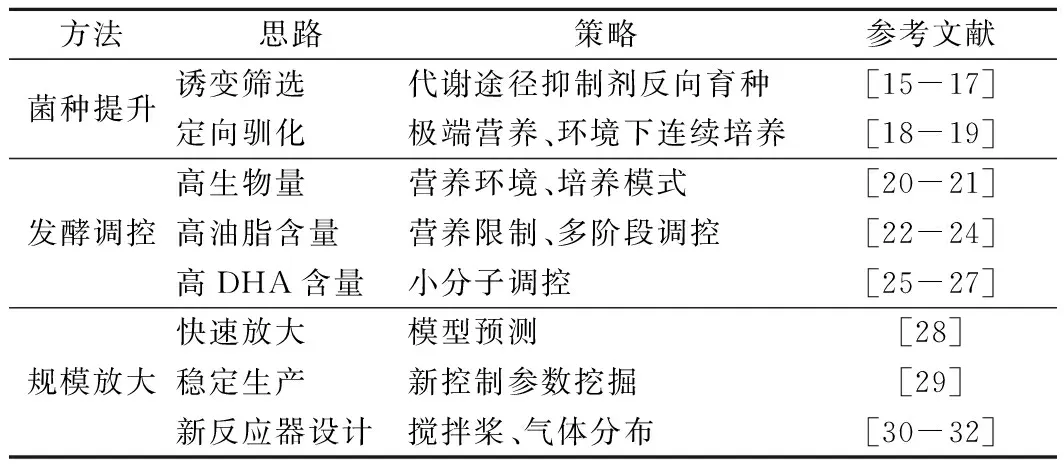
表1 裂殖壺菌發酵水平提升常用的研究策略Table 1 Common research strategies for the improvementof DHA production
在菌種提升方面,誘變育種和菌種馴化是2個主要的研究策略。練敏等[15]提出了利用丙二酸限制三羧酸循環的分流、碘乙酸抑制3-磷酸甘油脫氫酶的定向菌種選育方法,提升檸檬酸從線粒體向胞漿的分流和磷酸戊糖途徑的通量,獲得了多株高油脂含量生產菌株,其中DHA產量較原始菌提高了35%,油脂含量達到38.6 g/L。除此之外,乙酰輔酶A羧化酶催化乙酰CoA生成丙二酰CoA,而喹禾靈是乙酰輔酶A羧化酶的抑制劑。許永等[16]采用紫外誘變和喹禾靈反向篩選高產DHA的裂殖壺菌,生物量和DHA含量分別提高了11.57%和28.75%。FU等[17]利用低能離子束誘變結合蘇丹黑染色的方法進行篩選,DHA產量提高了60%。此外,微生物的適應性進化,又稱菌種馴化,是目前備受矚目的菌種改良技術,通過長期將微生物培養在脅迫環境中,在較短時間內有效地改變菌株的某些表型或者生理特性。孫小曼等[18]開發了不同環境刺激的裂殖壺菌馴化技術,利用高供氧(攪拌轉速230 r/min)連續馴化菌種的方法,迫使細胞長期處于氧化損傷狀態,改變了裂殖壺菌的氧適應性,在高供氧下也能保證高的DHA含量,同時角鯊烯含量降低了63%。采用高滲和低溫雙脅迫馴化技術[19],也可提升裂殖壺菌的產油能力和菌種的抗氧化脅迫能力。
在發酵調控方面,高密度發酵、油脂含量的提高、DHA占油脂比例的提升是研究的關鍵。高密度發酵是胞內產物高效積累的前提,分批補料發酵可以緩解高濃度底物的抑制作用,提高生產效率,分批補加碳源是常規手段。QU等[20]探究了不同補料方式對DHA產量的影響,發現反復分批補料效果最佳。LING等[21]創新性地采用氮源補加策略將細胞干重進一步提高了1倍。其次,營養限制和環境刺激是油脂積累的調控點,但細胞的快速增殖又需要豐富的營養物質和良好的環境條件,因此雙階段的發酵調控工藝在DHA生產中較為普遍,如雙階段控溫[22]既可以保證高的細胞生長速率又可以增加不飽和脂肪酸的比例,多階段氧供應[23]可解決生長的高氧需求和低氧消耗,雙階段滲透壓[24]可利用種子階段高滲刺激分裂、發酵階段低滲促進油脂積累提高油脂產率。此外,DHA合成的代謝途徑需要大量的ATP、NADPH、乙酰輔酶A等輔因子的參與,小分子添加也是常用的研究手段。本研究團隊[25]通過在發酵過程中添加蘋果酸和乙酸鈉的方法提高裂殖壺菌的NADPH和乙酰CoA供應,其中油DHA含量提高至60%;通過添加抗環血酸鈉[26]緩解發酵過程中的氧化損傷,胞內ROS降低了35%,DHA含量提高了44%。另外,考慮到裂殖壺菌的微藻屬性,一些植物激素如茉莉酸、萘氧基乙酸也用來調控裂殖壺菌的生長,提高油脂產率[27]。
在規模化放大方面,如何做到大規模發酵罐的精準放大并穩定生產是關鍵。瞿亮等[28]通過逐級放大的方法,建立了裂殖壺菌發酵產DHA的過程放大經驗方程,基于經驗方程設定大規模發酵罐下的工藝參數,發酵規模從10 L放大到7 t。在DHA生產穩定控制方面,郭東升等[29]研究了不同氧環境下DHA發酵過程中呼吸商RQ、氧氣吸收速率OUR、二氧化碳釋放速率CER的變化規律,提出OUR可以作為DHA生產過程中的精準控制指標,比溶氧DO有更好的指導意義。由于DHA發酵的高需氧性,DHA的發酵通常在多層槳葉生物反應器中進行,此類反應器中,攪拌槳的改變對發酵結果的影響至關重要。趙曉艷等[30]結合CFD模擬技術研究了3種不同攪拌槳組合對反應器流場和DHA產量的影響,發現直葉、箭葉、直葉的徑向流式攪拌槳組合混合效果較好,且能獲得較高的DHA產量。此外,近年來一些新型反應器,如膜曝氣生物反應器[31]、通氣強化膜反應器[32]等也應用到DHA的生產中,其中利用膜曝氣生物反應器,DHA發酵的細胞密度達到了151 g/L以上,油脂占細胞干重達到了68%,生產效率提高了83.77%。
3.2 裂殖壺菌合成DHA特殊的代謝途徑
傳統的多不飽和脂肪酸合成是在線粒體或內質網上通過脂肪酸延長酶和脂肪酸去飽和酶進行碳鏈延伸和雙鍵引入。但該途徑需要多種延長酶和去飽和酶的參與,伴隨著多種中間副產物的積累。除了這種常規合成途徑外,JAMES等[33]在 Science期刊上首次發現報道裂殖壺菌還存在一種類似迭代型聚酮合酶的復合酶催化合成長鏈多不飽和脂肪酸。近年來,人們也陸續在自然界發現多種催化不同多不飽和脂肪酸合成的迭代型聚酮合酶[34],并將此類利用聚酮合酶合成的脂肪酸定義為次級脂質,將此類基因簇稱之為脂肪酸聚酮合酶(FAS/PKS )基因簇[35]。脂肪酸聚酮合酶(FAS/PKS)包括β-酮酰合成酶(KS)、β-酮酰-ACP還原酶(KR)、烯酰還原酶(ER)、脫水酶/異構酶(DH/I)、酰基轉移酶(AT)和酰基載體蛋白(ACP)等功能模塊。類似于經典的脂肪酸合成酶催化過程,該酶以乙酰 ACP 為起始單元,以丙酰 ACP 為延伸單元,通過 KS、KR、DH、ER功能域的循環延伸碳鏈,但脂肪酸聚酮合酶會選擇性的缺失最后一步酰基還原(ER )步驟而在脂肪酸鏈中引入雙鍵[36]。對于DHA的合成,脂肪酸聚酮合酶需要引入6個雙鍵,但是目前對于該酶引入雙鍵的時機和次數控制機制仍然不夠清晰。脂肪酸聚酮合酶途徑可直接從頭合成長鏈多不飽和脂肪酸產品,與傳統的延長去飽和途徑相比,具有更高的能量利用效率。以DHA為例,延長去飽和途徑需要26個NADPH,聚酮合酶途徑僅需要14個,因此,裂殖壺菌胞內這種特殊的不飽和脂肪酸合成途徑具有更大的改造空間和應用價值。
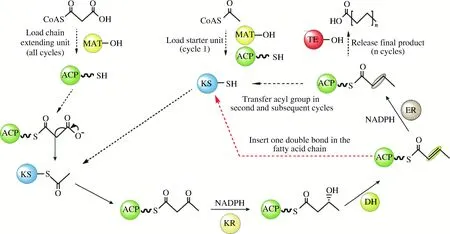
圖1 脂肪酸聚酮合酶催化合成不飽和脂肪酸的過程Fig.1 Polyunsaturated fatty acid biosynthesis catalysed by PUFA-PKS synthase
4 DHA油脂的提煉工藝
油脂為胞內產物,細胞破碎是油脂提取的前提,目前已報道的細胞破碎方法有多種,主要分為物理法(微波法、超聲法、均質法等)、化學法(酸熱法、堿法等)及生物法(酶法等)[37-39]。在DHA產業發展初期,均質法是工業上最常用的細胞破碎方法,但其能耗高,操作復雜,所需人力多。后續人們開發了酶法破碎工藝,篩選不同的酶進行破碎,該方法可直接在發酵罐中進行,無需增加設備,破碎效率比機械破碎高。一般來講,酶法提取主要利用蛋白酶進行破碎細胞,用量少,約為發酵液質量的0.1%~0.2%,每噸發酵液的處理成本約為100元左右。對于油脂的提取,溶劑提取是常規手段,溶劑的使用和回收使得提取工段的設備投入和成本巨大,同時也給生產過程帶來巨大的安全隱患,生產車間也需要防爆。近年來,無溶劑提取工藝[40]逐漸應用到裂殖壺菌的油脂提取過程(如圖2),該工藝操作簡單,生產效率大大提升。DHA毛油一般通過脫膠、堿煉、脫色、脫臭等工序,除去油脂中的蛋白膠質、皂角、色素和氣味性物質,最終獲得DHA精油。
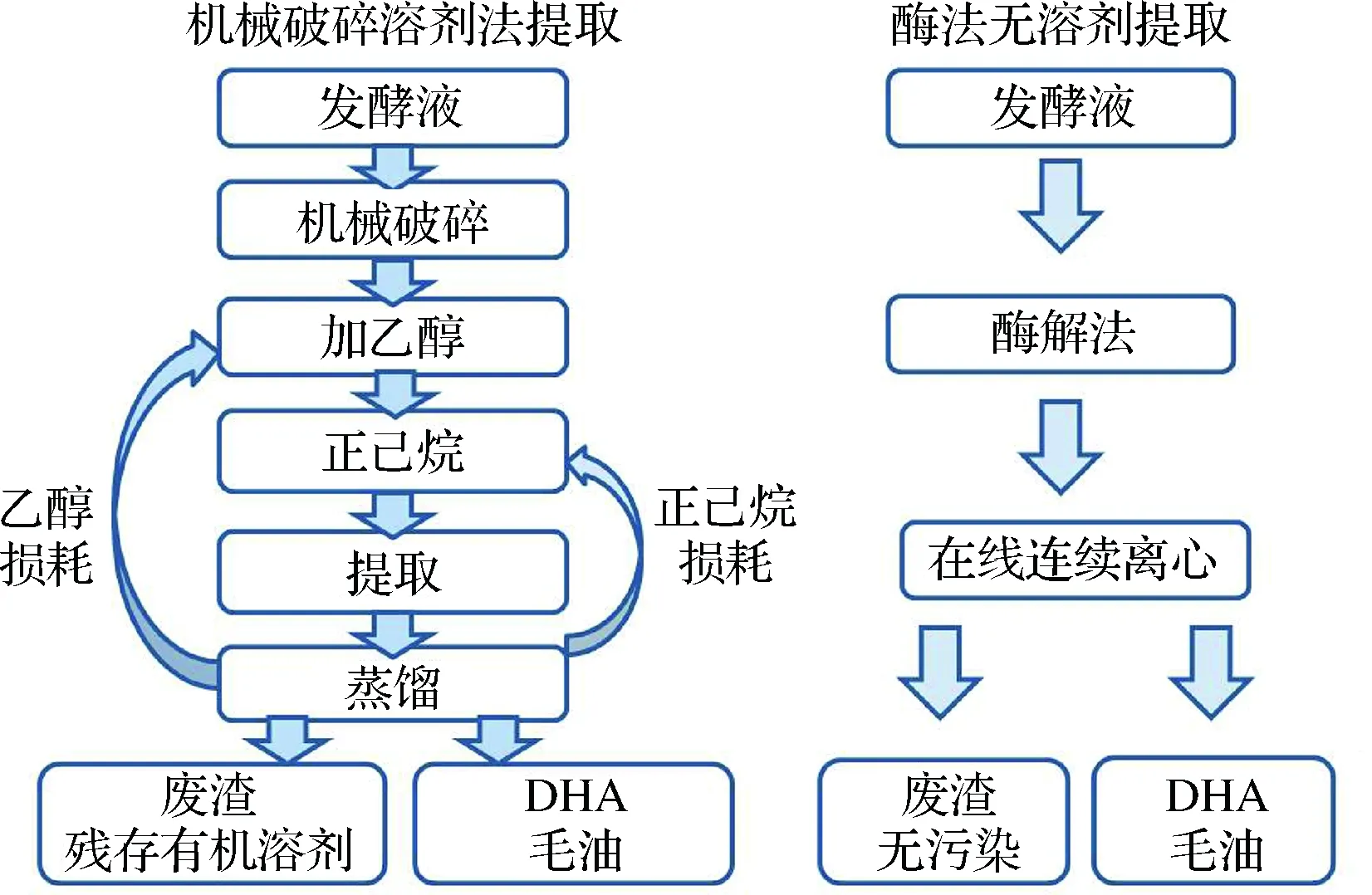
圖2 機械破碎溶劑法與酶法無溶劑油脂提取工藝比較Fig.2 Comparison of lipid extraction process between mechanical crushing-solvent method and enzymatic free solvent method
5 發展前景
隨著社會各界對嬰幼兒健康的關注,以及中國逐步進入老齡化社會,國民的健康需求不斷增長,DHA在營養強化劑領域的應用將繼續擴大。DHA藻粉還可作為飼料添加劑廣泛應用在養殖業,如利用DHA藻粉飼養禽類,獲得富含DHA的雞蛋,雞蛋中DHA存在于磷脂中,人體吸收率高達100%,還可應用于高檔魚蝦類的養殖,前景廣闊。此外,目前DHA油脂含量一般在50%以上,更高DHA含量的產品開發也將推進其在醫藥行業中的應用。魚油2015年需求量達到10.9億t,全球市場達到110億美元,進一步降低藻油價格,加快藻油DHA產品的國外認證,開發既含DHA又含EPA的藻油產品,替代部分魚油,也具有重要的推廣意義。
此外,裂殖壺菌生物量可達到200 g/L,油脂含量占60%以上,且具有獨立的飽和脂肪酸和不飽和脂肪酸合成系統,是極具潛力的微生物油脂加工廠。近年來,隨著裂殖壺菌全基因組測序、胞內代謝機制的解析以及裂殖壺菌遺傳操作體系的建立,在裂殖壺菌中構建其他脂質化學品的代謝途徑,有望推進更多的脂溶性營養化學品的開發。

