地諾前列酮栓引產出現宮縮過頻后不同取藥時機對分娩結局的影響
童美和 于海微
陰道穹窿放置地諾前列酮栓(商品名:欣普貝生)是妊娠晚期促宮頸成熟引產的重要方式,伴或不伴胎心改變的子宮過度收縮是其主要副作用[1]。宮縮過頻是其中較常見的一種,出現宮縮過頻需及時把欣普貝生自陰道取出[2],此時如果宮頸尚未成熟則宮縮大多會減弱甚至消失,需改用其他促宮頸成熟引產方式,甚至需剖宮產。繼續放置可能增加宮頸成熟率,但也可能出現胎兒窘迫、產道裂傷、羊水栓塞、胎盤早剝等并發癥。本文對88例欣普貝生促宮頸成熟引產過程中宮頸尚未成熟即出現宮縮過頻的產婦資料進行回顧性分析。現報道如下。
1 資料與方法
1.1 一般資料 回顧性分析2015年1月-2016年12月本院產科使用欣普貝生促宮頸成熟引產病例287例的臨床資料。宮縮過頻或過強診斷標準:10 min內宮縮≥5次,20 min連續胎心監測胎心正常[3]。納入標準:單胎頭位、足月妊娠產婦;引產過程中出現宮縮過頻或過強,但胎心正常。排除標準:發生宮縮過頻時宮頸已成熟;發生宮縮過頻時胎心異常。其中88例符合標準納入研究,根據發生宮縮過頻后是否立即取出欣普貝生將其分為立即取藥組(立即取出欣普貝生)54例和繼續放置組(繼續放置至宮頸成熟再取藥)34例。本研究已經本院倫理委員會審核批準。
1.2 方法 欣普貝生放置前后的臨床監測:采用Ferring Controlled Therapeutics Limited公司生產的欣普貝生,按照2013年欣普貝生臨床應用規范專家組制定的欣普貝生臨床應用規范專家共識的相關要求進行放藥及放藥后監測[3]。引產過程中如出現宮縮過頻,立即檢查宮頸成熟情況,如宮頸已成熟則取出欣普貝生,如不成熟則告知產婦及家屬病情及相關風險,產婦及家屬可從以下兩個方案中做出知情選擇,(1)立即取出欣普貝生,觀察宮縮情況,30 min后如宮縮消失則予小劑量催產素靜滴繼續引產;(2)普貝生繼續放置至宮頸成熟再取出,放置期間持續胎心監護,每小時檢查宮頸成熟度、母體生命體征和自覺癥狀,如有胎心異常、母體生命征不平穩、子宮破裂先兆等情況時仍需立即取出普貝生并做相應處理。
1.3 觀察指標 比較兩組產婦年齡、身高、體重、是否初產、孕周、引產前宮頸Bishop評分、引產指征、藥物放置時長、放藥至胎兒娩出時長、24 h內選擇分娩方式情況、羊水污染程度、經陰道分娩產道裂傷和會陰裂傷情況、產后2 h出血量、產前7 d內與產后2 d的血紅蛋白濃度差,以及新生兒體重、入住NICU比例、Apgar評分情況。
1.4 統計學處理 使用SPSS 20.0軟件對所得數據進行統計分析,正態分布計量資料用(±s)表示,比較采用t檢驗;非正態分布計量資料采用中位數(四分位數間距)[M(P25,P75)]表示,比較采用秩和檢驗;計數資料以率(%)表示,比較采用字2檢驗。以P<0.05為差異有統計學意義。
2 結果
2.1 兩組基線資料比較 兩組一般資料比較差異無統計學意義(P>0.05),具有可比性。見表1。
2.2 兩組產婦分娩結局比較 繼續放置組剖宮產2例(手術指征分別為活躍期停滯和持續性枕后位),立即取藥組剖宮產16例(手術指征為引產失敗7例、繼發胎兒窘迫4例、產程停滯試產失敗3例、進入產程前喪失試產信心,更改陰道試產意愿要求手術2例),比較差異有統計學意義(字2=24.103,P<0.001);繼續放置組有1例新生兒出生1 min Apgar評分7分,經復蘇后5 min Apgar評分9分,立即取藥組無Apgar評分≤7分者;兩組產婦均無子宮破裂、胎盤早剝、羊水栓塞、新生兒重度窒息等嚴重分娩并發癥發生;繼續放置組的藥物放置時長長于立即取藥組,放藥至分娩時長短于立即取藥組,24 h內陰道分娩比例高于立即取藥組,羊水污染程度輕于立即取藥組,比較差異均有統計學意義(P<0.05);兩組經陰道分娩的產道及會陰裂傷情況、新生兒體重、入住NICU比例、產后2 h出血量、血紅蛋白差值比較,差異均無統計學意義(P>0.05);其中繼續放置組24 h內陰道分娩的相對危險度(RR)為2.862[95%CI(1.750,4.680)],繼續放藥組剖宮產的RR為0.079[95%CI(0.019,0.321)],產婦中均無會陰3、4度裂傷。見表2、3。
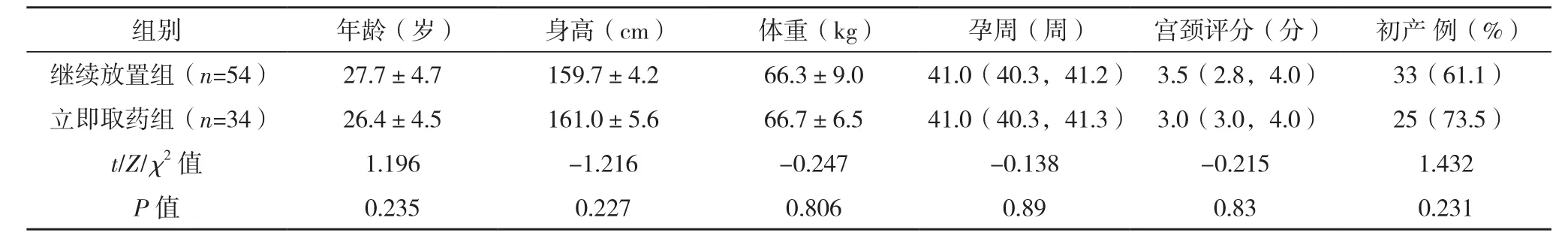
表1 兩組基線資料比較
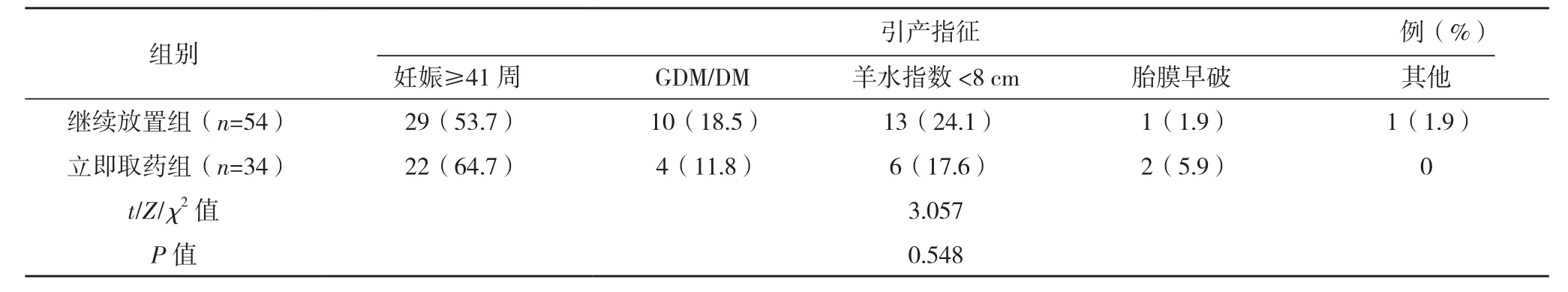
表1 (續)
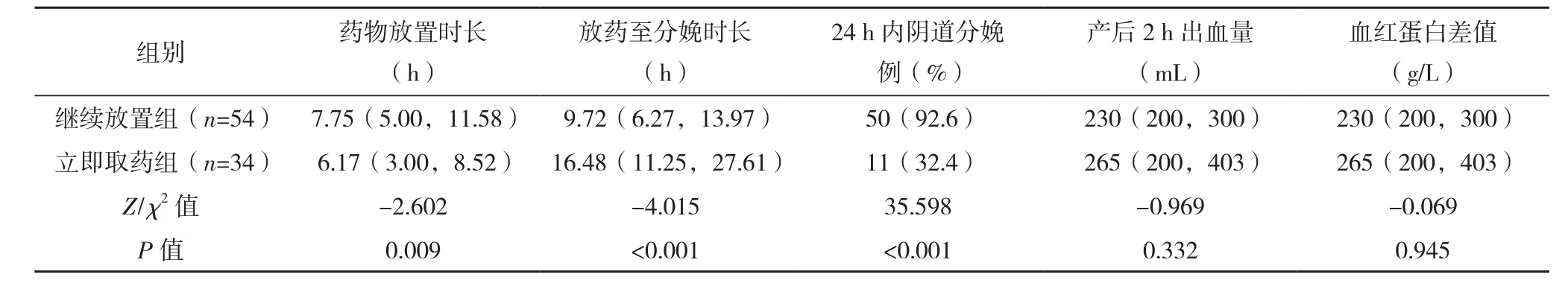
表2 兩組產婦分娩結局比較
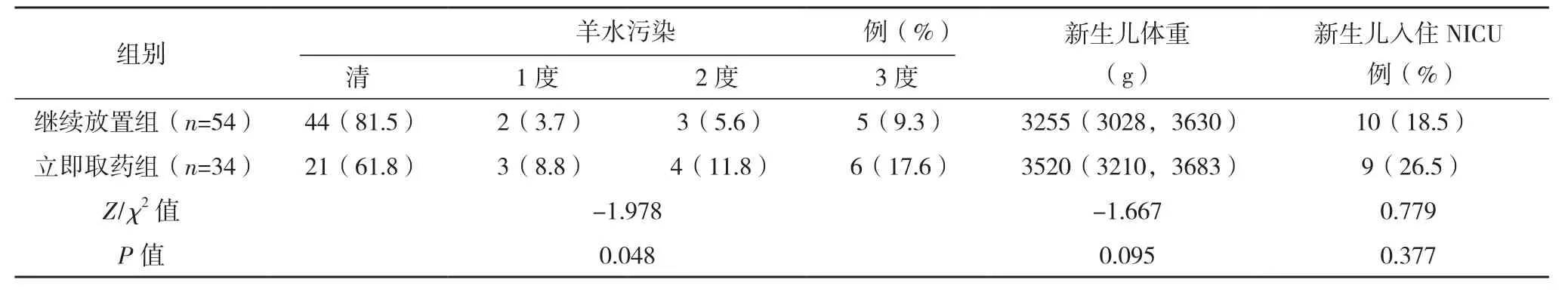
表2 (續)
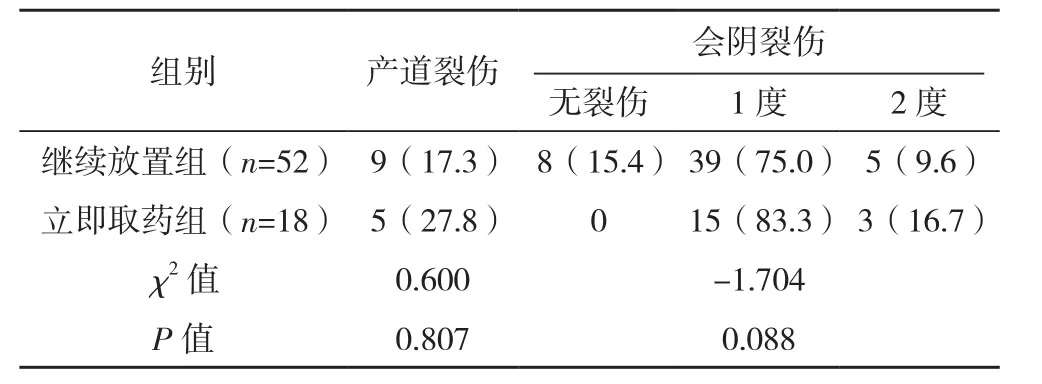
表3 兩組陰道分娩產婦產道及會陰裂傷情況比較 例(%)
3 討論
3.1 欣普貝生引產的機理、效果和主要副作用 欣普貝生是含地諾前列酮(PGE2)10 mg的陰道栓劑,具有控釋系統、可回復裝置,以近似0.3 mg/h的速度穩定釋放,持續24 h。藥物半衰期為1~3 min,在撤出后,其藥物的作用會迅速消失(90 s)。臨床研究表明,欣普貝生能有效促進宮頸成熟,提高24 h陰道分娩率,降低縮宮素使用率,其用于足月妊娠宮頸不成熟孕婦的引產效果明顯優于縮宮素[4-6]。用藥前先用生理鹽水把普貝生潤濕能縮短引產時間[7]。與口服小劑量米索前列醇引相比,從用藥至分娩的時間平均縮短約6 h[8],與水囊引產效果相當[9],也有研究認為效果優于水囊引產[10]。對于足月妊娠胎膜早破和有宮頸物理治療史的足月妊娠孕婦,其引產效果也很確切[11-12]。用于妊娠期糖尿病和妊娠期高血壓孕婦的引產,其風險性并無明顯增加[13-14]。但是,由于其在軟化宮頸、使宮頸成熟的同時,還有增加子宮平滑肌細胞間縫隙連接,誘發宮縮,增加子宮平滑肌對內源性及外源性催產素的敏感性,以及刺激內源性前列腺素的釋放等作用[5],導致欣普貝生促宮頸成熟過程中,因人而異出現強弱不等的宮縮,部分產婦可出現宮縮過頻、過強甚至子宮過度刺激等副作用,其中宮縮過頻的出現比例為從11.3%~70.0%不等[5,15-17],這可能與各研究者對宮縮過頻的診斷標準不同有關。2013年欣普貝生臨床應用規范專家組制定的欣普貝生臨床應用規范專家共識中指出,置藥后出現細小宮縮為藥物性宮縮,可繼續放置[3],但共識對該類宮縮缺乏頻率、強度、持續時間的規定,與宮縮過頻有時難以界定。2014年中華醫學會婦產科學分會產科學組制定的妊娠晚期促子宮頸成熟與引產指南中規定,出現宮縮過頻需及時取出欣普貝生[2],由于地諾前列酮藥物半衰期短,撤藥后其藥物的作用會迅速消失,部分產婦宮頸仍然不成熟,需采用其他引產方式,甚至需剖宮產。然而,目前其他促宮頸成熟引產方式也各有利弊,機械性方法會增加母嬰感染風險[17],靜脈使用催產素的促宮頸成熟效果較差。2011年WHO發布的引產指南中,對于子宮過度刺激的處理推薦使用宮縮抑制劑,但使用者與未使用者相比,僅在改善異常胎心方面有統計學意義,對于降低新生兒出生1 min Apgar評分低于7分比例、入住NICU比例、圍產兒死亡比例等方面沒有統計學意義[18]。所以,對于無胎心異常的宮縮過頻,使用宮縮抑制劑可能沒有必要。
3.2 發生宮縮過頻時不同取藥時機對分娩結局的影響 本研究結果顯示,繼續放置組的藥物放置時長長于立即取藥組,放藥至分娩時長短于立即取藥組,比較差異均有統計學意義(P<0.05)。漫長的引產過程往往意味著產科醫護人員工作量的增加,產婦醫療費用的增長以及對分娩滿意度的下降[19]。引產的目的是促使未臨產的孕婦進入產程,并最終自陰道分娩。本研究結果顯示,繼續放置組24 h內陰道分娩比例高于立即取藥組(P<0.05),繼續放置組比立即取藥組24 h陰道分娩比例提高了60.2%(92.6% vs 32.4%),繼續放置組24 h內陰道分娩的RR=2.862[95%CI(1.750,4.680)],表明出現宮縮過頻時繼續放置欣普貝生能提高引產有效性。繼續放置組的最終陰道分娩比例比立即取藥組高出43.4%(96.3% vs 52.9%),其發生剖宮產的RR為0.079[95%CI(0.019,0.321)],說明與立即取藥組相比,欣普貝生繼續放置能降低剖宮產率。欣普貝生取出后,由于宮頸尚未成熟,催產素促宮頸成熟引產效果較差,引產時間長,容易繼發母胎疲勞,導致宮縮乏力、產程停滯、胎兒窘迫,產婦易喪失陰道分娩信心,這些因素均可增加剖宮產率。
3.3 發生宮縮過頻時繼續放藥的安全性問題 本研究顯示,繼續放置組羊水污染程度輕于立即取藥組(P<0.05),兩組經陰道分娩的產道及會陰裂傷情況、新生兒體重、入住NICU比例、產后2 h出血量、血紅蛋白差值比較,差異均無統計學意義(P>0.05),可能與樣本量不足有關。單純宮縮過頻而不合并有胎心異常,說明胎兒尚能耐受,而有宮縮過頻的產婦產程往往較短,胎兒尚未缺氧就已順利娩出,所以繼續放置組的羊水污染程度反而較立即取出組輕,入住NICU比例也未增加,雖然繼續放置組有1例新生兒1 min Apgar評分為7分,但復蘇后很快恢復,5 min Apgar評分為9分。因此,出現單純宮縮過頻時,在嚴密監測下繼續放置直至宮頸成熟再取藥對母兒是安全的,但需加強監測,及時發現宮縮過強和子宮過度刺激。
綜上所述,欣普貝生促宮頸成熟引產過程中出現宮縮過頻時,在嚴密監測下繼續放置直至宮頸成熟才取出欣普貝生,能提高24 h內陰道分娩比例,減少剖宮產,未明顯增加分娩的母嬰并發癥。由于本研究為隊列研究,可能存在偏倚,且樣本量較小,對于發病率較低的分娩并發癥的檢驗效能低,本研究的結論有待后續大樣本隨機對照研究加以證實。

