Wnt信號通路在骨肉瘤發生機制中作用的研究進展
張熙 王東偉 劉爽
佳木斯大學(黑龍江佳木斯 154007)
骨肉瘤是起源于成骨間葉組織的原發性惡性骨腫瘤,約占小兒惡性腫瘤的5%。同時,骨肉瘤發病機制不明,預后較差,伴有較高的復發率和轉移風險[1]。因此,研究骨肉瘤發生發展機制對于預防、優化臨床治療方案,提高患者生存率具有深遠的意義。
近年來骨肉瘤細胞遺傳學和分子生物學機制已有了較為深入的研究,原癌基因C-myc、erbB-2、SAS等,抑癌基因 Rb、p53、DCC、PTEN等,以及血管內皮生長因子、環氧合酶-2等都已證實與骨肉瘤存在著密切關系。
一般認為,骨肉瘤的發生是由于成骨細胞分化異常所致,而Wnt/β-Catenin在成骨細胞的增殖、分化以及遷移過程中扮演著重要角色,許多骨腫瘤中已發現Wnt/β-Catenin信號通路的異常激活。異常的Wnt/β-Catenin信號通過上調致癌基因(如c-Myc、CCND1、c-MET)引起骨肉瘤的發生[1]。越來越多的研究表明Wnt/β-Catenin信號分子與骨肉瘤的發生發展存在著密切關系,本文綜述了wnt信號分子在骨肉瘤發生發展中的影響,望其成為治療骨肉瘤的突破口。
1 經典Wnt信號通路
目前,Wnt信號通路分為β-catenin依賴型經典Wnt信號通路和β-catenin非依賴型非經典wnt信號通路。非經典Wnt信號通路包括Wnt/Ca2+通路及Wnt/JNK通路。其中,經典Wnt信號通路被認為是最為關鍵且研究最多的Wnt信號通路。經典Wnt信號通路是一種在進化中高度保守的信號通路,在調節細胞遷移、極化、分化等方面發揮著重要作用。多篇文獻提出Wnt信號通路在骨骼惡性腫瘤以及腫瘤骨轉移灶中異常激活,如多發性骨髓瘤,尤文氏肉瘤,骨肉瘤,以及乳腺癌或前列腺癌骨轉移瘤。
經典Wnt信號通路作用機制是當Wnt配體蛋白存在時,Wnt蛋白與受體一旦結合將磷酸化低密度脂蛋白關聯受 體 5/6(low density lipoprotein receptor-related protein,LRP5/6),進一步與卷曲蛋白(Frizzled,Fz)形成Fz-LRP5/6復合體。Fz蛋白作用于胞質內的蓬亂蛋白(Dishevelled,Dsh),因Dsh和軸蛋白(Axin)都含有DIX結構域,易聚合,故促進了復合物(Wnt-Fz-LRP5/6)形成。LRP5/6因子的PPPSPXS區域磷酸化后與Axin結合,并且Axin、GSK3、CK1復合體形成又可促進激活LRP5/6因子的PPPSPXS區域,進一步導致Axin蛋白與LRP5/6的結合。與LRP5/6結合的Axin將不能與GSK-3/APC形成復合物,導致β-catenin不能被降解,沒有被降解的β-catenin在胞質內積累、聚集并進入細胞核與T細胞轉錄因子(TCF)/淋巴增強因子(LEF)結合形成復合體,β-catenin代替Croucho、Coop等抑制轉錄因子與TCF結合,從而激活下游靶基因轉錄,促進細胞分化增殖。當沒有wnt信號分子時,細胞質內累積的β-catenin與細胞膜上E-鈣粘蛋白(E-cadherin)結合,使之附著于細胞骨架蛋白肌動蛋白上,介導細胞與細胞之間粘附,少部分的β-catenin通過泛素化途徑被降解,導致TCF/LEF與多種轉錄抑制蛋白結合而阻止靶基因的表達[2]。
Wnt通路通過調控轉錄激活劑發揮作用,同時也受到分泌蛋白的調控,如wnt蛋白抑制因子(WIF-1)和分泌型卷曲蛋白(SFRP1)會抑制Wnt與Fz受體結合;Dickkopf相關蛋白 1(Dickkopf-related protein 1,Dkk1)能阻止 Wnt與LRP相互作用,從而抑制Wnt信號通路的激活[3](圖1)。
2 經典Wnt通路與骨肉瘤發生發展的相關性
2.1Wnt配體蛋白與骨肉瘤的相關性Wnt蛋白是一類富含糖基化位點的自分泌或旁分泌糖蛋白,由wnt基因編碼作為Wnt通路的起始蛋白[4]。
Wnt蛋白在成骨細胞中對其增殖、分化和遷移起著調節作用,并且在小鼠模型中對骨愈合起著重要的成骨作用。目前,研究發現Wnt受體、Wnt配體蛋白以及wnt抑制蛋白分泌的減少與骨惡性腫瘤密切相關。已經發現骨肉瘤細胞株(U2OS,HOS,143B和Saos-2)中wnt1,wnt4,wnt5a,wnt7a,wnt14蛋白表達,wnt5a和wnt7a在4種細胞株中均有表達,wnt4和wnt1也在2種細胞株中表達[5]。HOANG等[6]發現wnt1蛋白在HOS和Saos-2骨肉瘤細胞中表達增高;而HOS,143B和Saos-2表達wnt4;U2OS,HOS,143B和Saos-2中wnt5a和wnt7a均有一定的表達;4種細胞株中均沒有檢測到wnt11的表達。
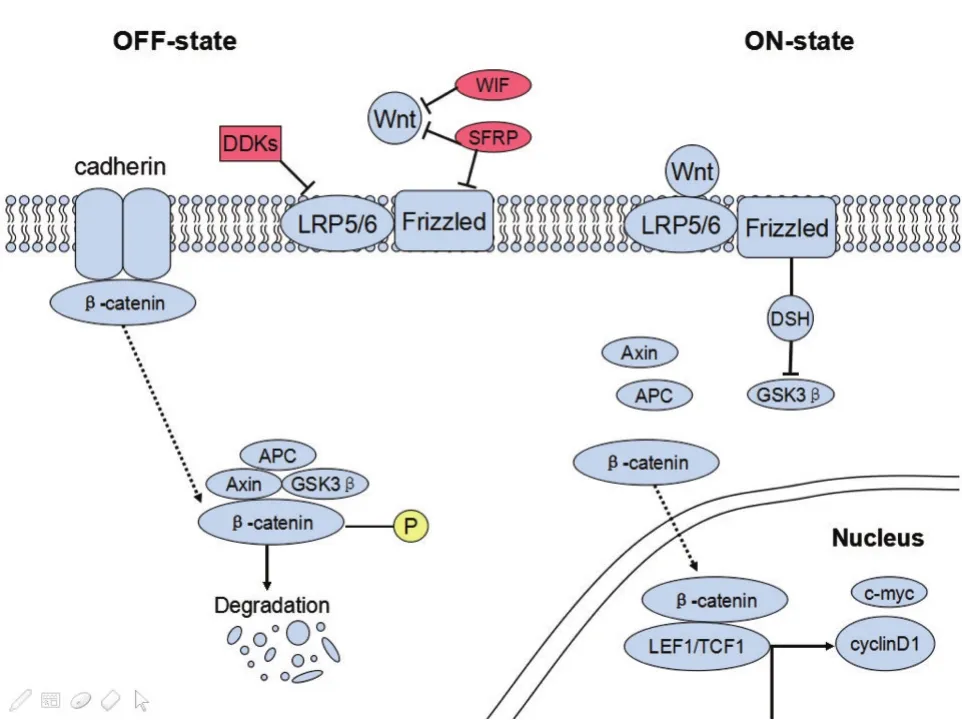
圖1 經典Wnt信號通路Fig.1 Classic Wnt pathway
另外,在人骨肉瘤細胞系MG63和HOS中也發現了多種wnt配體蛋白的表達。有學者在兩種鼠骨肉瘤細胞系K7M2 和 K12 中 發現 Wnt2,Wnt3,Wnt5a,Wnt6,Wnt7a,Wnt8a,Wnt10b,Wnt15配體蛋白表達。這些結果通過離體和臨床檢測都驗證了骨肉瘤的發生可能激活wnt相關蛋白。證明wnt配體蛋白通過自分泌或旁分泌的方式參與了骨肉瘤的發生發展。
MA等[10]用實時定量PCR研究比較了人骨肉瘤細胞(Saos-2)與人胚胎成骨細胞(hFOB)Wnt/β-Catenin信號通路組件的表達情況,發現Saos-2細胞的wnt3a、β-Catenin及LEF1較hFOB細胞高度上調[7]。基于這些研究,在骨肉瘤中多種wnt配體蛋白的過度表達表明wnt配體蛋白通過Wnt/β-Catenin信號通路及其下游相關基因使骨肉瘤發生,這為通過阻斷上游wnt相關蛋白抑制骨肉瘤的發生提供了新思路。
2.2Frizzled蛋白因子在骨肉瘤中的作用經典Wnt/β-catenin通路中wnt配體蛋白必須與膜上受體卷曲蛋白(Frizzled,Fz)結合才能發生級聯信號產生信號轉導。Frizzled蛋白作為wnt配體蛋白家族的主要受體,最初是從鼠骨肉瘤細胞系UMR-106中發現的,僅存在于動物細胞中[8]。Frizzled蛋白受體由細胞外N端保守的半胱氨酸富集結構域(CRD)、類似G蛋白偶聯受體的七次螺旋跨膜區和細胞質內C端的PDZ結構域組成。低密度脂蛋白相關受體(LRP)是細胞表面分子,為經典Wnt信號通路中識別wnt配體蛋白的共受體。當Wnt信號激活時,Wnt配體蛋白與細胞膜上的Frizzled受體與跨膜分子LRP5/6形成復合體共同將細胞外的Wnt蛋白信號轉導至細胞內[9]。
HOANG等[9]用RT-PCR在骨肉瘤細胞株(U2OS,HOS,143B和Saos-2)中研究wnt蛋白受體的表達情況,發現Frizzled1、Frizzled2、Frizzled4、Frizzled5、Frizzled9和LRP5在這4種細胞株中均有表達,而Frizzled8在其中的3種細胞中有表達,Frizzled3只在143B細胞中出現表達。同時發現在44例骨肉瘤患者中,50%的患者活檢切片有LRP5表達。提出LRP5在mRNA中的表達似乎與人類骨肉瘤的轉移潛能有明顯的聯系,可以作為骨肉瘤進展的候選標記[6]。在Saos-2中阻斷LRP-5信號通過E-cadherin/β-catenin通路抑制細胞上皮-間葉轉化,導致細胞活性降低。用LRP5抑制劑阻斷Wnt信號后腫瘤進程相關蛋白[鈣粘蛋白N(N-cadherin)、轉錄因子Snail、基質金屬蛋白酶2(MMP2)]下調,阻礙裸鼠體內骨肉瘤生長和遷移,這些證據表明LRP5可能成為輔助骨肉瘤治療的靶點。
最近發現在不同年齡犬骨肉瘤細胞中Frizzled6的表達均明顯高于犬成骨細胞[10],這使Frizzled6可能作為骨肉瘤細胞的標志物。同時,骨肉瘤組織與其鄰近非腫瘤組織以及骨肉瘤細胞與正常細胞中Frizzled8的表達情況的比較中,發現Frizzled8在骨肉瘤中被高度上調[11]。這些研究都表明Frizzled作為經典Wnt/β-catenin通路的主要受體與骨惡性腫瘤(骨肉瘤)有密切的相關性。
2.3β-catenin蛋白因子在骨肉瘤中的作用β-catenin是經典Wnt/β-catenin通路中的核心蛋白,含有12個armadillo重復區的棒狀超螺旋結構,可防止蛋白水解,在細胞的信號傳遞中有重要作用[12]。β-catenin主要位于細胞膜,少量游離在細胞質。當Wnt信號通路未激活時,β-catenin通常被磷酸化,然后經泛素酶途徑降解[2]。
β-catenin與骨惡性腫瘤的關系已經得到了越來越多的關注,許多研究已經發現了骨肉瘤中β-catenin的聚集。在小鼠骨肉瘤細胞(LM8)和Dunn骨肉瘤細胞的細胞質和/或細胞核中同樣發現了β-catenin蛋白染色。LM8細胞具有高度的肺轉移潛能,而其β-catenin染色明顯高于原位癌Dunn細胞,這表明β-catenin是骨肉瘤肺轉移潛在生物學標志。值得注意的是,這兩組研究的基因序列分析都沒有檢測到β-catenin基因外顯子3片段上的突變,這表明骨肉瘤中β-catenin的積聚不是由于自身的突變造成,而可能是在Wnt通路的調節中發生的變化。
敲除β-catenin會提高甲氨蝶呤誘導Saos-2細胞死亡率,抑制β-catenin蛋白能夠增強甲氨蝶呤對Saos-2細胞的凋亡作用[7]。β-catenin作為經典Wnt/β-catenin通路中實現細胞核內外信號轉導的關鍵信號因子,其本身能與細胞膜上的E-cadhine結合影響細胞的粘附,許多研究已經發現其在骨肉瘤中異常表達,影響骨肉瘤的發生、發展及轉移。這對于抑制骨肉瘤轉移性的研究具有較為深入的作用。
2.4細胞核內因子LEF1對骨肉瘤的作用淋巴樣增強因子-1(LEF1)是 T 細胞因子/淋巴增強因子(TCF/LEF)家族成員之一,為高遷移率組分(HMG)轉錄因子。LEF-1蛋白主要有兩個功能結構域,一是羧基端的DNA結合域,即HMG-Box;另一個是氨基端的β-catenin結合域。β-catenin進入細胞核后與LEF-1的氨基端β-catenin結合域結合,LEF-1羧基端HMG-Box可以結合靶基因啟動子區域,進而激活下游靶基因(c-myc、cyclin D1、MMP-7等),導致細胞異常增殖。
LEF1與骨肉瘤的發生和轉移有一定的關系。有研究在Saos2細胞和人成骨細胞中均發現LEF1被上調[7]。另外,通過免疫組化法發現LEF1在骨肉瘤組織中高表達,并用Western blot和RT-PCR檢測到與低增殖轉移能力的骨肉瘤細胞(F4)相比,高增殖轉移能力的骨肉瘤細胞(F5M2)中LEF1表達增高[13],提示LEF1可能與骨肉瘤轉移存在正相關。
2.5經典Wnt/β-catenin通路中其他因子與骨肉瘤的作用經典Wnt/β-catenin通路也受到一些抑制因子的調控。Wnt抑制劑主要分為兩大類,其中包括通過競爭性結合wnt受體復合物的LRP5/6來抑制Wnt信號通路的DKK家族蛋白;以及直接與Wnt配體結合從而抑制Wnt信號通路的Wif-1、frizzled相關蛋白(sFRP)家族等[14]。研究已經發現這些Wnt信號通路抑制因子在骨肉瘤中具有抑制腫瘤發生和轉移的潛能。
DKK家族蛋白是一類與Wnt信號通路共受體LRP5/6結合,從而抑制經典Wnt信號轉導的糖分泌蛋白。DKK3通過調節Wnt信號通路而被作為腫瘤抑制因子。有研究顯示在骨肉瘤細胞中DKK3使β-catenin重新分配到細胞膜上,聚集在細胞膜上的β-catenin與E-cadherin結合形成復合體,阻止β-catenin的核內轉位,從而抑制wnt信號通路下游TCF/LEF轉錄因子的激活,而E-cadherin與腫瘤侵襲密切相關。因此,DKK3可能降低骨肉瘤生長及轉移能力[15]。
Wif-1是一種Wnt配體拮抗劑,Wif-1的超甲基化在許多人類腫瘤中已經被證實,例如鼻咽癌、肺癌、中皮瘤、乳腺癌和胃癌[16]。研究表明,在大多數骨肉瘤細胞和組織中Wif-1被下調,并且在小鼠骨肉瘤組織中重新表達Wif-1減少了腫瘤生長和肺部轉移能力[17]。體研究顯示,Wif-1是成骨細胞分化所必需的,而組織中Wif-1的減少和丟失會激活wnt信號通路,加速骨肉瘤的進展[18]。還有許多因子能夠影響Wnt/β-catenin信號通路,進而影響骨肉瘤的發生、發展以及轉移。研究已發現針對骨肉瘤的治療中其相關因子發生了改變,如sFRP家族一些蛋白等,這為骨肉瘤靶向治療提供了更多的研究基礎。
3 總結
Wnt/β-catenin信號通路在一些骨惡性疾病中扮演著重要的角色。在骨肉瘤中,許多Wnt/β-catenin信號通路中的蛋白過度表達,包括Wnt配體蛋白、Frizzled受體、LRP5/6、β-catenin以及一些核內轉錄因子TCF/LEF等。同時,基因編碼內源性Wnt通路抑制劑,如:Wif-1、DDK3等的表觀遺傳沉默。這些現象都強調了異常Wnt信號在骨肉瘤發生、發展以及轉移中的重要影響。
雖然學者對Wnt/β-catenin信號通路在骨肉瘤中的機制有所了解,但仍有許多具體調控機制待研究。例如:在骨肉瘤中,Wnt配體與其受體是如何相互作用的;哪些信號蛋白對骨肉瘤的發生和進展發揮著關鍵性調節以及識別作用。骨肉瘤的發展是一個極為復雜的過程,涉及多種分子信號通路,而Wnt/β-catenin信號通路也與其他多條信號通路,如Notch、TGF、MAPK通路中的信號因子存在crosstalking。這些復雜的信號通路是如何在骨肉瘤中相互交叉發揮作用的需要更多更全面的研究。因此,經典Wnt/β-catenin信號通路在骨肉瘤中的具體作用機制仍需更多深入的探索。

