恩替卡韋與阿德福韋酯治療乙型肝炎失代償期肝硬化的療效及對甲狀腺功能的影響
李飛鵬
我國是一個乙型肝炎大國,近期調查顯示,HBsAg陽性率在15~29歲人群中接近5%,據估計全國HBV感染者超過9 000萬,其中有2 000萬CHB患者,而肝硬化是CHB患者發生癥狀的主要時期和首要死因。抗病毒治療是乙型肝炎治療中最重要的措施,也是減少門靜脈高壓性出血、肝性腦病和原發性肝癌等并發癥的發生風險[1]。恩替卡韋(ETV)是新近應用于臨床的抗病毒藥物,其用于失代償期乙型肝炎肝硬化的療效與經典乙型肝炎抗病毒藥物,如阿德福韋酯(ADV)的比較尚不十分明確。為此,我院在98例失代償期乙型肝炎肝硬化患者中進行了一項隨機對照研究,報道如下。
資料和方法
一、 診斷標準
失代償期乙型肝炎肝硬化的診斷符合以下標準[2]:(1)存在HBV慢性感染史(即HBsAg陽性史≥6個月),近期行HBV血清學檢查顯示HBV DNA陽性;(2)綜合臨床表現、實驗室檢查、影像學和/或組織病理學等檢查明確存在肝硬化;(3)有腹水、肝腎綜合征、食管胃底靜脈曲張破裂出血、肝性腦病等任意一種肝硬化門靜脈高壓的相關并發癥。
二、納入與排除標準
納入標準:(1)符合上述失代償期乙型肝炎肝硬化的診斷標準;(2)一般情況良好、病史資料完整的18~65歲患者;(3)既往未進行核苷(酸)類似物治療;(4)治療依從性較高。
排除標準:(1)合并酒精肝、脂肪肝、原發性肝癌、代謝性肝病、遺傳性肝病及肝血管性病變等其他肝臟病變;(2)存在甲型、丙型等其他肝炎病毒感染;(3)合并人類免疫缺陷病毒(HIV)或結核分支桿菌感染;(4)服用甲狀腺相關藥物,合并嚴重心腦血管疾病或其他系統嚴重疾病。
三、 實驗設計方法
本研究為隨機對照的單盲、單中心實驗。
四、一般資料
共納入患者98例,根據患者納入研究的序號,使用隨機數表法將患者分為ADV組(49例)和ETV組(49例)。ADV組患者平均年齡(43.62±6.29)歲,男性25例、女性24例,HBeAg陽性40例,Child-Pugh分級B級36例,乙型肝炎病史(8.17±2.44)年;ETV組患者平均年齡(45.03±6.72)歲,男性29例、女性20例,HBeAg陽性37例,Child-Pugh分級B級39例,乙型肝炎病史(8.33±2.28)年。兩組患者基線資料比較均差異無統計學意義(P>0.05)。本研究方案經醫院倫理委員會審核通過,與患者本人或其家屬簽署知情同意書。
五、治療方案
在給予低脂優質蛋白飲食和保肝治療的基礎上,ADV組和ETV組患者分別應用ADV和ETV進行抗病毒治療:(1)ADV組給予ADV分散片(珠海聯邦制藥,國藥準字H20070123,10 mg*20粒),10 mg/d;(2)ETV組給予恩替卡韋片(中美上海施貴寶制藥,國藥準字H20052237,1.0 mg*7片)。采取多種途徑提高患者的治療依從性,所有患者的抗病毒治療最低療程為24周;在24周時評估抗病毒治療的療效,如存在原發性不應答,換用替比夫定片(北京諾華制藥,國藥準字H20070028,600 mg*14片),600 mg/d;如存在應答不佳,ADV組換用替比夫定片,ETV組加用替比夫定片。
六、治療監測和隨訪
治療后監測:每個月門診復查血常規和肝功能、腎功能、心肌酶譜等生化指標;每3個月復查HBV DNA、乙型肝炎“兩對半”;每6個月復查肝硬度、腹部彩超和甲胎蛋白水平。記錄和督促患者的治療依從性,密切觀察相關嚴重不良反應發生情況,當存在明確的心肌炎、橫紋肌溶解、乳酸酸中毒以及腎功能異常時立即停藥并給予相應治療。
隨訪:療程結束前結合門診復查進行隨訪;療程結束后采用電話、微信等形式對患者進行隨訪。主要隨訪終點事件為肝細胞肝癌,次要終點事件為全因死亡。隨訪截止時間2017年10月31日。
七、觀察指標與療效評價
觀察指標:比較兩組患者治療前和治療24周后的病毒學指標(如HBV DNA載量、HBV DNA轉陰率和HBeAg轉換率),治療48周后的肝纖維化指數、肝功能(Child-Pugh分級)和甲狀腺功能(促甲狀腺素),2年死亡率和肝細胞肝癌發生率。纖維化指數采用肝臟瞬時彈性硬度檢查(FibroScan,法國Echosens公司)進行測量。肝功能Child-Pugh分級主要根據肝性腦病、腹水、血清膽紅素、血清白蛋白濃度及凝血酶原時間5個方面進行評價,每項分為3個等級賦值1~3分,總分5~15分,分值越高,肝功能越差。血清膽紅素、血清白蛋白濃度及TSH使用全自動生化分析儀(AU480,貝克曼庫爾特)及其配套試劑進行測定。
療效評價:原發無應答:正規抗病毒治療24周后HBV DNA較基線下降不足2 log10IU/mL。應答不佳:正規抗病毒治療24周后HBV DNA較基線下降>2 log10IU/mL,但仍高于1 000 IU/mL。HBV DNA轉陰:血清HBV DNA載量低于檢測下限(<300 IU/mL);HBeAg轉換:原有HBeAg陽性患者轉換為HBV e抗體(HBeAb)陽性。
八、統計學處理

結 果
一、 兩組患者治療前后病毒學指標的對比
與治療前相比,兩組患者治療24周后的HBV DNA載量均明顯降低(t=13.694,19.679;P=0.000,0.000)。與ADV組相比,ETV組治療24周后的HBV DNA載量和無應答率較低(t=5.421,P=0.000;χ2=4.438,P=0.035),HBV DNA轉陰率和HBeAg轉換率較高(χ2=10.485,6.823;P=0.001,0.009),詳見表1。
二、 兩組患者治療前后的肝纖維化指數、肝功能和TSH的對比
與治療前相比,兩組患者治療48周后的肝纖維化指數、肝功能和TSH均明顯降低(t=5.454,10.821,P=0.000,0.000;t=3.222,7.919,P=0.002,0.000;t=3.063,6.830,P=0.003,0.000),其中ETV組改善程度較ADV組更明顯(t=3.474,4.752,2.935,P=0.001,0.000,0.004),詳見表2。
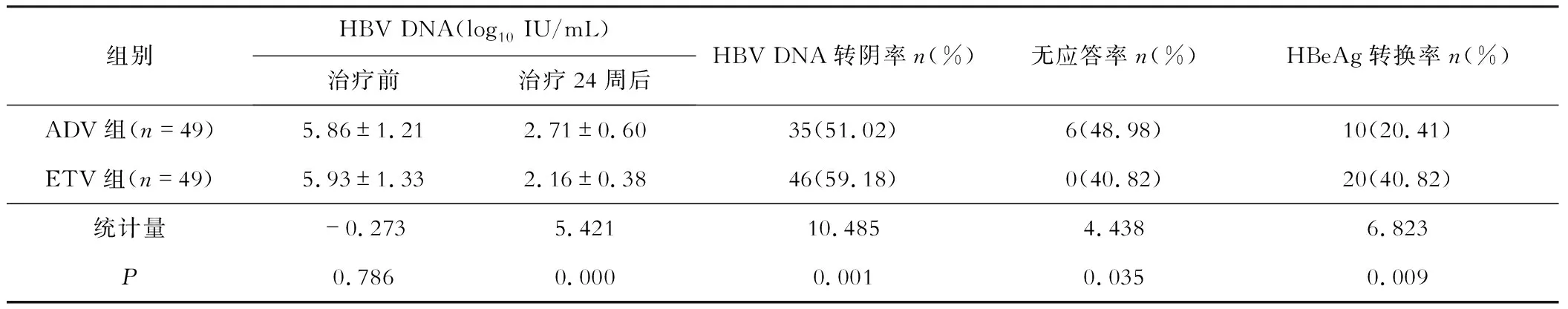
表1 兩組患者治療前后病毒學指標的對比

表2 兩組患者治療前后的肝纖維化相關指標和療效的對比
三、 兩組患者肝細胞肝癌和死亡的發生情況
在隨訪期間,ADV組和ETV組患者的全因死亡率分別為46.94%和30.61%(χ2=2.751;P=0.097),Log rank檢驗顯示,ETV組的死亡風險明顯低于ADV組(HR=0.547,P=0.042);兩組患者的肝細胞肝癌發生率分別為14.29%和4.08%(χ2=1.958;P=0.162),ADV組患者風險明顯高于ETV組(HR=0.263,P=0.047),詳見圖1。
四、 兩組患者的不良反應發生情況
ADV組和ETV組不良反應發生率分別為12.24%和6.12%,差異無統計學意義(χ2=0.489;P=0.494)。
討 論
核苷(酸)類藥物(nucleos(t)ide analogs, NAs)是一類可以快速、有效地干擾HBV復制的藥物,服用方便,具有較高的安全性,是目前CHB抗病毒治療的核心藥物。其抑制肝纖維化的進展,延緩失代償的發生和降低肝細胞肝癌發生風險的作用得到了大量研究證實[3]。
長期有效地抑制HBV復制是CHB治療的首要目標,也是延緩肝纖維化進展、減少失代償期并發癥出現及降低死亡風險的主要措施。病毒學應答則是衡量藥物抗病毒治療的重要指標,而低病毒應答與肝硬化患者的肝細胞肝癌發生風險密切相關[4]。本研究顯示,與治療前相比,兩組患者治療24周后的HBV DNA載量均明顯降低;而ADV組相比,ETV組治療24周后的HBV DNA載量基本達到檢測下限而不存在無應答,HBV DNA轉陰率和HBeAg轉換率較高,提示相對于ADV,ETV的抗HBV活性較高,而耐藥性極低。與Ahn等[5]對比了ETV與其他抗病毒藥物療效的研究結果相似,該研究還指出ETV在初始治療后的病毒學突破發生率較低,并具有較高的持續病毒學應答。此外,還有研究認為ETV可以有效抑制肝細胞內的HBV共價閉合環狀DNA,從而為控制HBV DNA水平,促進肝功能改善和HBeAg血清學轉化打下基礎[6]。

圖1 兩組患者的生存曲線和肝細胞肝癌發生情況
對比兩組患者治療前后肝纖維化相關指標,結果顯示,治療48周后,兩組患者的肝纖維化指數和PⅢNP水平均降低明顯,而ETV組降幅和治療有效率明顯優于ADV組。流行病學研究顯示,失代償期肝硬化的5年死亡率明顯高于代償期肝硬化(86%對18%),門靜脈高壓性出血和肝細胞肝癌是失代償期肝硬化最常見的死因。本研究顯示,盡管兩組患者的全因死亡率和肝細胞肝癌發生率均差異無統計學意義(P=0.097,P=0.162),但Log rank檢驗顯示,ETV組的死亡風險和肝細胞肝癌發生風險均明顯低于ADV組。這可能與ETV組患者的HBV低水平、肝功能改善及肝硬化進展得到遏制有關。而肝功能失代償期并發癥和肝細胞肝癌發生風險的明顯降低,為提高患者生存預期提供了良好的基礎[7]。
乙型肝炎肝硬化患者常伴有一定程度的甲狀腺功能異常。由表2可見,兩組患者治療前的TSH水平較高,而治療后,均出現了顯著降低,其中ETV組的改善更明顯。肝硬化患者的多種肝酶活性和水平嚴重下降,而失代償期患者更明顯。乙型肝炎肝硬化患者營養狀態較差,蛋白合成能力降低,甲狀腺素生成不足。肝臟中的5-脫碘酶是甲狀腺素T4向T3轉化的重要節點,5-脫碘酶活性降低可以導致有活性的FT3的減少[8]。

