血清高病毒載量和乙型肝炎發作孕婦的抗病毒治療*
林 蘇,朱月永
乙型肝炎病毒(hepatitis B virus,HBV)感染是中國重大公共衛生問題。2014年全國流行病學調查結果顯示,0~4歲、4~15歲、15~29歲人群 HBV感染率分別為0.32%、0.94%和4.38%,較2006年的調查結果明顯下降,但育齡女性HBV感染率仍然在6%~8%[1]。另一方面,隨著國家二胎生育政策的放開,如何正確處理HBV感染的育齡女性以及如何進一步減少HBV母嬰垂直傳播的問題仍是我們必須面對的重大課題。除了慢性乙型肝炎患者在抗病毒治療期間懷孕需要處理外,HBV感染女性在妊娠期間需進行抗病毒治療也有兩個情況:①因孕期慢性乙型肝炎(CHB)病情發作需及時進行抗病毒治療;②為減少HBV的母嬰垂直傳播需要進行的抗病毒治療。
1 乙型肝炎發作的抗病毒治療
女性在妊娠期出現特殊的生理改變,使得HBV感染的孕婦較同齡人在孕期及產后更容易出現HBV的激活,從而導致肝炎的發作[2]。一項多中心的回顧性研究發現,6%孕婦在妊娠期間出現血清轉氨酶升高,而在分娩后3個月內轉氨酶升高的比例可達到10%[3]。一方面,肝炎活動對胎兒的發育可能產生不利的影響,如容易出現低體質量兒、早產兒、胎兒宮內窘迫、死胎、新生兒窒息等[4,5];另一方面,乙型肝炎活動會增加孕婦產褥期感染的風險,妊娠期間的乙型肝炎活動嚴重時可導致肝功能衰竭,危及孕婦生命。因此,為降低孕產婦及胎兒發生疾病的風險,一旦孕期出現乙型肝炎活動,對具有抗HBV治療指征時應及時進行抗病毒治療,同時通過積極抗病毒治療后,降低血清HBV DNA水平也能減少母嬰傳播的機會,總體利大于弊,因此可適當放寬抗病毒治療的指征,在征求患者同意后選擇妊娠B級的核苷(酸)類似物治療[6]。關于妊娠期抗病毒藥物的選擇,多數指南推薦替諾福韋(TDF),部分指南也推薦替比夫定(LDT),少數指南提出拉米夫定(LAM)也可用于妊娠期女性(表1)。抗病毒治療的療程可參考普通人群慢性乙型肝炎的治療療程。
2 以母嬰阻斷為目的的抗病毒治療
母嬰傳播是新生兒感染HBV的最主要的傳播方式,血清HBeAg陽性母親新生兒HBV感染率為90%,而HBeAg陰性的母親新生兒感染率為30%。根據WHO的建議,所有新生兒均應在出生后第24 h內接受乙肝疫苗接種。中國專家共識也推薦HBsAg陽性母親分娩的嬰兒,應在出生后12 h內盡早接種乙肝免疫球蛋白100 IU和重組酵母乙肝疫苗10μg/0.5ml[6]。然而,在這種情況下,仍有5%~10%母嬰傳播發生率,高病毒載量和HBeAg陽性是HBV母嬰傳播的主要危險因素[6]。最新數據顯示,盡管在單因素分析中HBeAg狀態和HBsAg水平均影響母嬰傳播率,但高病毒載量才是造成母嬰傳播的獨立危險因素[7]。因此,降低母體病毒載量可能是在規范免疫接種前提下進一步減少母嬰傳播的最重要的手段。
2.1 高病毒載量的定義 針對阻斷母嬰HBV傳播的抗病毒治療,需根據孕婦的HBV感染狀態進行評估,孕婦的高病毒載量是重要的決定因素。但至今為止,對于高病毒載量的定義暫未統一。大部分研究認為,新生兒在規范接受乙肝疫苗和免疫球蛋白條件下,母體血清HBV DNA<5.3 lg IU/ml(相當于6 lg copies/ml)時,很少引起HBV傳播。隨著病毒載量的增高,母嬰傳播的風險逐步增加。當HBV DNA水平分別為6、7、8和9 log10 IU/ml時,嬰兒感染率分別為2.5%、5.7%、12.4%、24.7%[8],相當于每增加1個log10的HBV DNA,母嬰傳播的風險大約增加一倍。因此,盡管在不同的指南中對于母嬰阻斷的病毒載量的上限定義稍有不同(表1),但一般認為HBV DNA大于5.3 log10 IU/ml(6 log10 copies/mL)時,就可考慮采用抗病毒治療進行母嬰阻斷。
2.2 母嬰阻斷的效果 近期一項Meta分析結果顯示,病毒載量>5.3 log10 IU/ml的孕婦進行抗病毒治療能夠有效阻斷母嬰傳播的風險[9]。可選擇的抗病毒藥物包括TDF、LDT和LAM(表1),應用抗病毒藥物的時機為妊娠24~32 w。國內也有研究認為在妊娠12 w時開始抗病毒治療進行母嬰阻斷也安全有效[10]。大多數的隨機對照試驗(randomized controlled trial,RCT)研究支持應用LDT和LAM在母嬰阻斷方面的療效[11-14]。然而,近期兩項大型的有關TDF母嬰阻斷的研究則得出不同的結論。在Calvin Pan[11]的研究中,研究者招募200名HBV DNA>200 000 IU/ml的HBeAg陽性的母親,以1:1的比例隨機分配在TDF組或非抗病毒治療的對照組,抗病毒治療時間從妊娠30~32 w直到產后第4 w;產后第28 w檢測嬰兒血清HBsAg。意向性分析(5% 對18%,P=0.007)和完成性分析(0%對 7%,P=0.01)的結果均顯示,TDF組母嬰傳播率明顯低于對照組。泰國學者的類似研究卻得到了陰性的結果[15]。在泰國進行的這項多中心、隨機雙盲的臨床試驗中,研究者納入331名HBeAg陽性的孕婦,其中168名接受TDF治療,另163名接受安慰劑治療,治療時間從孕28 w至產后2 m。嬰兒出生時,除注射乙肝免疫球蛋白外,還分別在1、2、4、6個月注射乙肝疫苗。所有嬰兒在第6個月檢測HBsAg。TDF組中嬰兒(0%,95%CI:0~2)均未被感染,而安慰劑組中有3名(2%,95%CI:0~6)嬰兒感染,兩組間無統計學差異(P=0.12)。此項研究的陰性結果與大多數研究結論相反,而有些學者認為,樣本量太小、HBV基因型主要為C型、對照組羊膜腔穿刺和剖宮產比例低、出生后免疫接種比較及時、過早進行嬰兒HBsAg的檢測等原因可能影響了研究結果[16-18]。2016年的Meta分析顯示,抗病毒治療總體來說能夠降低母嬰傳播風險[9],而泰國學者最新的研究結果是否改變Meta分析的結果,還需要更新的Meta分析研究來驗證。另外,在更新Meta分析結果時,應當加入試驗序貫分析(trial sequential analysis,TSA)估算樣本量,以評估Meta分析結果的可靠性。
另外,盡管泰國的這項研究否定了抗病毒治療對于阻斷HBV母嬰傳播的療效,然而近期一項回顧性研究卻認為,即便病毒載量較低(≥3~6 log10 copies/ml)的孕婦也需要給予抗病毒治療以進行母嬰傳播的阻斷[19]。這項研究納入了211例HBV感染的孕婦,其中43例為高病毒血癥者(>6 log10 copies/ml),接受LDT治療,以89例高病毒血癥(>6 log10 copies/ml)和79例低病毒血癥(≥3~6 log10 copies/ml)患者為對照組,所有嬰兒規范接受免疫球蛋白和乙肝疫苗接種,在產后7 m對嬰兒進行檢測。結果提示,高病毒載量組接受LDT治療后,母嬰HBV傳播阻斷失敗率顯著降低(2.4%對16.9%),而未接受抗病毒治療的低病毒載量組的失敗率也高達10.1%。然而,這項研究為回顧性分析,因此病毒載量對母嬰傳播的影響可能需要更多的前瞻性研究或真實世界的研究確認。
3 產后哺乳與停藥
孕婦接受抗病毒治療進行母嬰HBV傳播阻斷后,分娩后停藥和哺乳也是大多數患者關心的問題。有研究顯示,產婦服用抗病毒藥物進行哺乳時,嬰兒血漿TDF水平比治療劑量低12500倍,并且94%嬰兒血漿測不出TDF水平[20],而嬰兒血液LAM水平僅為嬰兒推薦治療劑量的2%[21],但由于嬰兒接觸低水平藥物的風險還不清楚,并且藥物說明書建議在產婦服用抗病毒藥物期間避免母乳喂養,因此亞太和中國的專家共識不建議在抗病毒治療期間進行母乳喂養[6,22]。對于以母嬰傳播阻斷為目的的抗病毒治療的停藥時機,大多數應用核苷類藥物進行的母嬰傳播阻斷的RCT研究認為,停用抗病毒藥物后并不增加肝炎發作的機會[15];2018年亞太肝病學會(APSAL)收錄的國內學者的一項初步報告也提出,盡管抗病毒藥物在停藥后有50%患者出現轉氨酶水平高于正常上限,但未接受抗病毒治療者的這一比例更高(68%),故指南推薦在分娩后即刻或產后3個月可安全停用抗病毒藥物(表1)。但目前的大部分關于產后停藥的研究樣本量均不大,前瞻性研究更少,需要大規模的研究對其進行證實。
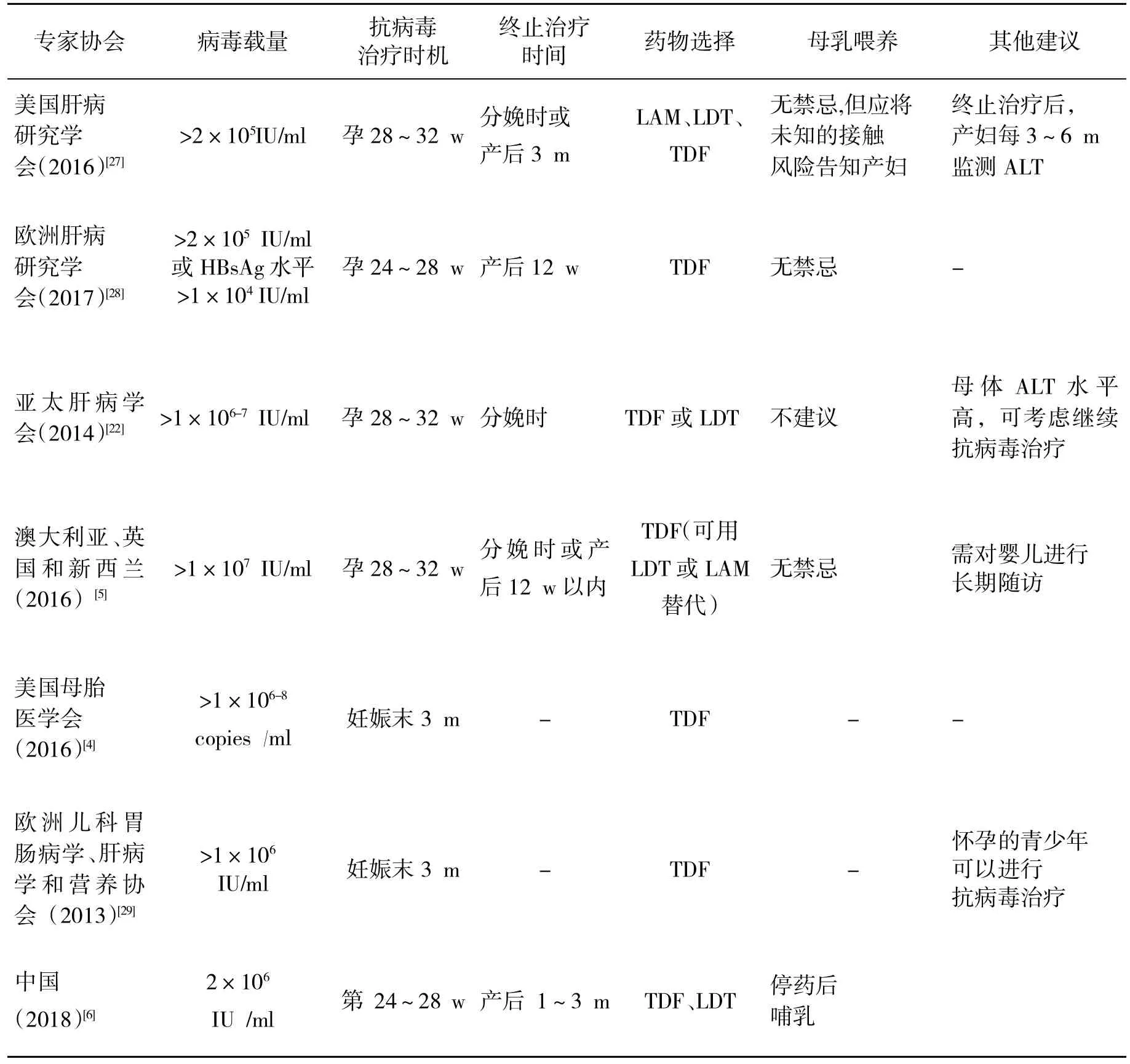
表1 國際專家協會對孕婦抗病毒治療預防乙肝母嬰傳播的建議
4 嬰兒安全性
大部分數據認為孕期使用LDT抗病毒對嬰兒是安全的。來自中國的兩項研究對服用LDT的孕婦分娩的嬰兒進行長達5年的隨訪,均未觀察到嬰兒的出生缺陷或嚴重不良事件,并且在隨訪至5歲時也未發現對生長發育有不良影響[23,24]。TDF對嬰兒的安全性似乎主要集中在骨磷代謝方面。在HIV感染的母親接受TDF治療的前瞻性研究中,449例嬰兒在1歲時的身高和頭圍數值稍低于未暴露于TDF的嬰兒,同時發現嬰兒的骨密度明顯降低[25]。另一項研究發現,母親懷孕期間服用TDF抗病毒藥物時,接受母乳喂養與未接受母乳喂養嬰兒的3年生存率無顯著性差異,也未發現先天性畸形、腎臟或生長發育異常,產后2歲嬰兒生長也不受TDF暴露的影響,但研究發現孕期服用TDF可引起嬰兒暫時性的血磷和肌酐清除率下降[26-29]。關于母親使用TDF治療對嬰兒的安全性目前尚缺乏長期隨訪的數據,需要進一步的研究證實。
5 結語
目前大多數指南的推薦意見認為,高病毒載量的孕婦接受抗病毒治療對減少母嬰HBV傳播具有重要的意義。然而,對于分娩后的處理以及長期的嬰兒安全性方面的問題則需要大規模的臨床試驗或真實世界的研究來進一步確認。

