小動物內鏡在在體成像中的應用研究*
張娜,楊西斌,屈亞威,高健翎,賈馥華,劉海峰
(1.安徽醫科大學武警總醫院臨床學院,安徽 合肥 230032;2.中國科學院蘇州生物醫學工程技術研究所,江蘇 蘇州 215163;3.武警總醫院 消化內科,北京100039)
在醫學和免疫學等相關基礎研究中,腸道相關疾病的動物模型作為腸道黏膜免疫系統、結腸炎和癌癥發展的關鍵研究工具,其重要性不言而喻。臨床醫生可通過內鏡系統對人的腸道病變(如腸道炎癥或腫瘤)進行觀察和監測,但由于動物體積較小,目前缺乏相關微型設備對動物腸道進行準確的在體評估。潰瘍性結腸炎(ulcerative colitis,UC)是一種局限于大腸黏膜和黏膜下層的慢性復發性非特異性腸道炎癥性疾病。目前,對UC模型的有效評估依賴于疾病活動指數(disease activity index,DAI)和體外組織病理學檢測。DAI評分指標包括小鼠的生活狀態、體重、大便的性狀和便隱血情況,具有一定的主觀性;病理學檢測則需要處死小鼠后分離腸道組織進行離體分析。以上方法存在以下缺陷:①無法對腸道病變進行在體評估和動態觀察,缺乏可重復性;②主觀個體差異及鼠間差異影響結果準確性;③離體組織分析需要更多的實驗小鼠數量,使研究的成本升高。此外,化學誘導結腸癌模型,如偶氮氧甲烷(azoxymethane,AOM)和1,2-二甲肼(1,2-dimethylhydrazine DMH),在結直腸癌發病機制及治療方法的研究中得到廣泛應用[1],但模型構建周期長達30周。采用致癌藥物聯用(如AOM/DSS,AOM/DMH),雖然縮短了誘導時間,但至少也需要10周[2]。長時間的誘導及小鼠間個體差異,很難確定每只小鼠腸道內腫瘤生長情況。目前,雖然已經有微型無創成像設備,如正電子發射斷層掃描(positron emission tomography,PET)和磁共振成像(magnetic resonance imaging,MRI)[3],可以對實驗動物進行在體觀察,但是這些方法成本高且耗時,而且對腸道病變不能進行清晰和精確的成像。
為了尋找一種安全、經濟和有效的方法,對小鼠腸道病變進行清晰成像和動態監測,本課題組自行組裝小動物內鏡成像系統,并且對此設備的應用進行了探索研究。
1 材料和方法
1.1 材料
Balb-c nu/nu小鼠(6~8周,體重約18~20 g),購于維通利華實驗動物中心;葡聚糖硫酸鈉(dextran sulfate sodiuln,DSS)(分子量 36 000 ~ 50 000),購自華美試劑公司,配置為3%水溶液;麻醉劑(5%氯胺酮+1%甲苯噻嗪)。
1.2 設備構建
依據電子內鏡成像原理,利用光源、信息處理器、視頻顯示系統和內鏡4個部分搭建小動物內鏡成像系統。系統主要依賴于鏡身前端裝備的成像設備進行圖像采集,經圖像傳感器將光學信號轉換為電子信號,后經圖像處理器對信息進行處理,再顯示在監視器的屏幕上。本系統采用CMOS傳感器,與CCD傳感器相比,具有成本小、集成度高、耗電量較小和硬件開發成本較低等優點。光源采用LED冷光源,具有發光性能穩定、體積小、產熱少和節能等優點。利用高清顯示屏進行成像,以提高圖像的清晰度。內鏡外直徑1.9 cm,鏡身長度60.0 cm。以上系統均與中國科學院蘇州生物醫學工程技術研究所合作研發。
1.3 實驗方法
1.3.1 UC模型構建 取6只小鼠,進行編號后,采用隨機數字表法將其隨機分為對照組和實驗組。實驗組自由飲用3% DSS水溶液,對照組給予蒸餾水飲用,連續飲用15 d。
1.3.2 內鏡下監測 內鏡操作前對成像探頭進行水潤滑,小鼠進行麻醉,麻醉劑使用方法為氯胺酮100 mg/kg+甲苯噻嗪10 mg/kg腹腔注射。待小鼠麻醉后,進鏡操作,平均進鏡深度約3 cm。根據UC內鏡下嚴重性評分(ulcerativecolitis endoscopic index of severity,UCEIS)標準[4]進行內鏡下評分,包括:血管模式(血管分布正常1分;血管結構模糊2分;血管閉塞或消失3分)、出血情況(無出血1分;可見陳舊性出血,用水沖洗后無血跡2分;可見血跡,用水沖洗后可見滲血3分;活動性出血4分)、糜爛和潰瘍(黏膜正常1分;黏膜粗糙、糜爛2分;可見淺表性潰瘍,表面覆白苔3分;可見潰瘍,且深度較深4分)。當實驗需要時,處死小鼠,取遠端結腸組織,根據DIELEMAN評分標準[5]從炎癥、隱窩損傷、黏膜再生情況、病變程度和范圍5個方面對結腸組織進行病理學評分,并與內鏡下評分進行對比。
2 結果
2.1 設備示意圖
小動物內鏡成像設備實物圖見圖1A。成像前端可見光源、相機及輔助操作通道(圖1B),調節范圍可達90°(圖1C)。
2.2 內鏡及病理學評估
內鏡下動態觀察小鼠腸壁黏膜變化,對照組未發現明顯變化,實驗組腸道黏膜動態成像結果見圖2。實驗開始第1天,腸道黏膜正常,內鏡下可以清晰地看到血管走行和分布(圖2A);飲用DSS第7天,腸道黏膜血管走行紊亂,黏膜發紅,粗糙呈顆粒狀,肛門處病變最明顯(圖2B);飲用第10天,腸壁黏膜血管走行模糊、紊亂,局部黏膜壞死,多處可見血跡(圖2C);飲用至第15天,內鏡下可見腸壁黏膜脫落,部分腸壁附著有膿性分泌物(圖2D)。分別于第1天、第7天、第10天和第15天,從每組中隨機各處死一只小鼠,分離遠端結腸組織,進行病理學評分,并與內鏡下評分進行對比。飲用15 d后兩組組織對比圖見圖3,肉眼可見對照組小鼠飲用蒸餾水15 d后,離體腸管組織黏膜呈淡粉色(圖3A),實驗組小鼠飲用DSS 15 d后,腸管組織黏膜明顯充血發紅(圖3B)。病理學檢查結果顯示:正常結腸組織黏膜上皮完整,結構清晰,上皮細胞排列整齊,腺體完整(圖3C),實驗組小鼠腸管組織黏膜表層糜爛,有潰瘍形成,腺體多數不完整,隱窩急性炎細胞浸潤,呈典型炎癥改變(圖3D)。依據UCEIS和DIELEMAN評分標準,分別對腸道病變進行內鏡和病理學評分,結果顯示:隨著DSS自由飲用時間的延長,實驗組小鼠腸道病變的內鏡與組織病理學評分一致呈增高趨勢。見圖4。

圖1 小動物內鏡成像設備實拍圖Fig.1 Small animal endoscopic imaging equipment actual diagram
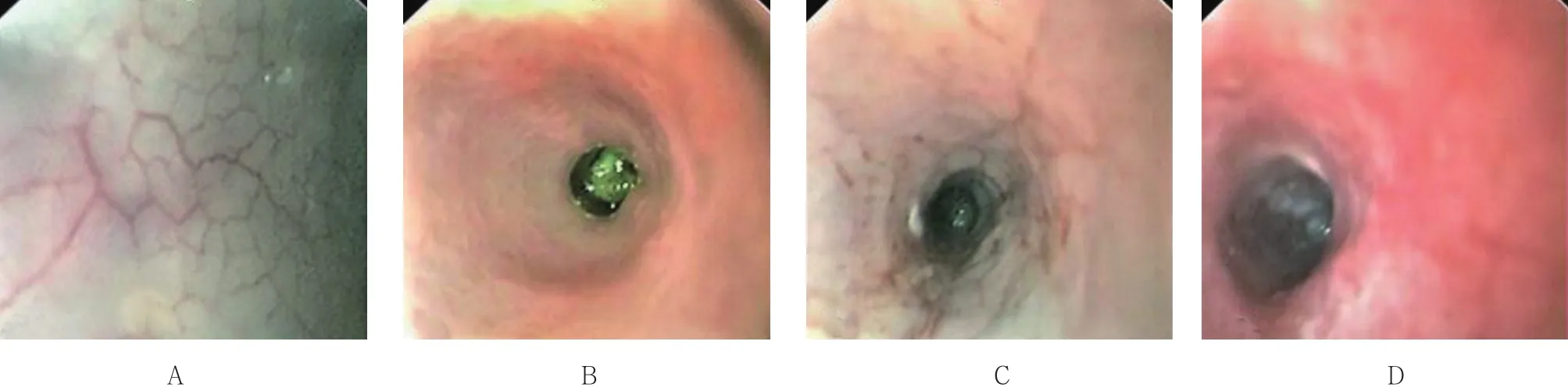
圖2 實驗組小鼠腸道內鏡下成像Fig.2 Endoscopic imaging of mice in experimental group
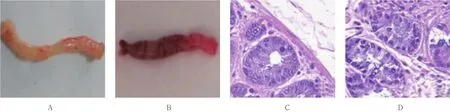
圖3 離體腸組織肉眼觀及病理學典型圖片Fig.3 Macroscopic view of isolated intestinal tissue and pathological picture
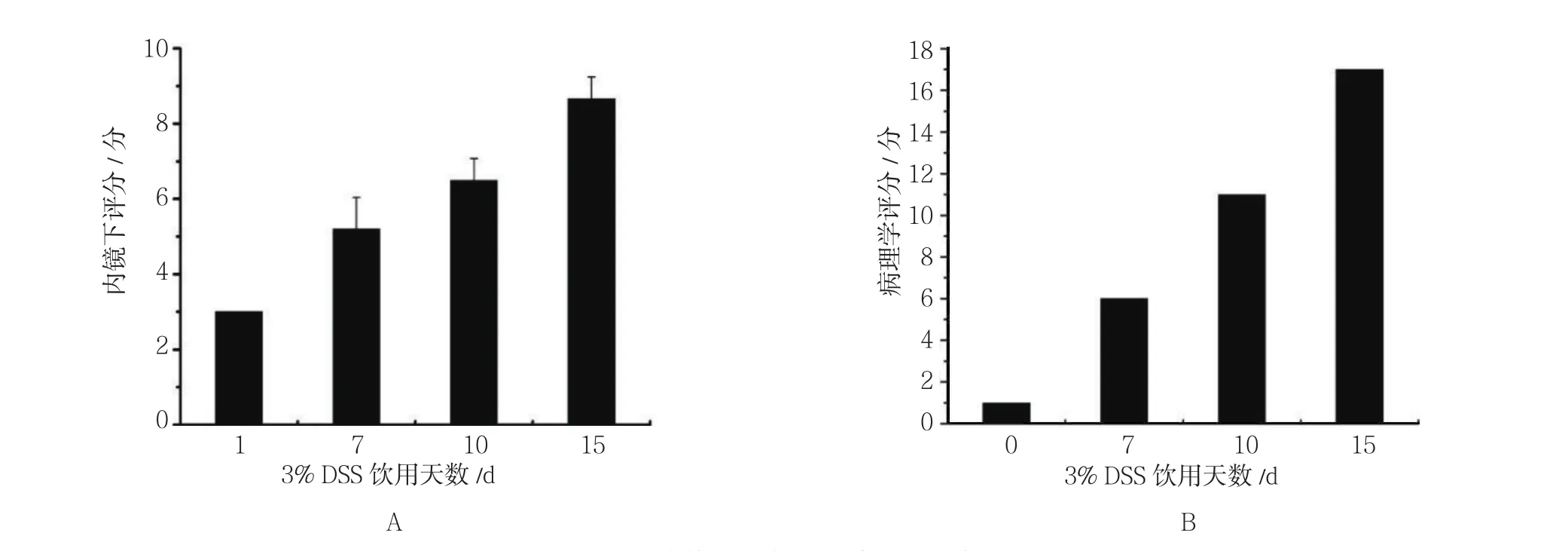
圖4 實驗組小鼠腸道病變內鏡及組織病理學評分Fig.4 Endoscopic and histopathological score of mice in experimental group
3 討論
在臨床應用中,內鏡聯合病理學檢查可以對患者腸道進行在體評估。然而,在動物研究中,對腸道病變進行有效評估的唯一方法為:處死小鼠取病變組織進行分析。因此,微型內鏡系統的研發對動物水平的研究具有重要意義。國外已有相關研究實現了動物腸道內成像,但是國內仍缺少相關領域的研究。故本課題組根據內鏡成像原理,自行搭建小動物成像平臺,并對其應用進行了探索。
UC的發病率在我國有明顯增加趨勢[6-8],而且該病具有癌變傾向。因為發病機制不明確,成為研究熱點之一。目前,有多種腸道病變模型構建方法,包括化學藥物誘導型、基因型、細胞移植型和自發性動物模型[9-11]。本研究采用自由飲用3% DSS的方式構建模型,并利用內鏡系統對小鼠進行腸道內成像,結果顯示:此內鏡系統不僅可以實現腸道黏膜的清晰成像,而且可以通過重復性的操作,對腸道病變進行動態監測。與傳統評價方式(如小鼠狀態、體重、糞便分析或處死后離體組織學分析)相比,內鏡下成像具有以下優勢:首先,動態觀察是一個連續的過程,可以觀察病變發展情況;其次,與自身形成對照,減少了鼠間個體差異,同時也有利于選擇最佳個體進行動物實驗研究,提高研究結果的一致性和可靠性;此外,操作的重復性可以減少實驗動物數量,有效降低研究成本;最重要的是,可依據成像結果對腸道病變進行直觀地評價。
目前,多數研究[12-13]使用的均為硬式內鏡,存在進鏡距離受限及操作難度高等缺陷,本系統采用軟式成像探頭,與現有的硬式內鏡相比,能有效調節進鏡角度、增加進鏡深度和降低操作并發癥的發生率;此外,此成像探頭直徑小,對小鼠造成的創傷較小。在未來的研究中,若與相關配件設備配合使用,可實現腸道黏膜下注射和在體活檢等多種操作。但是此成像系統與其他相關設備相比,仍存在成像模式單一的缺點。例如,MITSUNAGA等[14]應用的設備,可結合熒光探針進行熒光成像。SHAO等[15]的研究中,將高分辨顯微內鏡(high-resolution fiber-optic microendoscopy,HRME)成像技術與基于光纖的光聲內鏡(fiber-based,real-time C-scan optical-resolution photoacoustic microscopy,F-OR-PAM)相結合,構建新型內鏡成像系統,可以實現熒光和光聲雙模態成像,多種成像模式的結合,具有提高成像效果的作用。因此,本設備在未來還有待進一步的優化。

