衰老性肌萎縮癥的膳食營養調控研究進展
梁計陵,王岑依,陳 寧*,王 梅*
(1.武漢體育學院研究生院,湖北 武漢 430079;2.杜肯大學蘭格斯健康科學學院,美國 賓夕法尼亞 匹茲堡 PA15282;3.武漢體育學院健康科學學院,運動訓練監控湖北省重點實驗室,天久運動營養食品研發中心,湖北 武漢 430079)
隨著世界人口和社會的迅速老齡化,不同健康問題和衰老性疾病的患病率也相繼增加,衰老過程中以骨骼肌質量和力量下降為特征的衰老性肌萎縮癥的發生率也隨著年齡的增長而不斷上升[1]。衰老性肌萎縮癥的發生會導致老年人身體活動能力降低[2]、生活質量下降、心肺功能受損,使不利的代謝作用[3]、跌倒[4]、殘疾和死亡發生率增加[5],以及造成醫療負擔的加重[6]。衰老性肌萎縮癥的一個典型特征是“丟失”:即伴隨著骨量的丟失,肌肉質量和強度的降低,骨的脆性和骨折的風險也相應增加[1]。實際上,骨骼肌和骨的衰退過程是兩個并行的過程,而且相互影響,目前人們已認識到骨骼肌的減少會加速骨質的丟失。近年來,隨著我國人口老齡化加劇,骨折的發病率逐漸增加,衰老性肌萎縮癥也因此越來越受到廣泛關注。
衰老性肌萎縮癥的發生與營養、活動、激素、代謝、免疫等多種因素有關,其中營養和身體活動是兩項重要因素[7]。分子生物學、組織學和生物化學等的研究表明,骨骼肌受自由基氧化損傷及修復受損、骨骼肌蛋白質合成減少、神經肌肉功能衰退和運動單位重組、體內激素水平變化、線粒體功能紊亂等均與衰老性肌萎縮癥有關[8]。隨著年齡增長,在上述諸多因素的影響下,老年人由于衰老等生理變化引發的精神和身體損傷使得分解代謝日漸增強,且由于飲食方式單一和食物攝入量下降從而大多存在熱量及營養攝入不足等飲食問題,造成營養不良風險增加[9]。與年輕人相比,40~70 歲之間中老年人饑餓和口渴程度較低,吃得更慢更少,食物攝入量下降約25%[10],這會導致典型的“衰老性厭食癥”[11]:包括味覺和嗅覺的喪失、對食物飽足感敏感度上升、咀嚼困難,以及胃腸道功能的受損。“衰老性厭食癥”則會導致能量攝入量降低,包括進一步體質量和肌肉質量的減少[10]。而老年人肌肉力量和身體能力下降又可能增加營養不良的幾率從而形成“營養相關性衰老性肌萎縮綜合征”[12],加劇整體惡性循環。雖然衰老性肌萎縮癥的病因和治療方法尚未明確定義,但營養起著至關重要的作用是不容置疑的[13]。大量文獻表明營養在維持和增加肌肉質量及功能中起重要作用[14]。為此,有必要為衰老性肌萎縮癥補充額外的營養素,以減輕因肌肉減少導致的肌肉質量和功能相關性損失。其次,由于老年人攝食量下降,對他們來說,滿足其營養的飲食和微量營養素的要求顯得更高。因此,建立最佳營養指南,以確定最可行的膳食營養補充形式,從而提高衰老性肌萎縮癥的營養狀況。目前國內外有許多關于干預措施的研究,從提供營養支持到補充特定營養素,有關營養干預方式不斷更新且結論也不盡相同。針對衰老性肌萎縮癥,目前營養干預較為一致的方式包括蛋白質飲食,補充必需氨基酸補充劑、VD、肌酸、抗氧化營養素(VE等)和ω-3脂肪酸等營養素[15]。本文將總結和討論衰老性肌萎縮癥的定義和發病機制、目前營養方面對于衰老性肌萎縮癥的對策、相關營養食品對衰老性肌萎縮癥的作用機制,并提出保持肌肉質量和功能的新型營養策略。最后,闡述合理化飲食方式結合運動干預的協同效應,這將為衰老性肌萎縮癥的預防和治療提供更佳選擇。
1 衰老性肌萎縮癥病因及機制
目前對于衰老性肌萎癥的病因有許多不同觀點:肌肉脂肪變性增加、肌肉代謝受損、炎性標志物(即腫瘤壞死因子-α(tumor necrosis factor-α,TNF-α)和白細胞介素(interleukin,IL)-6)增加、氧化應激增加、線粒體功能障礙、激素失衡、毛細血管流量減少等[16-17]。其中,骨骼肌纖維數量下降、肌肉蛋白質凈合成減少、細胞氧化損傷及修復受損已成為公認的發病原因[18]。從病理生理學的角度來看,肌萎縮患者表現為肌肉質量的凈丟失,這是由于肌肉蛋白質合成(muscle protein synthesis,MPS)減少和肌肉蛋白質分解(muscle protein breakdown,MPB)增加造成的。相反,在健康的老年人中,肌肉蛋白質卻沒有改變。磷脂酰肌醇3激酶(phosphatidylinositol3 kinase,PI3-K)/蛋白激酶B(protein kinase B,Akt)/雷帕霉素敏感的哺乳動物雷帕霉素靶蛋白復合體1(mammalian target of rapamycin complex 1,mTORC1)信號通路作用于下游并且由叉頭框蛋白O(FoxO)激活的泛素連接酶促進細胞凋亡,如泛素蛋白連接酶E3,其中肌肉環指蛋白(musclespecific ring finger protein 1,MuRF-1)和肌肉萎縮盒F蛋白(muscle atrophy F-box protein,atrogin-1)被認為是調控MPB的主要因子[19]。隨著人體的衰老進程,胰島素抑制蛋白質水解激活PI3K-AKT-mTORC1通路,之后出現胰島素抵抗狀態同時增加MPB[20-21]。胰島素本身就是一種血管舒張激素,胰島素抵抗會導致血管流量減少,從而惡化胰島素對肌肉的影響,并限制營養物質和氧氣向肌肉的流動,從而降低MPS并增加MPB[22]。同樣,老年人常見的微血管和大血管病變也會影響到衰老性肌萎縮癥。例如:血清胰島素樣生長因子I(insulin-like growth factor-1,IGF-1)、支鏈氨基酸(branched chain amino acid,BCAA)、磷脂酸(phosphatidic acid,PA)能夠以不同的機制激活mTORC1;而糖皮質激素,肌肉生長抑制素(myostatin)和活性氧(reactive oxygen species,ROS)是mTORC1的負調控因子[23]。此外,慢性疾病和衰老也與促炎癥狀態分子如TNF-α、IL-1和IL-6的分泌增加有關。這些細胞因子有助于增加骨骼胰島素抵抗和肌肉蛋白水解激活泛素-蛋白酶體系統,抑制Akt/mTORC1途徑,拮抗IGF-1對肌肉的作用[24]。TNF-α通過激活Caspase-8和Caspase-3參與的外源性凋亡通路,從而在肌肉細胞凋亡中起關鍵作用[25]。ROS產生增多與衰老密切相關,伴隨著抗氧化系統的損害,導致氧化還原狀態的不平衡從而影響mTORC1通路并破壞脂質和蛋白質的結構。尤其是線粒體內膜的磷脂過氧化反應會損害線粒體呼吸鏈,從而引起線粒體的代謝功能障礙。這種功能障礙導致呼吸能力降低,ATP產生減少和ROS生成增加從而加劇惡性循環。氧化應激也是促進慢性炎癥的重要因素,通過激活細胞氧化還原狀態調控核轉錄因子-κB(nuclear factor-κB,NF-κB)進行調控;反過來,炎癥又會產生ROS,導致進一步惡性循環。因此,衰老、營養不良、身體活動缺乏、炎癥及氧化應激增加和線粒體功能障礙等都是衰老性肌萎縮癥發生的危險因素[23]。
2 目前食品營養物質補充類別
有效對抗衰老性肌萎縮癥的營養物質應該滿足于:1)提供足夠的熱量攝入及營養素作用于肌肉;2)確保提供適當的營養素,同時考慮到年齡、性別、代謝特征、健康狀況及身體活動能力;3)在適當的時間,即有生理需要時提供足夠數量的營養素。在此前提下,參考2010年衰老性肌萎縮癥消耗疾病學會專家小組制定的營養建議及中國營養學會老年營養分會牽頭組建的“肌肉衰減綜合征營養與運動干預中國專家共識起草組”共識[15,26]。國內外共識在承認運動干預的核心作用外,還強調了配合幾種營養素及足夠的熱量攝入的重要性,包括蛋白質和支鏈氨基酸、VD、抗氧化營養素、脂類脂肪酸和肌酸。下文將具體介紹對于支持這些和其他膳食因素的證據以及在衰老性肌萎縮癥中的具體作用機制。
2.1 膳食蛋白及蛋白補充劑
人體生理功能衰退的重要物質基礎是蛋白質,隨著年齡的增長,由于食欲不振、咀嚼或吞咽困難、胃排空減少、身體和精神損傷、藥物與營養的相互作用、多種疾病的存在以及荷爾蒙反應的改變、蛋白質和其他營養素的攝入不足,這會導致骨骼肌中蛋白質的合成受損[9]。蛋白質是補充老年人肌肉質量損失最重要的常用營養素;然而,老年人普通日常蛋白攝入量一般不會大于(0.6 g/(kg·餐mb))。研究表明,每天至少需要1.2~1.5 g/(kg·餐mb)的蛋白質攝入量才足夠達到人體所需量,并且應該調整不同的飲食和攝入量來抵消由于老年人蛋白質攝入量減少引起的合成代謝反應(圖1)[27]。由于刺激肌肉蛋白質合成的劑量約為35 g,因此,建議每餐都應該攝入至少25 g優質蛋白質才能最大限度地刺激肌肉蛋白質的合成,并保持肌肉質量(圖1)[28]。此外,在早餐和中餐中建議攝入速效蛋白質(如乳清蛋白),在睡前建議攝入大量低效蛋白質(如酪蛋白),以刺激生長激素的合成代謝作用,并且防止夜間因長時間禁食引起的分解代謝(圖1)。總而言之,高質量的蛋白質飲食已經被證明能有效地減少與年齡有關的肌肉質量損失,從而改善衰老性肌萎縮癥。
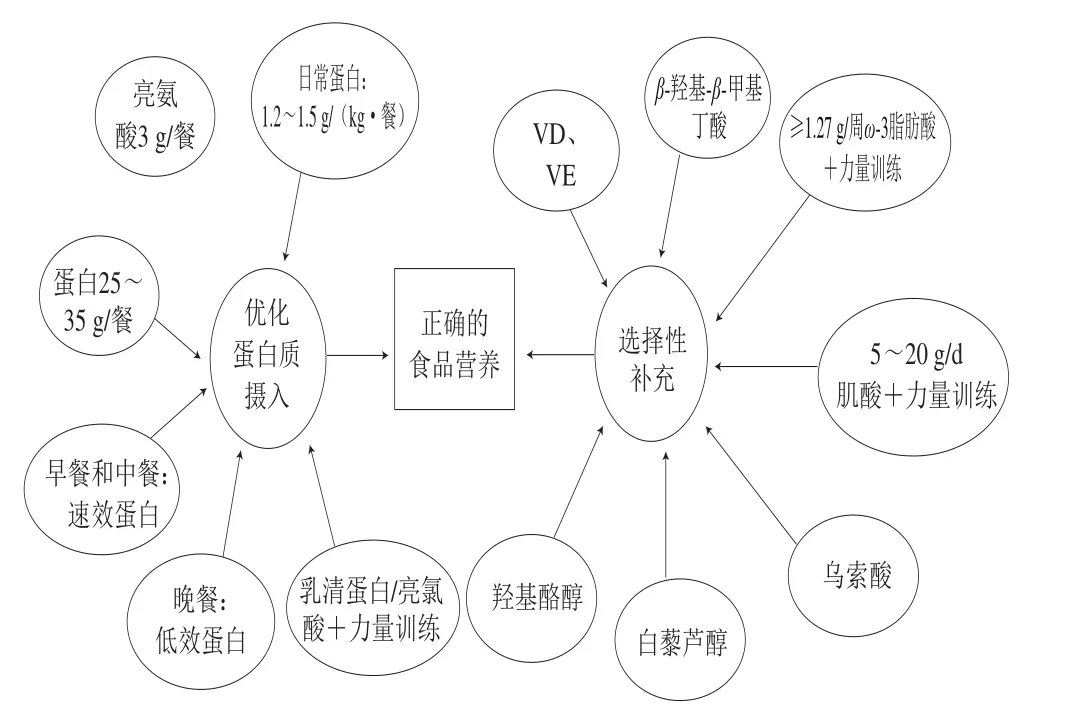
圖1 改善衰老性肌萎縮的營養策略Fig.1 Possible nutritional strategies to counteract sarcopenia
2.2 亮氨酸補充劑
膳食蛋白質的氨基酸組成對蛋白質的肌肉合成能力同樣有著顯著的影響。特別是,乳清蛋白中豐富的亮氨酸被認為是肌肉蛋白質周轉的主要膳食調節劑[29]。支鏈氨基酸不僅是蛋白質合成的底物,還可以通過活化并調節蛋白質周轉的細胞信號,刺激胰島素合成,增強胰島素敏感性,促進體內合成代謝[30]。由于其在合成代謝性質方面的優越性,推薦富含亮氨酸的蛋白質作為衰老性肌萎縮癥的最佳補充蛋白質[31]。同時,建議每餐可以攝入3 g亮氨酸作為保持肌肉質量的有效營養策略(圖1)。為此,可以選擇攝入含有1.4~1.7 g亮氨酸的100 g瘦肉、奶制品、牛肉或魚類等作為有效營養來源[32]。此外,也建議老年人可以在進行力量訓練前后2~3 h攝取快速蛋白質(如乳清蛋白)或如富含亮氨酸的補充劑,來進一步增強運動誘發的肌肉增大(圖1)[33]。因此,亮氨酸作為支鏈氨基酸可以為骨骼肌提供能量底物,是全身和骨骼肌蛋白質合成的重要調控因子,可以通過活化骨骼肌哺乳動物雷帕霉素(mammalian target of rapamycin,mTOR)信號途徑來激活線粒體蛋白質激酶S6刺激肌肉蛋白合成[34-35],并且抑制蛋白酶體途徑(圖2)[36],可作為衰老性肌萎縮癥防治的一個有效營養選擇。

圖2 膳食營養對衰老性肌萎縮癥的作用機制概述Fig.2 Overview of the underlying mechanisms of action of relevant dietary nutrition on sarcopenia
2.3 VD補充劑
老年人飲食攝入不足,陽光照射減少,皮膚在紫外線照射下合成VD的能力受損,以及25-羥基VD向其活性形式的腎轉化率降低,血清VD水平隨著年齡的增長而逐漸下降[37]。同時,血清25(OH)D<50 ng/mL與低瘦體質量、低腿部力量存在明顯正相關[38];VD影響肌肉肥厚,其缺乏與衰老性肌萎縮癥高患病率有關[39]。因此,有必要檢測所有衰老性肌萎縮癥老年人體內VD的水平,當老年人血清25(OH)D低于正常范圍時,應及時予以補充(圖1)。一項Meta分析顯示,當VD補充劑量達到700~1 000 IU/d可使老年人跌倒風險降低19%[40]。事實上,VD已經被證明可以增加肌肉蛋白合成,也能增強亮氨酸和胰島素對肌肉細胞蛋白質合成率的刺激作用。同時,VD可增加肌肉細胞中鈣的攝取,并對鈣通道具有調節作用,從而影響肌肉收縮活動。雖然毫無疑問VD會影響肌肉代謝和營養,但對骨骼肌纖維的作用仍然存有爭議。傳統觀點為:VD以其生物活性形式1,25(OH)D與肌肉細胞內VD受體(VD receptor,VDR)相結合,快速激活絲裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)信號通路(圖2)[41],從而刺激肌肉細胞的增大和生長[42]。VD的作用是通過與位于細胞表面和細胞核中的VDR結合而進行[43]。VD與膜上VDR結合觸發了非基因組途徑,從而調節鈣向細胞質中釋放,來滿足肌肉收縮的需要,從而刺激蛋白質的合成(圖2)[44]。無論具體的機制是什么,VD會改善肌肉骨骼功能,并對肌肉纖維的構成和形態產生積極的影響;同時增加了老年人肌肉力量,減少跌倒次數[45]。因此,建議肌萎縮老年人用富含VD的食物,例如飽含VD3(膽鈣化醇)的油性魚類;VD2豐富(麥角鈣化醇)的曬干蘑菇。此外,還有VD強化的食物(包括VD2和VD3),如牛奶、面包、酸奶等。
2.4 抗氧化營養素補充劑
根據衰老自由基理論可知,在生命過程中對細胞大分子的氧化損傷的積累是推動衰老過程的中心機制。隨著衰老發生,肌質網攝入Ca含量減少,而細胞內和線粒體Ca含量增加,ROS生成增多,形成氧化應激。氧化應激的增強可改變線粒體DNA(mitochondrial DNA,mtDNA),阻止蛋白質合成與ATP生成,導致肌肉細胞壞死和凋亡,同時使衛星細胞減少,增殖能力下降,以致肌纖維含量減少。外源性抗氧化物的補充可增強抗氧能力,改善氧化應激,降低mtDNA損傷,調節氮平衡。一些研究已經驗證可以通過增強抗氧化能力來延緩衰老過程的可能性[46]。例如:VE在上調的氧化應激和炎癥在年齡相關的骨骼肌功能障礙(衰老性肌萎縮癥)中起關鍵作用[47]。激活NF-κB與氧化還原信號和炎癥密切相關(圖2)[48-49]。活性氧損傷膜,包括線粒體膜和內質網,由于其疏水性,VE往往大量存在;足夠的VE可以有效地修復受損的肌肉質膜并保持其活性[50]。同時,VE能抑制炎癥介質的表達,包括NF-κB、TNF-α、IL-1、IL-6、IL-8(圖2)。相比之下,衰老性肌萎縮癥的抗氧化劑補充數據極為有限。并且,目前對于抗氧化治療的有效性還存在爭議,為此抗氧化治療在衰老性肌萎縮癥中主導的作用也有待進一步研究和探討[51]。但仍建議老年人應多食用富含抗氧化劑的食物,例如水果和蔬菜,因為其還含有大量健康營養素(例如維生素、礦物質和纖維素),并且復合制劑優于單獨補充(圖1)。
2.5 脂類脂肪酸補充劑
ω-3脂肪酸(也被稱為n-3脂肪酸)是多不飽和脂肪酸(polyunsaturated fatty acids,PUFAs),主要包括α-亞麻酸、二十碳五烯酸(eicosapntemacnioc acid,EPA)和二十二碳六烯酸(docosahexaenoic acid,DHA),具有許多潛在的益處。研究顯示,補充ω-3脂肪酸后老年人骨骼肌蛋白質合成代謝增強[52]。此外,在“地中海飲食”中的藍魚提供大量ω-3脂肪酸,它可以增強對不同刺激(運動干預、激素替代療法、蛋白質飲食)的肌肉合成代謝反應,降低氧化應激和胰島素抵抗[52-53]。有研究表明衰老性肌萎縮癥與慢性低度炎癥息息相關[54],補充ω-3脂肪酸可抵抗慢性炎癥,緩解肌肉減少,有利于維護心血管和大腦細胞,從而改善衰老性肌萎縮癥(圖2)。已發現ω-3脂肪酸可以激活骨骼肌mTOR靶標,刺激骨骼肌蛋白質的代謝,促進肌肉增大和力量增強[55](圖2)。此外,有研究得出老年婦女每天補充含有2 g EPA和DHA的魚油,結合抗阻力量訓練,在干預90 d后肌肉力量得到進一步的增強[56]。所以,每周食用不少于1.27 g的ω-3脂肪酸或不少于1 份脂肪魚可以有效提高骨密度及腿部肌肉力量(圖1)[57]。因此,建議通過每周食用至少2 份魚類來確保足夠的ω-3脂肪酸攝入量,從而改善衰老性肌萎縮癥相關功能障礙。
2.6 肌酸補充劑
肌酸(creatine,Cr)是一種胍基化合物,內源性肌酸在肝臟和腎臟由精氨酸、蛋氨酸和甘氨酸合成;外源性肌酸可從食物的肉和內臟中,但含量很少。隨著年齡增長,肌肉內Cr水平也隨之降低[58],肌酸以磷酸肌酸的形式存儲在于肌肉中。磷酸肌酸向ADP提供高能磷酸鍵,形成ATP,為骨骼肌收縮提供能量。Cr攝入可通過調節肌肉蛋白動力學,衛星細胞活性和含量以及合成代謝激素分泌來促進肌肉合成代謝。由Cr攝入誘導的蛋白質合成代謝反應可能與mTOR途徑的直接激活有關(圖2)[59]。研究表明,老年人力量訓練結合Cr能夠增加肌肉質量,并提高肌肉力量[60]。有趣的是,補充Cr的老年人會在干預結束后依然保留長時間的剩余有益效應。事實上有研究顯示,在老年男性中,12 周的Cr補充與力量訓練相結合,會使肌肉質量和力量得到顯著增強,而Cr停止補充12 周后依然保留部分效果[61]。此外,攝入肌酸可增加磷酸肌酸比例,從而改善細胞鈣調控和體內平衡,減少ROS生成(圖1)[62]。肌酸除了在增強肌力方面的作用外,對認知和心理活動、骨健康、肌肉骨骼損傷修復等功能和方面也有積極的作用[63]。水合肌酸作為一種廉價且有效的營養補充劑,服用后幾乎沒有副作用。當與力量訓練相結合時,能夠提高老年人的肌肉質量和運動功能表現。因此,對于參加力量訓練的肌萎縮老年人而言,短期補充Cr(例如,5~20 g/d的水合肌酸,持續2 周)是個值得推薦的有效選擇(圖1)。
3 新穎的飲食選擇和營養策略
3.1 β-羥基-β-甲基丁酸補充劑
由于β-羥基-β-甲基丁酸(β-hydroxy-β-methylbutyrate,HMB)具有促蛋白質合成代謝和脂肪分解作用,HMB長期以來一直被用作增效助劑[64]。研究結果表明,內源性HMB與年齡呈負相關;血漿濃度與年輕和年長成人的瘦體質量和肌肉力量呈正相關[65]。HMB補充劑已經在老年人中進行了實驗測試,越來越多的證據表明,HMB可能有助于減緩肌肉損失并改善肌肉力量[66]。對7 例老年人補充HMB的隨機對照實驗進行的薈萃分析顯示,與對照組相比,干預組的肌肉質量增加更多[67]。在骨骼肌中,HMB通過下調蛋白水解途徑抑制蛋白質分解,通過激活mTOR途徑刺激蛋白質合成,同時可以轉化為羥甲基戊二酰輔酶A改善肌纖維完整性,并增加脂肪酸氧化能力(圖2)[68]。HMB及其酸形式[69]通過激活不同途徑刺激來增加蛋白質合成并降低蛋白質降解;同時,加速肌肉衛星細胞激活(圖2)[70]。研究表明,補充HMB可以逆轉蛋白質凈合成代謝的缺陷,并改善肌肉老年人的肌肉力量,特別是與力量訓練相結合時作用更為明顯[71]。
3.2 羥基酪醇補充劑
羥基酪醇(hydroxytyrosol,HT)是一種天然多酚類化合物,主要以酯類的形式存在于橄欖中。特級初榨橄欖油中的羥基酪醇是“地中海飲食模式”中的重要營養組成部分,并且這種飲食方式中的大數量水果和蔬菜亦能作為限制氧化應激的抗氧化物質的豐富來源。越來越多的證據表明,這種飲食方式可能對肌肉功能有一定的好處[72]。嚙齒類動物和培養細胞實驗研究表示:HT能夠通過激活AMP依賴的蛋白激酶(AMP-activated protein kinase,AMPK),增強過氧化物酶體增殖物激活受體γ輔激活因子1α(peroxisome proliferator activated receptor γ coactivator-1α,PGC-1α)和核呼吸因子(nuclear respiration factors,Nrf)1和Nrf2表達(圖2)[73]。同時,HT可以激活AMPK,并且在劇烈的體育運動中可以有效減少肌肉損傷,炎癥和繼發性免疫缺陷[74]。此外,HT還是一種具有多效性的線粒體抗氧化劑[75]。目前,羥基酪醇等多酚類物質作為一類儲量豐富的可再生綠色資源,具有延緩機體衰老,預防心血管病、抗癌、降血糖降血脂、增強免疫功能、抗輻射等功能。但對于衰老性肌萎縮癥的研究還十分有限和稀少,其強大的抗氧化及清除自由基作用在肌萎縮的食品開發方向值得進一步去探究和研發。
3.3 烏索酸補充劑
烏索酸是一種蘋果皮中富含的親脂性五環三萜類化合物,也存在于其他水果(例如李子、蔓越莓和藍莓)及草藥(例如迷迭香、山楂、薄荷)等。有研究表明烏索酸能減少因禁食和肌肉去神經支配明顯的肌肉萎縮誘導的應激反應。同時,烏索酸可能通過抑制萎縮相關的骨骼肌基因表達來增加肌肉質量。例如對空腹或遭受脊髓損傷的小鼠及時給予烏索酸,其可通過抑制萎縮相關基因(atrogin-1和MuRF-1),上調PKB/Akt激酶、核糖體蛋白S6激酶和Insulin/IGF-1信號傳導的刺激來減輕肌肉損失(圖2)[76]。在相關后續研究中,給食用高脂肪飲食的小鼠補充烏索酸可增加小鼠肌肉質量和強度,改善葡萄糖耐量,降低白色脂肪組織質量和肝脂肪變性的程度[77]。最近,有研究在一種慢性腎臟病的小鼠模型中,進行烏索酸長期治療(口服給藥21 d),得出烏索酸可以通過減少肌肉萎縮抑制素(包括血清和肌肉)和炎癥細胞因子(IL-6、TNF-α等)的表達來削弱了肌肉萎縮(圖2)[78]。這些結果都清楚地表明烏索酸不僅具有抗炎特性,同時其作為中草藥中重要的成分,具有抗氧化的作用,能激活MAPK信號通路,參與在應激條件下細胞的免疫調節、炎癥反應和細胞凋亡過程,從而機體的免疫力[79]。目前,對于烏索酸的研究主要集中于抗致癌藥物的研究方向。因此,烏索酸作為一種在中藥中重要的營養補劑,其對于肌萎縮癥中降低氧化應激和炎癥因子的作用及機制值得進一步深入研究。
3.4 白藜蘆醇補充劑
研究表明,水果、蔬菜、谷物、藥草等植物中富含的生物活性物質,可以通過模擬信號來達到與熱量限制和體育鍛煉類似的衰老性肌萎縮癥治療作用[80-81]。例如,白藜蘆醇和其他多酚(槲皮素和姜黃素)具有強大的抗氧化能力并刺激線粒體生物合成[82]。特別是白藜蘆醇能維持由抗阻訓練引起的合成代謝過程[83]。研究表明:這些植物化學物質能夠激活熱量限制和運動所刺激的幾種途徑,包括PGC-1α、sirtuin 1(SIRT1)和AMPK(圖2)[84]。此外,有研究灌胃8 月齡大鼠100 mg/(kg·d)白藜蘆醇12 周,發現白藜蘆醇可以降低大鼠肌膜和肌原纖維內線粒體中的ROS水平,并且通過測定總超氧化物歧化酶活力發現其不僅增強了抗氧化能力,而且改善脛骨前肌中谷胱甘肽過氧化物酶和過氧化氫酶活力[85]。此外,白藜蘆醇作為重要的天然產物,其抗癌作用也備受關注。據報道,白藜蘆醇可以通過調節蛋白激酶B和AMPK的活性,從而抑制mTOR信號通路來誘導細胞自噬[86];而細胞自噬在衰老性肌萎縮中的清除損傷或衰老細胞器、ROS等代謝廢物,維持正常水平的骨骼肌蛋白質量控制等方面作用已經得到有效證實。因此,利用白藜蘆醇等天然產物預防和治療衰老性肌萎縮癥會成為未來治療的創新營養策略。
4 飲食方式及結合運動的協同效應
膳食營養成分之間存在著高度相關性,補充單一營養素可能達不到衰老性肌萎縮治療的理想效果。因此,需要了解不同營養素對衰老性肌萎縮癥的影響及其相互作用。“健康”的飲食模式有助于改善衰老性肌萎縮癥患者的肌肉力量,其特點是攝入豐富的水果和蔬菜,足量的全麥谷物和油性魚類[87]。同時,在有關于男性和女性動脈粥樣硬化風險研究中的也提到,對中年人而言,大量的水果和蔬菜攝入是有益處的健康飲食方式[88]。以膳食營養為基礎的“食療”干預不僅會改變一系列營養素的攝入量,并且比單一補充營養素更能有效地預防與年齡相關的肌肉萎縮程度。例如:Cr和乳清蛋白的結合可以在阻力運動期間增強2 種營養素的肌肉合成代謝作用。在為期10 周的全身力量訓練中,老年男性補充水合肌酸(0.1 g/(kg·d))和乳清蛋白(0.3 g(kg·d))實驗組與僅攝入Cr或等熱量碳水化合物安慰劑的對照組相比,非脂肪質量和肌肉力量的增加更多[89]。這一實驗表明Cr和高質量蛋白質攝入對肌肉蛋白質合成代謝有協同刺激作用。同時,力量訓練已被證明是一種增加肌肉力量和改善老年人身體功能的有效干預方式[90]。飲食和運動對身體功能的協同作用,在蛋白質/氨基酸補充方面得到了廣泛的研究。例如,食用高蛋白食物可以使老年人的肌肉蛋白質合成增加50%,而高蛋白飲食和力量訓練相結合則能使蛋白質的合成率提高100%以上[91]。但是,高蛋白飲食可能會增加體內酸負荷,從而對肌肉骨骼系統產生不利影響。低度代謝性酸中毒會刺激蛋白水解途徑,這種刺激可以通過增加糖皮質激素(如皮質醇)的產生來觸發[7,92-93]。為此,可在飲食中加入適當的堿性鹽用來減少尿氮排出,從而減少肌肉蛋白質分解來保護肌肉。因此,對于衰老性肌萎縮癥的營養干預策略,除了強調膳食營養的保護作用,還可以考慮飲食結合運動所帶來的協同效應,營養補充和運動干預相結合可能比單獨營養素攝入干預更為有效。
5 結 語
隨著年齡增長,肌肉質量和力量的丟失成為一個主要的健康問題。衰老性肌萎縮癥作為一種嚴重的老年病綜合征,具有漸進的、不可逆轉的性質。為了找到可行的預防與治療方法來對抗這種與衰老相關的疾病,需要進行廣泛的研究以了解其發病機制。毫無疑問,營養與運動干預在改善衰老性肌萎縮癥的肌肉質量損失方面起著核心作用;研究表明,不僅蛋白質、氨基酸、VD、抗氧化劑、ω-3脂肪酸和肌酸的具有改善衰老性肌萎縮癥的肌肉質量損失作用,新型的HMB、羥基酪醇以及植物中飽含的天然產物烏索酸和蛻皮甾酮等物質都可作為治療衰老性肌萎縮癥的營養策略。營養與運動干預肌萎縮癥的可能機制是:1)蛋白質和亮氨酸制劑主要通過Akt/mTOR途徑來刺激蛋白質合成,同時抑制泛素-蛋白酶體系統來抑制蛋白質降解,從而促進骨骼肌蛋白質合成增加;2)VD可以促進肌營養和代謝,刺激蛋白質合成;3)抗氧化營養素能改善氧化應激,加強抗氧能力和抗炎作用;4)ω-3脂肪酸可以通過mTOR途徑對肌肉合成代謝產生積極影響,同時起抗炎作用;5)肌酸可以改善細胞生物能量,減少ROS生成并調節肌肉蛋白動力學;6)HMB激活mTOR途徑刺激蛋白質合成,以逆轉蛋白質凈合成代謝的缺陷,并激活肌肉衛星細胞;7)烏索酸也可通過Akt/mTOR途徑來抑制肌肉萎縮蛋白的表達,從而緩解肌萎縮;8)羥基酪醇和白藜蘆醇則通過AMPK/mTOR自噬信號通路來調控,從而減少肌肉降解和丟失,同時又可改善線粒體內的ROS水平,提高線粒體抗氧化能力。
但目前對于衰老性肌萎縮癥食品營養的機制研究極為有限,深入研究每種營養物質的作用機制,可以幫助了解這些營養元素相互作用及聯合效果,為肌萎縮癥的食品營養研發提供一定理論參考依據。同時,為了優化營養策略對衰老性肌萎縮癥的作用,在充分考慮食品營養攝入的同時可結合一定運動干預,使其產生的協同效益更利于衰老性肌萎縮癥的防治。

